2020 年 53 巻 5 号 p. 425-434
2020 年 53 巻 5 号 p. 425-434
症例は75歳の男性で,上腹部痛を自覚し受診した前医で膵頭部に27 mmの囊胞性病変を指摘されたが,明らかな悪性所見はなく,分枝型膵管内乳頭粘液性腫瘍(intraductal papillary mucinous neoplasm;以下,IPMNと略記)として定期的に画像評価を行っていた.6年2か月後,囊胞内部に10 mm大の造影される壁在結節が出現した.High-risk stigmataを伴うIPMNと診断し,腹腔鏡補助下亜全胃温存膵頭十二指腸切除術を施行した.病理組織学的に,囊胞性病変は低異形度IPMNであった.IPMNの結節に一致してIgG4陽性形質細胞の浸潤を伴う炎症細胞の集簇,花むしろ状繊維化,閉塞性静脈炎を認めた.免疫染色検査で強拡1視野当たり100個以上の集簇したIgG4陽性形質細胞を認め,IPMNに1型自己免疫性膵炎が合併したために壁在結節状の所見を呈したと考えられた.
A 75-year-old man presented with upper abdominal pain. CT and MRI showed cystic lesions 27 mm in size with no malignant findings in the head of the pancreas. Under the diagnosis of intraductal papillary mucinous neoplasm (IPMN), the patient was followed-up with imaging studies. Six years after the initial presentation, a contrast CT scan showed an enhanced mural nodule 10 mm in size in the cyst, and the patient was referred to our hospital for further examination. CT and MRI revealed the cysts had shrunk compared to previous imaging findings. Pancreatic juice cytology showed no malignant cells. Based on detailed examination, a diagnosis of IPMN with high risk stigmata was made and laparoscopy-assisted pancreatoduodenectomy was performed. A histopathological examination revealed a cystic lesion consisting of IPMN with low-grade dysplasia, inflammatory infiltrates with lymphoplasmacytes corresponded to nodules in cysts, obliterative phlebitides, and storiform fibrosis. Immunohistochemical staining demonstrated that the infiltrating lymphoplasmacytes were positive for IgG4 and that IgG4+/IgG+ plasm cell ratio was over 40%. Finally, we diagnosed branch duct type IPMN associated with autoimmune pancreatitis type-1, mimicking an enhanced mural nodule. We encountered a rare case of IPMN associated with autoimmune pancreatitis. It can be suggested that serological and histological examinations, including blood IgG4 testing and ultrasound-guided fine-needle aspiration, should be considered in patients with IPMN that show rapid appearance of enhanced nodules and shrinkage of cysts.
膵管内乳頭粘液性腫瘍(intraductal papillary mucinous neoplasm;以下,IPMNと略記)は低異型度から浸潤癌まで広い異型度のスペクトラムを示す囊胞性膵腫瘍であり,high-risk stigmataなどの悪性を示唆する所見を認める場合に外科的切除が考慮される.一方,1型自己免疫性膵炎(autoimmune pancreatitis;以下,AIPと略記)は,びまん性膵腫大を特徴とするIgG4関連疾患の一つであるが,時に限局性の病変を形成し,膵癌との鑑別が困難となり,手術が施行される場合がある1).今回,1型AIPを合併し,造影される壁在結節状の画像所見を呈したIPMNの1例を経験したので,文献学的考察を加えて報告する.
患者:75歳,男性
主訴:上腹部痛
既往歴:高血圧症,脂質異常症,高尿酸血症,左海綿静脈洞部髄膜腫(摘出術後),胆囊結石症(摘出術後)
家族歴:膵癌の家族歴なし.
現病歴:上腹部痛を自覚し,前医で施行したCTとMRIで膵頭部に分枝型IPMNを指摘された.High-risk stigmata,worrisome featuresを認めず,定期的に画像評価を行っていたが,6年2か月後のCTで造影される壁在結節を指摘され,精査加療目的に当院へ紹介となった.
来院時現症:身長166.2 cm,体重71.2 kg,体温36.2°C,血圧106/58 mmHg,脈拍62回/分.表在リンパ節は触知せず,眼球結膜の黄染を認めなかった.腹部は平坦,軟であり,腫瘤は触知しなかった.
来院時血液検査所見:血算,生化学検査では異常を認めず,CEA,CA19-9,DUPAN-2,Span-1はいずれも正常範囲内であった.血清IgG4は226 mg/dlと高値であった.
前医画像検査所見:前医初診時に施行されたCT,MRIで膵頭部に27 mmの多房性囊胞性腫瘤を認めたが,充実成分は認めなかった(Fig. 1a).主膵管と連続しており,膵腫大は認めず,主膵管径は2 mmであった.初診時から4年10か月後に施行したCTまで著変を認めなかった.初診時から6年2か月後のCTで囊胞内に遅延性に造影される壁在結節が出現した.

CT at preoperative assessment. a: At the time of initial assessment, abdominal CT scan showed a 27-mm cystic lesion in the head of the pancreas. b, c: At preoperative assessment, abdominal CT scan showed a solid mass with delayed enhancement and shrunken locules (delay phase).
当院画像検査所見:CTで膵頭部に25 mmの多房性囊胞を認め,囊胞内に10 mm大の遅延性に造影される充実性成分を認めた.前医と比較して囊胞は縮小していた.リンパ節腫大や遠隔転移は認めなかった(Fig. 1b, c).MRIでは,CT同様に膵頭部に囊胞辺縁の一部に遅延性に造影される充実性腫瘤を認めた(Fig. 2a, b).拡散強調像では囊胞辺縁全体を取り囲むように高信号域を認めた(Fig. 2c).MRCPでは前医と比較して囊胞径が30 mmから27 mmに縮小し,上流主膵管は4.4 mmと軽度拡張していた(Fig. 2d, e).超音波内視鏡検査においても,膵頭部に25×23 mmの,辺縁に充実性成分を伴う囊胞性病変を認めた.明らかな浸潤所見は認めなかった(Fig. 3).内視鏡的逆行性膵管造影(endoscopic retrograde pancreatography;以下,ERPと略記)では膵頭部に囊胞性病変が造影され,その尾側の主膵管は軽度拡張していた.膵管の不整はなかった(Fig. 4).膵液細胞診は細胞質に粘液を含む異型に乏しい腺細胞を認め,class IIの診断であった.PET-CTでは膵頭部囊胞性腫瘍に一致してFDGの異常集積(早期像SUV max 2.9,遅延像SUV max 3.78)を認めた.細胞診では悪性の所見はえられなかったものの,high-risk stigmata(5 mm以上の造影される壁在結節)を伴う分枝型IPMNであり悪性化の可能性が高いと考えられた.明らかな浸潤所見を認めなかったことから,腹腔鏡補助下亜全胃温存膵頭十二指腸切除術(subtotal stomach-preserving pancreaticoduodenectomy;以下,SSPPDと略記)を施行した.再建は小開腹下にSSPPD-II-A-1法で行った.手術時間は6時間56分,出血量は314 gであった.術後,Grade Bの膵液漏を合併したが,ドレナージにより軽快し,術後39日に退院となった.

MRI at preoperative assessment. a: Early phase of contrast-enhanced MRI showed a low-intensity solid mass in cystic lesion in the head of the pancreas (arrow). b: Late phase of contrast-enhanced MRI revealed a delayed-enhancement solid mass in cystic lesion (arrow). c: On diffusion weighted images, a high intensity signal was recognized in the part corresponding to the solid mass as well as in the circumference of the cystic lesion (arrow). d: At the time of initial assessment, MRCP showed a cystic lesion in the head of the pancreas (arrow). e: At preoperative assessment, MRCP revealed shrunken locules (arrow) and upstream main pancreatic duct (MPD) dilation 4 mm in diameter.

EUS at preoperative assessment. EUS visualized a hyperechoic structure in the hypoechoic mass in the head of the pancreas (arrow, lesion; arrowheads, MPD). The size of the hypoechoic mass was 25×23 mm.
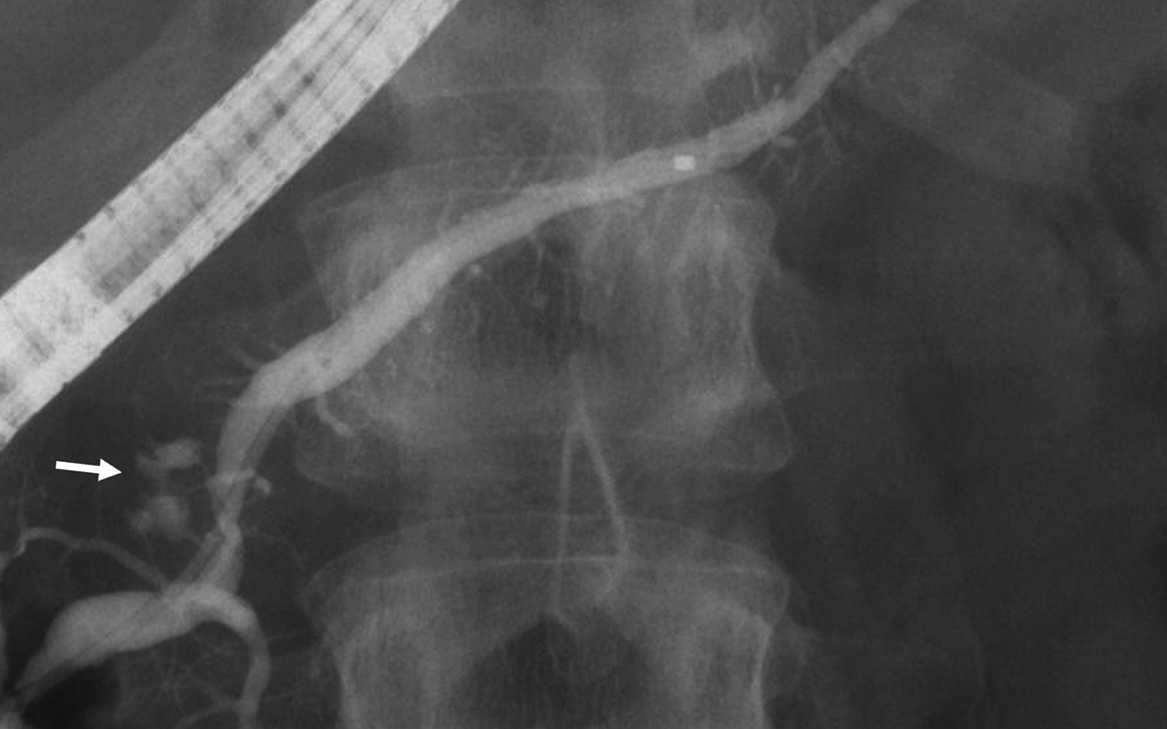
ERP at preoperative assessment. ERP showed cystic lesions on the head of the pancreas with upstream MPD dilation (arrow, cyst).
切除標本肉眼所見:膵頭部に30 mm大の境界不明瞭で白色調の,周囲に充実性腫瘤を認める囊胞性病変であった(Fig. 5).拡張した多房性囊胞より粘液が流出した.
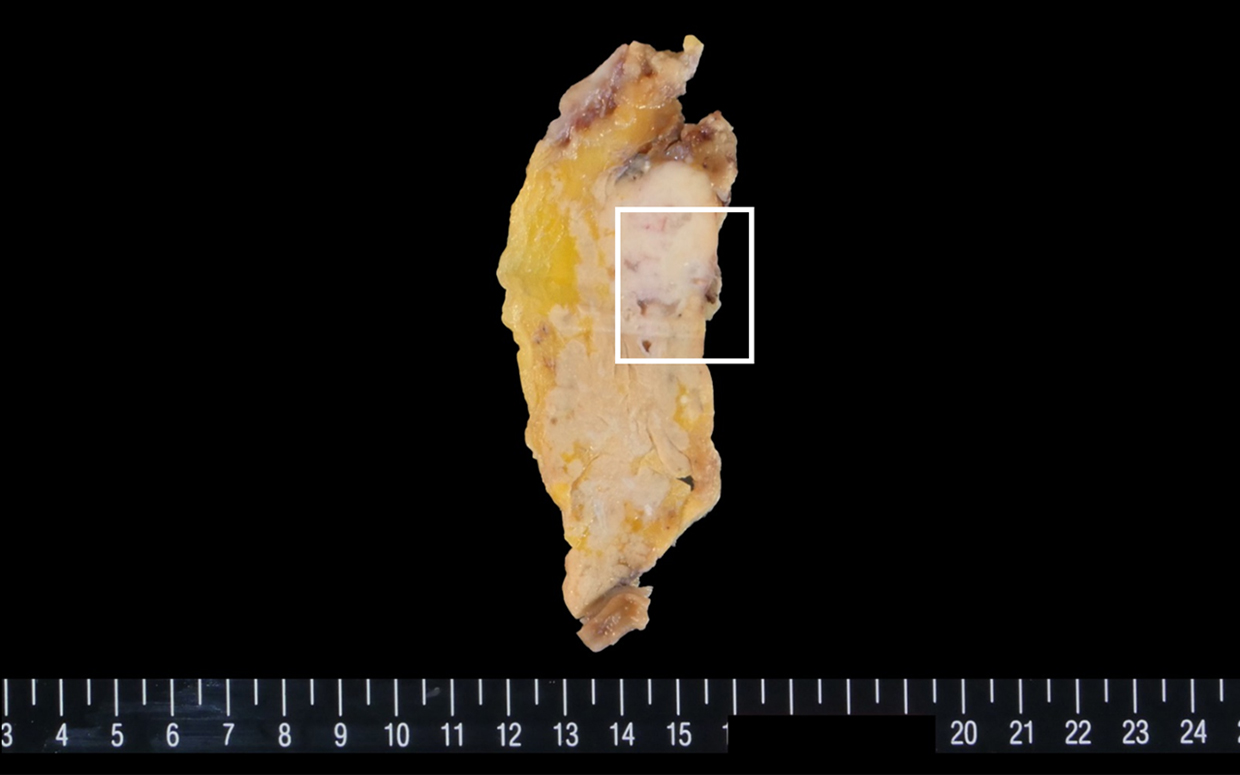
Macroscopic findings revealed a cystic lesion 30 mm in size, surrounded by a poorly-marginated and whitish solid lesion.
病理組織学的検査所見:ルーペ像では拡張した分枝膵管内に乳頭状構造を呈する病変があり,周囲の間質部はリンパ濾胞を伴った炎症性変化と線維化を認めた(Fig. 6).拡大すると,乳頭状構造は軽度異型を伴う粘液上皮で形成されており,間質には形質細胞の浸潤および花むしろ状の線維化を認めた(Fig. 7a~c).乳頭状上皮の免疫染色検査では,MUC1陰性,MUC2一部陽性,MUC5AC陽性,MUC6陽性,CDX2陰性であり,胃型IPMNの病理学的特徴と一致していた.さらに,腫瘍上皮の遺伝子解析でKRASとGNASの変異を認め,IPMNを裏付ける所見であった.強拡1視野当たり100個以上の集簇したIgG4陽性形質細胞を認めた(Fig. 8a).加えて閉塞性静脈炎の所見を認め(Fig. 8b, c),自己免疫性膵炎臨床診断基準20182)の1型AIPに合致するものであった.

Loupe view of the resected specimen showed papillary proliferative lesions in the expanded branch pancreatic duct, lymphoplasmacystic infiltration and fibrosis around the lesions (broken line).
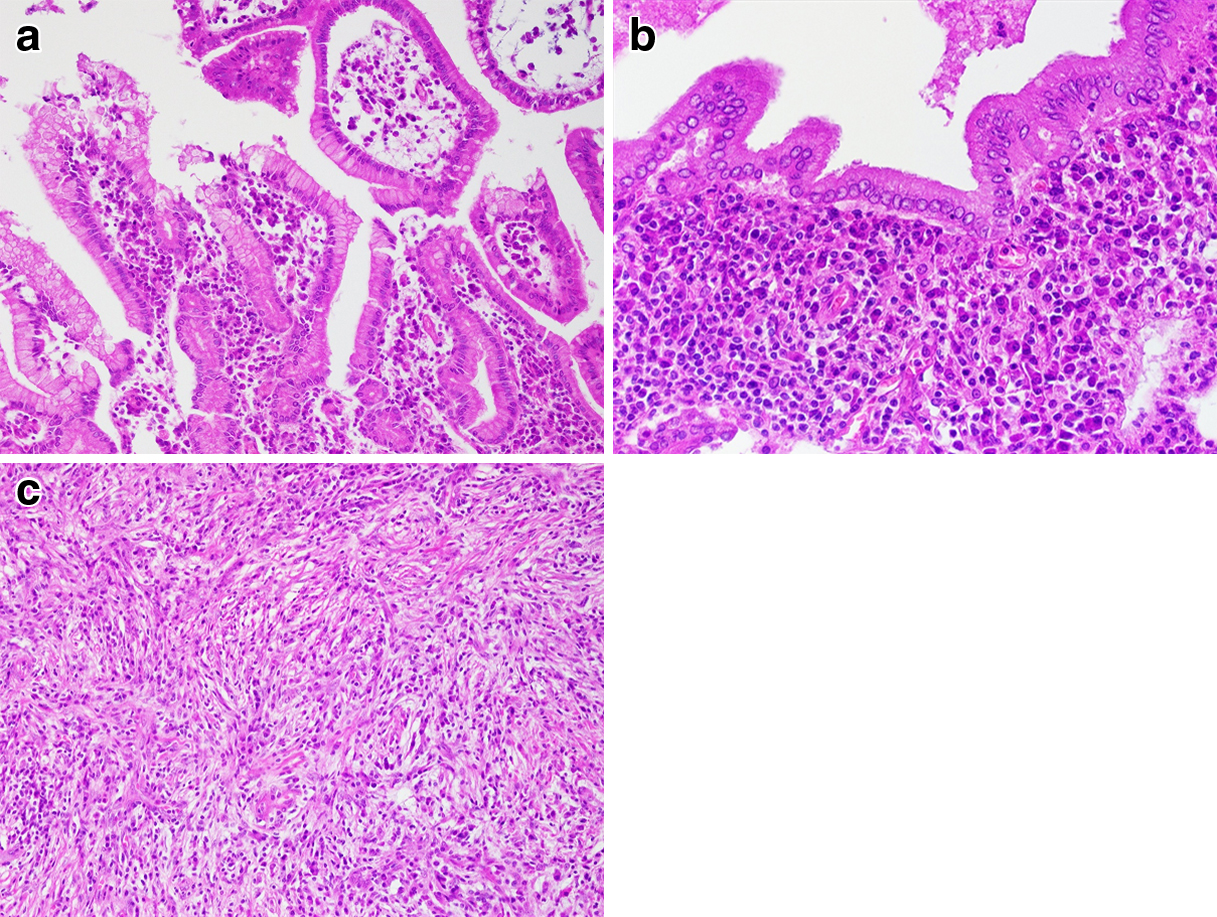
Histopathological features revealed epithelium including abundant mucus and papillary proliferative cylindrical cells (a: HE stain ×100), infiltration of many lymphocytes and plasmacytes under the epithelium (b: HE stain ×200), storiform fibrosis (c: HE stain ×100).

Histopathological features revealed increased IgG4+ plasma cells in the involved tissues, approximately over 100 per high-power field (a: immunostain ×200), obliterative phlebitis (b: HE stain ×100, c: EVG stain ×100).
以上から,低異型度の分枝型IPMNに1型AIPを合併したことにより,画像上,囊胞内に造影される壁在結節状の像を呈したと考えられた.
本症例はIPMNの経過観察中,囊胞内に10 mm大の壁在結節が出現し,high-risk stigmataを伴うIPMNと術前に診断した.膵切除術を施行し,切除標本の病理所見では画像で認められた結節の部位に一致してIgG4陽性形質細胞を中心とした炎症細胞の集簇が認められた.自己免疫性膵炎臨床診断基準20182)による病理組織学的確診基準を満たしており,最終的に1型AIPを合併した低異型度の分枝型IPMNの診断に至った.
IPMNの診療において,2017年国際診療ガイドライン3),2015年American Gastroenterological Association(AGA)ガイドライン4),2018年ヨーロッパ膵囊胞性腫瘍研究グループより専門家コンセンサスステートメント5)が発表されている.2017年国際診療ガイドライン3)では,10 mm以上の主膵管拡張,造影される5 mm以上の壁在結節,膵頭部病変例での黄疸といったhigh-risk stigmataを認める場合,全身状態が許せば切除の絶対適応となる.本症例における,10 mmの造影効果を伴う囊胞内の壁在充実性腫瘤を呈した所見はいずれのガイドラインにおいてもリスク因子とされており,悪性を疑い手術適応と判断した.精査の結果,high-risk stigmataを認めるものの明らかな浸潤癌の合併はないことから,腹腔鏡下での手術を選択した.
AIPに特徴的な画像所見として,びまん性腫大や膵周囲を取り巻く被膜様構造であるcapsule-like rim,腫瘤内に主膵管が貫通するduct penetrating signが挙げられるが,AIPの17%で限局性腫大を呈し6),膵癌との鑑別が困難な症例が存在する.本症例では病理組織学的にも限局性の病変を認め,これが画像上限局性の結節として描出されたと考えられた.医学中央雑誌において,「膵管内乳頭粘液性腫瘍」という単語が膵癌取扱い規約第4版で使用されるようになった1993年から2019年1月までの期間で「1型自己免疫性膵炎」,「膵管内乳頭粘液性腫瘍」を,PubMedにおいて,「intraductal papillary mucinous neoplasm」とWHOが定義した1996年から2019年1月までの期間で「intraductal papillary mucinous neoplasm」,「autoimmune pancreatitis」をキーワードとして検索したところ,近年,IPMNにAIPを合併した症例に対して膵切除術を施行した報告が散見され1)7)~13),超音波内視鏡下穿刺吸引法(endoscopic ultrasound-guided fine-needle aspiration;以下,EUS-FNAと略記)あるいはERP下の膵液細胞診で悪性所見が検出されなかった症例においても,最終的に悪性を否定することができずに膵切除を施行していた(Table 1).本症例においても,術前に血清IgG4の上昇を認めたが(135 mg/dl以上),CTで壁在結節状の所見を認めたことからIPMNの悪性化を否定することができなかった.低異型度のIPMNがAIPの合併により,囊胞内部に造影される結節像を呈したと考えられるが,このようにIPMN近傍にAIPの限局性腫瘤を合併した場合,臨床的にhigh-risk stigmataを伴うIPMNとの鑑別は極めて困難である.本症例では,他院CTで囊胞内に結節が出現していないことが確認された1年4か月後に壁在充実性成分が出現し,分枝型IPMNの悪性化としては経時的な変化が急速であった.また,IPMNの囊胞径拡大がworrisome featuresの一つであるが,本症例やUrataら11)の報告では結節の出現とともに囊胞の縮小を認めていた.さらに,CTでは囊胞壁の一部に造影される結節状の所見を認めたが,MRI拡散強調像では囊胞辺縁全体を取り囲むように高信号域を認めた.以上の点から,IPMN経過観察中の壁在結節の急速な出現や囊胞の縮小,MRI拡散強調像での囊胞全体を取り囲む高信号域などの所見を認めた際にはAIPを合併したIPMNを念頭に置き,IgG4測定といった血清学的診断や組織学的診断を検討する必要があると考えられた.
| No. | Author | Year | Age | Sex | Main complaint | Part | IPMN sub-type | IgG4 (Pre) | IgG4 (Post) | EUS-FNA | Pancreatic juice cytology | Procedure |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | Maeda1) | 2012 | 77 | M | none | body | NA | NA | NA | NA | negative | DP |
| 2 | Nakaji7) | 2013 | 76 | M | none | head | NA | NA | 1,260 mg/dl | NA | NA | PD |
| 3 | Naitoh8) | 2013 | 64 | M | abdominal pain | head | gastric type | normal | NA | negative | NA | PD |
| 4 | Bateman9) | 2013 | 75 | M | abdominal pain | head | intestinal type | NA | NA | NA | NA | PD |
| 5 | Bateman9) | 2013 | 74 | M | abdominal pain | head | gastric type | NA | NA | NA | NA | TP |
| 6 | Tabata10) | 2013 | 79 | M | none | body | gastric type | 627 mg/dl | 386 mg/dl | NA | negative | DP |
| 7 | Urata11) | 2013 | 70 | M | none | body | NA | NA | NA | NA | negative | PD |
| 8 | Vaquero12) | 2014 | 74 | F | abdominal pain | body and tail | pancreatobiliary type | 256 mg/dl | normal | negative | NA | DP |
| 9 | Vaquero12) | 2014 | 79 | M | abdominal pain | head | intestinal type | NA | NA | negative | NA | TP |
| 10 | Kibe13) | 2017 | 65 | M | abdominal distension | body | NA | NA | normal | NA | negative | Lap-DP |
| 11 | Our case | 75 | M | abdominal pain | head | gastric type | 226 mg/dl | NA | NA | negative | Lap-PD |
DP: distal pancreatectomy, PD: pancreatoduodenectomy, TP: total pancreatectomy, Lap: laparoscopic, Pre: preoperation, Post: postoperation
1型AIPの正確な発症機序はもとより,AIPとIPMNが合併する機序もまた現在まで明らかにされていない.IPMNにAIPを合併した11例中,本症例を含めた8例(72%)がIPMNに一致して限局性腫瘤を認めていた.また,AIPと診断されていない高異型度のIPMNにCD4やCD8陽性T細胞が集簇しているという報告もある14).このことから,IPMNにおける遺伝子変異により発現した変異蛋白が抗原となり,免疫反応がじゃっ起された結果,病変部に限局したAIPの状態をひき起こしているという可能性が考えられた.
AIPに対するステロイド奏効率は90%以上であり15),術前に診断ができれば侵襲的な手術の回避が可能である.自己免疫性膵炎診療ガイドライン201316)では「限局性腫大や腫瘤形成の場合には,ERPによる膵液細胞診や擦過細胞診,あるいはEUS-FNAにより悪性疾患の除外後にステロイドトライアルをすべきである」と推奨された.近年,AIPと膵癌の鑑別におけるEUS-FNAの有用性について検討されているが,AIPの診断に必要な検体量の採取が困難であるという理由でAIPの確定診断には限界があるといわれている17).分枝型IPMNの経過観察中に膵体部癌が疑われ,EUS-FNAで限局性1型AIPと診断し,膵切除術を行わずにステロイドで治療しえた報告もあるが18),本症例では囊胞内容の漏出による腹膜播種の可能性を懸念し,EUS-FNAを施行しなかった.ERPによる膵液細胞診で悪性所見を認めなかったため,術前にIPMNに合併するAIPを鑑別に挙げることができていれば,ステロイドトライアルも選択肢として考えられた.Mizunoら19)はステロイド治療の前後でPETによる評価を行うことで,7日以内にAIPと膵癌との鑑別が可能であると述べており,短期間のステロイド投与であれば病状の進行に対する懸念は少ないと思われた.
術前にhigh-risk stigmataを伴うIPMNと診断し,最終的に1型AIPを合併した低異型度の分枝型IPMNであった1例を経験した.非常にまれな病態であるが,IPMN経過観察中の急速な腫瘤の出現やそれに伴う囊胞の縮小,MRIの拡散強調像で囊胞辺縁全体を取り囲む高信号域などの所見を認める場合は,この病態も念頭に置き,血清学的診断,組織学的診断やステロイドトライアルを考慮するべきである.
利益相反:なし