2017 年 33 巻 2 号 p. 122-132
2017 年 33 巻 2 号 p. 122-132
近年のMRI装置の技術的向上により,高速撮像,3D撮像,拡散強調画像など様々なシーケンスが開発されている.小児の診療の現場においてなくてはならない画像診断検査のひとつとなり,MRIの適応は拡大している.拡散強調画像は,頭部疾患だけでなく,全身に用いられるようになり,ルーチンの撮像に組み込まれている.また,肝臓特異性のMRI造影剤が導入されて以降,小児肝臓疾患に対しても適応され,腫瘍性疾患だけでなく,胆道系疾患にも応用されている.MRIは解剖学的構造や疾患の病変の広がりを知るだけでなく,病変の質的診断,活動性,機能評価など様々な情報を得ることができる.しかしながら,MRIは,他の画像診断検査に比して検査時間が依然長く,乳幼児に対しては鎮静を必要とする.そのため,多様化された撮像内容を理解し,限られた時間のなかで,目的に応じた効率よいプロトコールの組み立てが必要である.本稿では,小児腹部疾患に対する拡散強調画像,EOB(gadolinium ethoxybenzyl diethylenetriamine pentaacetic acid; Gd-EOB-DTPA)造影剤の臨床応用について文献的考察を含めて報告する.
拡散強調画像(diffusion-weighted images; DWI)は,生体内の水分子の拡散運動を画像化したものである.正常組織は,自由な水分子の拡散があり,DWIでは信号の変化を示さないが,細胞浮腫や細胞密度が高い状態になると,この拡散運動が制限され,DWIで高信号を呈する.ただし,DWIは,T2強調画像の影響も受けるため,その解釈には注意を要する1).そのため,ADC mapというみかけの拡散係数を画像化したものを考慮して判断する必要がある.DWIで高信号を示すのは,ADC mapで低信号(拡散制限)と高信号を示すT2 shine-throughである2,3).
DWIは,脳虚血性疾患に対する臨床応用から始まり,急速に普及した.現在では,脳虚血性疾患にとどまらず,炎症性疾患,腫瘍性疾患,臓器の機能評価などに用いられる.DWIは,高い細胞密度,細胞性浮腫,粘稠な液体で,高信号を示すという特徴がある.そのため,正常な腹部実質臓器のなかにも,DWIで高信号を呈するものが存在する.Table 1に,代表的な臓器のDWIの信号変化について示す2,4).DWIで高信号を示す腹部臓器としては,脾臓,胆嚢,腎臓,卵巣,精巣,子宮内膜などがある(Fig. 1).その他,リンパ節も高信号を示す.このような特徴を応用して停留精巣の診断に用いることもある.正常な精巣組織は,細胞密度が高くDWIで高信号を示すため,停留精巣の位置を把握しやすく診断の一助となる(Fig. 2).炎症性疾患としては,膿瘍の評価に有用である(Fig. 3).膿瘍は,粘稠な内容物を反映しDWIで高信号となるため,必ずしも造影MRIを用いなくても臨床症状と合わせて判断することができる.また,急性腎盂腎炎や急性巣状細菌性腎炎の診断として,DWIを用いる場合があり,腎静態シンチの診断と有意差はないと言われている5).
| 臓器 | DWI | ADC map |
|---|---|---|
| 胸腺,脾臓,リンパ節 | 高信号 | 低信号 |
| 肝臓,膵臓 | 中等度信号 | 中等度信号 |
| 胆嚢,腎臓 | 高信号 | 高信号 |
| 卵巣,精巣 | 高信号 | 低信号 |
| 子宮内膜 | 高信号 | 高信号 |
| 骨格筋 | 中等度信号 | 軽度高信号 |
| 骨髄(赤色髄) | 高信号 | 中等度から低信号 |
| 骨髄(脂肪髄) | 低信号 | 低信号 |
| 骨幹端部,骨端部 | 高信号 | 高信号 |
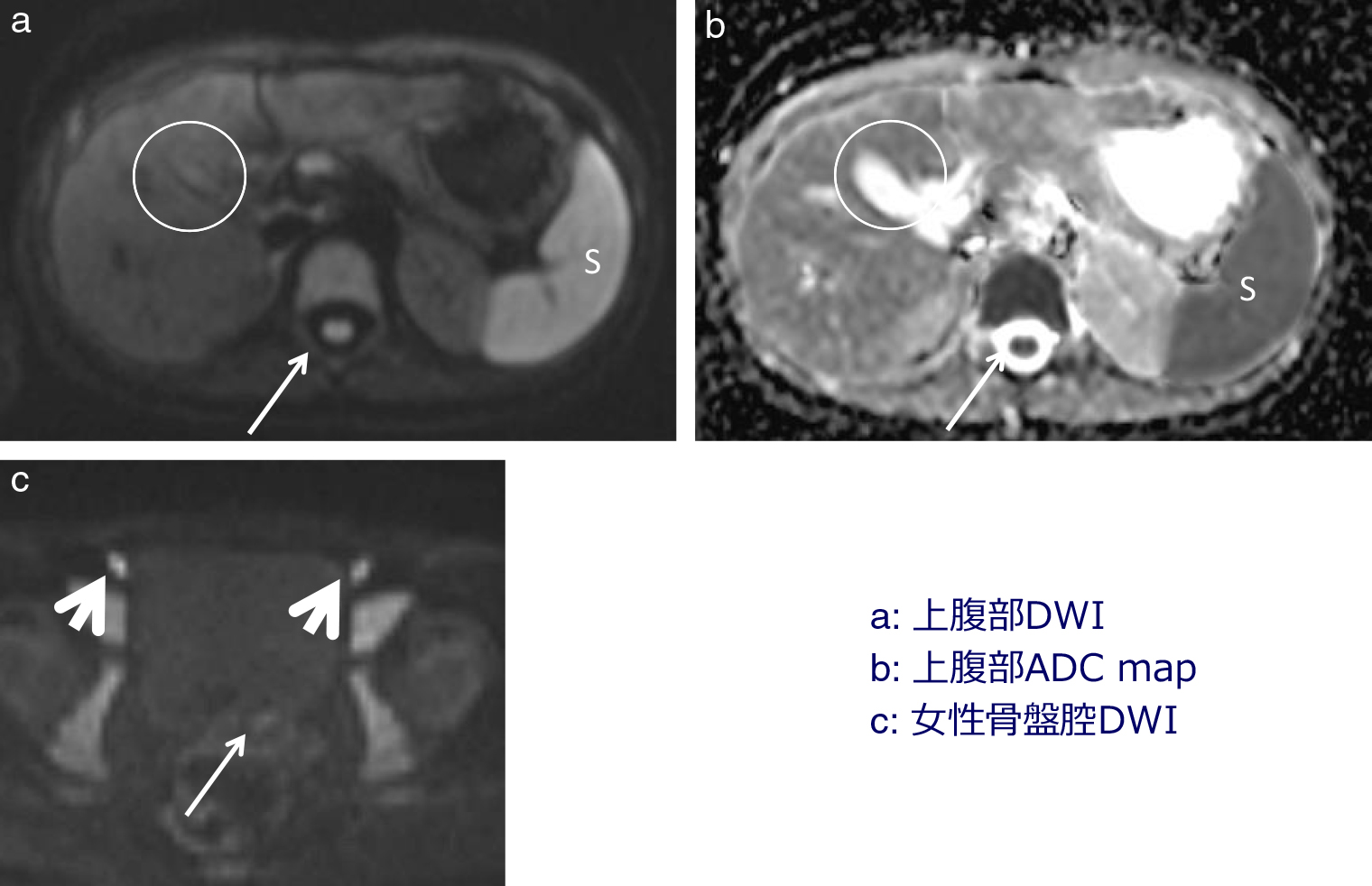
DWIでみる正常臓器の信号強度
DWI(a)で,脾臓(S),脊髄(矢印)は均一な高信号を示し,ADC map(b)で低信号となっている.胆嚢(丸枠)は,DWI(a)で淡い高信号,ADC map(b)で高信号を示す.骨盤腔レベルのDWI(c)で,子宮内膜(矢印)が淡い高信号,鼠径部のリンパ節も高信号である(矢頭).

停留精巣
左非触知精巣精査のため,超音波を実施したところ,膀胱の左側に停留精巣(矢印)を認めた(a).T2強調画像(b)では,超音波所見と同様に,膀胱の左側に停留精巣を認めることができるが,DWIでは周囲組織が抑制されているため,より一層高信号として描出される(c).正常な精巣の場合は,DWIで均一な高信号を示し,評価が容易である.

重複子宮,右膣閉鎖の女児
下腹部痛と炎症所見があり,骨盤腔MRIを施行したところ,拡張した右膣内に液体貯留(星印)を認めた(a).造影MRI(b)では,膣壁の肥厚と造影効果を認め,炎症性変化が疑われた.拡散強調画像(c)で内部は高信号(矢印),ADC map(d)で低信号を示し,膿瘍の合併が考えられた.その後,外科的にドレナージが施行された.
先述したように,DWIには,細胞密度が高いもの,細胞性浮腫,粘稠な液体貯留などで高信号を示すといった特徴がある.ADC mapを併用することによって,腹部腫瘍性疾患に対する腫瘍の組織学的診断,病変の検出,治療効果判定に用いられる4).一般的に,悪性固形腫瘍は,高い細胞密度を有するため,DWIで高信号を呈する傾向がある.一方,良性固形腫瘍は,細胞密度が低く,腫瘍の大きさに対する細胞膜の数も少ないため,拡散制限をきたしにくい傾向があるとされる(Fig. 4).ただし,悪性固形腫瘍のなかでも,嚢胞や壊死性変化を伴う場合は,必ずしも拡散制限をきたさない6)(Fig. 5, 6).小児腹部固形腫瘍の良悪性の判定としてADC valueのROCカットオフ値をGawandeらは1.29 × 10−3 mm2/s,Kocaogluらは,1.11 × 10−3 mm2/sを提示している6,7).小児悪性固形腫瘍として比較的頻度の高い肝芽腫,腎芽腫,神経芽腫,ユーイング肉腫などでADC valuesが低く,また,壊死性成分の混在する不均一な腫瘍より均一な腫瘍でADC valuesが低下する傾向があるとされている6).しかし,良性固形腫瘍のなかでも,ADC valuesが低値を示す場合もあり,腫瘍のもつ様々な生物学的要素により悪性腫瘍とのオーバーラップがある4,6,7).また,ADC valuesのROIの取り方やMRI装置,b valuesによっても変化するため,DWI,ADC valuesのみで判断するのではなく,他の画像や臨床所見なども合わせて診断することが大事である.

悪性と良性の鑑別診断
神経鞘腫:右胸壁に位置する境界明瞭な腫瘤あり,DWIで高信号(a),ADC mapで高信号を示している(b).ADC valuesは,1.7 × 10−3 mm2/sであった.
神経芽腫:左副腎部の腫瘤である.DWIで高信号(c),ADC mapでは低信号を示している(d).ADC valuesは,0.88 × 10−3 mm2であり,低値を示していた.

悪性腫瘍
悪性リンパ腫:膵頭部に位置する楕円形の腫瘤を認め,DWIで高信号(a),ADC mapで低信号を示している(b).ADC valuesは,0.58 × 10−3 mm2/sと低値を示している.
肝芽種:肝右葉に,DWIで境界不明瞭な不均一な低信号病変を認める(c).ADC mapでは肝実質と等信号であり(d),ADC valuesも,1.55 × 10−3 mm/sと必ずしも低値は示していない.

横紋筋肉腫
下腹部に大きな腫瘤あり,T2強調画像では不均一な信号を示している.腫瘍の右下部分は,DWIで高信号を示し(b),ADC valuesも低く,0.58 × 10−3 mm2/s(c)である.一方,腫瘍の左側の部分は,DWIで不均一な中等度の高信号,ADC mapも比較的高信号を示し,ADC valuesは1.89 × 10−3 mm2/sと比較的高値であった.一つの腫瘍のなかに性状の異なる成分が混在していることがわかる.
病変の検出としては,T2強調画像,DWIで高信号を示す病変には比較的容易に認識することが可能である.特に,DWIでは,他の臓器の信号が抑制され,病変が強調されるため,検出しやすい6)(Fig. 7).そのような特徴から,転移性病変の検出やstagingの決定として,whole-body DWIが,PET-CT(positron emission tomography-CT)に置き換わる検査として注目され,診断能は,ほぼ同等とされている.現在のところ,悪性リンパ腫に対する有用性の報告が中心であるが8)(Fig. 8),小児領域においても応用が広がっている.Whole-body DWIの欠点としては,PET-CTに比して,肺転移に対する診断能,リンパ節に対する良悪性の判断の難しさなどが挙がる8,9).しかし,小児にとって,放射線被ばくがない点は,大きな利点である.放射線による発癌感受性の亢進が知られているLi-fraumeni症候群などの遺伝性腫瘍症候群に対する早期発見のためのスクリーニング検査として期待され,AACR(American Association for Cancer Research; AAC)からはWhole-body DWIが推奨されている.
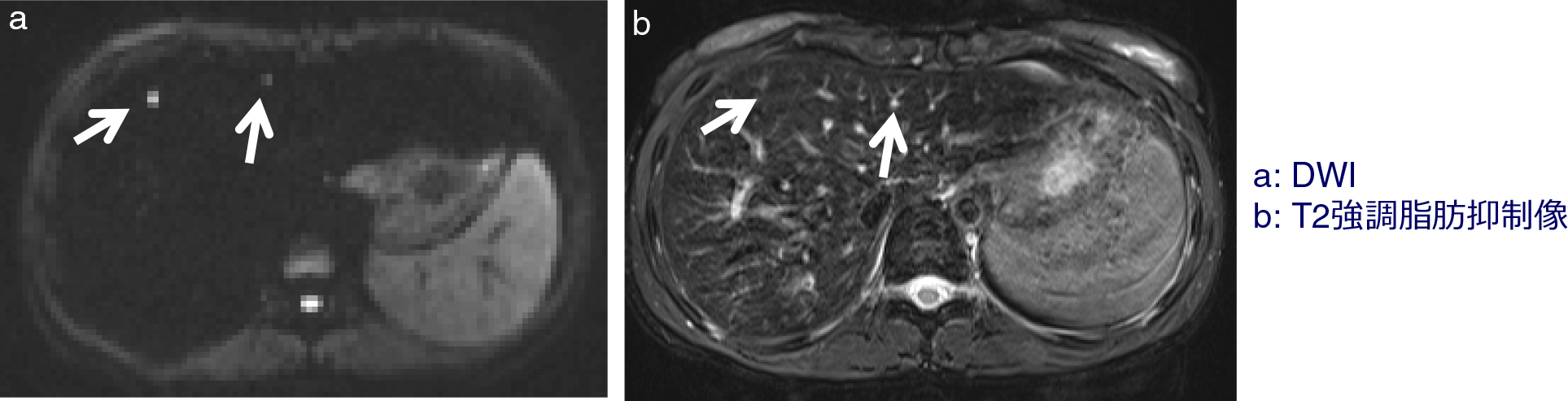
病変の検出
肝転移の病変は,DWIで点状の高信号として描出されている(矢印).同レベルのT2強調画像では,上下をスクロールしながら注意深く見ないと病変が認識しづらい(矢印).

Whole-body DWIによるstaging 決定
悪性リンパ腫の患児のwhole-body DWIである(a).横隔膜レベルの椎体脇(b)と左腸骨(c)に高信号病変があり,転移性病変を認める.横断像での再構成の画像作成により,より詳細に評価できる.
悪性腫瘍に対して化学療法,放射線治療が行われると,腫瘍細胞や細胞膜の破壊や損傷により水分子の動きが増え,DWIの信号が変化し,ADC mapで高信号化するようになると言われている.ADC valuesは,治療効果判定や残存腫瘍の評価として用いることができる(Fig. 9).小児腹部悪性疾患に対しての報告は,まだまだ少ないが,肝芽腫や腎芽腫の治療経過でADC valuesが高くなることが報告されている8,11).

治療効果判定
Fig. 8と同様の症例である.Whole-body DWIによる初診時(a)と1か月後(b)であるが,横隔膜レベル左側,左腸骨に認めていた異常信号は縮小している.PETの所見と遜色のない結果である(c).
近年,肝特異性造影剤であるEOBやDWIを用いることにより,肝臓に対する画像診断は,病変の検出,質的診断の向上だけでなく,肝線維化など機能評価に応用されている12).EOBは,通常のガドリニウム造影剤である細胞外液造影剤と同様の血行動態を反映したのちに肝細胞に取り込まれる.EOB造影剤の造影効果のパターンとT1,T2強調画像の所見の組み合わせによって肝腫瘍の質的診断が行われる(Fig. 10)12).特に転移性肝腫瘍の検出率は,EOB造影後20分の肝細胞相が造影CTよりすぐれ,クッパー細胞に取り込まれるSPIO造影剤による診断能に匹敵すると言われている(Fig. 11)12).成人例の転移性肝腫瘍に対するDWIとEOBの検出率の比較検討によると,DWIとEOB肝細胞相の結果に有意差は見られず,EOBにDWIを加えることで,特異度と陰性的中率が向上するとされている13,14).そのほか,EOBは,投与量の50%が胆道系に排泄されるという特性がある12).胆道系疾患への応用も報告されている12,15).ただし,EOBの胆道系への排泄は,肝機能に依存する.Tschichらは,肝硬変を伴う成人例に対するEOBの胆道系への排泄をChild-Pugh分類と比較検討している16).正常肝機能であるコントロール群は,造影剤注入後5~16分で総胆管への排泄があるのに対して,肝硬変例では造影剤排泄は投与後30分以降と遅延し,180分後まで排泄が見られなかった症例もあった報告している(Fig. 12).総ビリルビン値が3 mg/dL以上,Child-Pugh分類2または3で遅延する傾向があるとされる16,17).一方,肝線維症,肝硬変などの肝疾患に対するDWIを用いた報告も,散見されるようになっている4).小児例では,胆道閉鎖症の重症度や先天性心疾患に対するFontan術後の肝線維化の評価として,ADC valuesを用いた報告がある18,19).Pengらの32例の胆道閉鎖例に対するb value = 500 s/mm2で測定したADC valuesは,コントロール群に比して明らかに低値を示している(Fig. 13, 14)19).また,Fontan術後の患児において,進行する肝線維症の合併が注目されており,やはり正常児(1.1 × 10−3 mm2/s)に比してADC valuesは,0.82 × 10−3 ± 0.11 × 10−3 mm2/sと低値を示すことがわかっている15).今後,肝機能障害を評価するひとつの指標として,EOB,DWIの更なる検討が必要と考えられる15,16).

限局性結節性過形成
門脈大循環短絡のある男児,肝内に腫瘍性病変が疑われ,MRIを実施した.T2強調画像(a)で,肝左葉に類円形の淡い高信号を示す腫瘤を認める(矢印).DWIでは高信号(b),ADC mapでは肝実質と等信号(c)を示している.EOB造影剤投与後の肝細胞相(d)では,腫瘤に一致した造影効果があり,これらのパターンから限局性結節性過形成との診断となった.

肝転移
EOB造影後の細胞相(a)で,肝実質は,均一な造影効果を示している.比較的末梢に複数の結節を認め,転移性病変と考える(矢印).
肝内胆管,胆嚢に造影剤が排泄されている.
DWI(b)では,EOB肝細胞相で確認できた転移性病変が高信号となっている.病変の検出だけでなく,活動性についても評価可能である.

胆道系に対するEOB
十二指腸内の異物(矢印)による胆道閉塞に伴う総胆管の拡張を認める(a).EOB投与後20分をすぎても,胆道系に造影剤の排泄を認めない(b).尿路に造影剤が排泄されている(c).血液検査で,総ビリルビン値が,3 mg/dLを超え,肝機能障害を認めていた.

うっ血肝
Fontan術後の肝障害にてMRIを実施.T2強調画像にて,肝辺縁は凹凸があり,内部は不均一である(a).EOB肝細胞相でも,実質の造影効果は不均一であり,胆道系への造影剤の排泄が乏しい(b).DWI(c)でも,肝実質の信号は不均一で,ADC values(d)を測定したところ,1.07 × 10−3 mm2/sを示していた.

胆道閉鎖
T2強調画像(a),DWI(c)にて,肝の辺縁は不整で,実質は不均一である.EOB細胞相で不均一な造影効果を示している(b).肝実質のADC valuesを測定したところ0.87 × 10−3 mm2/sと低値であった.
小児腹部疾患に対するDWIの適応,臨床応用,EOB造影剤による肝疾患の診断および肝機能評価について,文献的考察を含め報告した.DWI,EOB造影剤の導入により,MRIは器質的疾患の評価はもちろんのこと機能評価へと進化し,注目されている.放射線被ばくのない利点もあり,小児腹部疾患に対する適応はますます拡大し,得られる情報も多くなっていくと思われる.