2019 年 35 巻 1 号 p. 27-31
2019 年 35 巻 1 号 p. 27-31
川崎病に罹患し冠動脈障害を合併した小児のフォローアップにおいてMagnetic Resonance Coronary Angiography(MRCA)は有用なツールである1).しかし長時間の安静臥床を要するために小児患者においては鎮静を施行される事が多い.MRCAの鎮静処置の問題点として過鎮静のリスクが高いことや磁性体を含むモニターが使用不可であること,基本的に外来検査であるために鎮静処置後の観察不足が起こり得ることなどが挙げられる.一方で,事前の検査説明を含めた準備(プリパレーション)を行うことにより,幼児へのMRI撮影において鎮静処置を軽減あるいは回避出来たという報告がある.今回我々は4~15歳の川崎病既往7例に事前の検査説明を含めたプリパレーションを行い無鎮静でMRCAを施行した.さらに同時期に撮影した心臓超音波所見との比較を行い両者の相関を検討した.幼児の無鎮静でのMRI施行例の報告は頭部領域では散見されるが,心臓領域,特に冠動脈撮影では非常に少なく重要な知見と考えられる.当院における無鎮静でのMRCAを用いた川崎病フォローアップの有用性を若干の文献的考察とともに報告する.
対象は2010年4月から2016年10月までに板橋区医師会病院においてMRCAを施行した15歳以下の全ての小児7例(男児6例,女児1例)を後方視的に検討した.MRCA撮影1か月前より患児への医師主導のプリパレーションを施行し,薬剤による鎮静を行わずに撮影を行った.プリパレーションの具体的な方法として,MRCA撮影の約1か月前に医師と患児だけでMRI装置を見学し,実際の機器に触れてもらい,機械音が大きいが全く問題がないことやMRI装置内に入っても操作室からモニターで見ているので心配がないこと,痛みや不安を感じる検査ではないことを確認させた.また保護者の協力を得て,自宅でも保護者の声掛けによるプリパレーションを毎日継続した.
使用したMR装置はPhilips社製Achieva 1.5T Single Gradient,使用コイルは12歳以下の小児には2チャンネルコイルのFlex-medjum coil,それ以上の年齢では2チャンネルコイルのSENSE cardiac coilを用いた.撮影は心電図同期法,呼吸同期法を併用し,使用シーケンスはb-TFE(balanced-turbo field echo)法で,得られたデータに3次元再構成を行い,maximum intensity projection(MIP),curved multi-planner reformation(MPR)で画像を作製し冠動脈の形態評価および径の計測を行った.またMRCAから1か月以内に施行された心臓超音波所見について各枝ごとに冠動脈径を測定し,MRCA所見と比較検討した.2群間の比較にはWilcoxonの順位和検定,相関についてはSpearmanの順位相関係数を用い,p < 0.05を有意水準とした.統計処理はJMP®,Version 13(SAS Institute inc., Cary, NC)を用いて行った.なお,画像の評価については放射線技師と小児科医師の2名でOpen label studyとして行なった.
対象の7例の詳細をTable 1に示す.MRCA撮影時の年齢は8.3 ± 4.1(4.8–15.9)歳であり,男児6名,女児1名に対し合計12回施行された.川崎病発症からMRCA実施までの平均経過年数は2.7 ± 2.8年であった.各症例の急性期所見は正常2例,冠動脈拡張4例,冠動脈瘤1例であり,発症から1年以降の慢性期所見では全症例において正常化していた.MRCAおよび超音波所見のいずれにおいてもプラークおよび石灰化,狭窄部は確認出来なかった.MRI室の滞在時間は約30分程度であり,全例が鎮静処置を行わずに中断なく撮影を施行出来た.
| Case number | Age (years) | Sex | The number of times | The duration from the onset (years) | Sedation | The Location of CAL | The findings of CAL | Plaque | Calcification | Stenosis | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Acute phase | Chronic phase* | MRCA | UCG | MRCA | UCG | MRCA | UCG | ||||||||||
| 1 | 5.8 | M | 1 | 3.4 | none | LMT | Dilatation | Normal | — | — | — | — | — | — | |||
| 2 | 6.7 | F | 2 | 2.1 | none | LMT | Dilatation | Normal | — | — | — | — | — | — | |||
| 3 | 5.1 | M | 4 | 0.3 | none | RCA | Aneurysm | Normal | — | — | — | — | — | — | |||
| 4 | 6.8 | M | 2 | 4.3 | none | LAD | Dilatation | Normal | — | — | — | — | — | — | |||
| 5 | 13.3 | M | 1 | 8.3 | none | LMT | Dilatation | Normal | — | — | — | — | — | — | |||
| 6 | 4.8 | M | 1 | 0.6 | none | none | Normal | Normal | — | — | — | — | — | — | |||
| 7 | 15.9 | M | 1 | 0.1 | none | none | Normal | Normal | — | — | — | — | — | — | |||
CAL: coronary artery lesion, LMT: left main trunk, LAD: left anterior descending artery, RCA: right coronary artery, UCG: ultrasound cardiography.
* Chronic phase means the period that had passed over one year since the onset.
MRCAと心臓超音波にて測定した各冠動脈枝の平均径と有意差,相関についてTable 2に示した.MRCAと同時期の心臓超音波所見が得られたのは左冠動脈主幹部8例,左前下行枝7例,右冠動脈枝9例であった.各枝共にMRCAでの測定値が心臓超音波よりも平均値が高く有意差を認めた.またMRCAと心臓超音波所見の冠動脈径の相関に関しては,各枝共に強い正相関を認めた.
| n | MRCA (mean ± SD mm) | UCG (mean ± SD mm) | p value | R | |
|---|---|---|---|---|---|
| LMT | 8 | 3.1 ± 0.7 | 2.6 ± 0.4 | <0.05 | 0.71 |
| LAD | 7 | 2.6 ± 0.5 | 2.2 ± 0.2 | <0.05 | 0.66 |
| RCA | 9 | 3.5 ± 0.9 | 3.0 ± 0.9 | <0.05 | 0.74 |
| Total | 24 | 3.1 ± 0.8 | 2.6 ± 0.7 | <0.05 | 0.76 |
SD: standerd deviation, p value: probability value, R: correlation coefficient.
6歳1か月,男児.4歳9か月時に川崎病に罹患した(Table 1の症例3に該当).
第6病日より免疫グロブリン超大量療法2 g/kg・アスピリン内服を施行し第8病日に解熱した.第12病日に施行した心臓超音波検査において,右冠動脈中間部と思われる部位に最大径5.1 mmの瘤状の構造を認めた.冠動脈瘤と考えられたが,右冠動脈起始部から瘤のある部位への連続的な観察は出来なかった.同様の所見が残存するために川崎病発症4か月後にMRCAを施行した.MRCAでは右冠動脈中間部に最大径4.8 mm大の冠動脈瘤を明らかに確認出来た(Fig. 1).
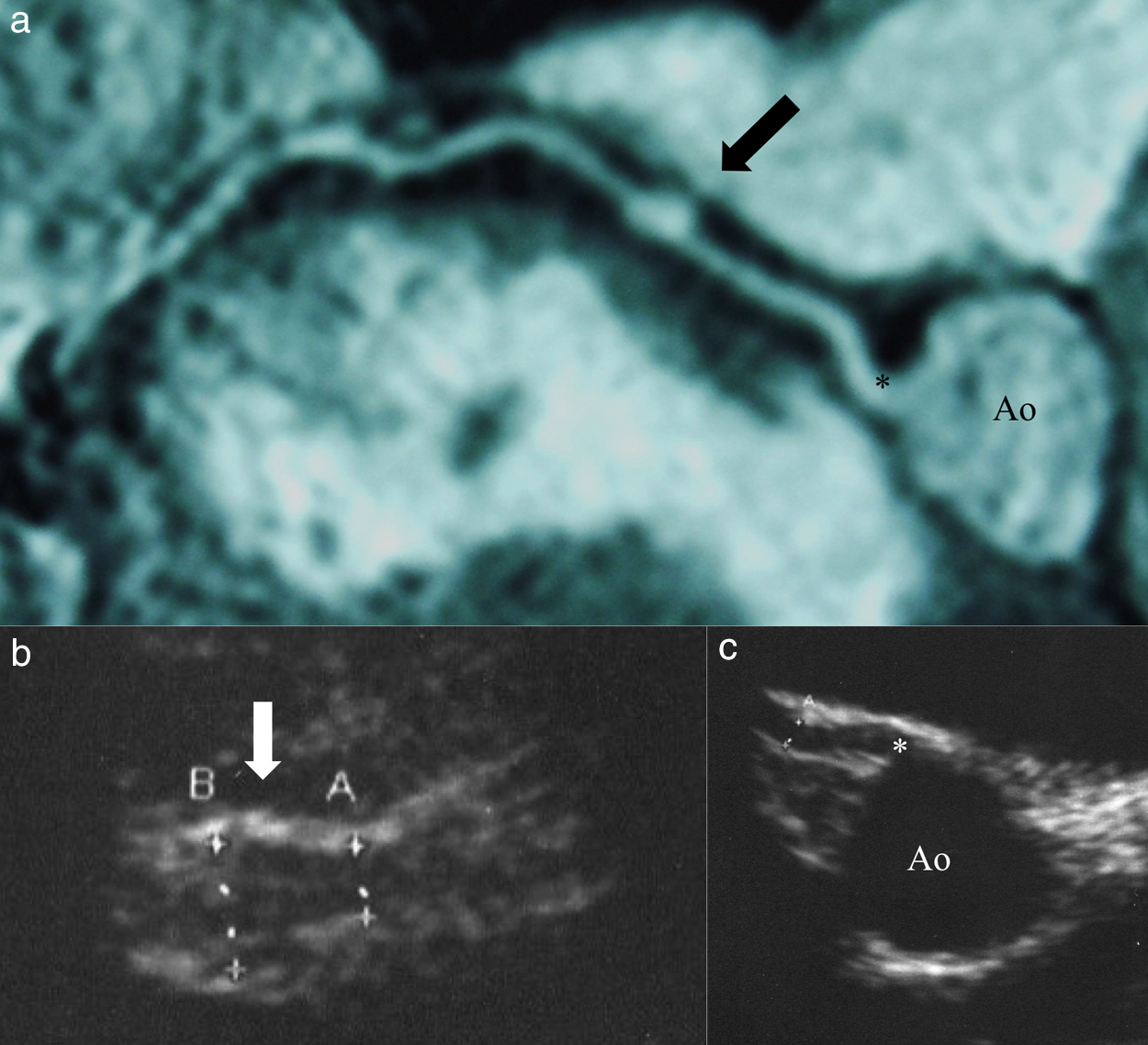
The findings of coronary artery in acute phase
Right coronary arterial aneurysm (arrow) was confirmed in curved multi-planner reformation image of MRCA at 4 months after the onset (a). Echocardiography also revealed aneurysm at the middle lesion (b) of right coronary artery. Proximal lesion (c) was normal. Ao: ascending aorta. * Right coronary artery.
以降,外来経過観察を続け1年後にMRIによる冠動脈撮影を再度施行した.MRI画像上では冠動脈瘤は退縮し,ほぼ正常な冠動脈が観察された(Fig. 2).

The progress of coronary arterial aneurysm
The regression of right coronary arterial aneurysm (arrow) was confirmed in the 3-dimentional reconstruction image of MRCA at 4 months (a) and 16 months (b) after the onset. Ao: ascending aorta. * Right coronary artery.
本邦における川崎病の新規発症例は毎年約1万5千人程度報告されており2)急性期の心障害は9.3%,発症後1か月以上残存する後遺症例は2.8%存在するとされている.川崎病に罹患する児の約85%は5歳未満である事から,冠動脈障害を残した患児は冠動脈病変の変化や心機能について幼児期からの長期間の経過観察が必要となる.経過観察における重要な課題は,フォローアップの質を担保しながらいかに冠動脈CTや冠動脈造影などの放射線被ばくや侵襲をともなう検査を軽減・回避するかである.
近年,川崎病罹患後の小児のフォローアップにおいて,MRCAによる冠動脈評価の役割は大きくなりつつある.MRCAの利点としてまず挙げられるのが,放射線被ばくがなく造影剤投与を必要としない点である.また幼児は基礎心拍数が高く息止めが困難である事が多いが,MRCAでは心電図同期法と呼吸同期法を併用することで撮影が可能である.また心臓超音波による観察領域を補完する意義も大きい.心臓超音波では術者の技量や鎮静の有無,患児の年齢や体格の要因において,しばしば冠動脈の描出が不良となる3).一方でMRCAは任意断面で画像を構築する事が可能であり,冠動脈を末梢まで全体的に観察する事が出来る.川崎病急性期と遠隔期の心臓超音波で冠動脈障害がないとされた症例のうちの5%,急性期に冠動脈拡張を認め遠隔期で退縮と判断されたうちの33%においてMRCAにて冠動脈瘤を認めたとの報告もある4).
しかし,小児におけるMRCAの問題点は長時間の安静臥床を要する点である.撮影条件にもよるが約30分程度の安静臥床が必要となることが一般的である.このため施設によっては,幼児の症例に対しては鎮静処置を行って撮影を行う場合もある.MRI特有の鎮静処置のリスクとして①長時間の不動化が必要であり過鎮静が起こりやすいこと,②通常使用しているモニターやシリンジポンプなどの磁性体が使用不可であること,③乳幼児はガントリ内に体全体が入ってしまい操作室からの観察が不良となることが挙げられる.実際に2010年の日本小児科学会医療安全委員会調査で,回答施設の35%(147施設)が鎮静の合併症を経験していることが明らかになった5).その中には呼吸停止や心停止などの重篤な合併症も含まれていた.この結果を受けて,2013年にはMRI中の鎮静処置を安全に行うために日本小児科学会・日本小児麻酔学会・日本小児放射線学会による共同提言も発行された6).MRCAが必要と判断された小児においては鎮静処置の適応を慎重に検討する必要があり,鎮静を行う場合には説明・同意に加えて適切なモニタリングと急変時の対応への準備が重要である.
今回の当院における検討では,プリパレーション後の無鎮静下MRCAが鎮静下MRCAと同程度の画質や感度・特異度をもつ検査になっているかについては検証出来ていない.しかし一般に鎮静が必要とされるMRCAにおいて 4歳から無鎮静で撮影が可能であったことを本研究で示すことが出来た.またMRCAを併用することによって心臓超音波において描出困難な冠動脈部位を補完して観察することが可能であった.超音波の観察可能範囲で異常所見が得られないが臨床経過が思わしくない症例,あるいは冠動脈異常の疑い症例に対して,無鎮静でのMRCAを選択することにより低侵襲的に診断感度を高めることが出来る可能性がある.なお,MRCAと心臓超音波検査の計測値が良好な相関を示した一方で,両者の計測値に有意差を認めたのは,計測位置の違いや時相の違い(拡張期か収縮期か),非造影下での撮影のためにMRCAにおいて冠動脈内腔の描出が不明瞭であったことによる影響が考えられる.
また本研究では,事前のプリパレーションにより無鎮静で中断なくMRCAを実施することが出来た.プリパレーションは鎮静処置の回避や不安・トラウマの軽減などに有効とされており,幼児へのMRI撮影において鎮静処置を軽減あるいは回避出来たという報告もある7,8).本研究では撮影機器の見学と説明がプリパレーションの主な内容であったが,アニメによる教育ビデオ9)や玩具で出来たシミュレーターなどによる疑似体験10)もプリパレーションとして有効であったと報告されている.また検査の環境として,遮音のためのヘッドホンの装着やアニメなどが見えるディスプレイの設置なども有用である11).欧米では痛み・不安を伴う検査の前に,医師の依頼をうけたHospital Play Specialist(HPS)あるいはChild Life Specialist(CLS)によりプリパレーションが施行されるが,日本ではHPSやCLSが配置された医療機関は少ない.本研究においてもプリパレーションは医師主導で実施されているが,日本の医療現場の実情を踏まえると,現段階では検査をオーダーする医師が率先して多職種と連携してプリパレーションを行っていくべきと考える.なお,本検討中には一般的には鎮静・事前のプリパレーションが不要と考えられる13歳と15歳も含まれている.しかし筆者らの経験では,成人例でさえ閉所の不安や撮像中の微細な体動の影響によると考えられる画質不良は少なくない.このため冠動脈をはじめとする体動の影響を受けやすい臓器の撮像では,成人であっても事前のプリパレーションが推奨される.
近年では機器の進歩もあり,32チャンネルコイルなどのマルチチャンネル化や,パラレルイメージング法などの撮像法の工夫によりMRCAの撮像時間の大幅な短縮が可能となってきており10),幼児の症例に施行しやすい状況となりつつある.医師主導のプリパレーションや環境整備を組み合わせることで鎮静処置を軽減したり無鎮静で施行できれば,MRCAは川崎病罹患後の小児におけるフォローアップにおいてさらに有用なツールとなることが期待できる.
MRCAと心臓超音波検査の計測値は良好な相関を認め,両者を組み合わせることにより冠動脈を詳細かつ客観的に評価することが可能であった.また医師主導のプリパレーションを行うことにより4歳の低年齢層から無鎮静でMRCAを施行出来た.適切なプリパレーションはMRCAにおける鎮静処置を軽減および回避させることに寄与する.