2018 年 60 巻 3 号 p. 139-146
2018 年 60 巻 3 号 p. 139-146
乳酸菌生成エキスは,整腸作用をはじめ,免疫賦活化作用などを有することが示唆されている。本研究の目的は,乳酸菌生成エキスの摂取による口腔内環境の変化を臨床パラメーターに加えて,唾液検査,細菌DNA検査により観察することである。被験者は,SPTに移行した成人男女20名とし,無作為に10名ずつ研究群とプラセボ群に分け,研究群に8週間,乳酸菌生成エキスを服用させた。なお,本研究は二重盲検法にて行った。測定項目は,臨床パラメーターとしてProbing pocket depth(PD),Bleeding on probing(BOP),Gingival Index(GI),Plaque index(PlI)を,唾液検査項目として免疫グロブリン(S-IgA),遊離ヘモグロビン(Hb),乳酸脱水素酵素(LD),細菌検査項目としてPorphyromonas gingivalis(P.g),Treponema denticola(T.d),Tannerella forsythia(T.f),唾液内総菌数を研究開始より0(飲用前),2,4,8週で計4回測定した。その結果,研究群において,4週後ではBOPおよびGIに,また4週から8週後にかけては,総細菌数の改善傾向が認められた。PDについても研究群において経時的改善率が高い傾向が認められた。S-IgA値に2群間の差は認められなかったが,乳酸菌生成エキスの服用が歯周炎の改善に影響を与えた可能性が示唆された。
抗生物質の汎用により,近年耐性菌・院内感染症の増加が顕著である。1929年にペニシリンが発見されてから,各種の抗生物質の開発が急速に行われてきたが,1961年にはメチシリン耐性黄色ブドウ球菌が既に出現した。結果として,巷では院内感染症の増加が顕著となり現在,抗生剤の汎用による薬剤耐性問題には注意が必要である。歯周治療においては,歯周炎の急性症状が認められる際の応急処置として,抗生剤の経口投与および,軟膏の歯周ポケットへの注入などが有効な治療法として行われている。しかしながら抗生剤は,有益菌も含めて殺菌するため,通常治療において汎用は避けたい。長期投与により,腸内細菌に影響を及ぼし,悪心・吐き気・下痢などの消化器系の異常を来すとの報告がある1)。
バイオジェニックスは,腸内の免疫を刺激したり,コレステロール・血糖・血圧を安定させたり,活性酸素を減少させるなど,体全体に作用することで生活習慣病や老化を防止する食品成分と定義される2)。その中で,乳酸菌の分泌物とその菌体物質は,腸内に存在する乳酸菌の菌体内酵素の活性化,増加を促進する。また,悪玉菌の増殖を抑制して,菌数を減少させる働きがある。乳酸菌の分泌物である乳酸菌生成エキスは,整腸作用をはじめ,免疫賦活化作用などを有し3,4),腸管免疫を活性化させ,自己免疫力,疾病への抵抗力を向上させることが期待できる。乳酸菌生成エキスの摂取により全身の免疫力を増強させ,結果として歯周病原細菌の抑制などの口腔内環境の改善または良好な状態の維持が抗生物質の使用を極力抑えて可能にすることができれば,歯周病や齲蝕を対象とした生体に優しいメインテナンス治療に繋がると考えられる。
一方で,歯周治療のメインテナンス,SPTにおいて,唾液中の生化学的検査,細菌検査を使用することは,臨床パラメーターの検査と同じく有用であるとの報告があり5,6),特に遊離ヘモグロビン(Hb),乳酸脱水素酵素(LD),細菌検査項目としてPorphyromonas gingivalis(P.g),Treponema denticola(T.d),Tannerella forsythia(T.f)は歯周病との関係が示されている。また,口腔粘膜における分泌型IgA(S-IgA)は,微生物,ウイルスの体内侵入を防ぐ第一の防御機構として作用する7)。従ってS-IgAは免疫能の指標になると考えられる。
本研究は,バイオジェニックスである乳酸菌生成エキスの飲用が歯周炎に及ぼす効果を調べるためのパイロット研究として,乳酸菌生成エキスの飲用による臨床パラメーター,ならびに唾液検査結果値の変化を解析するものである。
被験者は,日本医科大学千葉北総病院歯科通院中の患者で,軽度~中等度歯周炎患者で,歯周基本治療を終了しSPTに移行した成人男女20名とした(男性4名,女性16名,平均年齢70.4±9.2歳)。全身疾患のある患者,3か月以内に抗生物質を服用している患者は対象から除外した。また唾液サンプルを採取する研究のため,シェーグレン症候群などの自己免疫疾患により,唾液腺からの唾液分泌が抑制され,口腔内が乾燥している者,あるいは常用薬により唾液分泌が著明に抑制され,唾液採取が困難と考えられる者は,被験者から除外した。
2. 被験食品と研究デザイン被験食品は乳酸菌生成エキス,アルベックスⓇ(株式会社ビーアンドエス・コーポレーション)を用いた。大豆(豆乳)をベースに複数株乳酸菌による高密度発酵から得られる抽出エキスであり,腸内環境を改善・維持する食品成分である。形状は液体,原材料は乳酸菌生成エキス・クエン酸・乳酸・水,1包は10 mlであった。これに対しプラセボ食品は,成分内に乳酸菌生成エキスを含まないものとし,株式会社ビーアンドエス・コーポレーションにて作製されたものを用いた。なお,被験食品・プラセボ食品ともに,いずれかの区別がつかないよう株式会社ビーアンドエス・コーポレーションより提供されたものを用いた。
被験者には,1日2回,朝食前および夕食前に各1包を服用させた。飲用チェック表を被験者に渡し毎日記入させて,飲み忘れを防止した。また,上記のタイミングで飲み忘れた場合は,合計で1日2包飲用するよう指示した。被験者10名は,研究期間である8週間,毎日アルベックスⓇを飲用させてその効果を判定する研究群とし,プラセボ群10名との比較検討を行った。研究群・プラセボ群の割付は無作為割付として封筒法にて行い,本研究はランダム化プラセボ対照二重盲検平行群間比較試験とした。
3. 検査項目すべての測定項目は研究開始より0(飲用前),2,4,8週で計4回測定した。
1) 臨床パラメーター臨床パラメーターとしてProbing depth(PD),Bleeding on probing(BOP),Gingival Index(GI),Plaque Index(PlI)を測定した。対象歯はRamfjordの6歯,すなわち16,21,24,36,41,44歯とした。なお,修復物や欠損で測定不能の場合は,反対側の代替歯を測定歯とした。
2) 唾液パラメーター口腔内より,唾液を採取し以下の項目について測定した。なおこれらの測定は株式会社ビー・エム・エルに外注依頼した。
1) 唾液免疫グロブリン(S-IgA)静的唾液の採取より行いS-IgA測定用唾液サンプルを採取した。唾液採取用器具としてSaliva Collection Aid(SCA),Cryovial 2 ml(Salimetrics社)を使用し,口を容器につけて唾液を垂れ流すようにして約1 ml採取した。採取後すぐに凍結保管した。
2) 乳酸脱水素酵素(LD)・唾液中のヘモグロビン(Hb)・細菌数これら3項目の測定には刺激時唾液を採取して測定用検体とした。すなわち,被験者に5分間無味無臭のガムを咀嚼させて,LD用検体容器に3 ml刺激時唾液を採取した。採取した唾液から,スポイトを用いてHb検体0.1 ml・歯周病原細菌用検体1 mlを作成した。2検体採取後,検体容器の残存唾液をLD用検体とした。
歯周病原細菌数の測定は,PCRインベーダー法8)を用いて測定した。同一チューブで,PCR反応とインベーダー反応を同時に行わせることにより,高感度に定量的な検出が可能である。
対象はPorphyromonas gingivalis(P.g),Treponema denticola(T.d),Tannerella forsythia(T.f)のRed complex 3種類と,唾液10 μlあたりの総菌数とした。
なお,唾液内の細菌数は,日内変動することを考慮したが,すべての被験者において,厳密に唾液の採取時間を規定することが困難であったため,静的唾液の採取時期と同様に,午後昼食後の13時以降の時間帯に採取するようにした。
4. アンケート飲用前には,生活習慣アンケート調査を行い,現在の被験者の生活環境・習慣を把握することとした。すなわち,飲食の習慣・睡眠・運動・喫煙・飲酒・常用薬の有無・サプリメントの服用の有無であった。また腹部症状等問診票として,腹部症状・皮膚症状・体調・精神・生理の状態などを調査した。免疫状態は,ストレスとも関連があるため,簡易ストレス度チェックリスト9)を用いて評価した。また,歯周病リスクを調べるため歯周病リスク換算表を用いた。飲食・歯磨き,口腔内の様子,生活習慣,喫煙状況などについてアンケートを行った。なお生活習慣アンケート調査以外のアンケートは,0週,2週,4週,8週の4回全てにおいて行った。
5. 統計解析群内比較にはFridmanの検定による多重比較を,群間比較は対応のないt検定またはMann-WhitneyのU検定を用いた。危険率5%未満を有意水準とした。解析にはXLSTAT Ver.17.01を用いた。
6. インフォームド・コンセントおよび倫理委員会規定本研究はヘルシンキ宣言,医学系研究に関する倫理指針に準拠しており,日本医科大学千葉北総病院薬物治験審査委員会の承認を得ている(受付番号:527006)。その他,NPO法人日本歯周病学会の倫理規定に準拠した。
試験参加に同意した21名のうちプラセボ群1名が腹部の不調を訴え途中で脱落した。最終的な解析対象者は研究群10名,プラセボ群10名の計20名であった。研究開始時,2群間でLDにおいて有意差が認められたが,他の項目において有意差は認められなかった(表1)。
簡易ストレス度チェックに関しては,特に2群間で,ストレスの差は観察されなかった。また,研究に対して影響を及ぼすような重度ストレスを有する被験者は認められなかった。飲用によるストレスの顕著な軽減は認められなかった。
また歯周病リスクのアンケートに関しても,8週を通してリスクの増減は認められなかった。

研究開始時の研究群とプラセボ群のデーター比較 *:(P<0.05).
PD,BOP,GI,PlIの測定結果を図1に示した。研究群およびプラセボ群ともに良好なメインテナンスが行われており,臨床パラメーターが大きく悪化した者は認められなかった。4週間後においてBOPおよびGIにおいて2群間で有意差が認められ,研究群で改善が認められた(図1)。その後,4週から8週間後にかけてBOPとGIはやや悪化傾向を示したが,開始時と比較した場合には改善傾向を維持していた。PlIには両群ともに大きな経時的変化はなかったが,PDについては研究群の経時的改善率が大きい傾向が認められた。
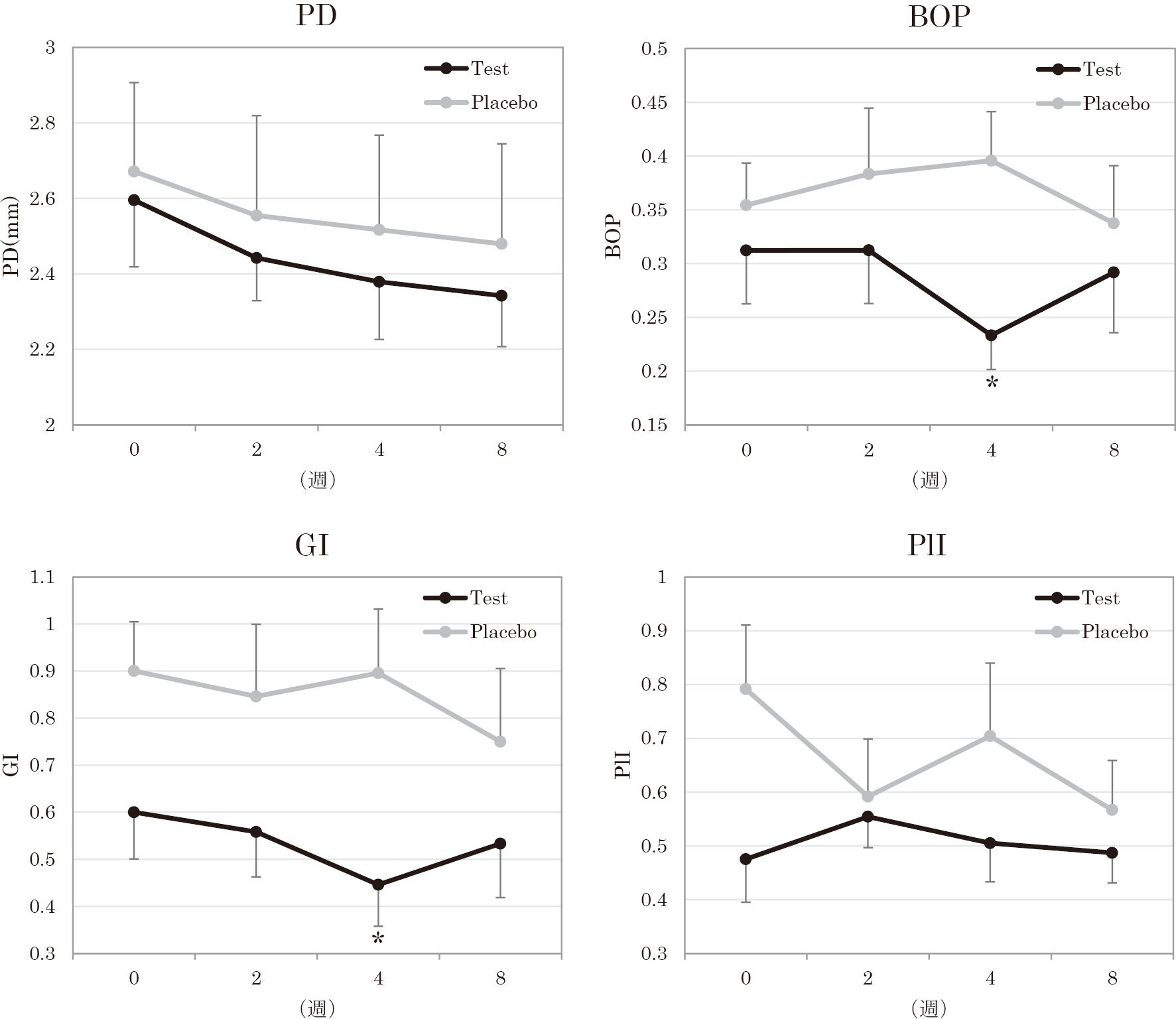
臨床パラメーターの推移 *:(P<0.05)
4週間後において BOP および GI において2群間で有意差が認められ,研究群で改善が認められた。4週から8週間後にかけても,開始時と比較した場合には改善傾向を維持していた。PlIには両群ともに大きな経時的変化はなかったが,PDについては研究群の経時的改善率が大きい傾向が認められた。
総細菌数は,4週から8週間後にかけて研究群において減少傾向が認められた。また,Red Complex 3菌種の菌数については大きな変動は認められなかった(表2)。
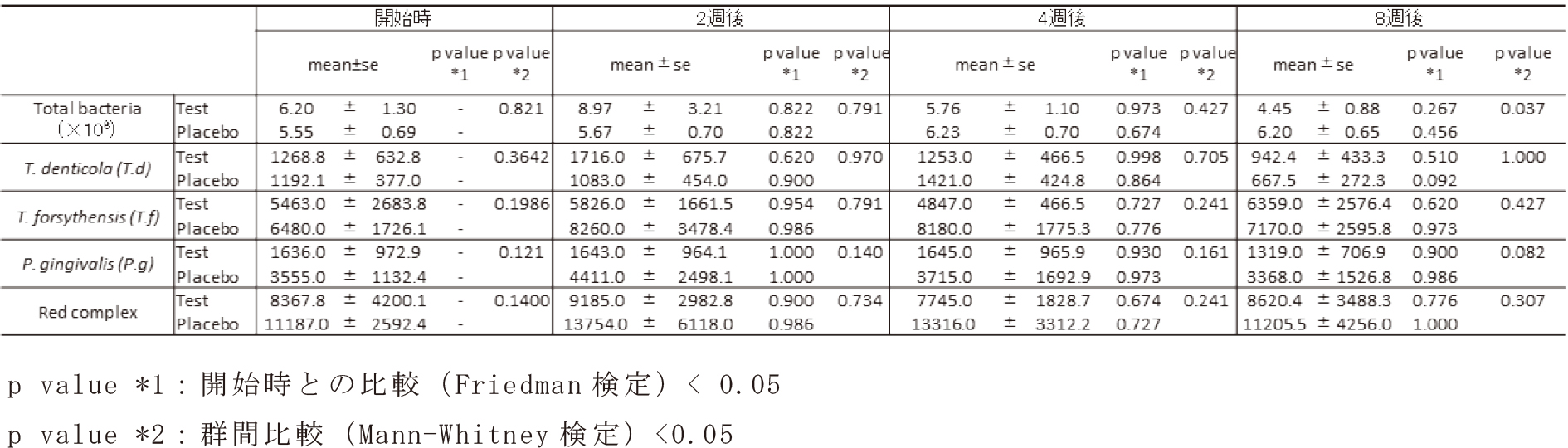
口腔内細菌数の推移
アルベックスⓇ服用開始前からLDは8週を通して,研究群で低値を示し,8週までプラセボ群よりも低値を維持した。HbならびにIgAについては有意な群間差は認められなかった。健常者における基準値であるLD350 U/L,Hb2 μg/mlに対して両群ともに高値を示しており,SPT期にはあるものの,歯周炎活動性のあることが伺えた(図2)。
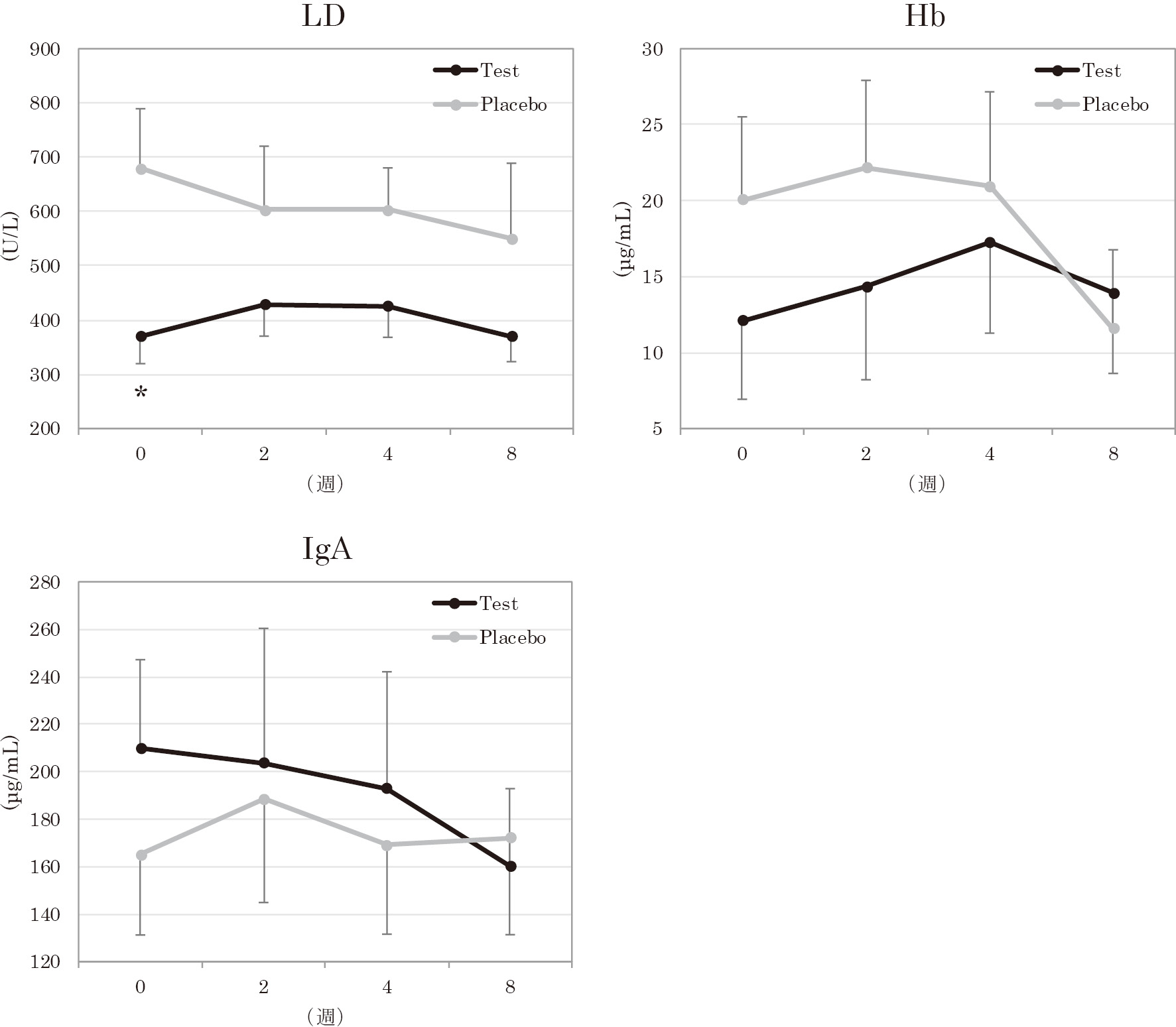
唾液パラメーターの推移 *:(P<0.05)
LDは,研究開始時に2群間で有意差が認められた。HbならびにIgAについては有意な群間差は認められなかった。
本研究では被験者のうち1名が,腹部の不快感により,途中で脱落した。まれにアルベックスⓇの服用により,腸内細菌叢の様相が変化することで,腹部のハリ,ガスが多くなることがあると添付文書にも記載があり,主訴から判断して,その状況が実際に起こったものと推察された。従って,特にアルベックスⓇの服用が,被験者に対して為害作用を及ぼしたものではないと考えられた。
簡易ストレス度チェック,歯周病リスクのアンケートに関しては,8週間を通してスコア,リスクの増減は認められず,アルベックスⓇの飲用による明らかな改善は認められなかった。
唾液の分泌量に関しては,平均年齢を考慮すると減少傾向にあると考えられるが,唾液の採取量・採取時間に関して,支障は認められなかった。予め,被験者の選定の際に,唾液分泌を抑制するような疾患を有する者,あるいは薬剤を服用する者を除外したことで,唾液採取が円滑に遂行したものと推察された。
研究開始時の臨床パラメーターは,4項目全てにおいて2群間で有意差は認められなかった。また,総細菌数・Red Complex3種の細菌数4項目においても,2群間で有意差は認められなかった。これらのことから,2群間の被験者の口腔内状況には概ね顕著な偏りがなく,研究開始時の被験者選定には問題がなかったこと,また外来患者における研究開始までのSPTが適切に行われていたことが推察された。
研究期間中の臨床パラメーターの推移は,4週目のBOP・GIにおいて研究群にてプラセボ群と比較して有意に減少が認められた。また細菌数に関しては,総細菌数が4週目から8週目にかけて減少傾向を示した。さらにPDについても,有意差はないものの,プラセボ群と比較して研究群で改善傾向が大きい結果を得た。一方で,BOPとGIの値は,開始時と比較して改善傾向は維持しているものの,4週目と比較した場合,8週目では若干の悪化傾向を示している。歯周炎は多因子疾患であり,様々な因子に影響を受けて病態が変化する。アルベックスⓇの効果を評価するためには,短期間の検査結果の変動を解析するだけでは不十分であり,今後はより長期的な臨床研究が必要になると考える。
乳酸菌生成物質が,ヒト好中球からの過剰な活性酵素の遊離を抑制して,正常組織の障害,あるいは治癒の遅延を防止することが判明し,炎症部位における組織障害を緩和する作用が示唆されている。また,ラットに対して,乳酸菌生成物質を含有した飼料を摂取させ,さらに乳酸菌生成物質を創部に塗布することにより,創傷治癒が促進されたとの報告10)もある。本研究では,PlIに変化がないにもかかわらず臨床パラメーターに改善傾向がみられた。これは,乳酸菌生成エキスの摂取による,炎症抑制効果に起因する可能性もある。
また,乳酸菌生成エキスの2か月の飲用により,P.g数とP.g菌比率が低値に維持され,歯周ポケットの改善が認められた11)との報告,あるいはS.mutansの有意な減少が認められたとの報告11,12)もある。さらに,in vitroにおいて,乳酸菌生成エキスがP.gの増殖を抑制し,乳酸菌などの有用菌に対しては増殖・促進作用を示し,腸内細菌叢の正常化に有効である可能性も示唆されている10)。これらの報告と同様に,本研究においても,乳酸菌生成エキスの成分が,直接的に口腔内細菌に作用し,細菌数を減少させたことにより,臨床パラメーターの改善に結びついた可能性も考えられる。
唾液パラメーターに関しては,アルベックスⓇ服用開始前にLDにおいて2群間に有意な差が認められ,研究期間を通して,プラセボ群よりも研究群で低値を維持した。LDは歯根膜細胞の破壊状況を反映し,歯周病原細菌および歯周病態の変動の指標となり,またHbの量は,歯肉炎症の程度を表している。実際に,唾液検査の項目として,LD・Hbが妥当であることが既に報告されており13),本研究でもこれらを指標として用いるに至った。今回の研究においては,服用開始時点で群間に差があったことから,アルベックスⓇの効果を示唆することはできないが,今後,被験者数を増やし,これら唾液パラメーターを活用していくことで,アルベックスⓇの効果をより詳細に検証できるものと考える。
近年,腸内細菌と宿主の生理機能との関連性が判明してきており,大腸疾患,ストレス等の体調と腸内細菌との関係が報告されている14)。また,これまでに,乳酸菌生成エキスによる,便通の改善効果や腸内環境の改善効果,in vitroでの腸管免疫の賦活化15),あるいは大腸内抗腫瘍効果16)等が報告されている。また,乳酸菌生成エキスの飲用により,腸内細菌叢および腸内環境因子が変動し,特にビフィズス菌の顕著な増加が認められたことも示されている4)。
また,プレバイオティクスであるラフィノースが,腸内のビフィズス菌の増加を促進して免疫賦活作用を示し,歯周病発症因子として生体の防御機能の低下が挙げられることからも,これが歯周病予防に有効であるという報告17)がある。
これらの報告から,本研究においても,乳酸菌生成エキスであるアルベックスⓇを飲用することにより,ビフィズス菌の増加をはじめとした腸内細菌叢の変化が予想される。前述したように,被験者の腹部の違和感の訴え等からも,腸内環境の変化が本研究においても推察される。しかしながら,本パイロット研究においては実際の腸内細菌叢の変化,あるいはそれに伴う腸内環境の改善を実際に解析していない。今後は,乳酸菌生成エキス飲用前後の糞便採取などから,ビフィズス菌などの特定腸内細菌群の定量解析4)および比較が必要になると考えられる。
本研究では,生体防御・免疫機能の関連項目として,唾液内のS-IgAの分泌量に着目した。IgAは涙腺,唾液腺,乳腺,呼吸器系,泌尿生殖器系,消化管の粘膜細胞近傍のBリンパ球により産生され,細胞内部を通過し,粘液性分泌物として分泌される免疫グロブリンである。粘膜免疫において重要な役割を有しており,口腔や肺,消化管などの脆弱な器官を侵入病原体から守る役割があることから,全身の免疫力の向上により,その分泌量が増加することが推察される。
一方で,口腔は消化管の入口に位置しているが,消化管は腸管関連リンパ組織(GALT)という腸間膜リンパ節,Peyer板,孤立リンパ節などから成り立つ免疫系を有し,唾液のS-IgA産生も,GALTより制御されていると考えられている18)。消化管におけるS-IgAの産生は,Peyer板などの抗原特異的リンパ球の活性を図るS-IgAの誘導組織,および活性化したリンパ球の帰巣(ホーミング)により抗体を産生する唾液腺などの影響組織で行われる19)。粘膜固有層に存在するリンパ球は,粘膜関連リンパ組織を構成しており,粘膜を介した免疫応答における実効組織,誘導組織間の経路が存在する,いわゆる粘膜免疫循環帰巣経路(CMIS)の概念がある。口腔内の免疫システムはこのCMISの影響下にあると考えられている。
乳酸菌生成エキスの飲用により,腸内ビフィズス菌の増加など,腸内細菌叢の変化が惹起された場合,これによりS-IgAの誘導組織であるPeyer板をはじめとしたGALTが何らかの刺激を受ける可能性が考えられる。CMISにより,分泌型細胞が誘導され,実効組織である唾液腺にそれらのホーミングが惹起されると,口腔内S-IgAの分泌量が増加すると考えられる。本研究においては,予想に反してS-IgAの分泌量増加は認められなかった。今後アルベックスⓇの効果を検証する際には,より長期的にS-IgA量の変化を調べるとともに,他の免疫学的因子の解析が必要となるかもしれない。
乳酸菌生成エキスの服用が,歯周炎の臨床パラメーターの改善,および口腔内細菌数の減少に効果を示す可能性が示唆された。
今回の論文に関連して,開示すべき利益相反状態はありません。