2025 年 37 巻 1 号 p. 51-56
2025 年 37 巻 1 号 p. 51-56
植物が遺伝的多様性を維持する戦略の一つに、雄花(♂)と雌花(♀)を別々の個体に分ける「雌雄異株化」がある。雌雄異株植物の多くは性染色体をもち、XY型の場合、Y染色体にオスを決定する遺伝子が存在する。性染色体は、元々は1対の常染色体から進化したものであり、時間とともにY染色体の分化が進み、X染色体とY染色体の大きさが異なる「異形性染色体」へと進化する。ナデシコ科の草本植物ヒロハノマンテマ(Silene latifolia)は、異形性染色体をもつ植物の代表例として研究されてきた。Y染色体には約500 Mbの大規模な組換え抑制領域が存在するため、性決定遺伝子の同定が長年困難であった。著者らはこの異形性染色体を詳細に解析し、雌ずいの発達を抑制する性決定遺伝子(Gynoecium suppressing function on Y: GSFY)を同定し、GSFYが雌ずいの矮小化に関与するシロイヌナズナのCLAVATA3遺伝子のオーソログであることを明らかにした。また、性染色体の進化過程において、X染色体ではCLAVATA3オーソログの機能喪失が生じ、Y染色体からは雌ずいを大きくするはたらきをもつWUSCHELオーソログが失われたことがわかった。この結果は、X染色体が性決定に関与することを示唆する初めての発見となった。
Plants maintain genetic diversity through strategies such as “dioecy,” where male flowers (♂) and female flowers (♀) are borne on separate individuals. Many dioecious plants have sex chromosomes, and in the XY system, the Y chromosome has the gene determining maleness. Sex chromosomes evolved from a pair of autosomes, with the Y chromosome diverging over time to form heteromorphic sex chromosomes, where the X and Y differ in size. Silene latifolia, a member of the Caryophyllaceae family, is a model species for studying heteromorphic sex chromosomes. Its Y chromosome contains a large recombination suppression region (~500 Mb), complicating the identification of sex-determining genes. By analyzing these chromosomes, the authors identified Gynoecium suppressing function on Y (GSFY), a gene that suppresses pistil development. GSFY was found to be an ortholog of the CLAVATA3 gene in Arabidopsis thaliana, involved in pistil reduction. Moreover, it was found that during the evolution of sex chromosomes, the X copy of the CLAVATA3 ortholog became nonfunctional, while the WUSCHEL ortholog, which is involved in pistil development, was lost from the Y chromosome but retained on the X chromosome. These findings suggest the X chromosome plays a role in sex determination, providing new insights into the evolution of plant sex chromosomes.
イチョウやキウイフルーツのように、植物のなかには雄花を咲かせるオスと、雌花を咲かせるメスの区別がある雌雄異株植物が存在する。雌雄異株は種子植物25万種のうちの約6%を占め、なかには動物と同じようにXY性染色体で性を決定するものがある。被子植物の性染色体は、1923年にカナダモ、カナムグラ、スイバ、セキショウモ、ヒロハノマンテマ、ホップにおいて発見された(Matsunaga and Kawano 2001)。これらは、ヒトの場合と同様、雌雄異株のオス株とメス株との間で数や形の異なる染色体として発見された。Y染色体やW染色体のサイズがX染色体(或いはZ染色体)のサイズと大きく異なるため異形性染色体と呼ばれる。一方、近年では、シーケンス技術の発達により、顕微鏡下ではXとY(あるいはZとW)の間の違いが判別できないような同形性染色体も、マメガキをはじめとする数多くの種で同定されており(Akagi et al. 2014)、性決定遺伝子の同定と性染色体の進化に関する研究が飛躍的に進められてきた。
植物でも動物でも、性染色体は、1対の常染色体から誕生したと考えられている。1対のうちの一方に性決定遺伝子が誕生し、性決定遺伝子が座乗する領域で組換えが抑制されることにより生じた(Charlesworth 1996)。一度、組換えが抑制されると、組換え抑制領域では有害な変異を排除できなくなり、転移因子などが蓄積してY(或いはW)染色体特異的な領域が拡大していく。このような性染色体の分化は不可逆なプロセスであり、初めは同型性染色体であったものが徐々に異形化していく運命にある(Hayashi et al. 2024)。植物に当てはめると、マメガキ、キウイフルーツ、アスパラガス、ポプラ、ブドウなどにみられる同型性染色体は比較的分化の初期段階にあり、ホップ、アサ、ヒロハノマンテマ、スイバなどにみられる異形性染色体はより分化の進んだ段階にある。
ヒロハノマンテマ(Silene. latifolia) は、Y染色体がX染色体の約1.4倍を示す顕著な異形性染色体をもつ。顕微鏡下での性染色体の観察が容易であり、植物ホルモンや気温などの外的刺激によって性が変化しないことから、1923年の発見以降、植物における性染色体研究のモデルシステムとされてきた。ヒロハノマンテマを用いた初期の遺伝学的研究により、Y染色体上に雌しべ抑制因子(Gynoecium Suppressing Factor, GSF)と雄しべ促進因子(Stamen Promoting Factor, SPF)の2つの性決定遺伝子の存在が明らかとなった(Westergaard 1946)。これらの遺伝子が欠失すると、それぞれ両性花および無性花が発生することが示されており(Farbos et al. 1999, Lardon et al. 1999)、これは、性決定と性染色体進化を説明する「二重突然変異」モデル(別名「二遺伝子」または「二因子」モデル)と一致している。このモデルは、雄しべや花粉の成熟を阻害する突然変異に続き、雌しべを抑制する突然変異が起こることで、雌雄異株が両性花植物から進化するというものである(Westergaard, 1958, Charlesworth and Charlesworth 1978)。二因子モデルは、雌雄異株と性染色体の進化を同時に説明できることから、多くの植物性染色体研究者に支持されている。対照的に、単性花からの進化モデル(別名「一遺伝子」または「一因子」モデル)では、雌雄異株は単性花植物から一つの性決定遺伝子の進化によって発生するとされる(Renner 2014, Boualem et al. 2015, Renner and Müller 2021)。一因子性決定システムは、マメガキ (Diospyros lotus) やヤナギ属 (Poplus spp.) のような一部の雌雄異株種で見つかっている(Akagi et al. 2014, Müller et al. 2020, Xue et al. 2020)。
上述の通り、ヒロハノマンテマは、植物のなかでは進化の進んだ異形性染色体をもち、遺伝的に安定した二因子型の性決定システムをもつ植物である。したがって、ヒロハノマンテマにおける性決定遺伝子の同定により、二因子モデルの性決定システムをもつ巨大な異形性染色体がどのように進化したかに迫ることができると期待される。しかしながら、約500 Mbもの巨大な組換え抑制領域を含むY染色体からの性決定遺伝子の同定は困難を極め、性染色体発見から99年が経つまで誰も成し得なかった。本総説では、筆者らがヒロハノマンテマにおいて性決定遺伝子の1つGSFYを同定し、メスの全ゲノム配列を決定することによって明らかとなった植物性染色体進化の新知見について述べたい。
ゲノム解読が行われていなかったヒロハノマンテマにおいて、500 Mb程度の巨大な組み換え抑制領域から性決定遺伝子を同定するため、Y染色体に欠失を導入し、その欠失の分布から候補領域を絞り込む欠失マッピングを行なった。まず、ヒロハノマンテマに重イオンビームを照射し、雌ずいと雄ずいとの両方をもつ両性花変異体(図1A)、どちらももたない無性花変異体の作出を行なった。両性花変異体はGSFを、無性花変異体はSPFを欠失していると考えられる。これらを含む41系統の変異体についてY染色体特異的な69個のPCRマーカーでPCRを行った。次に欠失したマーカーの一番もっともらしい並び順を推定する新規開発プログラム、DelMapper(デルマッパー)を用いて、Y染色体の詳細な欠失マップを作成し、GSF領域とSPF領域を同定した(Kazama et al. 2016)。このうち、最も欠失領域が小さい両性花変異体2個体と、オス、メスについてゲノムシーケンスを行なった。さらに花芽を顕微観察により12ステージに分類し、雌ずいの発達が形態的に判別できるステージ4以前の花芽をサンプリングしてRNA-seqを実施した。これらのシーケンスデータを統合することで、オスにのみ存在しメスや11個体の両性花変異体が共通してもたない遺伝子を、GSFYとして同定した。in situハイブリダイゼーションの結果、GSFY遺伝子はオスの発達初期(ステージ1-3)の雌ずい原基で発現していた。GSFYは、モデル植物シロイヌナズナのCLAVATA3(CLV3)遺伝子と高い相同性を示した。CLV3は12アミノ酸からなる小さなペプチドとして作用し、分裂組織を小さくする役割をもつ(図1B)。そこで、GSFYペプチドをヒロハノマンテマのメスの花芽に塗布したところ、雌ずいの発達が抑制された(図1C)。また、GSFYのゲノム断片をシロイヌナズナに導入したところ、雌ずいの発達が抑制され雌花様の花を咲かせた。以上より、Y染色体に存在し、11個体の両性花変異体で共通して欠損していて、雌ずいの初期発達ステージで発現し、雌ずいの発達の抑制能をもつ遺伝子GSFYを性決定遺伝子として同定した(Kazama et al. 2022)。

図1 ヒロハノマンテマの花と雌ずいの発達抑制に関わる性決定遺伝子GSFYおよびそのX染色体パラログ(GSFX)。(A)雄花(♂)、雌花(♀)、両性花変異体を示す。 Bar = 1 cm. (B) GSFY, GSFX, シロイヌナズナのCLV3がコードするペプチド(それぞれGSFY, GSFX, CLV3)、およびCLV3の機能欠損型変異体clv3-1/clv3-5 がコードするペプチド(CLV3m)のアミノ酸配列を示す。GSFXもCLV3m も6番目のグリシン残基がアラニン残基に変異していた。(C) 両性花変異体EGP14株の花芽にGSFYおよびGSFXペプチドを処理して撮影した走査型電子顕微鏡写真を示す。Bar = 500 μm. 図はKazama et al. (2022) より引用・改変した。
筆者らは、X染色体上に、GSFYのパラログ遺伝子GSFXを同定した。GSFXはGSFYと同様に茎頂分裂組織と雌ずい原基で発現していたが、CLV3ペプチドの活性に重要なアミノ酸残基に変異が入っていた(Gly→Ala)(図1B)。この変異は、シロイヌナズナのヌル変異体であるclv3-1 及びclv3-5と同一であった。そこで、GSFYとGSFXがコードするペプチドを人工合成し、ヒロハノマンテマの茎頂や花芽に処理してペプチドの活性を評価したところ、GSFXペプチドは雌ずいや茎頂を抑制する能力がなく、機能を失っていることが示唆された(図1C)。GSFXとGSFYの同義置換率は0.18であり、ヒロハノマンテマ1塩基あたり1世代ごとの突然変異率(m = 7.31×10⁻⁹)を元に(Krasovec et al. 2018)、両遺伝子の分化年代を推測すると1800万年前と推定された。これは、ヒロハノマンテマの種分化の時期とほぼ一致することがわかった。以上の結果より、GSFYの獲得は、ヒロハノマンテマが性染色体を獲得した時期と一致し、GSFYはX染色体上のGSFに変異が生じてGSFXが機能を失ったことにより誕生したことが示された。
前述のように、性決定遺伝子GSFYはCLV3のオーソログである。シロイヌナズナでは、茎頂のサイズを小さくするはたらきをもつ遺伝子がCLV3であるのに対し、茎頂のサイズを大きくするはたらきをもつ遺伝子がWUSCHEL(WUS)である。CLV3とWUSは互いに発現量を調整し、茎頂のサイズを維持している(Perales et al. 2016, Plong et al. 2021)。また、WUSが欠損すると雌ずいが矮小化する(Laux et al. 1996)。このことから、WUSは雌ずいの発達領域を増大させるはたらきをもつと言える。興味深いことに、ヒロハノマンテマのX染色体には、WUS遺伝子のオーソログ(SlWUS1)が存在し、Y染色体にはSlWUS1は存在しない(Kazama et al. 2012)。すなわち、SlWUS1はオスでは1コピーであるのに対し、メスでは2コピー存在することになる。このSlWUS1のコピー数の違いは、X染色体が雌ずい発達を促進し、性決定に関与する可能性を示唆する。X染色体が雌ずい発達に与える影響は、1946年にWarmkeによって行われたコルヒチン処理による倍数体の作出実験にもみられる(Warmke 1946)。定量的な解析はされていないものの、コルヒチン処理で作出したXXXY個体やXXXXY個体では、雌ずいが発達し両性花を咲かせたのである。
X-Y間(もしくはZ-W間)での遺伝子のコピー数の違いは、多くの生物において遺伝子量補償という機構で転写産物の量が均一化される。ヒロハノマンテマもその一つであり、X染色体上の多くの遺伝子がオスではメスよりも高発現することで、オスとメスとの間での発現量比を均一化している(Papadopulos et al. 2015, Krasovec et al. 2019, Muyle et al. 2022)。しかしながら、SlWUS1の花芽における発現量比はオス:メス=1:2であり、遺伝子量補償を全く受けない(Kazama et al. 2012)。SlWUS1は、GSFXと同様に、X染色体の組換え抑制領域のうち最も古い領域に位置している(Yue et al. 2023)。後述する組換え抑制領域の拡大の要因の1つが、遺伝子量補償の獲得にあるという最近のモデルを考慮すれば、SlWUS1はより遺伝子量補償が生じやすい位置に座乗している(Lenormand and Roze 2022, Muyle et al. 2022)。それにもかかわらず、SlWUS1が遺伝子量補償を受けないのは、おそらくSlWUS1の発現量に性差があることが必要であり、遺伝子量補償によってその性差が崩されるべきでないということを意味しているのかもしれない。以上のことから、ヒロハノマンテマのX染色体はSlWUS1を介して性決定に関与している可能性が高いと著者は考えている(Kazama et al. 2023, Kobayashi et al. 2023)。
二因子モデルによれば、祖先的な両性株から雌雄異株への移行は、原始X染色体上の潜性の機能欠損型雄性不稔変異と原始Y染色体上の顕性の機能獲得型の雌性不稔変異をともなう(Westergaard 1958, Charlesworth and Charlesworth 1978)。GSFXの機能喪失変異の発見は、雌性不稔変異もまた、X染色体上の機能欠損で生じたことを明らかにした(Kazama et al. 2022)。さらに、SlWUS1のY染色体からの消失のシナリオは、雌雄異株への移行には2つではなく少なくとも3つの変異、すなわち雄性化のための1つの変異(SPF:未同定)と雌性化のための2つの変異(X染色体上のGSFXの機能喪失とY染色体上のSlWUS1の喪失)が関与した可能性を示唆している(図2)。雌性の抑制が複数の変異によって進化することは驚くべきことではない。というのも、雌性機能の喪失は適応度の観点からコストが高く、少なくとも2倍の雄性機能による繁殖成功率の向上で補われなければならないからである (Lloyd 1976, Aonuma et al. 2021)。したがって、ヒロハノマンテマに見られた段階的な雌ずい発達抑制機能の獲得は、従来のモデルよりも雌雄異株への移行を完了するためのより現実的な方法とも考えられる。
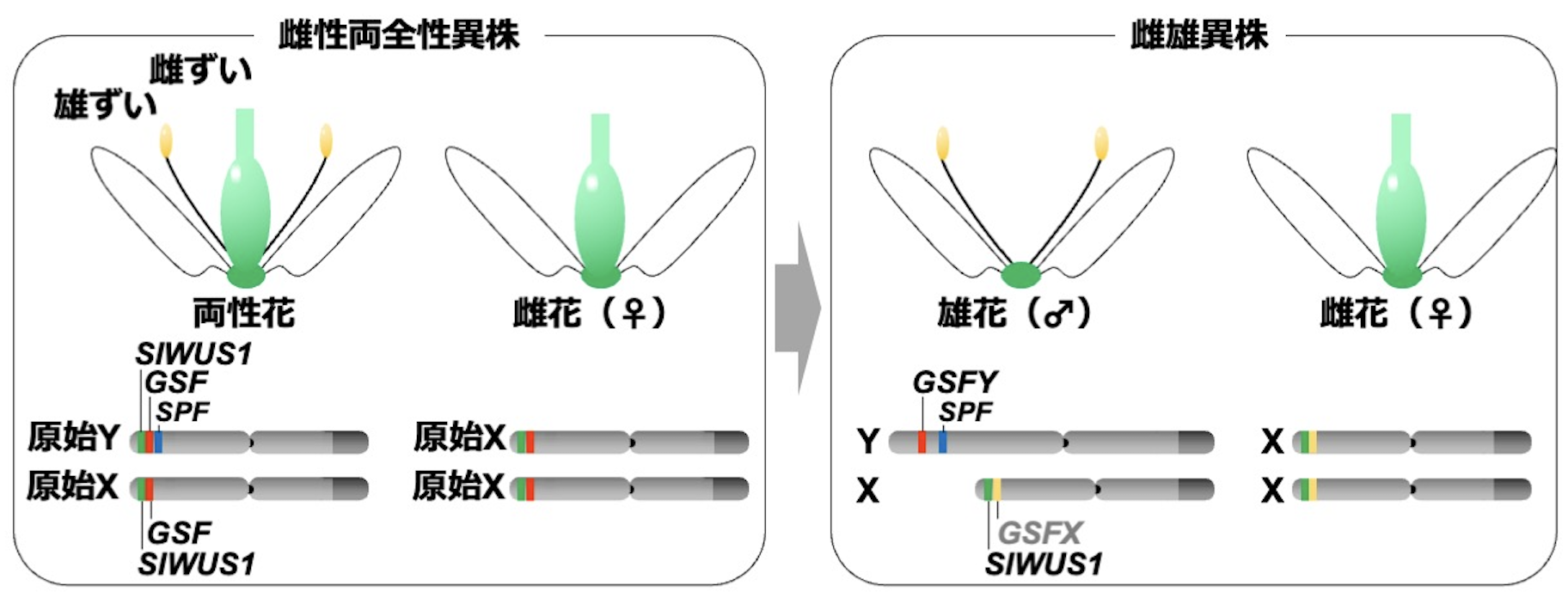
図2 雌性両全性異株から雌雄異株への進化の模式図。雌性両全性異株から雌雄異株へと進化する際に、X染色体上ではGSFXの機能が失われ、Y染色体からはSlWUS1が消失した。
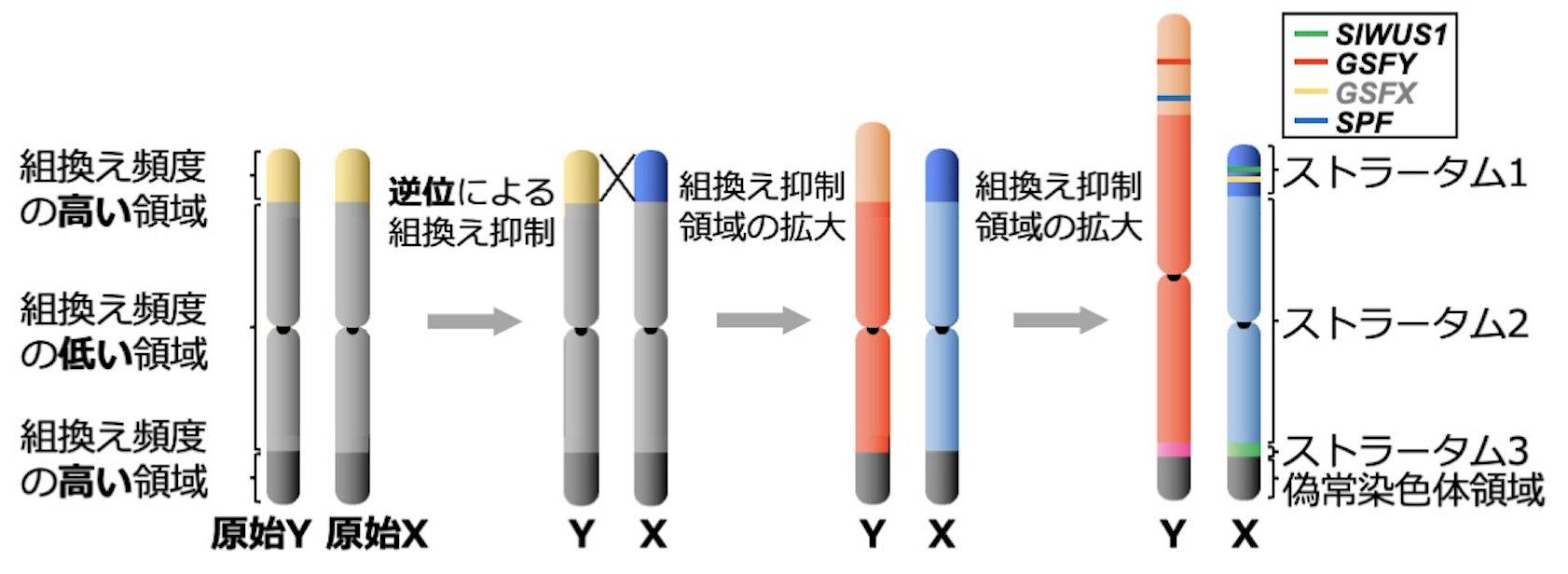
図3 ヒロハノマンテマの性染色体の進化の模式図。X染色体上の一端で逆位が生じて初期の組換え抑制が生じた。次に組換え頻度の低い領域から順に組換え抑制領域が拡大した。その結果、ストラータム1、ストラータム2、ストラータム3と、現在でも組換えが起きている偽常染色体領域が誕生した。
性染色体上の組み換え抑制領域は徐々に拡大していくことが知られている。ヒロハノマンテマのX染色体では、組み換え抑制が3段階で進んだことがわかっており、これらを進化的階層(Evolutionary strata)と呼ぶ。これらの3段階の組換え抑制領域は、古い順にストラータム1、ストラータム2、ストラータム3に分けられる(Filatov 2024)。組換え抑制領域の段階的な拡大の要因は、長い間、「性的拮抗仮説」で説明されてきた(Rice 1992)。性的拮抗とは、グッピーの体色のように、ある形質が一方の性に有利にはたらきもう一方の性に不利にはたらくことで、種としてその形質を最適化できない状態のことを指す。そのため、例えば、オスに有利でメスに不利な形質を担う性拮抗アリルが雄性決定遺伝子の近傍に位置した場合、雄性決定遺伝子と性拮抗アリルとの間で組換えが抑制されるという仮説である。しかし、組換え抑制を実際に引き起こした性拮抗アリルが同定された例はこれまでになく、ヒロハノマンテマに見られるような巨大な組換え抑制領域がどのように発達したのかについては全くの謎であった。その一旦が、メスゲノムの解読と性染色体をもたない近縁種との遺伝学的地図の比較により明らかとなった。まず、最も古いストラータム1の組換え抑制は、X染色体の末端の逆位によって誕生したことがわかった(図3, Yue et al. 2023)。次に、最も巨大なストラータム2は、常染色体の頃から組換えがほとんど起きない領域であったこともわかった。そのため、組み換え抑制領域として固定しやすかったのであろう。従って、ヒロハノマンテマの組み換え抑制領域は性的拮抗アリルが無くても拡大することが可能であったと考えられる。また、雌ずいの発達抑制に関わる遺伝子は全てストラータム1に存在することも明らかとなった(Yue et al. 2023)。これは、性染色体が構築された時にGSFYとGSFXとの間で組換えが抑制されたことを意味する。また、SlWUS1もストラータム1に座乗していることから、Y染色体へのSlWUS1の転移も、X染色体へのGSFYの転移も起こりえなかったことがわかる。すなわち、上述のような段階的な雌ずい発達抑制機構の進化は、逆位によるX-Y間での物理的な組み換え抑制が存在する上で成立したことがわかった。
性染色体による性決定を安定化させるためには、X-Y間(あるいはZ-W間)で組換えが抑制される必要がある。一度、組換えが抑制されると、Y染色体(あるいはW染色体)から有害な変異を除去することができなくなり、その結果、Y染色体(あるいはW染色体)から遺伝子が徐々に失われていく運命にある。実際、ヒトのY染色体には42個の遺伝子しか残っておらず(Rhie et al. 2023)、Y染色体が巨大化しているヒロハノマンテマであっても、Y染色体の分化が進んでおり、遺伝子の45%は発現が停止し23%にはナンセンス変異が生じている(Papadopulos et al. 2015)。このように、有害変異が蓄積して遺伝子が失われていくY染色体(あるいはW染色体)は、「進化の袋小路」にあると長らく考えられてきた(Charlesworth 1991, Bellot et al. 2014)。しかし近年、Y染色体を失ったアマミトゲネズミが新たな性染色体を獲得した例(Terao et al. 2022)に代表されるように、性染色体が再び生まれ変わるという説、「性染色体サイクル仮説」が提唱されている(Furman et al. 2020, Hayashi et al. 2024)。ヒロハノマンテマのX染色体がWUS-CLV3機構を介して性決定の役割を担うとすれば、Y染色体が消失した後も、X染色体上のSlWUS1の発現量を変化させることで性決定能を維持できる可能性がある。例えば、SlWUS1の発現量が低下した場合、X染色体が2コピーある個体では雌ずいが発達し、1コピーの場合には雌ずいが発達しないといった、X/O型の性決定が起こり得るかもしれない(Kazama et al. 2023)。X/O型の性決定は異形性染色体をもつスイバでも観察されている(Navajas-Pérez et al. 2005, Manzano et al. 2017)。植物においても、Y染色体が性決定能を失った後にX染色体が性決定能を維持し続けることで、「進化の袋小路」からの脱却が生じる可能性がある。異形化性染色体の研究の進展により、植物の性染色体の運命が明らかになる日も近いかもしれない。
本総説は 2024 年平瀬賞受賞の内容とその背景を中心にまとめたものである。本研究遂行にあたり、当該論文 の共著者である、鬼頭萌さん、小林壮生さん、石井公太郎博士、Marc Krasovec博士、安井康夫博士、阿部知子博士、Dmitry A. Filatov博士には深く御礼申し上げたい。また、本研究をご評価いただき、本稿で紹介する機会をくださった日本植物形態学会の皆様のご高配に感謝を申し上げたい。本研究は、JSPS 科研費 JP21KK0128,JP22H05071, JP22H05069の助成を受けたものである。Figure1は、クリエイティブ・ コモンズ・ライセンス(表示4.0 国際)のもとに改変して作成した。https://creativecommons.org/licenses/by/4.0/