2025 年 37 巻 1 号 p. 19-26
2025 年 37 巻 1 号 p. 19-26
真核細胞内に発達したオルガネラは、それぞれ特有の酵素群や代謝物を内包することで独自の機能を発揮する。その機能的独自性から、オルガネラは空間的に独立して存在すると考えられてきた。しかし近年の研究により、異なるオルガネラ膜が直接結合する「オルガネラ膜間コンタクトサイト (Membrane Contact Site, MCS)」が発見され、異なるオルガネラ同士がこれまで考えられていたよりも密接に連携しながら機能することがわかってきた。 MCSという新しい視点が加わったことで、オルガネラ研究に大転換期が訪れていると言っても過言ではない。本稿では出芽酵母の研究を例に、MCS研究の最新動向、特にMCSが関与する脂質輸送機構について概説する。
Organelles compartmentalize specific sets of enzymes and metabolites, enabling them to perform their characteristic functions. Due to this functional specialization, organelles have long been considered spatially independent structures. However, recent research has identified membrane contact sites (MCS), regions where different organelle membranes are directly connected, revealing that organelles collaborate more closely than previously thought. The discovery of MCS has introduced a paradigm shift in organelle research, offering a new perspective on how organelles function. In this article, I will provide an overview of the latest trends in MCS research, with a particular focus on the mechanisms of lipid transport via MCS in yeast.
細胞内に発達したさまざまなオルガネラは、環境に応じてその量や機能を変化させる動的な膜構造である。このようなオルガネラの動的な機能調節機構を理解するためには、細胞内でどの脂質分子を、いつ、どこで、どれだけ合成し、合成した脂質分子をどのオルガネラ膜へどれだけ輸送するのかといった、脂質分子の生合成機構の解明が必須となる。しかしながら、これまでタンパク質の生合成機構に関しては精力的に研究が推進されてきた一方で、脂質の生合成機構、特に細胞内脂質輸送機構に関しては研究が遅れている。
脂質分子の多くは小胞 (ER) で合成された後、ER膜から小胞輸送経路によってゴルジ体、エンドソーム、リソソーム(液胞)、細胞膜に輸送される。小胞輸送が細胞内脂質輸送の主要経路であることは間違いないが、小胞輸送経路から独立したミトコンドリアなどのオルガネラ膜への脂質輸送には異なる輸送機構が存在するはずである。最近の研究によって、オルガネラ膜同士が近接するオルガネラ膜コンタクトサイト (Membrane Contact Site, MCS) が脂質輸送に重要な役割を持つことが明らかにされた (Tamura et al. 2019)。本稿では出芽酵母を例に、MCSを介した脂質輸送機構に加え、MCSの新しい解析手法やMCSの動的変化を介した新しい細胞ストレス応答機構といった最新の知見についても解説する。
疎水性分子であるリン脂質が、水溶性環境であるサイトゾルを通過してER膜からミトコンドリア膜に移動する過程は、熱力学的に非常に不利な反応である。それにもかかわらず、細胞内では多数の脂質分子がERとミトコンドリアの間を行き来している。例えば、ホスファチジルエタノールアミン (PE) とカルジオリピン (CL) はそれぞれミトコンドリア内膜に局在する酵素Psd1とCrd1によって合成されるため、これらの前駆体リン脂質であるホスファチジルセリン (PS) やホスファチジン酸 (PA) はERで合成された後、ミトコンドリア内膜へ輸送されなければならない(図1)。PEは、ミトコンドリア内膜で合成された後、ERへと輸送され、ER膜に局在する酵素Cho2, Opi3によってメチル化されることでホスファチジルコリン (PC) へと変換される(図1)。このようにERとミトコンドリアの間で行われるリン脂質輸送はリン脂質を適切に合成するために欠かせない重要なイベントである。

図1 出芽酵母における主要リン合成、輸送経路、ER-ミトコンドリア間のリン脂質輸送はERMES複合体が、ミトコンドリア外膜から内膜へのリン脂質輸送はUps1/2-Mdm35複合体が仲介する。PA:ホスファチジン酸、CDP-DAG:CDPジアシルグリセロール、PGP:ホスファチジルグリセロールリン酸、PG:ホスファチジルグリセロール
ER-ミトコンドリア間のリン脂質輸送を担うERMES (ER-Mitochondria Encounter Structure) 複合体は、Kornmannらによる遺伝学スクリーニングによって同定された (Kornmann et al. 2009)。Kornmannらは、ミトコンドリア外膜とER膜を直接結合できる人工タンパク質ChiMERAを設計し、その発現が細胞増殖に有利になる突然変異株をセクタリングスクリーニングで単離した。ChiMERAはN末端にミトコンドリア外膜局在化配列であるTom70のN末端膜貫通領域と、C末端にER膜局在化配列であるUbc6のC末端膜貫通領域を融合したGFPであり、その発現は通常細胞の増殖に必要ない。一方、遺伝子変異によってER-ミトコンドリア間結合に異常が生じれば、ChiMERAの発現が細胞の増殖に有利になると予想される。セクタリングスクリーニングではプラスミドを保持した細胞は赤色を、プラスミドを消失した細胞は白色になる仕掛けとなっている (Hieter et al. 1985)。ChiMERAを発現するためのプラスミドを持つ酵母細胞を富栄養培地で培養し、プラスミドをマーカー遺伝子で選択しないと、酵母細胞はプラスミドを自発的に落とし、赤色のコロニー内に白色の細胞が扇形に混ざった状態となる。一方、遺伝子変異によってER-ミトコンドリア間結合に異常が生じてChiMERAの発現が細胞の増殖に有利になれば、細胞がプラスミドDNAを保持し続けてコロニーが赤一色のまま維持される。コロニーの色を指標にChiMERAの発現が細胞増殖に有利になる突然変異株を単離した結果、Mdm12をコードする遺伝子に変異が入っていることが判明した。Mdm12は過去の研究によってMmm1, Mdm10, Mdm34と呼ばれるタンパク質と複合体を形成し、ミトコンドリアの形態維持に関与する事が報告されていた (Burgess et al. 1994, Berger et al. 1997, Dimmer et al. 2002, Boldogh et al. 2003, Meisinger et al. 2007) 。興味深いことにこれらの4つの因子の内1つでも欠損すると全て共通して、ミトコンドリアの球状化、ミトコンドリアDNAの消失、外膜タンパク質の輸送異常、強い増殖阻害を示す。これらの4つの因子は全てミトコンドリア外膜タンパク質だと考えられていた。しかしKornmannらによってMmm1がER膜タンパク質であることが判明したことで、Mmm1, Mdm10, Mdm12, Mdm34から構成される複合体がER-ミトコンドリア間をテザリングする機能を持つことがわかり、ERMES (ER-Mitochondria Encounter Structure) 複合体と命名された (図1,Kornmann et al. 2009)。
Kornmannらは14C-セリンを用いたパルスチェイス実験により、ERMES構成因子が欠損するとERで合成されたPSのPCへの変換が顕著に遅れることを見出した。PS→PCの変換はER-ミトコンドリア間のリン脂質輸送に依存するため、ERMESがリン脂質輸送に関与することが強く示唆された (Kornmann et al. 2009)。筆者らは、ミトコンドリアとERを含む膜画分を用いて、これらのオルガネラ間のリン脂質輸送を評価できるin vitro実験系を開発し、 ERMES構成因子の欠損がPS輸送に影響することを確認した (Kojima et al. 2016a)。さらに精製Mmm1-Mdm12複合体がリン脂質輸送活性を示すことがわかり、ERMESがリン脂質輸送を直接仲介する因子であることが証明された (Kawano et al. 2018)。Mmm1, Mdm12, Mdm34は一次配列からSMPドメインと呼ばれるリン脂質結合ドメインを持つことが予測され (Kopec et al. 2011)、実際に結晶構造解析を含む生化学的な解析から、これらのタンパク質がリン脂質と直接結合することが示された (Kawano et al. 2018, Jeong et al. 2016, 2017)。最近、出芽酵母のcryo-CLEM解析によってERMES複合体の形状解析を行った結果、ジグザグ型のERMES複合体がER-ミトコンドリア間MCS (MCSER-Mito) に約25個存在し、リン脂質を輸送するトンネルを形成していることが報告された (Wozny et al. 2023)。
ERMES複合体が欠損した酵母細胞は、ミトコンドリア形態の異常や強い増殖阻害を示す。しかしながらERMESの欠損株を培養し続けると復帰突然変異株が現れることが知られていた。この復帰突然変異株の原因遺伝子を解析したところVPS13が同定された (Lang et al. 2015)。Vps13は3,000 アミノ酸以上から構成される巨大なタンパク質で、その点変異が ERMES の機能不全による表現型(増殖阻害やミトコンドリア形態異常)をほぼ完全に相補できることから、ERMES と同様に脂質輸送タンパク質であることが示唆された (Lang et al. 2015)。実際、ヒトの Vps13 の N 末端側 1350 アミノ酸領域がリン脂質結合に適したリン脂質結合ポケットを持ち、リン脂質を輸送する活性を持つことが示された (Kumar et al. 2018)。Vps13 は PxP モチーフを持つミトコンドリア外膜タンパク質 Mcp1、液胞やエンドソーム局在する Ypt35、前駆胞子膜に結合する Spo71 と直接結合することでER膜からさまざまなオルガネラ膜へと脂質を輸送すると考えられる (John Peter et al. 2017, Bean et al. 2018)。MCP1 遺伝子は筆者らの研究により、ERMES 欠損株の増殖阻害を抑制するマルチコピーサプレッサーとして同定されていた因子であり、過剰発現することにより Vps13 をミトコンドリア側に引き寄せると考えられる (Kojima et al. 2016b)。Vps13は酵母から植物、ヒトにも保存されている (Lang et al. 2015, Kumar et al. 2018, Tangpranomkorn et al. 2024) 。哺乳類に存在する VPS13 ファミリー (VPS13A-D) は全てヒトの神経変性疾患の原因遺伝子として報告されており、細胞内リン脂質輸送機構の研究はヒトの疾患克服の面からも重要な意味を持つと考えられる (Rampoldi et al. 2001, Ueno et al. 2001, Kolehmainen et al. 2003, Lesage et al. 2016, Gauthier et al. 2018, Seong et al. 2018)。
ERMES複合体やVPS13の解析から、MCSがオルガネラ膜間のリン脂質輸送の場として重要であることが明らかとなった。脂質輸送以外にも、カルシウムイオン輸送やミトコンドリアの分裂などMCSが関与する生命現象が報告されており (Szabadkai et al. 2006, Lewis et al. 2016)、MCSの解析を進めることでMCSの新規機能の解明が期待される。MCSの機能解析を進めるためには、生きた細胞を用いてMCSの動態を解析することが必須であるが、MCSの検出は電子顕微鏡解析やProximity Ligation Assayといった細胞を固定する方法が主流であった。FRETやddFP (Dimerization-Dependent Fluorescent Protein) を用いることで生細胞のMCSを解析した例も報告されているが (Csordás et al. 2010, Alford et al. 2012, Miner et al. 2024)、少なくとも筆者らが実際に実験を行った印象ではMCSの検出感度は低かった。そこで筆者らは、簡便に効率よくMCSを可視化する手法としてSplit-GFPを用いることを着想した (Magliery et al. 2005, Cabantous et al. 2005)。原理は単純で、これまでタンパク質間相互作用の研究に用いられてきたSplit-GFP(GFPを構成するβストランドのN末端側10本 (GFP1-10) と、C末端側の1本 (GFP11) に分割した分子)をそれぞれ異なるオルガネラ膜上に発現させ、これらのオルガネラが近接したMCSでGFPが再構成することでMCSを可視化するというものである(図2A)。実際に出芽酵母のER膜とミトコンドリア外膜にSplit-GFPタンパク質を発現させたところ、Split-GFPタンパク質自体はオルガネラ膜全体に拡散して局在するものの、生じたGFPシグナルはこれらのオルガネラのごく一部の領域で観察された (図2B, Kakimoto et al. 2018)。またこのGFPシグナルが ERMES複合体と共局在したことから、Split-GFPがMCS空間特異的に再構成することを確認した(図2C)。本実験系は任意のオルガネラMCSの可視化にに利用することが可能で、ER、ミトコンドリア、ペルオキシソーム、液胞、脂肪滴のいずれの組み合わせにおいてもSplit-GFPによるMCSの可視化が可能であった (Kakimoto et al. 2018, Tashiro et al. 2020)。また同様の実験系は筆者以外の研究グループからも報告されており、出芽酵母だけでなく、ヒト培養細胞や、植物細胞、ゼブラフィッシュにおいてもMCSの可視化が可能であることが報告されている (Cieri et al. 2018, Shai et al. 2018, Yang et al. 2018, Vallese et al. 2020, Li et al. 2020)。

図2 Split-GFPを用いたMCSの可視化手法、(A) Split-GFPを用いたMCS可視化の概念図、(B, C) ER-ミトコンドリア間MCSを可視化するためのSplit-GFPを発現した出芽細胞を示す。(B) ER膜上に発現させるSplit-GFP (GFP11) にmCherryを付加している。ER-mCherry-GFP11が典型的なERパターンを示している。(C) Split-GFPに加えMmm1-mScarletを発現させている。Scale Bar, 5 µm。Kakimoto et al. (2018) より改変。
Split-GFPを用いてMCSを簡便に可視化できる実験系を確立できたため、この系を出芽酵母のER-ミトコンドリア間MCS (MCSER-Mito) の数を制御する因子の探索に応用した。筆者らはMCSER-Mitoの動態を制御する因子が存在するとすれば、少なくともその一部はミトコンドリア外膜に局在すると考えた。この仮説を検証するために、ミトコンドリア外膜に局在することが知られるタンパク質50種類をデータベースから選別し、それらの因子が欠損した酵母株のMCSER-MitoをSplit-GFPタンパク質で可視化し、 MCSER-Mitoの数や範囲が変化する因子を探索した (Kakimoto-Takeda et al. 2022)。その結果、ミトコンドリア分裂因子であるFis1が欠損した細胞においてMCSER-Mitoを示すドット状のGFPシグナルの1細胞あたり数が減少し、1ドットあたりのGFP強度が増加した。Fis1はミトコンドリア分裂の実行因子であるダイナミン様GTPase、Dnm1のレセプターとして機能する因子である (Mozdy et al. 2000)。そこでDnm1欠損株においてもMCSER-Mitoを可視化したところ、Fis1欠損株と同様の結果が得られた。実際のMCSER-Mito形成因子であるERMES複合体を蛍光タンパク質で標識し、そのドット状シグナル(ERMESドット)の数をFis1やDnm1の欠損株で計測したところ、野生型細胞では1細胞あたり5個程度観察されるERMESドットが半数程度に減少し、1ドットに含まれる蛍光シグナルが倍増していた(図3A)。以上の結果から、MCSER-Mitoを形成するERMES複合体は会合しやすい性質を持ち、ミトコンドリアの適切な分裂がERMES複合体同士の会合を負に制御していると考えた(図3B)。この仮説が正しければ、逆にミトコンドリアの融合を阻害してミトコンドリアの断片化を促進させた際に、ERMES複合体の会合が阻害されて、その数が増加するはずである。ミトコンドリア融合因子であるFzo1やMgm1を欠損した細胞でERMESドットを観察したところ、予想通りERMESドットの数が野生型の倍程度に増加していた(図3A)。さらに、GFPもしくはmScarletを融合したMmm1を発現させるMatingタイプの異なる一倍体酵母株を接合し、2倍体となった細胞を観察したところ、Mmm1-GFPとMmm1-mScarletが示すERMESドットが共局在した。これらの結果から、ERMESドット同士が会合しやすい性質を持ち、ミトコンドリアの適切な融合分裂がERMES複合体同士の会合を調節することで、MCSER-Mitoの数が調節されることが示唆された。
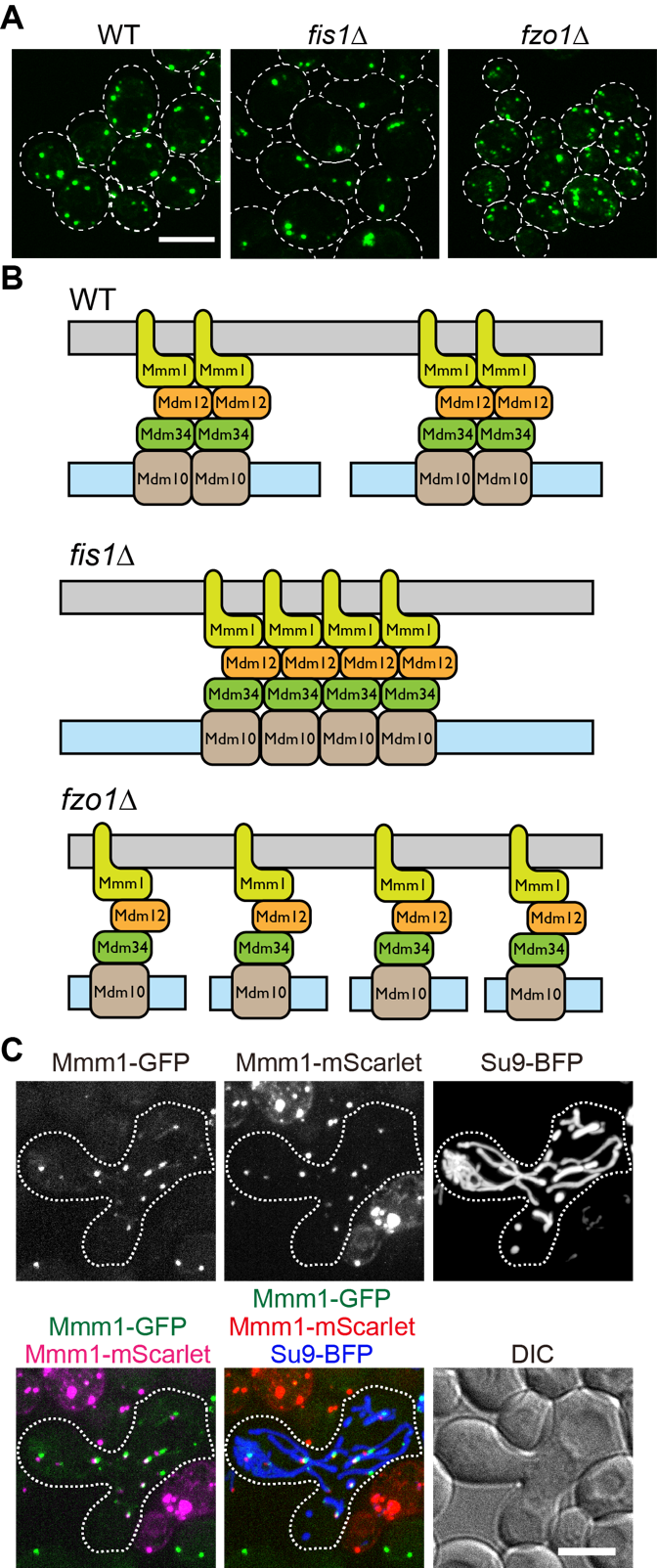
図3 ERMES複合体の数を制御するメカニズム、(A) ERMESのクラスター構造がミトコンドリアの適切な融合分裂によって制御される概念図、(B) Mmm1-GFP発現野生株(WT)、Fis1欠損株(fis1∆),Fzo1欠損株 (fzo1∆) を蛍光顕微鏡で観察した。(C) Mmm1-GFP もしくはMmm1-mScarletを発現するMating typeの異なる酵母株を接合し、蛍光顕微鏡で観察した。Scale Bar, 5 µm。Kakimoto et al. (2018) より改変。
ERMES複合体の数の調節は、ER-ミトコンドリア間の脂質輸送に影響するのだろうか?ER-ミトコンドリア間の脂質輸送量が変化すれば、これらのオルガネラの膜量も変化するはずである。過去に、ERストレス時にリン脂質合成が活性化されることでER膜が拡大し、ERストレスが軽減されることが報告されていた (Cox et al. 1997, Schuck et al. 2009)。しかしながらER膜だけを拡大させるためには、リン脂質合成を活性化するだけでは不十分で、合成されたリン脂質がER外にでていかないようにする脂質輸送の調節が必要だと考えられる。興味深いことに、筆者らはERMESドットの数がERストレス条件下で倍増することを見出した (Kakimoto-Takeda et al. 2022)。超高速超解像顕微鏡を用いたライブセルイメージング (Kurokawa et al. 2013) により、ERストレス条件下ではERMES複合体が解離し、その結果ERMESドットの数が増加していた。筆者らの試算ではERMESドット1つに、数百分子のERMES複合体構成因子が集積していると考えられる。ERストレス環境下では何らかの要因により、このクラスター構造が解離していることがわかった。14C-セリンを用いてPSをパルスラベルしその運命をチェイスしたところ、ERストレス環境下ではPS→PCの変換が顕著に遅れていた。この結果は、ERストレス依存的にERMES複合体が解離した状態では、ERからミトコンドリアへのリン脂質の輸送が抑制されていることを示す。興味深いことにERストレス依存的なERMESドットの解離が起きにくい変異株mmm1-1では、ERストレス依存的なER膜の拡大が抑制され、ERストレス誘導剤であるツニカマイシンに脆弱になっていた。これらの結果から、ERストレス環境下ではERMES複合体が解離することで、ER膜からミトコンドリアへのリン脂質輸送が抑制され、その結果のER膜が拡大することが示唆された(図4)。興味深いことにERMES複合体の解離はERストレスセンサーであるIre1やその下流の転写因子であるHac1に依存しなかったことから、ERMESの解離は既知のERストレス応答機構とは全く異なる現象であることがわかった。今後の研究により新しいERストレス応答メカニズムの解明が期待される。

図4 ERMES複合体の解離を伴うERストレス応答機構、 Takeda-Kakimoto et al. (2022) より改変。
Split-GFPを用いた方法ではMCSのライブセルイメージングによる動態解析は可能となったが、MCSに局在するタンパク質を直接探索することはできない。MCSの機能を理解するためにはMCS局在タンパク質の同定が必須となる。スタンフォード大学のTingらは分割したビオチンリガーゼsplit-TurboIDを用いることで、MCSに局在するタンパク質を空間特異的にビオチン化して同定する方法を開発した (Cho et al. 2020)。Split-GFPを用いた方法と原理は同じで、MCS領域特異的に再構成したTurboIDがMCSに局在するタンパク質をビオチン化することでMCS局在タンパク質を網羅的に探索できる。ただしこの方法では、TurboIDが再構成した場所をビオチン化タンパク質を検出することでしか確認できないという欠点があった(ビオチン化されたタンパク質の拡散によってSplit-TurboIDが本当にMCS特異的に再構成したか判断が難しくなる)。そこで我々は、split-GFPとsplit-TurboIDをタンデムに融合した人工タンパク質を利用することで、GFPによるMCSの可視化と、TurboIDによるMCS局在タンパク質のビオチン化を同時に可能にした新たなMCS特異的近接ラベリング手法、CsFiND法 (Complementation assay using Fusion of split-GFP and TurboID) を開発した (Fujimoto et al. 2023)。Split-GFPとsplit-TurboIDをタンデムに融合したCsFiNDタンパク質をER膜とミトコンドリア外膜に発現させ蛍光顕微鏡で観察した(図3A)。その結果、Split-GFPを用いた場合と同様にドット状のGFPシグナルが生じ、このGFPシグナルが、ER-ミトコンドリア間MCSを形成するERMES複合体の構成因子Mmm1と共局在することを確認した(図3B)。この結果は、CsFiNDタンパク質が標的のMCSで再構成したことを示している。さらにCsFiNDタンパク質によってビオチン化されたタンパク質をストレプトアビジンビーズを用いて精製し、ウェスタンブロッティングで解析したところ、CsFiNDタンパク質自身に加え、ERMES複合体構成因子であるMmm1, Mdm12, Mdm34がビオチン化され、濃縮されていることがわかった(図5C)。LC-MSMS解析においても既知のMCSER-Mito局在因子であるLam5/6, Num1, Gem1, Fmp27といった因子が同定された。以上の結果から、CsFiNDがMCS局在タンパク質を探索するために有効の手法であることがわかった。

図5 MCS局在タンパク質の同定手法CsFiND、 (A) CsFiNDコンストラクト。ミトコンドリア外膜、ER膜局在化シグナルとしてそれぞれTom71, Ifa38を使用した。(B) (A)で示したCsFiNDタンパク質とMmm1-mScarletを発現する細胞を蛍光顕微鏡で観察した。Scale Bar, 5 µm、 (C) ビオチン存在下で培養したCsFiND発現細胞から調製した膜画分を可溶化後、ストレプトアビジンを用いてビオチン化タンパク質を精製した。精製したタンパク質をストレプトアビジンCy5 (SAv-Cy5)、CsFiNDタンパク質 (FLAG, V5)、ERMES構成因子 (ERMES)、ミトコンドリア外膜 (OMM)、ミトコンドリア内膜 (IMM)、ER膜 (ER) に局在するタンパク質に対する抗体を用いて解析した。**はTom70抗体が認識したCsFiNDタンパク質 (Tom71-TurboID-N-V5-GFP11) を示す。Takeda-Kakimoto et al. (2022) より改変。
本総説は、日本植物学会第88回大会シンポジウム「植物/微生物/オルガネラの相互作用をイメージングで解き明かす」の講演内容に関連してまとめたものである。今回このような機会を下さったオーガナイザーの永田典子教授(日本女子大)、豊岡公徳博士(理研)に感謝いたします。