2023 年 5 巻 3-4 号 p. 119-123
2023 年 5 巻 3-4 号 p. 119-123
神経性やせ症(anorexia nervosa;以下,ANと略)では,様々な臓器障害を合併し,治療に難渋する.今回,重症AN治療中,血清リン値の激減により心停止となった症例を経験した.症例は19歳,女性.AN治療中,意識障害となり,前医より転院となった.来院時,body mass index:10.7 kg/m2とるい痩著明,ショック状態であり,輸液,カテコラミン投与を行った.Refeeding syndromeの高リスクであったが,低血糖と肝機能障害があり,糖質投与にて予定とした初期エネルギー投与より増加した.血清リン値は正常であったが,翌日に激減し,心停止となった.以後,リンの補充を行い,循環は安定した.本症例のように低血糖があるANでは,ある一定以上のエネルギー投与は避けられず,血清リン値が激減する可能性があり,血清リン値が正常であっても,再栄養開始とともに頻回に血清リン値を測定し,リン製剤の補充のタイミングを逸さないことが重要である.
神経性やせ症(anorexia nervosa;以下,ANと略)は,極度の栄養不足と脱水,電解質異常から,様々な臓器障害を合併する.中でも,refeeding syndrome(以下,RSと略)は,低リン血症を背景に多臓器不全を合併し,突然死を招くことがある.RSの予防には,初期エネルギー投与を低くし,緩徐に増量し,同時に,電解質補充を行うことが推奨されている1).今回,低血糖を伴った重症AN治療中,血清リン値の低下が心停止の一因と考えられた症例を経験したので報告する.なお,症例報告にあたり,個人情報保護法に基づき匿名化し,患者様御本人・御家族に同意を得た.
19歳,女性
1. 現病歴2020年7月よりダイエットを始め,4カ月後には17 kg減量し,体重31 kgとなった.翌月には体重29 kgで体動困難となり,ANにて前医入院となった.前医では,経口摂取,補液(420 kcal/day)にて栄養管理をされていたが,実際には摂取しておらず,「やせているとは思わない.骨盤がはっきり見える方が綺麗」といった発言があった.入院1カ月後,意識障害にて当院搬送となった.
2. 既往歴なし
3. 現症身長162 cm,体重28 kg,body mass index(以下,BMIと略):10.7 kg/m2
GCS6(E1V1M4),瞳孔(R/L):3 mm/3 mm,対光反射(R/L):+/+
呼吸数16回/分,SpO2(room)99%
脈拍数40回/分,血圧測定不能,総頸動脈触知可
体温(腋窩温)36.1°C
4. 入院時検査所見血液検査では,血小板低下,凝固能低下,BUN/Cr上昇,肝逸脱酵素上昇,コリンエステラーゼ低下,低血糖,中性脂肪低下,Low T3を呈していた(表1).心電図は補充調律であった(図1).心臓超音波検査(目視)では,全周性に左室壁運動は低下し,ejection fraction(以下,EFと略)40%程度であった.
| Complete blood cell count | Biochemistry | ||||
| WBC | 4,470/μL | TP | 5.4 g/dL | T-Cho | 187 mg/dL |
| RBC | 394 × 104/μL | Alb | 3.4 g/dL | LDL-C | 69.1 mg/dL |
| Hb | 11.3 g/dL | T-Bil | 2.0 mg/dL | TG | 8 mg/dL |
| Ht | 34% | GOT | 1,132 U/L | ||
| Plt | 9.7 × 104/μL | GPT | 814 U/L | Blood gas analsis | |
| CHE | 138 U/L | pH | 7.435 | ||
| Coagulation | CK | 182 U/L | PaCO2 | 37.9 mmHg | |
| PT% | 30% | BUN | 42.5 mg/dL | PaO2 | 195.3 mmHg |
| PT-INR | 2.49 | Cr | 0.47 mg/dL | HCO3– | 24.9 mmol/L |
| APTT | 42.6 sec | Na | 143 mmol/L | BE | 0.8 mmol/L |
| FDP | 4.5 μg/mL | K | 4.1 mmol/L | Lactate | 13 mg/dL |
| ATIII | 76% | Cl | 105 mmol/L | ||
| Ca | 7.9 mg/dL | ||||
| Endocrine | P | 4.0 mg/dL | |||
| FT3 | 0.90 pg/mL | Mg | 2.1 mg/dL | ||
| FT4 | 1.02 ng/dL | NH3 | 52 μg/dL | ||
| TSH | 1.56 μU/mL | Glu | 46 mg/dL | ||
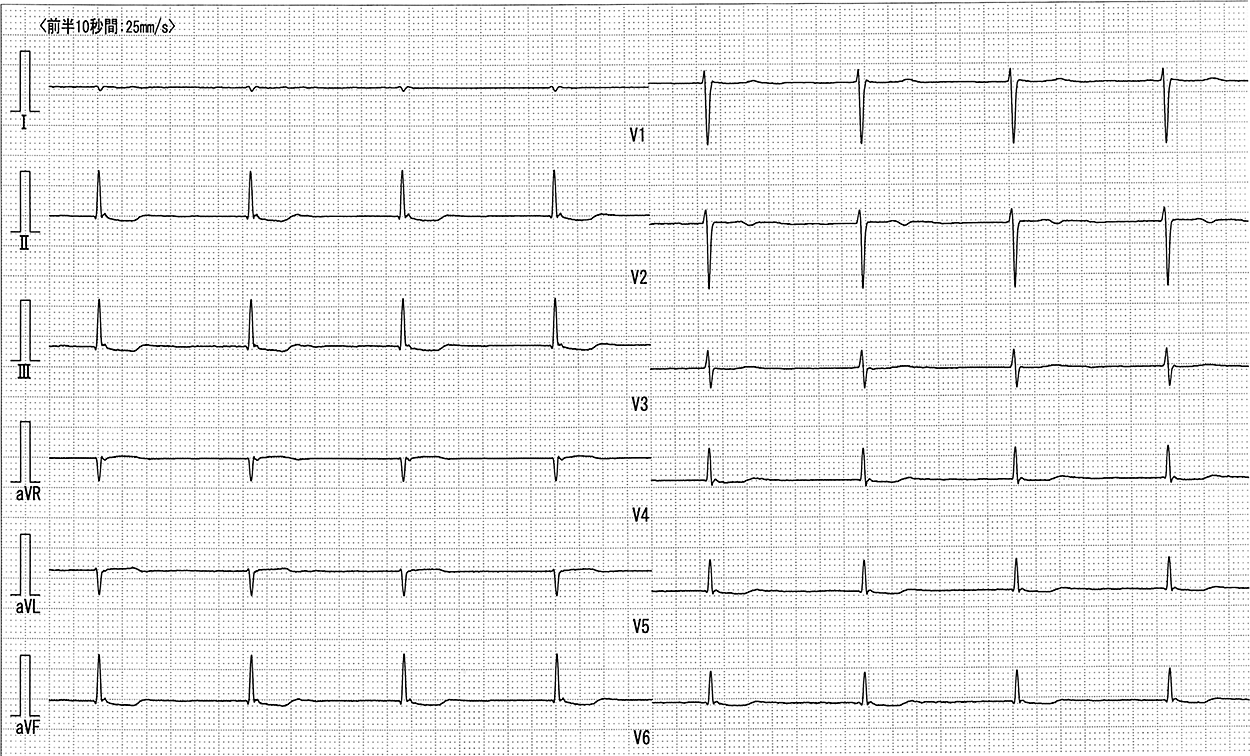
脈拍数47回,補充調律が見られる.
初療時,脱水と心機能低下によるショックと考え,輸液,ノルアドレナリン0.05 μg/kg/minより開始した.低血糖に対して,ブドウ糖とリン酸チアミンジスルフィド100 mgを投与した.ICU入室後は,RS予防目的に,現体重を基本に初期エネルギー量を280 kcal/day(10 kcal/kg/day)とし,ビタミンB1(フルスルチアミン塩酸塩1,500 mg/day)投与を行う予定としたが,肝機能障害があり,糖質を含む輸液を行い,投与エネルギー量は490 kcal/day(17.5 kcal/kg/day)と予定より増加した.血清リン値は4.0 mg/dLであり,リンの投与は行わなかった.第1病日,ノルアドレナリン0.1 μg/kg/minで血圧80/40 mmHg程度で経過した.血糖補正後も意識障害は遷延した.血液ガスにてカリウム3.1 mmol/Lと低下していたため,塩化カリウム製剤を投与した.第2病日,血液検査で血清カリウム3.5 mmol/L,血清マグネシウム2.0 mg/dLであったが,血清リン1.6 mg/dLと低下していた.心臓超音波検査では,EF25%と低下し,心尖部から中部にかけて高度な低収縮が見られ,たこつぼに類似する形態であった.心電図ではV2-5誘導でJ波が見られた(図2).当日,pulseless VTとなり,心肺蘇生術にて約30分後に心拍再開した.心停止直前の血液ガス検査では,pH 7.470,乳酸 17 mg/dL,カリウム3.5 mmol/L,血糖206 mg/dLであった.急激な血清リンの低下による心停止が考えられ,リン酸水素ナトリウム製剤の補充を行い,循環は安定し,不整脈出現もなかった(図3).入院後,低血糖性脳症,急激なリンの低下,心停止後症候群によると思われる意識障害が遷延したが,第30病日には意識清明となった.栄養療法,リハビリテーションを継続し,第135病日,精神科的加療目的で転院となった.
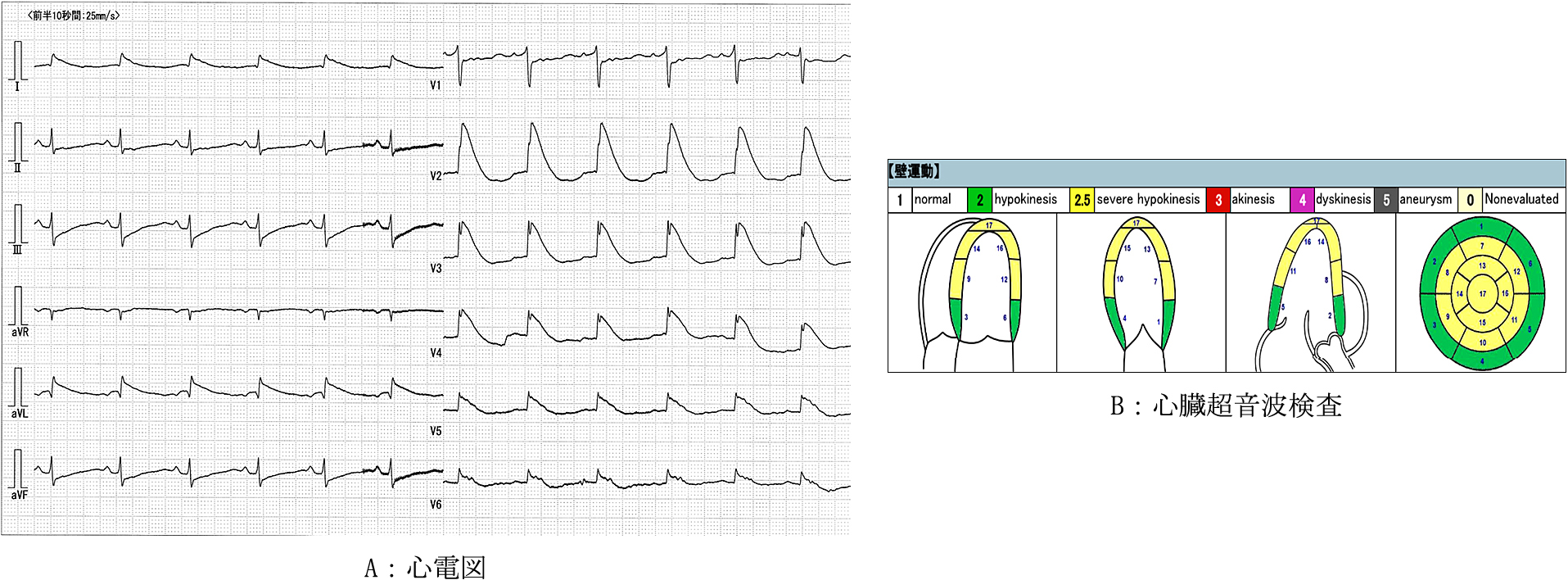
A:心電図 V2–5にかけてJ波が見られる.
B:心臓超音波検査 心基部以外の壁運動は高度に低下している.
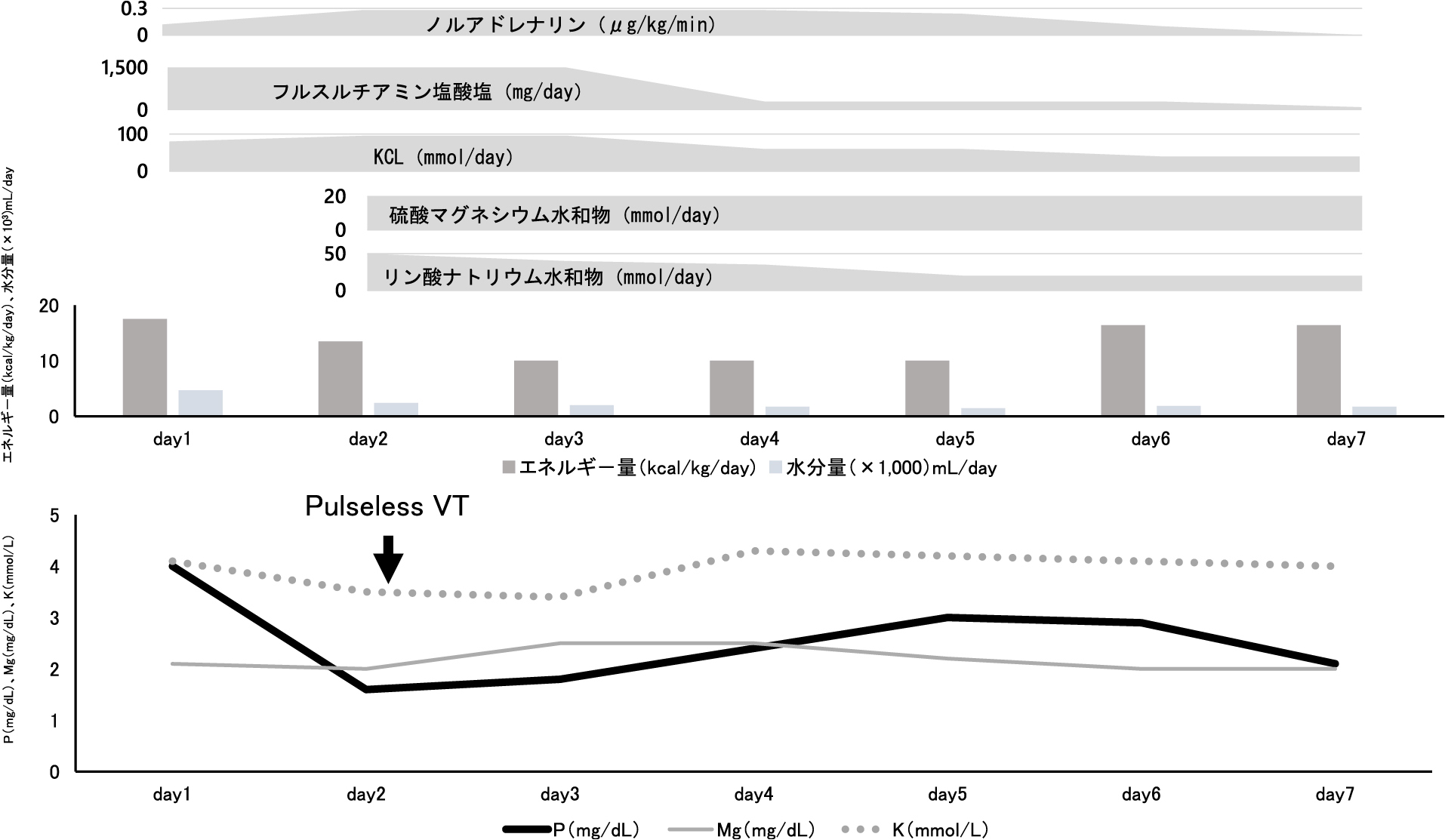
第2病日,血清リン1.6 mg/dLまで激減し,同日にはpulseless VTとなった.
ANでは,脱水に加え,心容積減少,左室心筋重量低下などのsmall heartやlow T3症候群が合併し,心拍出量低下による徐脈と低血圧を示すことが多い.本症例も同様であった.
ANでの全身管理では,RS予防を念頭におく必要がある.RSとは,血清リン,カリウム,マグネシウム値のいずれかが栄養開始や増量から5日以内に10%以上減少したものと定義され,重症度が分類されている2).本症例では,前医よりエネルギー投与が増加し,2日目に血清リン値が60%低下しており,重症RSであった.
RS予防には,初期エネルギー量を10 kcal/kg/day以下から開始し,徐々に増量し,電解質補充を並行すべきとされるが,BMI <14 kg/m2といった超高リスクでは5 kcal/kg/dayを上限に開始するとされる1).本症例は,超高リスクであったが,入院時,低血糖,肝機能障害があり,糖質を含む輸液を行い,初期エネルギー投与が予定より増加する結果となった.
RS予防には,リンの補充も重要である.RSの症状は血清リン値が1.0 mg/dL以下でなければ明確に出現しない3)とされるが,リンの絶対値よりも急激な低下が神経症状を引き起こすとも報告4)されており,神経症状以外でも同様の可能性はある.RSでは,低リン血症,低カリウム血症,低マグネシウム血症やビタミンB1欠乏症が出現し,心収縮力低下から心不全や致死的不整脈を併発することがある.本症例では心停止直前,血清カリウムは3.5 mmol/Lであり,心停止の原因としては否定的であった.ビタミンB1は未測定だが,乳酸値の上昇はなく,入院時よりビタミンB1投与を継続しており,ビタミンB1欠乏症も否定的であった.一方,血清リン値は低下していた.同日の心臓超音波検査でEFはさらに低下し,たこつぼに類似した形態であり,心電図ではJ波が見られた.たこつぼ症候群の心電図でのJ波の存在は,急性期に見られ,心室性不整脈や心停止の指標となるとされ,心筋虚血によると考えられている5).血清リン≤2.5 mg/dLの低リン血症を対象とした研究では,心疾患がないにも関わらず心室性不整脈が見られ,低リン血症は著しい左室機能障害と関連し,うっ血性心筋症を引き起こす可能性があるとしている6).低リン血症は,細胞内のアデノシン三リン酸(adenosine triphosphate;以下,ATPと略)低下とそれに伴う心筋障害を引き起こすとされる7).リンは2,3-diphosphoglycerate(以下,2,3-DPGと略)の構成成分であり,低リン血症により2,3-DPGが不足し,ヘモグロビンから酸素の放出が抑制される.本症例では,低栄養による心機能低下と血清リン値の低下での2,3-DPGやATP不足による心筋への酸素供給低下が重なり,心停止になったと推察された.
RSの高リスクでの,再栄養前の電解質が正常の場合,電解質の予防的投与は推奨されていない2).今回,入院時の血清リン値は正常であり,予防的なリンの投与は行わなかった.一方,再栄養前の血漿濃度が高値であっても,予防投与はすべきとの報告もある8).RS予防には,頻回の血清リン値の測定とリンの補充が重要であるが,本症例のように,低血糖を伴ったANでは,血清リン値が正常であっても,再栄養開始とともに,少なくとも,1日2回(午前1回,午後1回)は血清リン値を測定し,リン製剤の補充のタイミングを逸さないことが重要である.
低血糖を伴うANの場合,ある一定以上のエネルギー投与は必須であるが,血清リン値の低下により致死的病態を招く可能性がある.低血糖を伴うANでは,血清リン値が正常であっても,再栄養開始とともに頻回に血清リン値を測定し,リン製剤の補充のタイミングを逸さないことが重要である.
本論文に関する著者の利益相反なし