2015 年 32 巻 2 号 p. 86-90
2015 年 32 巻 2 号 p. 86-90
進行・再発HER2陽性乳癌に対してトラスツズマブとは異なるHER2タンパクに結合するペルツズマブ,トラスツズマブに抗癌剤の一種であるDM1を結合したT-DM1が使用可能となった。ペルツズマブは1次治療を対象としたトラスツズマブ,ドセタキセル併用療法に加えることにより,PFS(progression free survival),OS(overall survival)ともに延長した。現在,このトラスツズマブ,ペルツズマブ,タキサン治療が進行・再発HER2陽性乳癌の1次治療として推奨される。T-DM1についてはトラスツズマブ,タキサンの治療歴を有する再発乳癌患者を対象にラパチニブ,カペシタビン併用療法と比較した試験でPFS,OSともに延長したことから2次治療以降で使用されるべき薬剤と考えられる。
両薬剤とも術前,術後治療などの試験が進行中である。
HER2タンパクは細胞膜上の受容体型増殖因子であり,HER2過剰発現乳癌は乳癌全体の20~25%を占め,予後が悪いことが1987年に報告された。このHER2をターゲットに設計されたヒト化抗体薬トラスツズマブはHER2陽性乳癌の予後を劇的に改善した。これは乳癌のみならず癌治療の新しい時代の到来を示す出来事であった。2013年6月にトラスツズマブとはHER2タンパクの違う部位に結合するヒト化抗体薬であるペルツズマブをトラスツズマブに併用することによりHER2陽性進行・再発乳癌において著明に無増悪生存期間を延長し認可された。さらに今年トラスツズマブにチュブリン阻害剤を結合したT-DM1が使用できるようになった。治療選択肢が増え,臨床現場ではこれら抗HER2薬をどのように用いていったらいいか混乱も予想される。そこで本項では最近使用可能となったペルツズマブとT-DM1についてまとめた。
トラスツズマブと同じヒト化モノクローナル抗体であり,分子量,構成アミノ酸数はトラスツズマブと同じであるがHER2タンパクへの結合部位がトラスツズマブとは異なる。トラスツズマブと同様に,抗体依存性細胞介在性細胞障害作用(antibody-dependent cellular cytotoxicity:ADCC)や補体依存性細胞障害作用(complement-dependent cytotoxicity:CDC)がある。トラスツズマブがHER2タンパクの細胞外ドメインのアンカー部分(ドメインⅣ)に結合するためHER2のダイマー形成を阻害できず耐性に関与している可能性がある。ペルツズマブはダイマー形成の際の結合部位(ドメインⅡ)を認識し結合するためダイマー形成を阻害することができる[1]。HER2陽性の再発・進行乳癌の1次治療としてドセタキセルとトラスツズマブ併用療法にさらにペルツズマブとプラセボを追加比較する第Ⅲ相試験(CLEOPATRA試験)においてペルツズマブ追加でPFS(progression free survival)を有意に延長した[2](図1)。2013年6月下旬に本邦でも認可され,1次治療での使用でOS(overall survival)を15.7カ月延長したことから[3],今後1次治療ではタキサンとともに使用されるべき抗HER2療法と思われる。抗癌剤との併用効果については今のところタキサンのデータしかないが,他の薬剤についてはいくつかの試験が進行中である。トラスツズマブとペルツズマブを使用して進行した症例(beyond PD症例)にトラスツズマブにペルツズマブを継続して抗癌剤を変更した方がいいかどうかは不明である。

抗癌剤を併用しないトラスツズマブ,ペルツズマブのみの治療効果はトラスツズマブ,タキサン併用の治療での進行症例で奏効が24%,クリニカルベネフィット率が50%,PFSの中央値が24週と報告されている[4]。ペルツズマブがトラスツズマブ耐性の一部を克服しているのは確実である。本邦では保険診療上は抗癌剤との併用が必要とされているがトラスツズマブ,ペルツズマブのみでも一定の効果は期待できる。前述のCLEOPATRA試験でも両群ともドセタキセルは平均8サイクル(約6カ月)で終了していたがトラスツズマブ,ペルツズマブ併用群ではPFSの中央値が約18カ月であったことから約12カ月はトラスツズマブとペルツズマブのみで進行を抑制していたことになる。
トラスツズマブ,ペルツズマブ併用は術前治療としても検討されている。ランダム化第Ⅱ相臨床試験であるNeoSphere試験において,HER2陽性乳癌の術前療法として,トラスツズマブ+ドセタキセル群,ペルツズマブ+トラスツズマブ+ドセタキセル群,ペルツズマブ+トラスツズマブ群,ペルツズマブ+ドセタキセル群の4群に無作為に割り付けられた。主要評価項目として手術時のpCR(病理学的完全奏効)率が比較検討された。トラスツズマブ+ドセタキセル群29.0%,ペルツズマブ+トラスツズマブ+ドセタキセル群45.8%,ペルツズマブ+トラスツズマブ群16.8%,ペルツズマブ+ドセタキセル群24.0%であり,トラスツズマブ+ドセタキセルにペルツズマブを上乗せすることで統計学的に有意にpCR率が改善した[5]。このことからHER2陽性早期乳癌に対して術前のペルツズマブ併用がアメリカ食品医薬品局(FDA;Food and Drug Administration)から認可されている。この試験ではドセタキセルを含まないペルツズマブ+トラスツズマブ群でも16.8%でpCRが得られており,抗癌剤を含まない分子標的治療のみでの治療を模索する試みとして興味が持たれる。TRYPHAENA試験も無作為化試験で,HER2陽性の局所進行型乳癌,早期乳癌の患者225人に対してトラスツズマブ+ペルツズマブ+アントラサイクリン系化学療法薬を3サイクル投与後,4~6サイクルにはペルツズマブ+トラスツズマブ+ドセタキセルを投与する群(Arm A),アントラサイクリン系化学療法薬を3サイクル投与後、4~6サイクルにはペルツズマブ+トラスツズマブ+ドセタキセルを投与する群(Arm B),ペルツズマブ+トラスツズマブ+ドセタキセル+カルボプラチンを6サイクル投与する群(Arm C)に割り付けた。pCR率は副次評価項目(主要評価項目は心臓に対する安全性)であったが,Arm Aが61.6%,Arm Bは57.3%,Arm Cは66.2%といずれの群も高いpCR率を達成していた[6]。
ペルツズマブはHER2のホモダイマー,ヘテロダイマー形成を阻害することができると考えられているが,ペルツズマブ単剤ではあまり効果なく,トラスツズマブとの併用が必要である[7]。これについてはペルツズマブがリガンドに依存する(ligand-dependent)HER2-HER3のヘテロダイマーを阻害するのに対してトラスツズマブはリガンドに依存しない(ligand-independent)HER2-HER3のヘテロダイマーを阻害するためと考えられている[8]。HER3のリガンドとしてヘレグリンがあるが今まではHER3にヘレグリンが結合して初めてHER2とのヘテロダイマーを形成できるとされていたが,HER3はリガンドが結合していない状態でもHER2とのヘテロダイマーが形成でき,下流にシグナル(主にPI3K-AKTシグナル)を送ることができると考えられている。このためリガンドに依存するヘテロダイマーのみペルツズマブで阻害しても効果があまりなくリガンドに依存しないヘテロダイマーを阻害するトラスツズマブが必要と考えられている。
術後療法でのペルツズマブ併用の有効性を探るAPHINITY試験(表1)が本邦も含めグローバルで行われ,結果を待っている状況である。
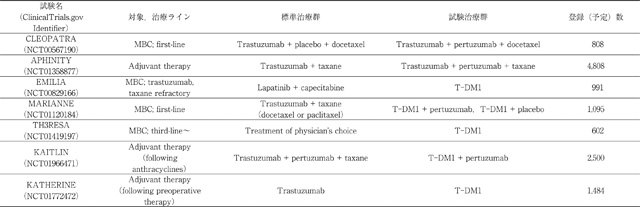
HER2陽性乳癌を対象にしたペルツズマブ,T-DM1を用いた第Ⅲ相試験
トラスツズマブに微小管重合阻害剤であるDM1(メイタンシン誘導体)をリンカーで化学結合した分子標的治療薬である。メイタンシンは強力な細胞障害活性を有していたが副作用の面から臨床的には不適とされていた。トラスツズマブと結合させることにより腫瘍選択的に投与することが可能となった。T-DM1一分子あたりDM1が平均3.5個結合されている。T-DM1もトラスツズマブ同様にADCCやシグナル伝達阻害作用があるとされている。また,HER2と結合することで腫瘍細胞内に取り込まれ,リソゾームで分解されることによりDM1が放出されアポトーシスを誘導する。主な有害事象としては血小板減少と全身倦怠感,肝機能異常である。血小板減少はT-DM1が多核巨細胞と結合することにより誘導される。
トラスツズマブ,タキサンの治療歴を有する再発乳癌患者を対象にT-DM1単剤とラパチニブ,カペシタビン併用療法を比較したEMILIA試験では有意にPFS,OSともにT-DM1が有意に優れていた[9](図2)。従って現状では進行・再発HER2陽性乳癌の1次治療としてトラスツズマブ,ペルツズマブ,タキサンの併用療法,2次治療としてはT-DM1が推奨され,ラパチニブ,カペシタビン併用療法は3次治療以降に推奨される治療と考えられる。進行・再発HER2陽性乳癌の1次治療でトラスツズマブ,ドセタキセル併用療法とT-DM1を比較した第Ⅱ相試験ではPFS,全奏効期間はT-DM1の方が有意に良好な成績であった[10]。抗HER2療法の前治療歴のある3次治療以降の再発乳癌患者を対象にしたTH3RESA試験でも主治医選択治療に比べ優れていたことから今後,頻用されると考える[11]。しかし,HER2陽性進行・再発症例の1次治療でのペルツズマブとの併用を検討したMARIANNE試験ではトラスツズマブとドセタキセルの併用群,T-DM1単剤群,T-DM1とペルツズマブ併用群で主要評価項目のPFSで差がなかったことがプレスリリースされた。詳細は今年のASCO年次総会で発表される見込みである。T-DM1にペルツズマブを加えても効果を改善しなかったことについては不明であるが,培養細胞を用いたin vitroの研究ではペルツズマブがT-DM1に対してアンタゴニストとして作用するといった発表が2014年のサンアントニオ乳癌シンポジウムでされている[12]。今後のさらなる研究が待たれる。
T-DM1についても術後治療についてもいくつかの試験が行われている。術後で抗癌剤,トラスツズマブ,ペルツズマブ併用に対してT-DM1とペルツズマブ併用を比較するKeitlin試験(表1)は登録が終了している。術前に抗癌剤,トラスツズマブ療法を行い術後に腫瘍が遺残した症例に対してトラスツズマブとT-DM1を比較するKatherine試験も進行中である。
臨床現場ではトラスツズマブ,ラパチニブ,ペルツズマブ,T-DM1といった抗HER2薬が使えるようになった。臨床医としては乳癌が再発した患者さんもQOLを保って長く生きられるようにこれらの薬剤をうまく使って行く必要がある。海外ではこれら抗HER2薬を併用して抗癌剤を用いる試験も行われている。また,細胞内のシグナル伝達など基礎的な研究も急速に進歩し,細胞内シグナルを阻害する薬剤もできている。進行・再発乳癌は現在,根治が困難な疾患と考えられているが根治を目指した治療も模索されている。根治を目指した治療が最初に行われる乳癌のサブタイプはHER2陽性乳癌と私は考えている。