2019 年 36 巻 2 号 p. 90-95
2019 年 36 巻 2 号 p. 90-95
転移性乳癌における主たる目的は「生存期間の延長」と「QOL維持・改善」である。特に,エストロゲン受容体陽性転移・再発乳癌においては,化学療法に比べて,より副作用が軽微である内分泌療法を軸とした治療が基本とされてきた。しかし,昨今の臨床試験の結果からCDK4/6阻害薬・mTOR阻害薬といった分子標的薬との併用も重要な治療手段となっている。本項では,エストロゲン受容体陽性転移・再発乳癌に対する治療として,内分泌療法を中心に治療の基本的な方針について述べる。
転移・再発乳癌において,新規薬剤の開発がすすんだ昨今において再発後の生存期間は延長しているものの,治癒は困難であり,その主たる目的は「生存期間の延長」と「QOL維持・改善」である。このため,内分泌療法感受性がある場合はできるだけ副作用の少ない内分泌療法を軸とした治療を順次投与し,長期間,内分泌療法を継続することが肝要である。
内分泌療法の選択に関しては,治療効果予測因子であるエストロゲン受容体(ER),プロゲステロン受容体(PR),human epidermal growth factor receptor 2(HER2)の評価を必ず行うべきである。
原発巣と転移巣のER,PRを比較した研究では,ERは28.5%の患者で再発時に陰転下し,8.3%が陽転化,PRは35.7%の患者で陰転化,8.7%で陽転化していたとの報告もある[1]。また,同一症例内の転移巣2か所以上を生検し比較した研究では,全55症例のうち転移巣間でのサブタイプ不一致率はER/PR/HER2の順に10.9%/30.9%/3.6%であった[2]。このように転移再発治療に関しては,原発巣と転移巣のbiologyが少ないながらも変化していることがあるため,NCCNガイドラインにおいても初回再発は可能な限り再発巣に対して生検を行うよう記されている[3]。治療手段が限られるトリプルネガティブ乳癌の場合には,再発巣に対する生検を特に考慮することが勧められる。
薬剤選択は,再発時期や術後内分泌療法の種類によって決められる。American Society of Clinical Oncology(ASCO)ガイドラインでは,術後内分泌療法終了後12カ月以内の再発をその内分泌療法に対する耐性を有する症例と定義している[4]。European School of Oncology (ESO),European Society of Medical Oncology(ESMO)のガイドラインでは術後内分泌療法を開始して2年以内に再発した症例を「primary(de novo)endocrine resistance」,開始2年以降の再発を「secondary(acquired)endocrine resistance」と定義している[5]。一般的には再発時期が早い症例ほど内分泌療法に対する効果が低い可能性があり,術後内分泌療法中,もしくは内分泌療法終了から1年以内の再発例に対しては,術後内分泌療法とは異なる薬剤を選択する。
治療開始時には閉経状況を確認する必要がある。一般に閉経は下記のように定義される。
・60歳以上の女性
・60歳未満の場合
・両側卵巣摘出術を受けている。
・月経が自然に停止してから12カ月以上経過しており,病理学的原因および生物学的原因が他にない。
・化学療法後,またはTamoxifen,Toremifen投与中の症例においては血清エストロゲン値が閉経レベルになっていること。
転移再発乳癌に対する内分泌療法の適応は,内分泌療法感受性があり,かつ,life-threateningではないことである。
癌性リンパ管症などを有する場合は,より早急に効果を得る必要があるため内分泌感受性がある症例においても化学療法のよい適応となる。また,化学療法の効果が得られた症例に対して,内分泌療法による維持療法を継続することにより化学療法継続よりもQOLの改善は期待できる。ESO,ESMOのガイドラインでは「化学療法後の内分泌療法による維持療法は,ランダム化比較試験での評価はなされていないが妥当な選択肢である」と記載されている[4]。また,後方視的研究であるが,一次化学療法で奏効または病勢安定が得られたER陽性転移再発乳癌500例を対象としては解析では,内分泌療法により維持療法が施行されなかった252例に比べて,内分泌療法による維持療法が施行された308例で無増悪生存期間や全生存期間が優れていたという報告がある[6]。
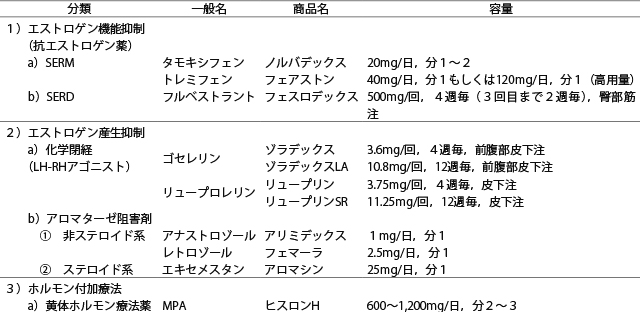
乳癌の内分泌療法薬
エストロゲン機能抑制には選択的エストロゲン受容体モジュレーター(selective estrogen receptor modulator:SERM)と選択的エストロゲン受容体ダウンレギュレーター(elective estrogen receptor downregulator:SERD)がある。SERMはERにエストロゲンと競合的に結合し,エストロゲンがERに結合することを阻害することによりエストロゲンの作用を抑制する。これに対してSERDは標的組織においてERの分解を促進し,ERを介した作用をブロックすることによりエストロゲンの作用を抑制する。
(2)エストロゲン産生抑制閉経前乳癌に対してはエストロゲン産生源である卵巣の機能を抑えることは有効な治療法の一つである。卵巣摘出のほか,薬物療法としてゴセレリンやリュープロレリンなどのLH-RHアゴニストが用いられる。LH-RHアゴニストはLH-RHの類似物質であり,高濃度で連続投与することにより下垂体のLH-RH受容体と持続的に結合し,非結合型の受容体を抑制させる。このためLH,FSHの分泌が抑制され,卵巣からのエストロゲン分泌が低下し,無月経状態となり,血中のエストロゲン濃度は閉経後と同等となる。
閉経後におけるエストロゲン産生の最も重要な因子はアロマターゼであり,この酵素の働きを抑制することによりエストロゲン産生を抑える。アロマターゼ阻害薬(AI)はその化学構造およびアロマターゼに対する薬理作用に基づき,非ステロイド系とステロイド系に分類される。アナストロゾールやレトロゾールなどの非ステロイド系AIはアロマターゼのチトクロムP-450に結合し,その酵素活性を阻害する。このチトクロムP-450との結合は可逆的である。これに対して,エキセメスタンはアロマターゼの基質結合ポケットに結合し,アンドロステンジオンなどの基質がこのポケットに結合し,エストロゲンへ変換することを阻害する。この基質結合ポケットとの結合は非可逆的である。これらの薬剤はアロマターゼ活性を95%以上阻害し末梢エストロゲン濃度を80%以上低下させることができる。
(3)ホルモン付加療法合成黄体ホルモン薬である酢酸メドロキシプロゲステロン(MPA)の作用機序は十分解明されていないが,治療用量のMPAにより副腎皮質ステロイドの合成を抑制し,血中エストロゲン濃度を低下させる。また,内分泌作用以外にも,乳癌細胞に対する直接的な抗腫瘍効果や血管新生抑制作用なども有する。
エチニルエストラジオールは,本邦では閉経後の末期乳癌に適応がある。長期エストロゲン枯渇状態にある乳癌細胞は通常量のエストロゲン刺激でアポトーシスに誘導できることが基礎研究で示されており[7],AI使用後の治療,および長期エストロゲン枯渇後の耐性獲得例への耐性克服薬としての意義が再検討されている。
(4)分子標的薬内分泌療法の耐性機序には数々の分子機構が関与しており,その分子を標的とした分子標的薬が多数開発されている。内分泌療法とこれら分子標的薬を併用することにより内分泌療法単剤に比し良好な結果が得られている。
内分泌療法の耐性機序の一つにPI3K/Akt/mTORシグナル伝達経路の活性化がある。mTORはPI3キナーゼ系のkey moleculeでAktの下流にあるセリン・スレオニンキナーゼであり,細胞の生存や増殖に深く関与している。また,ERやERの転写共益因子のリン酸化を介してER転写亢進にも関与している。一方,膜型ERはPI3K系やMAPK系などのシグナル伝達経路を活性化することができ,両者の間にクロストークが存在する。このクロストークを遮断するmTOR阻害薬と内分泌療法薬との併用療法がアロマターゼ阻害薬抵抗性乳がんに対して有用であることが示されている。
CDK4/6阻害薬(palbociclib,abemaciclib)に関しては別項を参照していただきたい。
一次治療は前述の通り,術後内分泌療法の実施の有無とその最終投与から再発までの期間に基づいて行われる。日本乳癌学会 乳癌診療ガイドラインでは,AI単剤,AIとCDK4/6併用,フルベストラント(FUL)(500mg)のいずれも強く推奨されている。その使い分けに関しては,現在のところ明らかなバイオマーカーや臨床学的因子はなく,議論の分かれるところである。それぞれの薬剤の特徴を理解し,患者希望,病勢を勘案して薬剤選択が行われる(図1)。
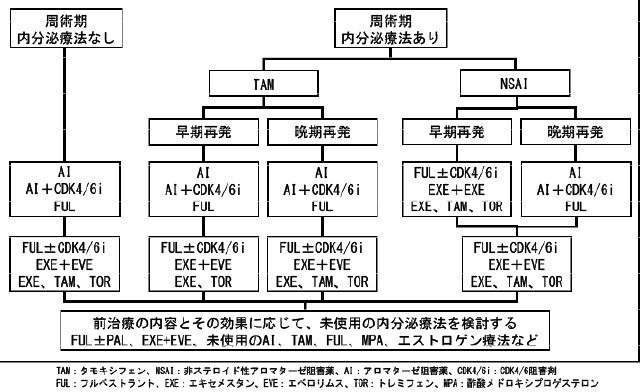
閉経後ホルモン受容体陽性転移・再発乳癌の内分泌療法のフローチャート(ASCO型)
二次治療は図1に示す通り,FUL±CDK4/6阻害薬,エべロリムスとEXE併用療法,TAM,TORなどその選択肢は多岐にわたる。一次内分泌療法で用いた薬剤,奏効期間によって選択されるべきである。
三次治療として内分泌療法単独で,Best Supportive Care,化学療法と比較して優位に成績が改善した治療は存在しない。しかし,前治療の内分泌療法への反応性や,有害事象とのバランスを考慮したうえで,一次もしくは二次治療に使用されていない内分泌療法は選択肢となりうる。このようなlate-lineの薬剤としてMPA,トレミフェン,低用量エストロゲン療法などがある。
(1)アロマターゼ阻害薬(AI)AI単剤は,AI+CDK4/6阻害薬との併用療法やFLU単独療法に比べProgression free survival(PFS)は劣るものの,経口投与である点,有害事象が軽微である点を鑑みた場合,一次治療の選択肢となりうる。この場合,AI単剤におけるPFSは表2の示すように13.8~14.7カ月と見込まれる[8~10]。

閉経後,転移・再発乳癌の一次内分泌療法の比較試験
また,AIには3剤(レトロゾール(LET),アナストロゾール(ANA),エキセメスタン(EXE))あるものの,臨床的効果に関して3剤に相違はないことが明らかになっている[11]。
(2)内分泌療法とCDK4/6阻害薬の併用療法CDK4/6阻害薬に関しては別項を参照して頂きたい。
(3)フルベストラント(500mg)(FUL)FALCON試験において進行再発乳癌に対する一次治療として,FULとANAの比較試験が行われている。平均観察期間25カ月の時点で,PFSは16.6カ月vs13.8カ月とFULが優っていた(HR for progression or death 0.80,95%CI:0.637~0.999)。特に,肺・肝への転移がない症例に関しては22.3カ月vs13.8カ月とその差は著明であった[10]。
また,FULはAI耐性後の2次治療として選択される薬剤の一つと考えられるが,一次治療にCDK4/6阻害薬が併用されていない場合は,併用療法が選択されるべきである。二次治療としてのFUL単剤療法(一部に閉経前症例を含む)のPFSは,表3の通り3.8~9.3カ月と報告されている[12~14]。
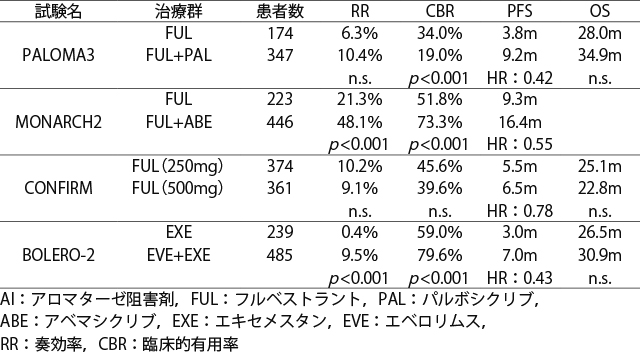
閉経後AI耐性,転移・再発乳癌の二次内分泌療法の比較試験
BOLERO-2試験[15~17]において,非ステロイド性AI既治療例の2次治療以降の内分泌療法として,EVEとEXEの併用療法と,EXE単独療法が比較されている。この結果,併用療法はPFSを有意に延長(7カ月vs3カ月,HR:0.43, 95%CI:0.35~0.54)した。また,臨床的奏効率も併用療法が有意に良好(9.5% vs 0.4%)であった。しかし,最終解析ではOS中央値は併用群30.9カ月,単独群は26.5カ月であり,併用療法により有意な延長は認めなかった。
閉経前ホルモン受容体陽性転移・再発乳癌に対する一次治療は,下記の通り,卵巣機能抑制(LH-RHアゴニスト(LH-RHa),両側卵巣摘出術)とタモキシフェンの併用療法が第一選択となる。
二次治療として質の高いランダム化比較試験はPALOMA-3試験とMONARCH 2試験があり,LH-RHa,FUL,CDK4/6阻害薬の3剤の併用療法が勧められる。
その他には卵巣機能抑制(LH-RHa,両側卵巣摘出術など)を行い,AIなどの閉経後に用いる内分泌療法薬との併用も候補となる。欧米のガイドラインでは閉経前のホルモン受容体陽性転移・再発乳癌に対してはまず卵巣機能抑制を行い,閉経後と同様の治療を行うように推奨している[18~20]。
(1)LH-RHアゴニストとタモキシフェン併用療法閉経前ホルモン受容体陽性転移・再発乳癌に対する一次内分泌療法としてタモキシフェン(TAM),卵巣機能抑制,およびその両者併用の治療法を比較した小規模のランダム化比較試験やそれらのメタアナリシスが行われている。
LH-RHa単独,TAM単独およびその両者併用とのランダム化比較試験(n=161)において,両者併用が各単独投与に比べ生存期間の有意な延長を示した(生存期間中央値:2.5年,2.9年,3.7年;ハザード比(HR):LH-RHa vs 併用,1.95,95%CI:1.23~3.10;TAM vs 併用:1.63,95%CI:1.03~2.59)[21]。
また,LH-RHaとTAMの併用とLH-RHa単独を比較した4試験のランダム化比較試験のメタアナリシス(n=506)では両者併用において生存期間の延長を認めた(生存期間中央値:2.5年vs 2.9年;HR:0.78,95%CI:0.63~0.96)[22]。
以上の結果から閉経前ホルモン受容体陽性転移・再発乳癌に対する一次内分泌療法としては,卵巣機能抑制(LH-RHa,両側卵巣摘出術)とTAM併用療法が第一選択となる。
CDK4/6阻害薬の登場によりホルモン受容体陽性転移・再発乳癌に対する治療は大きく変化した。しかし,CDK4/6阻害薬の効果を予測する明らかな因子が分かっていないこと,どのlineで使用するのが最も効果的であるのか,さらにはCDK4/6阻害薬耐性となった後の内分泌療法の効果など不明な点が山積している。
また,PI3K阻害薬,HDAC阻害薬など新たな分子標的薬の登場も期待されており,これら分子標的薬と内分泌療法をどのように使用していくのか,これからの課題となる。