2024 年 73 巻 2 号 p. 278-284
2024 年 73 巻 2 号 p. 278-284
全自動血液凝固測定装置CN-6500(シスメックス株式会社)(以下,CN-6500)は,凝固線溶系分子マーカー項目の測定機構を兼ね備えた機器である。今回,CN-6500を用いた凝固線溶系分子マーカーのトロンビン-アンチトロンビンIII複合体(TAT),プラスミン-α2プラスミンインヒビター複合体(PIC)と組織型プラスミノゲンアクチベータ・プラスミノゲンアクチベータインヒビター1複合体(tPAI-C)の基礎的性能評価を行った。評価内容は,併行精度,室内再現精度,直線性,検出限界,干渉物質の影響,ビオチン添加試験,およびCN-6500とHISCL-5000(シスメックス株式会社)の相関とした。併行精度,室内再現精度,直線性評価と検出感度は3項目とも良好であった。溶血ヘモグロビン,ビリルビンCおよびF,乳びによる干渉物質の影響は認めなかった。しかし,3項目ともビオチンにより相対値 −10%以上の影響を認めた。対象機器間の相関性(HISCL-5000: x, CN-6500: y)は,TATがy = 1.013x − 0.269(r = 0.998),PICがy = 1.026x − 0.134(r = 0.998),tPAI-Cがy = 0.944x + 0.028(r = 0.999)と良好であった。ビオチンによる影響を一部認めたが,CN-6500は凝固線溶系分子マーカーの院内検査化に有用な装置であると考えられる。
The CN-6500 fully automated blood coagulation analyzer (CN-6500; Sysmex Corporation) is an instrument that combines a measurement for coagulation-fibrinolysis molecular markers. In this study, we evaluated the basic performance of the CN-6500 in measuring thrombin-antithrombin III complex (TAT), plasmin-α2 plasmin inhibitor complex (PIC), and tissue plasminogen activator-plasminogen activator inhibitor complex (tPAI-C), which are molecular markers of the coagulation-fibrinolysis. The evaluation included repeatability, reproducibility, linearity, limit of detection, influence of interfering substances, biotin addition test, and correlation evaluation between CN-6500 and HISCL-5000 (Sysmex Corporation). The results of repeatability, reproducibility, linearity and limit of detection were favorable. No influence of hemolytic hemoglobin, bilirubin C and F, or interfering substances was observed. However, the three subject items were affected by biotin as a relative value of −10% or more. The correlation between the instruments (HISCL-5000: x, CN-6500: y) was good for TAT (y = 1.013x − 0.269, r = 0.998), PIC (y = 1.026x − 0.134, r = 0.998) and tPAI-C (y = 0.944x + 0.028, r = 0.999). Although the biotin effect was partially observed, the CN-6500 is considered to be a useful analyser for in-hospital testing of molecular markers of the coagulation-fibrinolysis.
本邦において,血栓症は高齢化や生活習慣の欧米化に伴い近年増加傾向にある。とくに心筋梗塞,脳梗塞,肺血栓塞栓症(pulmonary thromboembolism; PTE)のように生命予後に関わる血栓性疾患は早期診断,早期治療が重要である。播種性血管内凝固症候群等の早期診断のために多数の凝固線溶系分子マーカーが開発され,血栓症やその他の病態診断にも応用されている。凝固・線溶系検査により,PTEや深部静脈血栓症(deep vein thrombosis; DVT)などの静脈血栓塞栓症(venous thromboembolism; VTE)の発症リスクを予測したり,血栓性素因を診断したりすることができる。凝固線溶系分子マーカーは,プラスミンを中心とした線溶系マーカーとトロンビンを中心とした凝固系マーカーとして区分することができる。線溶系マーカーであるプラスミン-α2プラスミンインヒビター複合体(plasmin-α2plasmin inhibitor complex; PIC)によりフィブリン分解能を把握することが可能であり,凝固系マーカーのトロンビン-アンチトロンビン複合体(thrombin-antithrombin complex; TAT)と比較することで,凝固線溶系異常を引き起こす病態を分類することが可能である1)。また,組織型プラスミノゲンアクチベータ・プラスミノゲンアクチベータインヒビター1複合体(tissue plasminogen activator-plasminogen activator inhibitor complex; tPAI-C)は血管内皮細胞の障害を示す指標として知られている2)。
従来の凝固測定装置では,凝固線溶系分子マーカーを測定することができず,全自動免疫測定装置による測定や外注委託検査で対応していた。そのため,凝固項目と凝固分子マーカー検査における作業効率が悪く,外注委託検査の場合,結果報告までに2~4日を要していた。シスメックス株式会社の全自動血液凝固測定装置CN-6500(以下,CN-6500)は,従来の凝固・線溶系項目に加えて,化学発光酵素免疫測定法(chemiluminescent enzyme immunoassay;CLEIA法)を用いた測定ユニットを搭載し,凝固線溶系分子マーカー項目の測定機構を兼ね備えた機器である。
今回,凝固線溶系分子マーカーの院内検査化の有用性評価としてCN-6500によるTAT,PICおよびtPAI-Cの基礎的性能評価を行った。
2022年10月から2023年6月に提出された入院及び外来患者30例の検査後3.2%クエン酸ナトリウム加残血漿を用いた。なお,本研究は岐阜大学医学部生命倫理委員会の承認を得て施行した(承認番号:2022-086)。
2. 使用機器および試薬検討機器は全自動凝固測定装置CN-6500(シスメックス株式会社)を用い,対照機器は全自動免疫測定装置HISCL-5000(シスメックス株式会社)を使用した。測定試薬は,HISCL TAT試薬,HISCL PIC試薬およびHISCL tPAI-C試薬(シスメックス株式会社)を用いた。併行精度と室内再現精度には,TATコントロール,PICコントロールおよびtPAI-Cコントロール(シスメックス株式会社)を用いた。干渉物質の影響評価には,干渉チェック・Aプラス(シスメックス株式会社)およびビオチン注1mg「フソー」(扶桑薬品株式会社)を用いた。
3. 方法 1) 併行精度・室内再現性度TAT,PICおよびtPAI-Cコントロール2濃度の各試料を10回連続測定して併行精度を検証した。また同じく,TAT,PICおよびtPAI-Cコントロール2濃度の試料を使用してそれぞれ2回連続測定を20日間行い,室内再現性度を検証した。
2) 直線性3濃度の高値試料として,TAT(87.2 ng/mL, 75.0 ng/mL, 98.2 ng/mL),PIC(38.2 μg/mL, 24.1 μg/mL, 31.1 μg/mL),tPAI-C(98.3 ng/mL, 61.3 ng/mL, 49.1 ng/mL)の各3濃度域を用いて,0濃度を含む6段階の希釈系列試料を作製し測定した。試料の希釈にはtPAI-Cのみ生理食塩水を用い,それ以外の2項目はHISCL検体希釈液(シスメックス株式会社)を用いた。
3) 検出限界正常血漿を用いて0濃度を含む7段階の希釈系列試料を作製して5回測定を行い,各濃度の測定平均値 ± 2.6SDと,他の希釈系列の測定平均値が重ならない最小濃度から検出限界を算出した。
4) 干渉物質の影響3.2%クエン酸ナトリウム加プール血漿と干渉チェック・Aプラス,ビオチン溶液を用いて,溶血ヘモグロビン,ビリルビンF,ビリルビンC,乳びとビオチン溶液の6段階希釈系列を作製した。干渉物質を含まない場合のブランクの測定値を100%としたときの相対値を用いて評価を行った。測定は各濃度2回連続測定を行った。干渉物質の影響評価時のブランクは干渉チェック・Aプラス同梱のブランクを使用した。ビオチンの影響評価時のブランクにはHISCL検体希釈液を使用した。
5) 相関性患者血漿30検体をCN-6500および対照装置のHISCL-5000で測定し,一次回帰式と相関係数を求めた。
TAT,PICおよびtPAI-Cコントロール2濃度を使用した併行精度の変動係数(coefficient of variation; CV)は,TATが1.73%および1.08%,PICが2.02%および1.28%,tPAI-Cが1.68%および2.48%であった(Table 1)。一方,室内再現性度におけるCVはTATが1.69%および2.45%,PICが2.51%および1.57%,tPAI-Cが2.38%および3.10%であった(Table 2)。
| 項目 | TAT(ng/mL) | PIC(μg/mL) | tPAI-C(ng/mL) | |||
|---|---|---|---|---|---|---|
| コントロール種別 | Low | High | Low | High | Low | High |
| 測定回数 | 10 | 10 | 10 | 10 | 10 | 10 |
| 平均値 | 9.87 | 39.59 | 2.12 | 7.34 | 5.21 | 19.28 |
| 標準偏差 | 0.170 | 0.428 | 0.043 | 0.094 | 0.088 | 0.478 |
| 変動係数(%) | 1.73 | 1.08 | 2.02 | 1.28 | 1.68 | 2.48 |
| 項目 | TAT(ng/mL) | PIC(μg/mL) | tPAI-C(ng/mL) | |||
|---|---|---|---|---|---|---|
| コントロール種別 | Low | High | Low | High | Low | High |
| 測定日数 | 20 | 20 | 20 | 20 | 20 | 20 |
| 平均値 | 9.55 | 35.58 | 2.36 | 8.08 | 3.99 | 14.92 |
| 標準偏差 | 0.162 | 0.873 | 0.059 | 0.127 | 0.095 | 0.463 |
| 変動係数(%) | 1.69 | 2.45 | 2.51 | 1.57 | 2.38 | 3.10 |
高値希釈直線性は,TATで98.2 ng/mL,PICで38.2 μg/mLおよびtPAI-Cで98.3 ng/mLまで良好であった(Figure 1)。

TAT(A),PIC(B),tPAI-C(C)の3濃度の高値試料による希釈直線性
検出限界は,TATで0.2 ng/mL,PICで0.015 μg/mL,tPAI-Cで0.35 ng/mLであった(Figure 2)。

正常血漿を用いてTAT(A),PIC(B),tPAI-C(C)の各濃度の測定平均値 ± 2.6SDと,他の希釈系列の測定平均値が重ならない最小濃度を検出限界とした。
溶血ヘモグロビン,乳び,ビリルビンCおよびFのいずれにおいてもTAT,PICおよびtPAI-Cの測定値に大きな影響は認められなかった(Table 3)。一方,ビオチン添加前濃度からTATがビオチン濃度83.3 ng/dLで−11.7%,PICがビオチン濃度2,500 ng/dLで −13.7%,tPAI-Cがビオチン濃度83.3ng/dLで−18.1%の相対変動率を認めた(Table 4, Figure 3)。
| 溶血ヘモグロビン濃度 (mg/dL) |
TAT | PIC | tPAI-C | |||
|---|---|---|---|---|---|---|
| 測定値(ng/mL) | 変動率(%) | 測定値(μg/mL) | 変動率(%) | 測定値(ng/mL) | 変動率(%) | |
| 500 | 25.7 | −1.5 | 4.9 | 4.3 | 16.5 | −6.3 |
| 400 | 25.7 | −1.5 | 5.0 | 6.4 | 16.3 | 7.3 |
| 300 | 25.5 | −2.3 | 4.9 | 4.3 | 16.8 | −4.6 |
| 200 | 25.9 | −0.8 | 5.0 | 6.4 | 17.0 | −3.4 |
| 100 | 26.3 | 0.8 | 4.9 | 4.3 | 17.6 | 0.0 |
| 0 | 26.1 | 0.0 | 4.7 | 0.0 | 17.6 | 0.0 |
| 濁度 (FTU) |
TAT | PIC | tPAI-C | |||
|---|---|---|---|---|---|---|
| 測定値(ng/mL) | 変動率(%) | 測定値(μg/mL) | 変動率(%) | 測定値(ng/mL) | 変動率(%) | |
| 7,800 | 26.1 | −6.1 | 4.7 | 0.0 | 18.2 | 0.6 |
| 6,240 | 26.7 | −4.0 | 4.9 | 4.3 | 17.6 | −2.8 |
| 4,680 | 27.3 | −1.8 | 4.9 | 4.3 | 17.9 | −1.1 |
| 3,120 | 27.2 | −2.2 | 4.8 | 2.1 | 17.9 | −1.1 |
| 1,560 | 27.6 | −0.7 | 4.8 | 2.1 | 18.1 | 0.0 |
| 0 | 27.8 | 0.0 | 4.7 | 0.0 | 18.1 | 0.0 |
| ビリルビンC濃度 (mg/dL) |
TAT | PIC | tPAI-C | |||
|---|---|---|---|---|---|---|
| 測定値(ng/mL) | 変動率(%) | 測定値(μg/mL) | 変動率(%) | 測定値(ng/mL) | 変動率(%) | |
| 20.4 | 24.3 | −7.6 | 7.0 | 1.4 | 18.7 | −2.6 |
| 16.32 | 24.7 | −6.1 | 6.9 | −1.4 | 18.6 | −3.1 |
| 12.24 | 25.1 | −4.6 | 7.0 | 1.4 | 19.0 | −1.0 |
| 8.16 | 25.7 | −2.3 | 6.8 | −1.4 | 18.6 | −3.1 |
| 4.08 | 25.5 | −3.0 | 6.9 | 0.0 | 18.6 | −3.1 |
| 0 | 26.3 | 0.0 | 6.9 | 0.0 | 19.2 | 0.0 |
| ビリルビンF濃度 (mg/dL) |
TAT | PIC | tPAI-C | |||
|---|---|---|---|---|---|---|
| 測定値(ng/mL) | 変動率(%) | 測定値(μg/mL) | 変動率(%) | 測定値(ng/mL) | 変動率(%) | |
| 20.4 | 28.4 | −8.7 | 7.6 | 8.6 | 20.3 | −2.9 |
| 16.32 | 29.5 | −5.1 | 7.6 | 8.6 | 20.3 | −2.9 |
| 12.24 | 30 | −3.5 | 7.6 | 8.6 | 20.2 | −3.4 |
| 8.16 | 28.8 | −7.4 | 7.4 | 5.7 | 20.1 | −3.8 |
| 4.08 | 30.1 | −3.2 | 7.2 | 2.9 | 20.3 | −2.9 |
| 0 | 31.1 | 0.0 | 7.0 | 0.0 | 20.9 | 0.0 |
| ビオチン濃度(ng/dL) | 測定値(ng/mL) | 変動率(%) |
|---|---|---|
| 88.3 | 30.9 | −11.7 |
| 4.17 | 35.3 | 0.0 |
| 20.8 | 36.2 | 2.6 |
| 10.4 | 35.5 | 0.6 |
| 5.2 | 37.7 | 6.8 |
| 0 | 35.3 | 0.0 |
| ビオチン濃度(ng/dL) | 測定値(μg/mL) | 変動率(%) |
|---|---|---|
| 2,500 | 15.1 | −13.7 |
| 1,250 | 16.8 | −4.0 |
| 625 | 16.6 | −5.1 |
| 312.5 | 16.8 | −4.0 |
| 0 | 17.5 | 0.0 |
| ビオチン濃度(ng/dL) | 測定値(ng/mL) | 変動率(%) |
|---|---|---|
| 83.3 | 27.4 | −18.1 |
| 41.7 | 31.9 | −4.2 |
| 20.8 | 32.6 | −2.1 |
| 10.4 | 33.4 | 0.3 |
| 5.2 | 32.6 | −2.1 |
| 0 | 33.3 | 0.0 |
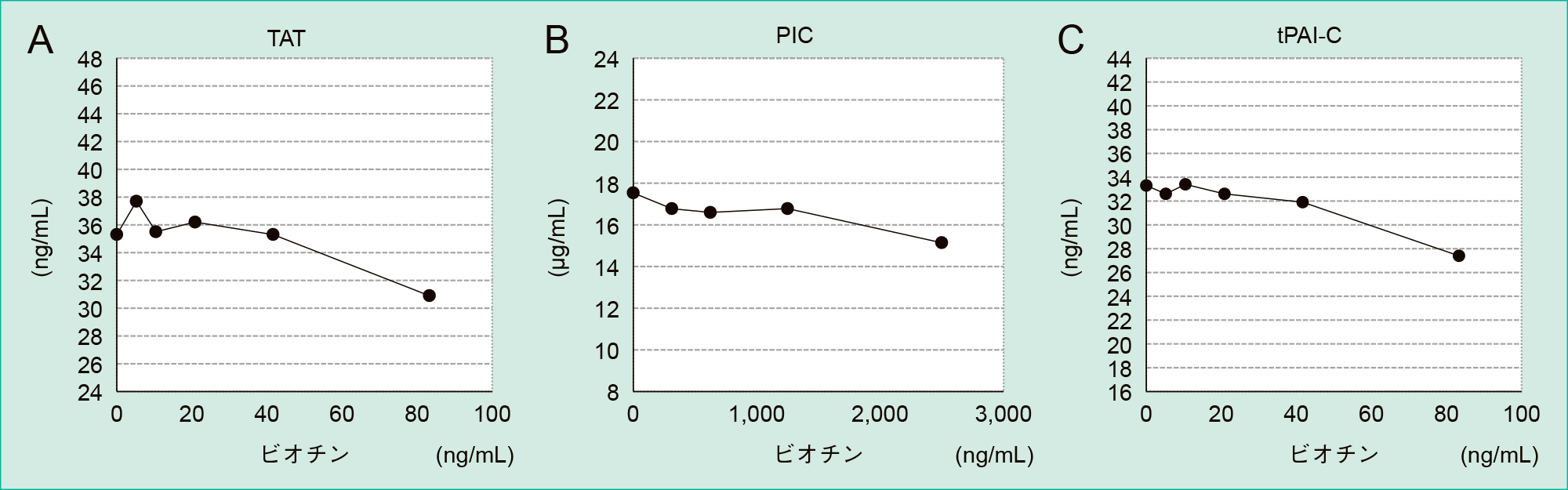
TAT(A),PIC(B),tPAI-C(C)のビオチン添加による影響を,ブランクの測定値を100%としたときの相対値を用いて評価した。
対象機器間の相関性(HISCL-5000: x, CN-6500: y)は,TATがy = 1.013x − 0.269,PICがy = 1.026x − 0.134,tPAI-Cがy = 0.944x + 0.028と良好であった。Spearmanの相関係数はTATがr = 0.998,PICがr = 0.998,TATがr = 0.999であった(Figure 4)。

HISCL-5000(x)とCN-6500(y)でのTAT(A),PIC(B),tPAI-C(C)測定値との相関性を評価した。
近年,医療機関を取り巻く環境は急速に変化し,鏡視下手術やロボット支援手術に代表されるような高難度の先進的手術手技が次々と導入されている。また,胸・腹部大動脈瘤のような長時間に及ぶ手術の件数も増加傾向にある。手術中は,長時間手術台に横たわり同じ体勢をとり続けることで,手術の影響で止血機能が亢進することから,DVTが生じやすくなっている。中でも,DVTが原因でおこるPEはVTEが引き起こすもっとも危険な周術期合併症である。
そのような背景において,凝固線溶系分子マーカーはVTE発症リスクを予測できるため,凝固・線溶系検査として迅速に結果報告できる院内検査体制の構築が必要である。しかし,多くの医療施設内では凝固線溶系分子マーカーを院内検査室内で実施することができないため,外部委託検査室に提出し結果報告までに時間を要している現状がある。
今回の結果から,TAT,PIC,tPAI-Cの併行精度および室内再現精度は,3項目ともCVが3%未満であり,優れた精確性を確認した。希釈直線性は,TAT,PIC,tPAI-Cの3項目とも相関係数が0.99以上であったことから,高値希釈測定を行っても測定結果に影響がないことを確認した。相関性は,TAT,PICおよびtPAI-Cの3項目とも相関係数が0.998以上であり良好であった。最小検出感度は,試薬添付文書の範囲以下であり,試薬性能を確認できた。干渉物質の影響評価からも,溶血,乳び,ビリルビンC,ビリルビンFに関しては,各干渉物質の濃度を上昇させても,測定結果の変動率が10%を超えなかった。しかし,一定濃度のビオチンが含まれる血漿では,TAT,PICおよびtPAI-Cの測定結果の変動率が10%を超えた。
PICは測定時に検体が40倍希釈されるため,無希釈測定となるTATとPICとは変動率が10%を超えるビオチン添加濃度が異なっていたが,ビオチンが検討に使用した試薬において測定値に影響を及ぼす可能性があることが明らかとなった。その理由として,今回測定に使用したHISCL試薬にはビオチンが用いられていることが原因であると考えられる。HISCL試薬の反応試薬系には標識酵素としてALPやビオチンが用いられている。今回使用したHISCL TAT試薬,HISCL PIC試薬およびHISCL tPAI-C試薬はそれぞれビオチン結合抗トロンビンモノクローナル抗体(マウス),ビオチン結合抗プラスミノーゲンモノクローナル抗体(マウス)およびビオチン結合抗PAI-1モノクローナル抗体(マウス)が使用されている。そのため,干渉物質としてビオチン溶液を測定試料に添加した後に測定を行った際,反応系試薬に含まれているストレプトアビジン結合磁性粒子と添加したビオチン溶液が反応し,反応系試薬中のストレプトアビジン結合磁性粒子が消費されてしまい測定値が偽低値となることが考えられる。しかし,治療で使用されているビオチン注1mg「フソー」では,投与しても最高血中濃度が3.8 ng/mLであるため,TATやtPAI-C測定で影響があった83.3 ng/mLと比較すると非常に低値であり,臨床的な影響はないものと考える。また,ビオチンはサプリメントとして摂取されることもあるが,日本の栄養表示基準において,「一日当たりの摂取目安量として500 μgを超える量を表示してはならない」とされており,健常人から採取した検体におけるビオチン濃度は,1 ng/mL以下と考えられている3),4)ため,日常検査の範囲内においては測定値への影響はないと考えられる。一方で,海外製品に関しては,多量のビオチンが含まれたサプリメントが販売されており,検体中のビオチンと競合し偽低値になるとの報告もあり5),TAT,PIC,tPAI-Cの測定に影響を及ぼす可能性があると考える。2017年に血栓止血学会が改訂したDICの新診断基準6)では,凝固線溶分子マーカー項目が新たに追加された。食生活の欧米化や高齢化が進む中で,血栓性疾患の増加が注目されており7),凝固・線溶活性の評価として凝固線溶分子マーカーの検査結果は迅速性が求められている8)。また,近年増加の一途をたどる透析患者においても動脈硬化病変に伴う血栓症や血管合併症が予後を左右する重要な問題となっている9)。特に,動脈硬化に伴う血管合併症が高頻度にみられる糖尿病性腎症患者では血管内皮傷害や止血異常が認められるため,凝固線溶分子マーカーが測定できる院内検査体制の構築は今後ますます需要が増すことが予想される。
CN-6500は,TAT,PIC,tPAI-C測定において,十分な精度を有しており,日常検査に使用しても問題がないことが確認できた。但し,TAT,PIC,tPAI-Cに限らず,免疫学的測定法にはアビジン-ビオチンシステムを用いた検査項目も多く,ビオチンによる偽低値を防ぐためにも,常用サプリメントのカルテ記載の必要性があると考える。
本論文に関連し,開示すべきCOI 状態にある企業等はありません。