2013 年 46 巻 9 号 p. 700-707
2013 年 46 巻 9 号 p. 700-707
Desmoplastic small round cell tumor(以下,DSRCTと略記)は若年者に好発する予後不良のまれな疾患である.症例は23歳の女性で,肛門部痛を主訴に前医を受診した.骨盤部CT上,肛門部に50 mm大の腫瘤と両側鼠径部リンパ節腫大を指摘され,加療目的に当院へ紹介された.生検の結果,DSRCTと診断され両側鼠径部リンパ節郭清を含めた腹会陰式直腸切断術を施行した.再発予防のため術後放射線治療を行ったが,6か月目に遠隔転移を来した.全身化学療法はVDC-IE交替療法を18クール,gemcitabine+docetaxelを13クール施行した.長期にわたり腫瘍増殖の抑制をえられていたが再び腫瘍の増大を来し,診断より4年4か月後に死亡した.今回,肛門周囲の発生したDSRCTの1例を経験したため報告する.
Desmoplastic small round cell tumor(以下,DSRCTと略記)は,1989年Geraldら1)によって初めて報告された,若年者に好発する非常にまれな予後不良の疾患である.比較的新しい腫瘍概念で,現在も統一された治療指針は示されていない.今回,我々は集学的治療が有効であったDSRCTの1例を経験したので,若干の文献的考察を加え報告する.
症例:23歳,女性
主訴:肛門部痛
既往歴:特記事項なし.
家族歴:特記事項なし.
現病歴:2008年に肛門部痛を主訴に近医を受診した.骨盤部CT上,肛門部に50 mm大の腫瘤と両側鼠径部リンパ節腫脹を指摘され精査目的に当院へ紹介された.
血液検査所見:血液生化学所見は正常範囲内であった.腫瘍マーカーは,CA125が125.3 U/mlと上昇していた.
骨盤部CT所見:肛門を中心に52 mm大の腫瘤を認めた.腫瘍周囲および両側鼠径部のリンパ節腫大がみられた.明らかな遠隔転移や腹膜播種の所見は認めなかった(Fig. 1).

Pelvic CT revealed a 50-mm tumor in the anal canal (arrowhead) and swollen lymph nodes in the bilateral inguinal region (arrows).
右鼠径部リンパ節生検を行い,病理組織学的検査の結果,DSRCTと診断された.
全身の転移検索で明らかな遠隔転移は指摘できず,両側鼠径部リンパ節郭清を含めた腹会陰式直腸切断術を施行した.
手術所見:下腹部正中切開で開腹した.明らかな腹水や腹膜播種はみられなかった.リンパ節は下腸間膜動脈周囲に加え,両側側方郭清および両側鼠径部リンパ節郭清を行った.肛門操作では,膣を温存し腫瘍が摘出可能であった.左下腹部に結腸ストマを造設し手術を終了した.
切除標本:肛門管に80×50 mm大の亜全周性の腫瘤を認めた(Fig. 2).

Gross finding showed 80×50 mm subcircumferential tumor in the anal canal.
病理組織学的検査所見:N/C比の高い小型の異型細胞が間質の線維化を伴って浸潤性に増殖していた.両側鼠径部リンパ節,結腸傍リンパ節にそれぞれ転移を認めた.免疫染色検査ではvimentin,desmin,NSEが陽性であり,DSRCTと診断された(Fig. 3).
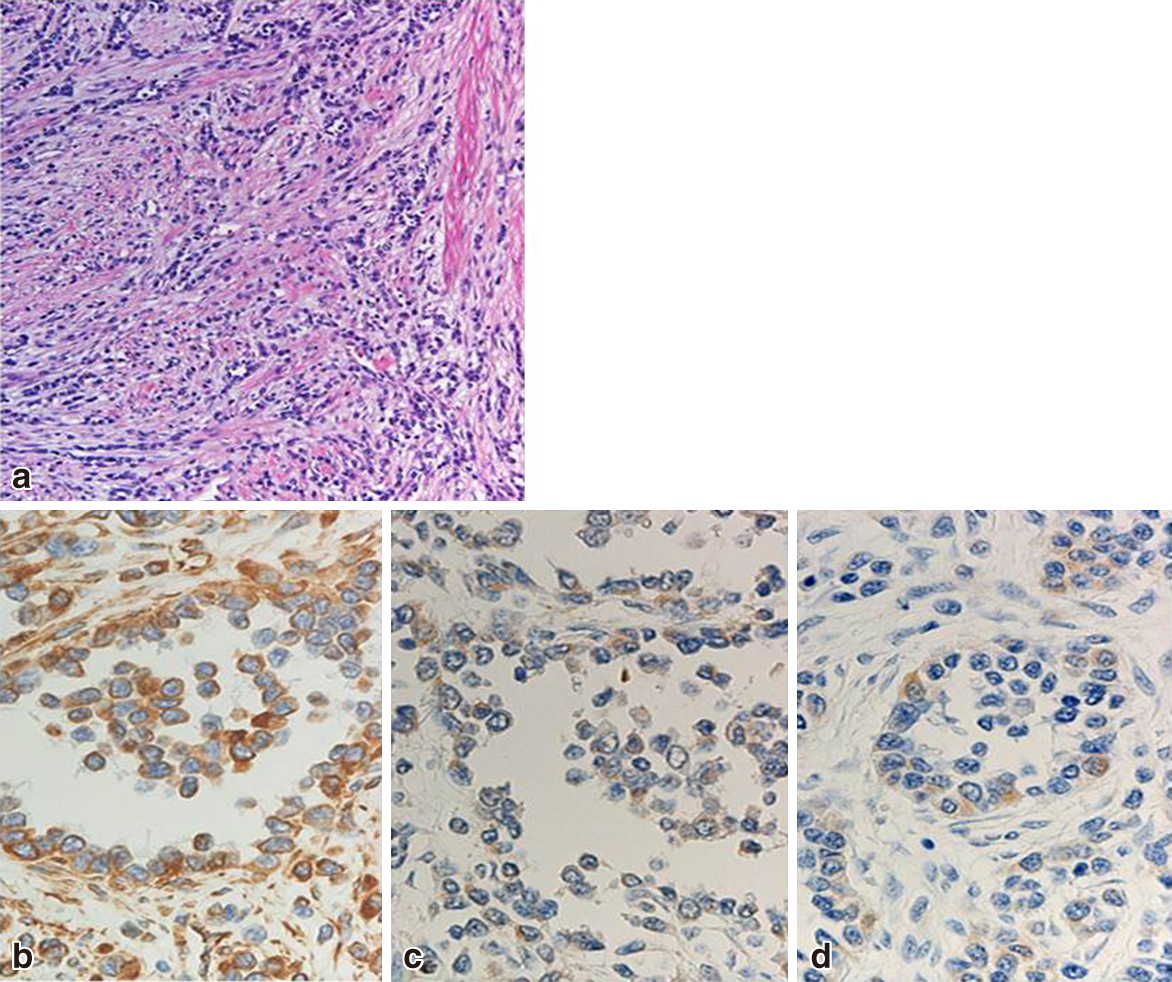
Histologically, the tumor displayed a diffuse proliferation of small size with irregular nucleus surrounded by fibrous stroma (a: ×200). Immunohistochemistry showed the tumor cells to be positive for vimentin (b: ×400), positive for NSE (c: ×400), and focally positive for desmin (d: ×400).
臨床経過:術後は再発予防のため,L4/5から肛門までの骨盤部および左右鼠径リンパ節転移の術後腫瘍床に放射線治療(59.4 Gy/33 fr)を施行した.しかし,術後6か月目の胸部CTで右乳房に結節を指摘され生検を行ったところ,DSRCTの再発と診断された.FDG-PETでは全身にhot spotが認められ,全身化学療法の適応と判断しVDC-IE交替療法を開始した(vincristine 2 mg/m2(day 1),doxorubicin 50 mg/m2(day 1,2),cyclophosphamide 1,600 mg/m2(day 1),ifosfamide 2,500 mg/m2(day 21~25),etoposide 130 mg/m2(day 21~25)).4クール終了時にはPET-CTで指摘されていたhot spotは消失した(Fig. 4a).腹部CTで指摘されていた転移巣も消失または縮小がみられRECISTガイドライン(version 1.1)においてPRと評価した(Fig. 4b).その後,治療経過中にgrade 3の好中球減少を2回経験したため投与量の減量を行ったが治療継続は可能であった.18クール目にCA125が94.7 U/mlと上昇したため,全身CTを施行したところ縦隔および右肺門リンパ節の腫大を認めた.腫瘍の再燃と判断し,レジメンをgemcitabine+docetaxel療法に変更した(gemcitabine 675 mg/m2,day 1, 2,docetaxel 100 mg/m2,day 21).レジメン変更後,4クール終了時の採血でCA125は26.2 U/mlに低下していた.しかし,13クール終了後に縦隔リンパ節および気管再発を来し,診断より4年4か月後に永眠された(Fig. 5).

After 4 courses of VDC-IE chemotherapy, hot spots disappeared in positron emission tomography (a). Abdominal CT revealed marked shrinkage of metastatic lesions (arrows) (b).

Patient’s clinical course. CA125 was elevated according to tumor growth except during the period of first recurrence.
DSRCTは若年者に好発するまれな腫瘍で,3年生存率が29%と予後不良である1)2).男女比は5:1と比較的男性に多く発症するといわれている3).主に腹腔内に発生し腹膜,骨盤内に好発するが特徴的な臨床症状に乏しく,腹部膨満,腹痛,腫瘤触知などさまざまな症状を呈する3).また,画像所見でも特徴的な所見はなく,原因不明の腹腔内腫瘤として指摘され,精査を行われることが多い4).
確定診断は主に病理組織学的検査所見で行われ,大小の胞層状に集簇した腫瘍細胞と膠原繊維が豊富な間質を認め,腫瘍細胞が小円形で密に造成する.免疫組織染色検査では多様な染色を示し,cytokeratin,vimentin,desmin,NSEなどの上皮性,神経原性,筋原性のマーカーが陽性になるのが特徴である5)6).本症例も,間質の線維化を伴う小円形細胞の増殖を認め,免疫染色検査でvimentin,desmin,NSEが陽性であったためDSRCTと診断した.
DSRCTに対する統一された治療指針はいまだに示されておらず,組織学的に類似するsarcomaに準じた治療が選択されることが多い7).Kushnerら8)は多剤併用療法であるP6 protocol(1,2,3,6コースにcyclophosphamide 2,100 mg/m2(day 1, 2),doxorubicin 75 mg/m2(day 1, 2),vincristine 0.67 mg/m2(day 1)を投与,4,5,7コースにifosfamide 1,800 mg/m2(day 1~5),etoposide 100 mg/m2(day 1~5)を投与)を推奨しており,手術療法と併用することで5年生存率が35%と良好な成績であった.また,手術療法単独群と手術療法,化学療法,放射線療法の集学的治療群を比較した報告では,3年生存率がそれぞれ27%,55%と集学的治療群で良好であり,積極的な治療が有用と結論付けている8).我々も,手術後に再発予防のため放射線治療を行った.再発後はVDC-IE療法やgemcitabine+docetaxel療法など多剤併用療法を行うことで長期にわたり腫瘍増殖を抑制できた.
医学中央雑誌にて「desmoplastic small round cell tumor」,「線維形成性小円形細胞腫瘍」をキーワードに,1983年から2013年1月までに37の文献が検索された(Table 1)7)9)~40).年齢は0歳~63歳(平均25.3歳)で,男女比は27:11と男性に多くみられた.占居部位は27例(71.1%)が腹膜原発で,うち20例は診断時に播種を認めていた.女性患者11症例のうち7例は卵巣の腫瘤として発見されており,若年者で腹膜播種を呈する卵巣腫瘍の場合は本症の可能性も考慮すべきである.
| Age | 25.3 (0–63) | Operation | radical resection | 5 | |
| Sex (M/F) | 27 : 11 | debulky resection | 15 | ||
| Symptom | abdominal pain | 12 | not resectable | 18 | |
| abdominal distention | 11 | Radiation | 2 | ||
| general fatigue | 1 | Chemotherapy | 30 | ||
| swelling of scrotal | 1 | ICE (IFM/Etoposide/CBDCA) | 4 | ||
| urinary frequency | 1 | P6 regimen | 3 | ||
| swelling of eye lid | 1 | 5-FU/CDDP/DXR | 2 | ||
| none | 5 | 5-FU/CDDP/MTX/Etoposide | 1 | ||
| unknown | 6 | CPA/CDDP/DXR | 1 | ||
| Location | peritoneal cavity | 27 | BEP (Bleomycin/Etoposide/CDDP) | 1 | |
| ovary | 7 | ID (IFM/DXR) | 1 | ||
| rectum | 1 | GEM+CDDP | 1 | ||
| scrotal | 1 | CDDP/Etoposide | 1 | ||
| eye lid | 1 | PTX/CBDCA | 1 | ||
| mediastinum | 1 | unknown | 14 | ||
| Metastasis | dissemination | 20 | Elevation of tumor marker | CA125 and NSE | 4 |
| liver | 9 | CA125 only | 7 | ||
| lymph nodes | 2 | NSE only | 3 | ||
| none | 4 | not elevated | 9 | ||
| unknown | 3 | unknown | 15 |
DOC; docetaxel, GEM; gemcitabine, VCR; vincristine, DXR; doxorubicine, CPA; cyclophosphamide, IFM; ifosfamide, MTX; methotrexate, CBDCA; carboplatine
手術は20例(52.6%)に施行されていたが,そのうち根治切除はわずか5例であった.そのうち1例は6か月後にリンパ節再発,1例は4か月後に局所再発,3例は短期のフォローであり根治切除の長期予後は不明であった.我々の症例では,術後再発予防のため放射線治療を行った.6か月後に遠隔転移再発を来したが全経過にわたり局所再発は認めておらず,放射線治療により局所制御が得られていたと考えられる.今回の検索の中で放射線治療を受けていたのは病変が局所に限局した2症例のみであった.海外では播種病変に対して全身放射線療法(whole abdominopelvic intensity modulated radiation)の有用性が報告されており,今後本邦でも考慮すべき治療法と考える41).
化学療法は30例に施行されていた.レジメンの記載があった17例のうち12例が3剤以上の多剤併用療法で治療されており,ICE療法が4例,海外で推奨されているP6 protocolが3例と多く選択されていた.しかし,平均生存期間はそれぞれ26.6か月,11.6か月と不良で,5年生存例は認めなかった.また,多剤併用療法を施行した症例のうち副作用や患者拒否で治療継続が困難となった症例が7例(58%)にみられた.今回,我々はNCCNガイドラインよりsarcomaに推奨されているVDC-IE交替療法,gemcitabine+docetaxel療法を選択した.本邦でDSRCTに対してVDC-IE交替療法を施行した報告はこれが初めてであるが,投与抗癌剤量の調整と対症療法により34か月と長期間にわたり治療継続と病勢コントロールが可能であり,有力なレジメンの一つと考えられる.今後さらなる症例の蓄積による最適な治療レジメンの開発が望まれる.
利益相反:なし