2015 年 48 巻 8 号 p. 669-676
2015 年 48 巻 8 号 p. 669-676
胃癌に対する胃全摘術後の吻合部再発は比較的まれであり,その治療法はいまだ確立されたものはない.今回,胃癌胃全摘後の吻合部再発に対して化学療法を行った後に,再切除術を施行した2例を経験したので報告する.症例1は64歳の男性で,胃癌に対する胃全摘術施行後2年7か月に吻合部再発と診断した.S-1+CDDP療法を2コース行った後,吻合部を含む食道空腸部分切除術を施行した.摘出標本には腫瘍を認めず,病理学的complete response(CR)と診断した.術後は化学療法を行わず,術後7か月現在外来にて無再発経過観察中である.症例2は65歳の男性で,同じく胃癌に対する胃全摘術施行後2年6か月に胃癌の吻合部再発と診断し,weekly PTX療法を計12コース施行した.化学療法終了後も他に再発は認めず,吻合部を含む食道空腸部分切除術を行った.術後3か月現在化学療法は行わず経過観察中である.
胃癌の再発はsystemic diseaseの一形態ととらえられ,これまで外科治療の対象とされてこなかったが,近年化学療法の進歩に伴い,stage IV胃癌,特に胃癌肝転移に対して手術治療を行い比較的良好な結果を得ている報告もある1).胃癌術後吻合部再発は局所再発の一部にあたり,比較的まれな再発形式であるが2),腹膜播種などと比べて比較的予後が良く3),手術により狭窄症状が改善したという報告や4),長期生存を認めたという報告もある5).根治性を求めるには化学療法の併用が必要と考えられるが,化学療法を行うタイミングについてははっきりとしたものはない.今回,我々は再手術前に化学療法を行い良好な経過をたどった2例を経験した.
症例1:64歳,男性
主訴:嚥下困難
既往歴:特記事項なし.
現病歴:2010年12月,U領域の4型胃癌に対して胃全摘術を施行した.CY1であったため脾臓を温存するD1+郭清とし,結腸後経路でRoux-en Y再建を行った.切除標本の病理組織学的検査所見は,por2,T4a(SE),INFb,ly3,v1,N3,PM0(25 mm),DM0(160 mm),CY1となりR1切除となった(Fig. 1).
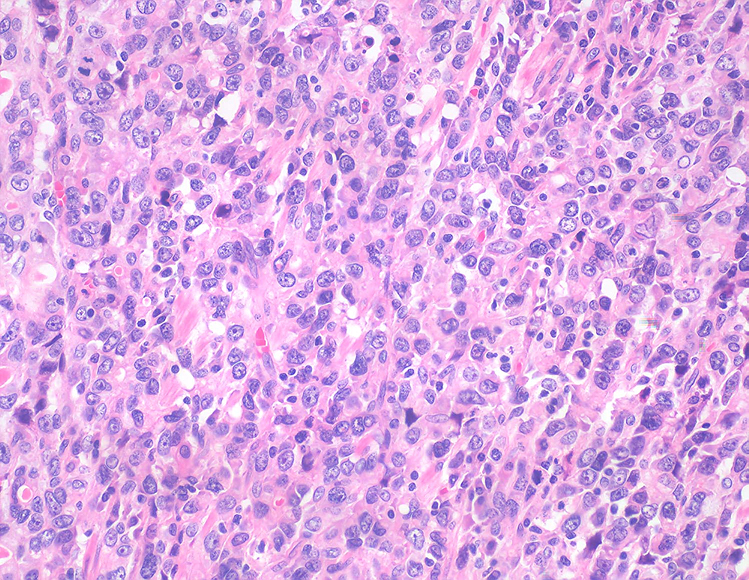
Histopathological findings of the resected specimen of the first operation show poorly differentiated adenocarcinoma (Case 1; HE stain ×20).
術後S-1+CDDP療法(S-1 100 mg/日,CDDP 60 mg/m2)を3コース行ったところで,食思不振と全身倦怠感の副作用が強く中止となり,以後経過観察となった.
初回手術後2年7か月の2013年7月より嚥下困難が出現した.吻合部狭窄を疑い上部消化管内視鏡検査を行った.
現症:身長168 cm,体重54 kg.
上部消化管内視鏡検査所見:食道空腸吻合部の狭窄を認め,吻合部口側3 cmの食道左壁側に島状,平板隆起性の病変を認めた(Fig. 2).組織生検結果は低分化腺癌で,初回手術時の組織像と類似していた(Fig. 3).

Upper gastrointestinal endoscopy before chemotherapy shows an elevated islet lesion in the lower esophagus (Case 1).

Histopathological findings of the biopsy specimen of recurrent lesion also show poorly differentiated adenocarcinoma (Case 1; HE stain ×20).
腹部造影CT所見:食道空腸吻合部頭側で食道壁の肥厚を認め,不均一に造影効果を認めた.
FDG-PET/CT所見:食道空腸吻合部頭側に集積亢進を認めた.他に集積亢進を呈する部位は認めなかった.
血液検査所見:CEA 2.0 ng/ml,CA19-9 42.2 U/ml.
初回原発巣の脈管侵襲が高度であり,生検での組織所見が初回原発巣の組織所見と類似していたことから,胃癌の吻合部再発と診断した.初回手術時CY1であったため,画像検査には描出されない微小な腹膜播種再発などの同時再発を伴っている可能性を考え,手術先行ではなく化学療法を行い,経過観察する方針とした.初回手術後と比べて,再発時は全身状態が改善しており,S-1+CDDP療法の副作用に耐えうると判断して,高い抗腫瘍効果が望めるS-1+CDDP療法(S-1 100 mg/日,CDDP 60 mg/m2)を再度2コース行い,特に副作用を認めることがなかった.また,吻合部狭窄により経口摂取困難であったため,経鼻的にfeeding tubeを空腸内に留置し,濃厚流動食による経腸栄養を開始した.化学療法2コース施行後,効果判定のため上部消化管内視鏡検査で吻合部を観察したところ,隆起性病変は縮小傾向であったが狭窄は改善していなかった(Fig. 4).また,CTを施行したところ,吻合部頭側の壁肥厚は縮小傾向で他に新たな再発は認めなかった.

Upper gastrointestinal endoscopy after chemotherapy shows that the tumor is diminished but a stricture still exists (Case 1).
化学療法によりpartial response(以下,PRと略記)となったと判断し,他に再発所見も認めないことから,切除可能と判断して,初回手術後2年11か月経過した2013年11月に手術を施行した.
術中所見:左第6肋間からアプローチして開胸開腹した.腹腔内の癒着は比較的強固であったが,腹膜播種や腫瘍の周囲臓器への浸潤は認めず,胸腔内に癒着は認めなかった.吻合部から口側は食道を4 cm切除し,肛門側は空腸を4 cm切除した.術中に口側断端陰性を確認した.再建は後結腸経路でRoux-en Y再建とした.挙上空腸の緊張がやや強かったため空腸動脈を1本処理し,後結腸経路で空腸を挙上したところ緊張なく吻合することができた.手術時間329分,出血量341 gであった.
摘出標本肉眼検査所見:吻合部周囲には腫瘍性病変を認めなかった.
病理組織学的検査所見:吻合部周囲に線維性瘢痕を認めるのみで,腫瘍は認めなかった.また,背景にバレット食道は認めなかった(Fig. 5).

Histopathological findings of the resected specimen of the second operation show only fibrous scars around the anastomotic site (Case 1; HE stain ×10).
術後経過は良好で,術後10日目に退院となった.また,経口摂取も可能となった.吻合部再発は病理学的complete response(以下,CRと略記)と診断し,術後7か月の現在,化学療法を行わず外来にて無再発経過観察中である.
症例2:65歳,男性
主訴:つかえ感
既往歴:狭心症,総胆管結石
現病歴:2010年4月,U領域の2型胃癌に対して,胃全摘,脾臓摘出術(D2郭清)を施行した.結腸前経路でRoux-en Y再建を行った.切除標本の病理組織学的検査所見はpap+tub1,T2a(MP),INFb,ly2,v1,N1,PM0(10 mm),DM0(80 mm),stage IIであった(Fig. 6).

Resected specimen of the first operation includes both papillary and moderately differentiated adenocarcinoma. The part of moderately differentiated adenocarcinoma is shown in this figure (Case 2; HE stain ×20).
術後補助化学療法としてS-1(4投2休:100 mg/日)を7コース施行し,経過観察としていたが,初回手術後2年6か月経過した2012年10月よりつかえ感が出現した.
現症:身長168 cm,体重52 kg.
血液検査所見:CEA 1.7 ng/ml,CA19-9 48.7 U/ml.
上部消化管内視鏡検査所見:食道空腸吻合部から口側に広がる隆起性の病変を認め,組織生検結果は腺癌だった(Fig. 7).

Upper gastrointestinal endoscopy before chemotherapy shows an elevated lesion spreading in the lower esophagus (Case 2).
腹部造影CT所見:食道空腸吻合部頭側にわずかな壁肥厚を認めた.
初回原発巣の脈管侵襲が高度で,再発巣も吻合部を中心に発生していることから,胃癌吻合部再発と診断した.吻合部再発以外にも再発巣が出現する可能性もあると考え,手術ではなく化学療法を行うこととした.すでに術後補助化学療法としてS-1を7コース施行し,総投与量も多くなっていたため,S-1に対する耐性が出現している可能性を懸念して,weekly PTX療法(3投1休:80 mg/m2)を6コース施行した.
初回手術後3年3か月経過した2013年7月に上部消化管内視鏡検査と腹部造影CTを施行し,腫瘍は少し縮小しておりPRと診断した.その後さらにweekly PTX療法(2投2休:80 mg/m2)を6コース施行し,PET/CTを施行したところ,食道空腸吻合部に高集積域を認めた.
化学療法を施行し経過を見たが,吻合部以外に明らかな再発はなく,根治切除の可能性もあるとして初回手術から3年11か月経過した2014年3月に手術を施行した.
手術所見:左第6肋間で開胸開腹したが,腹膜播種と腫瘍の周囲臓器への浸潤は認めず,剥離可能だった.吻合部から口側4 cmの位置で食道を切離し,術中迅速組織診にて断端陰性を確認し,Roux-en Yにて再建した.後結腸経路で空腸を挙上することで食道空腸吻合部の緊張がなくなった.手術時間335分,出血量361 gであった.
摘出標本肉眼検査所見:吻合部から口側の食道に隆起性病変が散在していた.
病理組織学的検査所見:吻合部口側の食道の粘膜下から発生するように進展する径2 cmまでの腫瘍が散在しており,中分化腺癌であった(Fig. 8).背景にバレット食道は認めなかった.

Histopathological findings of the resected specimen of the second operation (Case 2). A: Tumor infiltrates from submucosal layer of the esophagus (HE stain ×4). B: Moderately differentiated adenocarcinoma is observed in the recurrent site (HE stain ×20).
術後創感染を認めたが,縫合不全など高度の合併症はなく経過し,術後15日目で退院した.R0切除ができ,他に再発を認めなかったため,術後3か月現在,化学療法は行わず経過観察中である.
胃癌の再発形式としては,本邦で行われたACTS-GC試験によると,腹膜播種が46%と最も多く,その後肝転移が34%,リンパ節転移が22%,局所再発が7%と続いている2).吻合部再発は局所再発の一部とされているが,吻合部再発のみを集計した報告はこれまでなく,まれな再発形式であることが考えられる.予後については,小林ら3)の報告によると腹膜播種再発の平均生存日数が155日,リンパ節再発で137日であるのに対して,吻合部再発を含む局所再発では580日と比較的予後が良い傾向があるとしている.
吻合部再発の発生機序としては,1)口側断端陽性,2)口側断端陰性だが,脈管侵襲のため断端部に微小な腫瘍細胞が残存した,3)転移リンパ節が残存し,壁外性に吻合部に浸潤した,4)手術操作によるimplantation,5)血行性転移や腹膜播種からの二次的増殖などが考えられる6).自験例では2例とも初回手術時は断端陰性であったものの,脈管侵襲が高度であったため,断端部の微小な腫瘍細胞の遺残が原因と推測される.症例1において初回手術時はCY1であったものの,再手術時に腹膜播種病変は認めなかったため,腹膜播種からの二次的増殖による再発の可能性は低いと考えた.また,2例とも病変は吻合部を中心に認められ,初回原発巣と再発病変の病理組織学的検査所見が類似していることから病変が新規原発巣である可能性は低いものと考えた.特に症例2においては,腫瘍が粘膜下から進展する病理組織像を示しており,新規原発巣とするには矛盾する所見を認めた.
吻合部再発はまれな再発形式であるために,治療法についてはいまだ画一化されたものはない.最近の化学療法の進歩に伴い再発胃癌の生命予後の延長を認め,SPIRITS試験ではS-1+CDDPを使用することで再発胃癌全体の生存期間中央値は13か月まで延長している7).なかには,吻合部再発に対する化学療法を行うことで通過障害が改善したという報告8)~10)や,CRを得られたという報告8)9)11)も見られる.しかし,一般的に化学療法でCRが得られることはまれであり,腫瘍が残存するかぎりは化学療法を継続する必要がある.
症例2においてS-1による術後補助化学療法後再発時にPTXを選択したが,術後補助化学療法後再発例に特化した臨床研究は少なく,どのレジメンを選択すべきかの見解はまだ得られていない.S-1による術後補助化学療法後再発例に対して,S-1を含まないレジメンのほうがS-1を含むレジメンよりも無増悪生存期間が良好だったという後方視的検討があるが,全生存期間に差は認めなかった12).
吻合部再発に対する再切除術は,化学療法が進歩する以前から行われている治療法である.医学中央雑誌にて「吻合部再発」,「胃癌」をキーワードとして1977年から2014年5月までの期間を検索したかぎりでは,胃全摘後吻合部再発に対して再切除術を施行した報告は自験例を含めて13例あった(Table 1)4)~6)13)~19).なかには術後長期生存を認める報告5)13)14)もあり,R0切除を行うことで根治術となる可能性もある.また,吻合部に再再発した症例は1例のみであり13),多くは通過障害の改善によるQOLの向上が期待できる.一方で,術式としては胸腔内吻合を要するため,縫合不全が生じれば重症化してしまう危険性がある.また,再切除を行う際に他臓器への浸潤があれば合併切除を要し,さらに高侵襲の手術となる.実際これまでの報告例では肝臓,肺,横隔膜,左副腎,左腎,横行結腸,膵臓などが合併切除されている14)15).このように安易に手術療法を選択すべきではないが,自験例においては2例とも術前のCTで周囲臓器への明らかな浸潤所見がないことを確認して,吻合部のみを切除する最低限の侵襲での手術を5時間程度の手術時間で行うことができた.手術操作においては,腹腔内の癒着は強固だったものの,吻合部はいずれも癒着のない胸腔内に認めたため,腫瘍周囲の剥離は容易に行えた.また,術後も2週間程度で退院することができ,症例1においては術前にfeeding tubeを用いて経管栄養を十分に行い,全身状態の改善が図れたことが良好な経過を辿る一要因だった可能性がある.自験例2例を経験して,栄養状態の改善や病変の評価を十分に行い,切除可能と判断すれば,積極的に手術療法を選択しても良いものと考えられた.また,吻合部の緊張は縫合不全の一つのリスク要因であるが,自験例においては,後結腸経路で空腸を挙上し,緊張の原因となっている空腸動脈を処理することで余裕をもって吻合することができた.
| No. | Author/ Year |
Age/ Sex |
PC | AC | Interval of recurrence | Operation | Approach | Operation time (minute) | Loss of blood (ml) | Outcome |
|---|---|---|---|---|---|---|---|---|---|---|
| 1 | Tanemura6)/ 1994 |
55/M | no | done | 10y6m | esophago-jejunectomy | left thoracolaparotomy | NR | NR | alive (6m) |
| 2 | Kusuyama13)/ 1995 |
64/M | no | no | 4y4m | esophago-jejunectomy | left thoracolaparotomy | NR | NR | dead (2y7m) |
| 3 | Kusuyama13)/ 1995 |
64/M | no | no | 1y8m | esophago-jejunectomy | left thoracolaparotomy | NR | NR | alive (5y7m) |
| 4 | Kamei14)/ 1997 |
52/M | no | done | 2y1m | multiple organ resection | NR | NR | NR | alive (6y6m) |
| 5 | Kobayashi4)/ 1998 |
48/M | no | done | 4y4m | subtotal esophagectomy | right thoracolaparotomy | 900 | 1700 | alive (2y5m) |
| 6 | Yoshida5)/ 1999 |
62/M | done | no | 7y3m | esophago-jejunectomy | NR | NR | NR | alive (6y5m) |
| 7 | Kosaka15)/ 2002 |
73/M | no | no | 8y1m | multiple organ resection | laparotomy | NR | NR | alive (2y) |
| 8 | Sugano16)/ 2004 |
67/F | no | done | 13y | multiple organ resection | left thoracolaparotomy | NR | NR | alive (1y3m) |
| 9 | Matsuyama17)/ 2010 |
72/M | no | no | 3y6m | esophago-jejunectomy | left thoracolaparotomy | NR | NR | alive (1y) |
| 10 | Nakamura18)/ 2010 |
76/F | no | no | 4m | esophago-jejunectomy | left thoracolaparotomy | NR | NR | alive (1y6m) |
| 11 | Shimomura19)/ 2012 |
64/M | no | done | 1y | subtotal esophagectomy | right thoracolaparotomy | 480 | 319 | dead (1y) |
| 12 | Our case 1 | 64/M | done | no | 2y11m | esophago-jejunectomy | left thoracolaparotomy | 329 | 341 | alive (7m) |
| 13 | Our case 2 | 65/M | done | no | 3y11m | esophago-jejunectomy | left thoracolaparotomy | 335 | 361 | alive (3m) |
*NR: not reported, PC: preoperative chemotherapy, AC: adjuvant chemotherapy
胃全摘術後吻合部再発に対して術前に化学療法を行った症例は自験例を含んで3例のみだったが5),自験例においては再発診断後,手術を前提とする術前化学療法として行ったわけではない.胃癌はsystemic diseaseとして再発することが多いために,吻合部切除術という高侵襲の手術を行っても根治性が得られる可能性は低いと判断し,姑息的に化学療法を開始した.化学療法開始後,腫瘍縮小を認め,また他に再発病変の出現を認めなかったことから手術に踏み切った.症例1においては切除標本ではCRとなっていたが,狭窄症状は持続しており,症状改善のためにも手術は妥当だったと考える.再発病変が二つ以上ある胃癌の予後は5~11か月と非常に厳しく,手術適応については慎重になるべきである20)21).自験例では化学療法施行中に,他の再発巣の出現の有無を観察することができ,結果的に手術適応のある症例かどうかの選別ができた形となった.
胃癌胃全摘術後の吻合部再発はまれであり,症例ごとに最善の治療を検討していく必要があるが,患者の全身状態と腫瘍の評価を行い,耐術可能であれば手術療法を行っても良く,化学療法を行って手術適応のある症例を選別する選択肢もあると考える.
利益相反:なし