2015 年 48 巻 8 号 p. 653-660
2015 年 48 巻 8 号 p. 653-660
目的:エンドトキシン吸着療法(polymyxin B immobilized fiber column direct hemoperfusion;以下,PMX-DHPと略記)を要した重症腹膜炎手術症例の予後因子について検討した.方法:過去8年間に当科で経験した68例を対象とし,生存群(50例)と死亡群(18例)に分けて,患者背景とPMX-DHP施行前後のパラメーターおよびその推移を比較検討した.結果:単変量解析では年齢,catecholamine index,Cr,Plt,Glasgow Coma Scale,アシドーシスの有無,Acute Physiology and Chronic Health Evaluation II score,Sequential Organ Failure Assessment score(以下,SOFA scoreと略記)に有意差を認めた.また,PMX-DHP施行により生存群ではアシドーシス,endotoxin値が有意に改善していたが,死亡群ではPltが高度減少し,SOFA scoreが有意に悪化していた.多変量解析ではPMX-DHP施行後のSOFA scoreが独立したリスク因子であった.結語:重症腹膜炎は死亡率が高く,特にSOFA scoreで高値を呈すような多臓器不全症例は,PMX-DHP施行によっても救命困難であると思われた.
消化管穿孔をはじめとした重症腹膜炎は致死率が高く,消化器外科領域における救急疾患の代表である1).救命のためには手術による早期の病因治療に加え,術後集学的治療の充実が必須である.1994年に保険適応となったエンドトキシン吸着療法(polymyxin B immobilized fiber column direct hemoperfusion;以下,PMX-DHPと略記)はその一環として期待されており,当科においても10年程前より必要と判断した症例には積極的に導入してきた.しかし,本邦におけるPMX-DHPの有用性に関する検討は後方視的文献が散見されるのみで,生命予後の改善効果に関してはいまだ議論が尽きない.今回当科においてもPMX-DHPの施行判断の一助となるべく,重症腹膜炎術後PMX-DHP施行症例の生命予後について検討したので報告する.
重症腹膜炎に対する緊急手術後PMX-DHP施行症例の生命予後因子を明らかにする.
本検討は重症腹膜炎に対する緊急手術の術後PMX-DHP施行症例を対象としたretrospective studyである.2005年1月から2012年12月までの期間に当科で経験したPMX-DHP施行症例は113例存在し,そのうち手術を要しなかった症例やデータなど記録詳細が曖昧な症例を除外した68例を対象とした(Fig. 1).
Enrollment and outcomes.
PMX-DHP施行後30日以内の在院死亡症例を死亡群,残りを生存群と定義した.生存群と死亡群の患者背景,また各群におけるPMX-DHP施行前後のパラメーターおよびその推移を比較し,生命予後因子について検討した.
患者背景として,年齢,性別,基礎疾患(消化管穿孔の場合は穿孔部位),発症から手術までの時間,手術時間,発症から初回PMX-DHP施行までの時間について比較した.
PMX-DHP施行前後のパラメーターとして,体温,平均血圧(mean arterial pressure;以下,MAPと略記),catecholamine index(以下,CAIと略記),心拍数,呼吸数,pH,PaO2/FiO2 ratio(以下,P/F ratioと略記),PaCO2,HCO3–,BE,WBC,Plt,Cr,CRP,endotoxin値,Glasgow Coma Scale(以下,GCSと略記),Acute Physiology and Chronic Health Evaluation II score(以下,APACHE II scoreと略記),Sequential Organ Failure Assessment score(以下,SOFA scoreと略記),SIRS(systemic inflammatory response syndrome)該当項目数について比較した.パラメーターに関して,vital signsはPMX-DHP施行前後2時間値を,採血データなどは術後またはPMX-DHP施行後2~6時間後の測定値とした.
当科におけるPMX-DHPの適応基準は,①敗血症性ショックに対するearly goal-directed therapy(以下,EGDTと略記)にもかかわらず,catecholamineが必要なショック症例,或いは②今後それに至る可能性が高いと考えられた高リスク症例である.吸着カラムはPMX-20Rを,vascular accessは内頸静脈または大腿静脈を使用した.抗凝固剤はnafamostat mesilate(フサン®)を15~24 mg/hrで投与し,activated whole blood clotting time(ACT)は150~180秒に,血流量は60~100 ml/minに設定した.1回当たりの施行時間はvital signsの変動を見ながら2~12時間継続し,1回目終了後に主治医が必要と判断した場合は2日連続2回まで施行した.
なおPMX-DHP以外の治療法としては,EGTDに加え広域スペクトラムの抗生剤および,γ-globulin製剤(ヴェノグロブリン®)を使用した.播種性血管内凝固症候群(disseminated intravascular coagulation;以下,DICと略記)を呈する場合はnafamostat mesilate(フサン®)を使用し,症例に応じてantithrombin III製剤(ノンスロン®)やrecombinant thrombomodulin製剤(リコモジュリン®)を使用した.また,乏尿を呈し,腎機能が悪化する症例には持続的血液濾過透析(continuous hemodiafiltration;CHDF)を主治医の判断で施行した.
統計学的手法として単変量解析はMann-Whitney U検定もしくはχ2検定で行った.多変量解析は単変量解析で有意差を認めた項目を共変量,生命予後を従属変数としたロジスティック回帰分析(変数増加法)で行い,いずれの統計手法ともP<0.05を以て有意差ありと判断した.
全症例68例中,生存群は50例,死亡群は18例であった(死亡率26.5%)(Fig. 1).平均年齢は62(±18)歳で,男性42例,女性26例であった.生存群の平均年齢は59(±17)歳,死亡群は71(±19)歳で,死亡群で有意に高齢であった(P=0.028).
原因疾患として,胃・十二指腸潰瘍穿孔が6例(生存3例/死亡3例),小腸穿孔が10例(8/2),右結腸穿孔が7例(5/2),左結腸穿孔が9例(4/5),直腸穿孔が11例(9/2),結腸癌や直腸癌などの下部消化管術後縫合不全が9例(9/0),絞扼性腸閉塞が10例(8/2),上腸間膜動脈塞栓症や非閉塞性腸間膜虚血症(non-occlusive mesenteric ischemia;NOMI)などのその他の疾患が6例(4/2)であった(Table 1).
| Survivors (n=50) | Non-survivors (n=18) | Mortality (%) | |
|---|---|---|---|
| Perforation (43) | 29 | 14 | 32.6 |
| Stomach/duodenum (6) | 3 | 3 | 50 |
| Small intestine (10) | 8 | 2 | 20 |
| Right side colon (7) | 5 | 2 | 28.6 |
| Left side colon (9) | 4 | 5 | 55.6 |
| Rectum (11) | 9 | 2 | 18.1 |
| Anastomotic leakage (9) | 9 | 0 | 0 |
| Strangulated obstruction (10) | 8 | 2 | 20 |
| Others (6) | 4 | 2 | 33 |
発症から手術までの時間,手術時間,発症から初回PMX-DHP施行までの時間には生存群と死亡群との間で有意差は認めなかった.
体温は死亡群で低い傾向にあり,特にPMX-DHP施行前は有意に低体温であった(P=0.049).MAPも死亡群で低くcatecholamineを多く要していたが,PMX-DHP施行後のCAIを除いて統計学的有意差は認めなかった.心拍数・呼吸数も死亡群でやや多い傾向にあったが,統計学的有意差は認めなかった.P/F ratio,PaCO2も両群間に有意差を認めなかった.動脈血液ガス分析においてpH,HCO3–,BEはいずれも死亡群で有意にアシドーシスであった.Crも死亡群で有意に高値であった(P=0.04).WBC,CRPに関しては両群間で有意差は認めなかった.Pltは死亡群で低い傾向を示し,特にPMX-DHP施行後は有意に低値であった(P=0.005).Endotoxin値も死亡群において高値を示していたが,統計学的有意差は認めなかった.GCSは死亡群で低く,APACHE II score(P=0.005/0.003),SOFA score(P=0.044/0.0005)もPMX-DHP施行前後とも死亡群で有意に高値であった.一方,SIRS該当項目数は両群間で有意差を認めなかった(Table 2).
| PMX | Survivors (n=50) | Non-survivors (n=18) | P value | |||
|---|---|---|---|---|---|---|
| Age (yr) | 59±17 | 71±19 | 0.028 | |||
| Time to operation | 28:50±39:20 | 22:20±20:20 | >0.05 | |||
| Operation time | 2:22±1:40 | 3:32±2:10 | >0.05 | |||
| Time to PMX | 39:30±41:20 | 36:20±20:30 | >0.05 | |||
| Body temperature (°C) | Pre | 36.9±1.0 | 36.2±1.2 | 0.049 | ||
| Post | 37.1±0.6 | P>0.05 | 36.9±1.1 | P>0.05 | >0.05 | |
| MAP (mmHg) | Pre | 82.0±15.8 | 78.7±17.7 | >0.05 | ||
| Post | 83.2±15.4 | P>0.05 | 76.0±20.9 | P>0.05 | >0.05 | |
| CAI | Pre | 3.55±3.3 | 7.33±9.4 | >0.05 | ||
| post | 3.20±4.1 | P>0.05 | 10.1±10.8 | P>0.05 | 0.015 | |
| MAP/CAI | Pre | 47.1±34.9 | 30.7±35.4 | >0.05 | ||
| Post | 54.6±35.8 | P>0.05 | 40.5±41.5 | P>0.05 | >0.05 | |
| Heart rate (/min) | Pre | 109.5±23.1 | 113.5±25.9 | >0.05 | ||
| Post | 101.9±17.8 | P>0.05 | 108.4±26.5 | P>0.05 | >0.05 | |
| Respiratory rate (/min) | Pre | 19.5±5.2 | 21.6±8.6 | >0.05 | ||
| Post | 18.2±4.8 | P>0.05 | 19.2±6.1 | P>0.05 | >0.05 | |
| PaO2/FiO2 | Pre | 298.6±121.4 | 305.1±136.2 | >0.05 | ||
| Post | 301.8±96.3 | P>0.05 | 279.5±112.8 | P>0.05 | >0.05 | |
| PaCO2 (Torr) | Pre | 37.7±7.9 | 39.3±4.7 | >0.05 | ||
| Post | 38.2±6.1 | P>0.05 | 36.3±5.4 | P>0.05 | >0.05 | |
| pH | Pre | 7.409±0.06 | 7.343±0.12 | 0.027 | ||
| Post | 7.443±0.04 | P=0.002 | 7.363±0.13 | P>0.05 | 0.017 | |
| HCO3 (mEq/l) | Pre | 23.1±3.5 | 21.4±4.5 | >0.05 | ||
| Post | 25.3±4.0 | P=0.004 | 20.7±5.6 | P>0.05 | 0.004 | |
| BE (mEq/l) | Pre | –0.88±3.31 | –3.99±6.13 | 0.054 | ||
| Post | 1.66±3.46 | P=0.0002 | –3.99±7.36 | P>0.05 | 0.005 | |
| Cr (mg/dl) | Pre | 1.05±0.66 | 1.55±0.93 | 0.046 | ||
| Post | 0.96±0.60 | P>0.05 | 1.62±1.05 | P>0.05 | 0.019 | |
| WBC (/mm3) | Pre | 9,940±8,831 | 8,155±7,805 | >0.05 | ||
| Post | 10,744±6,677 | P>0.05 | 8,522±4,269 | P>0.05 | >0.05 | |
| Plt (×103/mm3) | Pre | 18.1±11.3 | 13.7±6.6 | 0.052 | ||
| Post | 12.9±7.4 | P=0.008 | 7.98±5.5 | P=0.008 | 0.005 | |
| CRP (IU/dl) | Pre | 15.4±10.3 | 10.4±9.9 | >0.05 | ||
| Post | 22.8±9.3 | P=0.0003 | 19.9±11.5 | P=0.01 | >0.05 | |
| Endotoxin (pg/ml) | Pre | 1.13±2.35 | 8.00±19.9 | >0.05 | ||
| Post | 0.21±0.65 | P=0.01 | 0.48±1.25 | P>0.05 | >0.05 | |
| GCS | Pre | 10.3±2.6 | 8.72±2.4 | 0.025 | ||
| Post | 10.4±2.8 | P>0.05 | 8.50±2.4 | P>0.05 | 0.008 | |
| APACHE II score | Pre | 14.8±5.4 | 21.2±8.1 | 0.005 | ||
| Post | 13.5±5.3 | P>0.05 | 19.4±6.9 | P>0.05 | 0.003 | |
| SOFA score | Pre | 6.70±2.72 | 8.44±3.11 | 0.044 | ||
| Post | 7.00±2.77 | P>0.05 | 11.2±4.03 | P=0.03 | 0.0005 | |
| SIRS | Pre | 2.02±0.99 | 2.16±1.20 | >0.05 | ||
| Post | 1.44±1.10 | P=0.02 | 1.61±1.20 | P>0.05 | >0.05 | |
| PMX times | 1.74±0.44 | 1.89±0.32 | >0.05 |
Values are expressed as mean±SD.
PMX-DHP施行前後でパラメーターを比較した場合,生存群ではpH(HCO3–,BE)の有意な改善(P=0.002)とendotoxin値(P=0.01),SIRS該当項目数(P=0.02)の改善を示した.一方,Pltは減少し(P=0.008),CRPは有意に上昇していた(P=0.0003).死亡群ではPMX-DHP施行にもかかわらず改善を示したパラメーターはなく,有意なPltの減少(P=0.008)とCRPの上昇(P=0.01),そしてSOFA scoreの悪化(P=0.003)を示した(Table 2).単変量解析で有意差を認めたパラメーターに関しては,経過を提示した(Fig. 2).
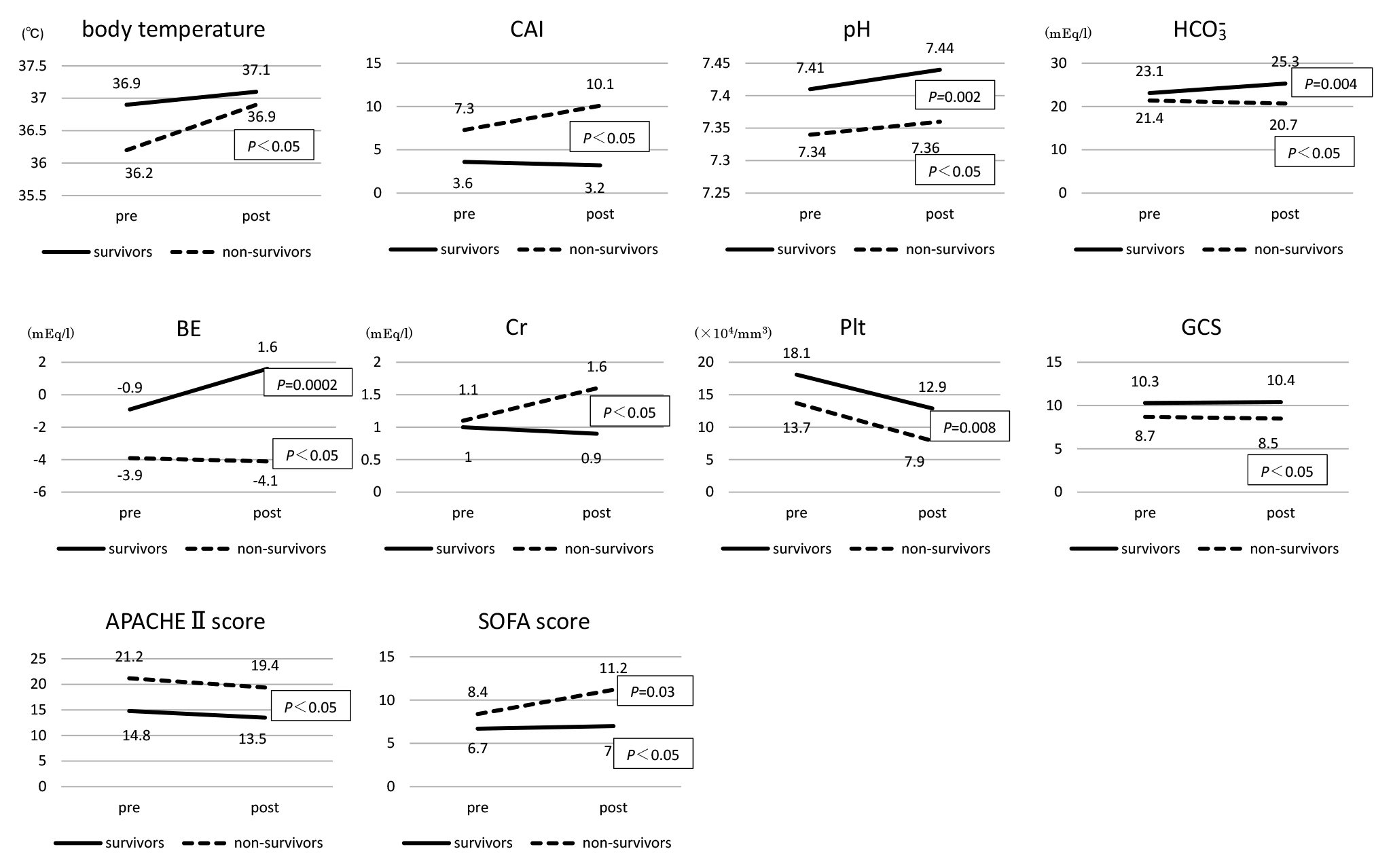
Clinical course of the statistically significant factors identified via univariate analysis.
単変量解析で有意差を認めたパラメーターのうち,scoring systemに含まれる共通項を除外し,PMX-DHP施行前後のAPACHE II scoreおよびSOFA scoreを共変量として多変量解析(ロジスティック回帰分析,変数増加法)を行った.その結果,PMX-DHP施行後のSOFA scoreのみが独立したリスク因子として抽出された(Table 3).
| P value | Odds ratio | 95% confidence interval | |
|---|---|---|---|
| Pre APACHE II score | >0.05 | — | — |
| Post APACHE II score | >0.05 | — | — |
| Pre SOFA score | 0.056 | 0.674 | 0.449–1.010 |
| Post SOFA score | 0.0001 | 1.92 | 1.335–2.761 |
消化管穿孔をはじめとした汎発性腹膜炎は早期にグラム陰性菌による菌血症を発症し,不幸な転帰をとることが多い.患者救命のためには緊急手術などによる病因治療に加え,EGTDに沿った集学的治療の充実が望まれる.PMX-DHPは本邦で開発された装置で,endotoxin吸着のみならず二次的に炎症性サイトカインを抑制すると考えられているため,敗血症性ショックの治療の一環として多施設で利用されている.近年,PMX-DHPカラムはanandamide(ANA)や2-arachidonyl grycerol(2-AG)といった内因性大麻を吸着して血管拡張作用を阻害し,血圧の改善に寄与することが分かってきた2)~4).また,それらのearly mediatorだけでなく,late mediatorであるhigh mobidity group box-1(以下,HMGB-1と略記)も制御する可能性が指摘されている5)6).
EUPHAS(early use of polymyxin-B hemoperfusion in abdominal sepsis)の多施設合同研究では,緊急手術を要する汎発性腹膜炎による敗血症性ショック症例に対し,PMX-DHPが血行動態の改善をもたらし院内死亡率や生存期間を有意に改善すると報告している6).本研究は現在,結果が判明している世界唯一のPMX-DHPに関する大規模randomized controlled trial(以下,RCTと略記)であるが,試験自体が早期終了になっていることなど問題も多く指摘されている.
PMX-DHPは本邦においても多くの施設で施行されてきたにもかかわらず,消化管穿孔術後敗血症に有効であったとする報告7)8)や,救命に寄与しなかったとする報告9)もあり,導入当初から20年程経った現在でもその有効性に関しては一定の見解が得られていない.現状はPMX-DHPの導入・開始基準,施行時間,施行回数なども実施施設が独自の基準に従って施行していると思われる.秋吉ら10)はPOSSUM(physiological and operative severity score for the enumeration of mortality and morbidity)で予測死亡率が50~70%の症例がPMX-DHPのよい適応だと述べている.また,導入のタイミングとしては,hyperdynamic stateの時期に,可及的早期の導入が望ましいとの意見が多い8)11)12).当科においても適応と判断すれば早期導入を行っていたが,発症からPMX-DHP施行までの時間に統計学的有意差は認めなかった.これは発症から手術までの時間も含めて,個々のデータにバラツキが大きかったことが一因と考えられる.ただし,生存群のPMX-DHP施行前体温は死亡群に比べて有意に高値であり,これは敗血症性ショックにおけるhyper-dynamic stateでの導入の有効性を示唆するものと考えられる.また,PMX-DHPの1回当たりの施行時間は,添付文書によると通常2時間とされている.これはPMX-DHPの臨床効果を反映した施行時間ではなく,動物実験において吸着カラムが平衡状態に達するとされる時間に他ならない.実際PMX-DHPの2時間以上の長時間使用による安全性と臨床効果改善の報告は複数ある11)13).当科でも1回当たりの施行時間や2回目施行に関する明確な基準はなく主治医の判断で施行しており,最適施行時間・施行回数の基準制定も今後の課題の一つである.
以前よりPMX-DHPが末梢血管抵抗を改善させることで昇圧効果を有し14),その結果,肺酸素化能が改善することが報告されている15).また,PMX-DHP自体の作用としての組織酸素化の改善機能も指摘されている16).Vincentら17)はPMX-DHPにより循環動態が改善すると報告しており,また安田ら18)は循環動態の改善が良好な予後に直結すると述べている.本邦の過去の報告例を検証してみると,PMX-DHP施行後は生存群・死亡群にかかわらず有意な血圧上昇,或いは循環動態の改善を示しており,CAIの低下が治療効果判定の目安になるとする報告が多い13)14)19)20).また,中村ら21)はPMX-DHPが腎機能を著明に改善させると報告している.本検討でも,MAP,PaO2/FiO2,Crともに生存群で有意差は認めないが,若干の改善傾向を示していた.しかし,死亡群ではむしろ増悪傾向を示しており,これはPMX-DHPの効果を否定するものではなく,患者の状態自体が重篤であったことが要因と思われる.
本検討において,Pltは両群ともにPMX-DHP施行前後で有意な低下を示した.これは病態そのものによる消費に加え,カラム内での凝集・補足の影響が強いものと思われる22)23).
Endotoxinはグラム陰性桿菌の外膜を構成するlipopolysaccharideの一部分であり,敗血症に関与するpathogen associated moleculer patterns(以下,PAMPsと略記)の一つとして測定・利用されている.しかし,血中endotoxin値とサイトカイン濃度は相関しておらず16)24),また必ずしも病勢や臨床経過を良好に反映しているとはいえないようである25).本検討ではendotoxin値に生存・死亡群間で有意差を認めなかったが,生存群においてはPMX-DHP施行により有意に改善していた.PMX-DHPにより血中endotoxin値が有意に改善するという報告は複数存在し7)26)27),その変化は治療効果や生命予後を判断する上で有用である可能性がある.ただし,上記の理由でendotoxin値単体のみで病勢評価を行い,PMX-DHP導入判定基準とすることは多少強引と思われるため,今後はHMGB-1など他のPAMPs測定が充実すれば,それらとの組み合わせで判断することが望ましいであろう.特にPMX-DHP導入の判断材料となるような,或いは臨床経過を反映するようなPAMPs測定の開発・普及が望まれるところである.
本検討における重症度scoring systemに関する検討では,APACHE II scoreおよびSOFA scoreとも他文献7)8)同様に,死亡群で有意に高値を示していた.特に多変量解析の結果が示す通り,PMX-DHP施行にもかかわらずSOFA scoreが悪化する症例は生命予後が芳しくないと思われる.このような多臓器不全を有する症例にはPMX-DHPによる救命効果は期待できず,その限界点を示唆するものと思われる.本検討ではscoring systemのcut off値についての検討は行っていないが,斎藤ら28)によるとAPACHE II score >20,SOFA score >10の症例,4臓器以上の臓器障害合併例はPMX-DHP施行によっても救命困難であると報告している.また,POSSUMに関していえば,予測死亡率70%以上の症例には有効でないとする報告もある10).PMX-DHPは高額かつ高度侵襲を伴う医療行為であり,安易な導入は控えるべきであり,適応判断の際にはその限界点も十分に考慮する必要がある.
現在PMX-DHPの有用性に関して,欧米で二つの大規模RCTが進行中であり,フランスにおけるABDO-MIX,アメリカにおけるEUPHRATES trialがそれに当たる29)30).本邦においてこのようなRCTは倫理的な問題から実施困難であるため,それらの研究結果によって一定の方向性が示されるのではないかと期待される.
利益相反:なし