2015 年 48 巻 8 号 p. 698-705
2015 年 48 巻 8 号 p. 698-705
今回,我々は大動脈周囲リンパ節転移陽性の膵癌に対しgemcitabine+S-1併用療法(以下,GS療法と略記)後にR0切除が可能となった症例を経験したので報告する.患者は66歳の女性で,背部痛で近医を受診し,大動脈周囲リンパ節転移を伴う膵頭部癌と診断された.手術適応外のためGS療法(gemcitabine:1,000 mg/body;day 1,8,S-1:80 mg/body;day 1~14,1コース21日)を開始した.3コース施行後,大動脈周囲リンパ節は著明に縮小しPETは陰性化した.1コース追加後に幽門輪温存膵頭十二指腸切除術を施行した.病理組織学的検査で大動脈周囲リンパ節の転移は消失しており,R0切除しえた.術後13か月目の現在,無再発生存中である.手術適応外の膵癌に対するGS療法は,手術へのconversionを目指すことができる症例では選択肢の一つになりうると考えられた.
遠隔転移を伴う切除不能膵癌に対する化学療法はゲムシタビン塩酸塩(gemcitabine;以下,GEMと略記)やS-1により生存期間の延長を認めるようになった1)2)が手術にconversionできる症例はまれである.今回,我々は大動脈周囲リンパ節転移陽性の膵癌に対しGEM+S-1併用療法(以下,GS療法と略記)後にR0切除が可能となった症例を経験したので報告する.
患者:66歳,女性
主訴:背部痛
既往歴:10歳時に虫垂炎で虫垂切除術
家族歴:特記すべき事項なし.
現病歴:背部痛で近医を受診し,大動脈周囲リンパ節転移を伴う膵頭部癌と診断された(Ph,39×23 mm,TS2,cT3(DU),cN3(n8a,n16a2,n16b1),cM0,cStage IVb).手術適応外のためGS療法(GEM:1,000 mg/body;day 1,8,S-1:80 mg/body;day 1~14,1コース21日)を開始した.3コース施行後,大動脈周囲リンパ節は著明に縮小しPET上では陰性となった.膵頭部癌と周囲リンパ節も縮小したがPETは陽性のままであった.大動脈周囲リンパ節の縮小とPET陰性化により切除可能と判断し,当科に紹介された.
入院時現症:身長160 cm,体重64.4 kg,血圧112/68 mmHg,脈拍78回/分,体温36.6°C,腹部は平坦・軟で腫瘤は触知しなかった.
入院時検査成績:血中CEAは5.5 ng/mlと高値であったが,化学療法前(14.7 ng/ml)と比べ低下していた.CA19-9は8.17 U/mlで正常範囲内だった(化学療法前は10.5 U/ml).WBC 3,050/μl,好中球数869/μl,Plt 7.4×104/μlと化学療法による血液毒性を認めた.
腹部造影CT所見:化学療法前は膵頭部に39×23 mmの低吸収域を認めたが,4コース終了後は27×15 mmに縮小していた(Fig. 1).大動脈周囲リンパ節(16b1)も化学療法前は21×12 mmに腫大していたが,4コース終了後は11×5 mmに縮小していた(Fig. 2).RECISTによる治療効果判定はpartial response(以下,PRと略記)であった.

Abdominal enhanced CT scans show low density area 39×23 mm in diameter at pancreas head (a). After 4 courses of chemotherapy, the low density area decreased to 27×15 mm in diameter (b).
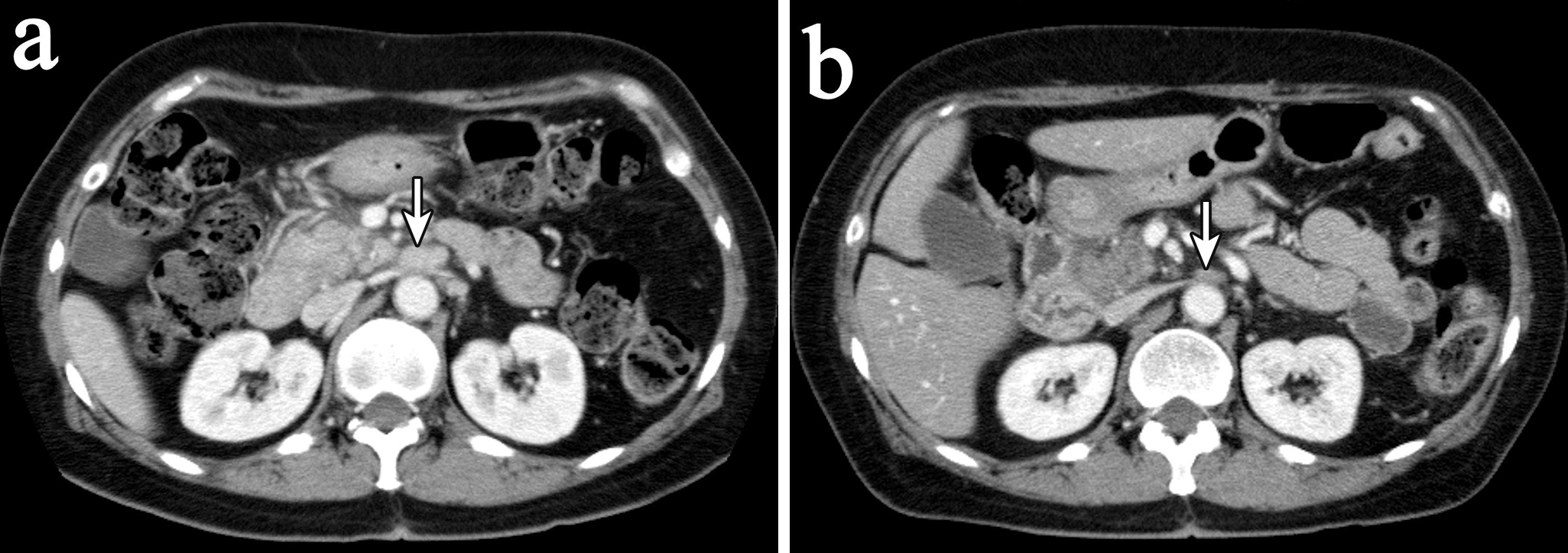
Abdominal enhanced CT scans show swollen paraaortic lymph nodes 21×12 mm in size (a). After 4 courses of chemotherapy, the para-aortic lymph nodes decreased to 11×5 mm in size (b).
PET-CT所見:化学療法前は膵頭部にSUVmax 5.5のFDG集積を認めたが,4コース終了後は2.5に低下していた(Fig. 3).大動脈周囲リンパ節(16b1)のFDG集積も化学療法前(SUVmax 5.0)に比べて,4コース終了後は1.4に低下していた(Fig. 4).
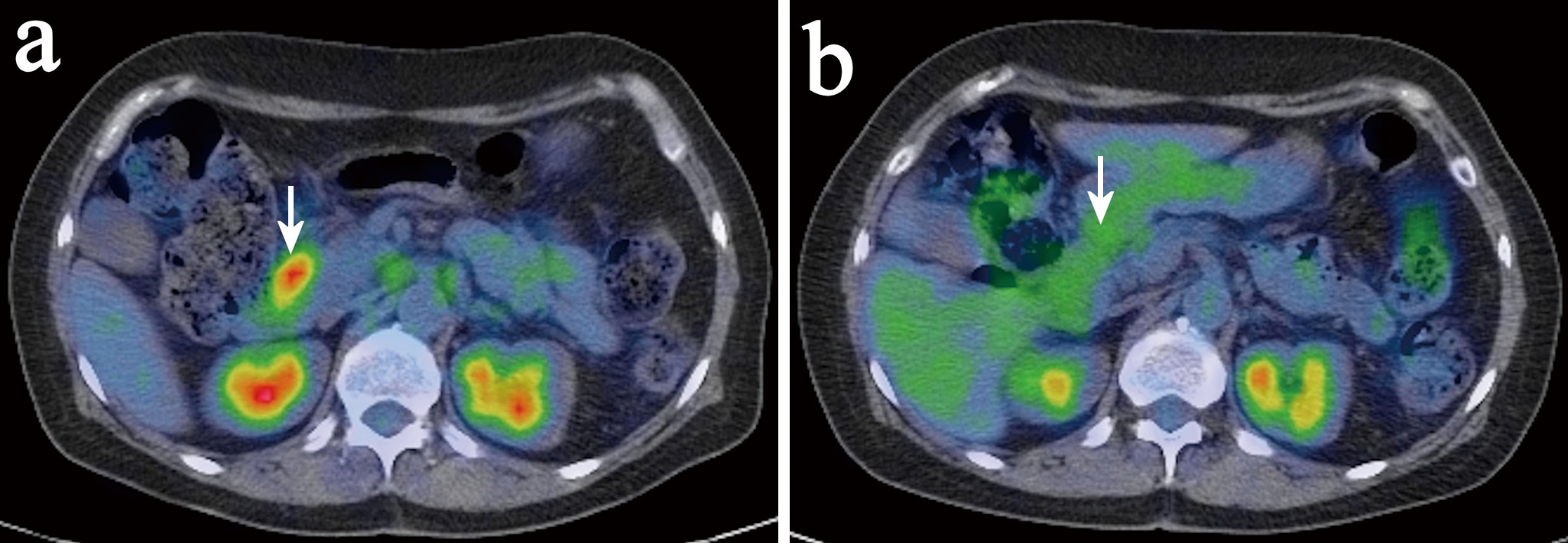
PET-CT reveals high FDG accumulation in the pancreas head, with a standardized uptake value (SUVmax) of 5.5 (a). After 4 courses of chemotherapy, FDG accumulation decreased to 2.5 (b).

PET-CT reveals high FDG accumulation in the para-aortic lymph nodes, with a SUVmax of 5.0 (a). After 4 courses of chemotherapy, FDG accumulation decreased to 1.4 (b).
入院後経過:4コース目の化学療法後7日目に入院されたが,Grade 3の好中球減少とGrade 2の血小板減少を認めた.血液毒性のため長期間の化学療法継続が困難な状況で,治療効果判定はPR,大動脈周囲リンパ節が縮小し,PETで陰性化したことから切除可能と判断し,手術への切り替えを選択した.1週間の休薬期間をおいて血液毒性が回復したことを確認後,手術を施行した.
手術所見:幽門輪温存膵頭十二指腸切除術(PPPD-II A-1,D2郭清)+大動脈周囲リンパ節(16a2,16b1)郭清を施行した.大動脈周囲リンパ節は瘢痕様に縮小・硬化していた.
摘出標本所見:膵頭部に27×22×18 mmの白色充実性腫瘤を認めた(Fig. 5).
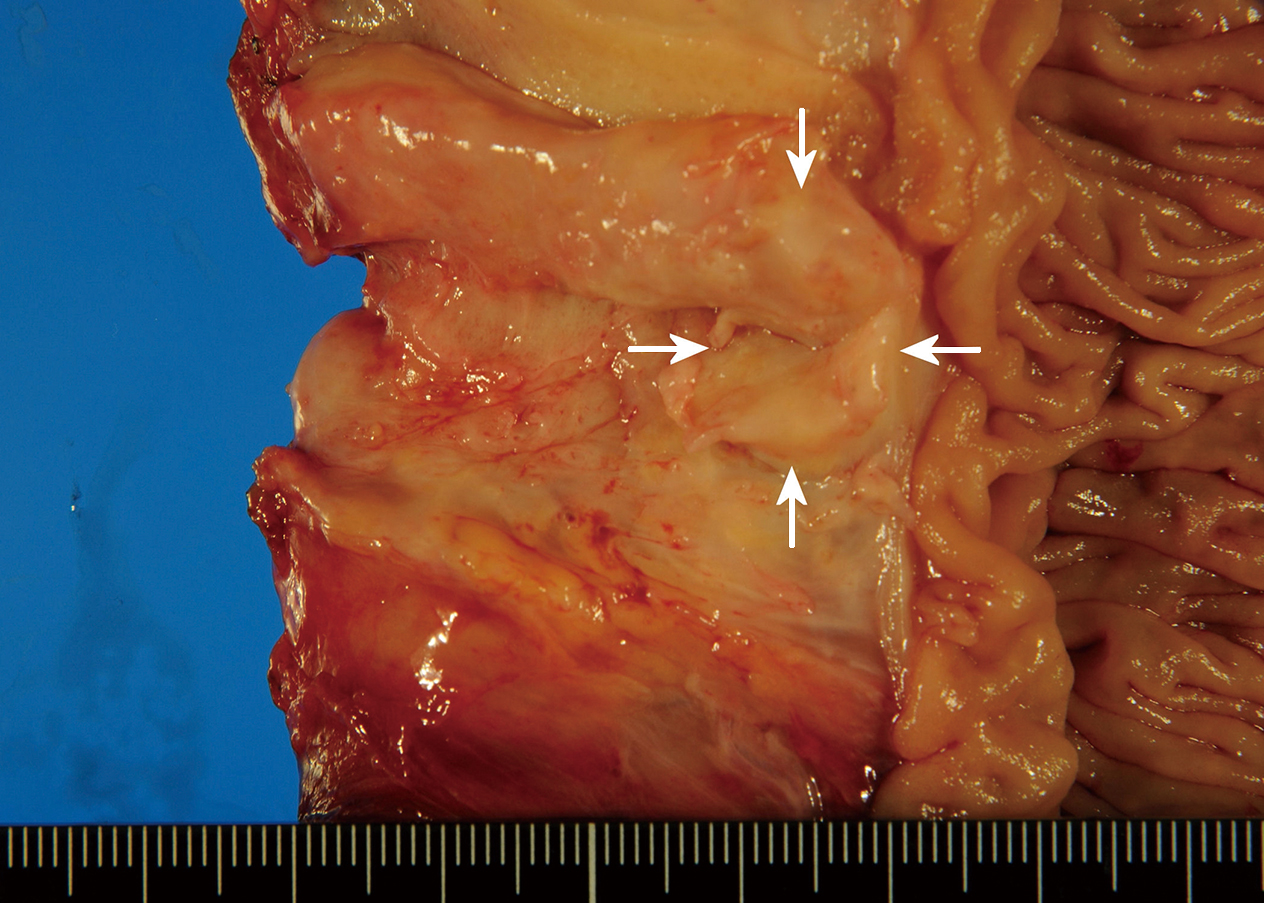
Macroscopic findings show a whitish solid tumor 27×22×18 mm in size at pancreas head.
病理組織学的検査所見:Invasive ductal carcinoma,well differentiated tubular adenocarcinoma,ly0,v0,ne0,mpd(–),pCH(–),pDU(–),pS(–),pRP(–),pPV(–),pA(–),pPL(–),pOO(–),pN2(6:1/7,8a:1/3,8p:0/1,12a:0/4,12b:0/2,12p:0/1,13a:0/2,14p:0/2,14d:0/1,16a2:0/3,16b1:0/7,17a:2/2),pPCM(–),pBCM(–),pDPM(–),pT2pN2sM0,fStage III,D2,R0であった.膵頭部癌は変性した線維性被膜に覆われており,間質は線維化していたが上皮には高分化管状腺癌が残存していた.組織学的効果判定はEvans分類3)に準じ,Grade IIaであった(Fig. 6).大動脈周囲リンパ節は大部分が線維化しており,癌細胞は認めなかった(Fig. 7).総肝動脈幹前上部リンパ節(8a)は一部に膵頭部癌の転移を認めた.
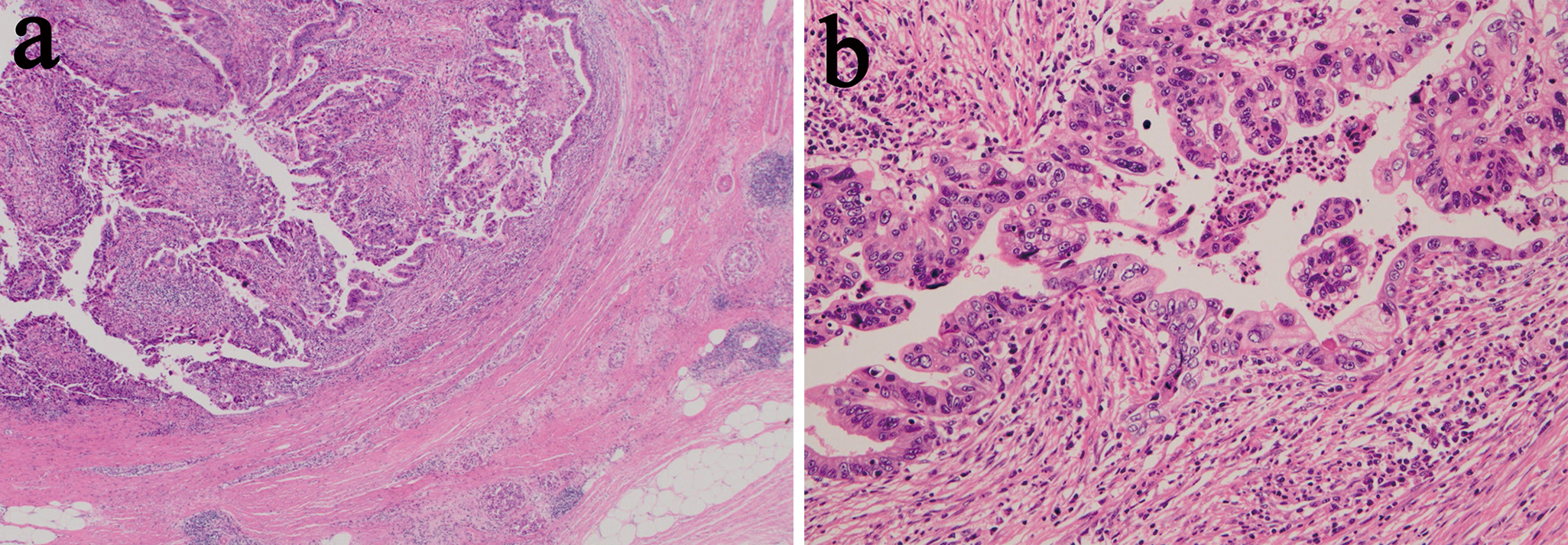
Histopathological findings show interstitial fibrosis and residual well differentiated tubular adenocarcinoma epithelial lining cells in the pancreas head tumor, and which is covered with a degenerated fibrous capsule (HE ×20 in a and ×100 in b).
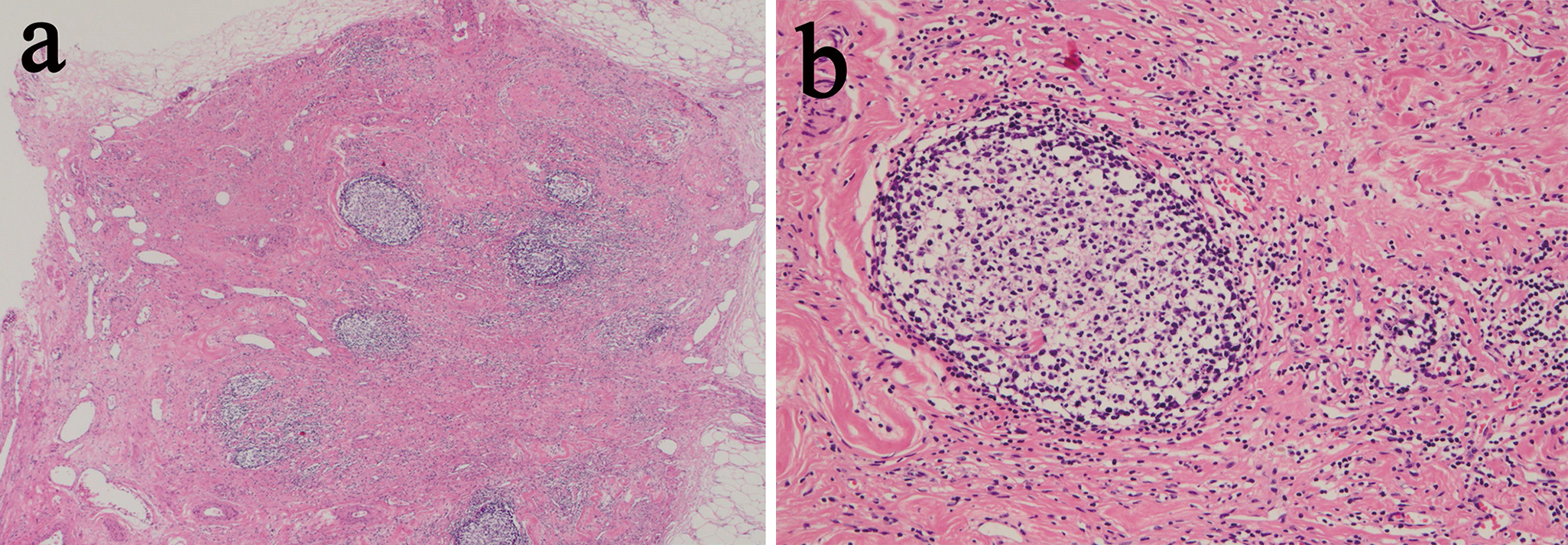
The cancer cells could not be observed in the paraaortic lymph node (HE ×20 in a and ×100 in b).
術後経過:術後経過は良好で,術後第20病日からS-1による術後補助化学療法を開始し,術後第28病日に退院された.その後は前医でS-1内服を継続しており,術後13か月目の現在,無再発生存中である.
切除不能膵癌は極めて予後不良の疾患である.その治療方針として膵癌診療ガイドライン4)では,局所進行切除不能の場合には放射線化学療法,転移切除不能の場合には化学療法が推奨されている.しかしながら,これらの治療成績には限界があり,長期生存を得るためには根治的な外科切除を行うことが唯一の手段である.そこで近年,化学(放射線)療法施行後に有効性を認めた症例に対して根治手術を行う“adjuvant surgery”の概念が導入されてきている5)~8).
特にborderline resectable膵癌を含めた局所進行膵癌では,放射線化学療法によってadjuvant surgeryを施行できる症例も少なからず存在し9)~11),R0切除率の向上や生存期間中央値の改善を認める報告12)もあることから最近の有効な治療手段となっている.一方,転移を伴う切除不能膵癌の場合は化学療法により生存期間の延長を認める1)13)14)もののadjuvant surgeryを施行できる症例はまれである.医学中央雑誌にて「膵癌」,「ゲムシタビン」をキーワードに1977年から2014年6月の論文報告(会議録除く)を検索した結果,転移を伴う切除不能膵癌に対しGS療法施行後にadjuvant surgeryを施行できた症例は自験例を含めて4例のみだった(Table 1)15)~17).これらの化学療法前の切除不能因子は大動脈周囲リンパ節転移が2例,肝転移が1例,腹膜播種が1例であった.原発部位は膵頭部が2例,体部が1例,体尾部が1例で,組織型は高分化型管状腺癌が2例,中分化型管状腺癌が1例,退形成癌が1例であった.一方,GEM単剤療法施行後にadjuvant surgeryを施行できた症例は1例18)のみだった.
| Case | Author/ Year |
Age/Sex | Location | Histological type | Site of metastasis | Cycles of chemotherapy | Adverse events (Grade 3<) | Outcome |
|---|---|---|---|---|---|---|---|---|
| 1 | Sawada15) 2011 |
60s/F | body and tail | mod | peritoneum | 13 | neutropenia | 23m died |
| 2 | Fukui16) 2012 |
77/F | body | anaplastic | liver | 15 | none | 16m alive |
| 3 | Kakizawa17) 2013 |
60s/F | head | well | paraaortic lymph nodes | 21 | none | 4m alive |
| 4 | Our case | 66/F | head | well | paraaortic lymph nodes | 4 | neutropenia | 13m alive |
膵癌診療ガイドラインでは一次化学療法のレジメンとしては,GEM単剤,GEM+エルロチニブ,S-1単剤の3療法が推奨されている.GS療法は,GEST試験2)の結果からGEM単剤,S-1単剤と比較して全生存期間で有意差を認めず,有害事象が高頻度であったことから推奨されていない.一方,同様の比較であるGEMSAP試験19)とJACCRO PC-01試験20)ではGEM単剤と比べてGS療法で生存期間の延長を認めている.奏効率は,いずれの試験でもGS療法の方が高かった.
GEST試験でのGS療法の有害事象としては,血液毒性と食欲不振,下痢,口内炎などの消化器症状の頻度が高いことが報告されている2).今回の集計でも自験例を含めた4例中2例にGrade 3の好中球減少を認めたが中止には至らなかった.
各試験のdose intensityについては,薬剤添付文書のとおりGEM単剤は1コース4週間で4,800 mg,S-1単剤は1コース6週間で3,360 mgに統一されている.一方,GS療法は試験によって投与スケジュールが若干異なり,GEST試験2)では1コース3週間でGEMが3,200 mgとS-1が1,400 mgであるのに対し,GEMSAP試験19)では1コース4週間でGEMが3,200 mgとS-1が1,680 mg,JACCRO PC-01試験20)では1コース3週間でGEMが3,200 mgとS-1が1,680 mgであった.自験例は1コース3週間でGEMが2,000 mgとS-1が1,120 mgであった.自験例は他の試験と比べてdose intensityが少ないがGrade 3の好中球減少を認めたことから,これ以上の増量は困難であった.しかし,その用量でも抗腫瘍効果はあり,大動脈周囲リンパ節転移を消失させることができた.GS療法の各試験における有害事象例の中には,自験例のdose intensityであれば副作用なく投与できるものも存在した可能性があり,効果はあるが副作用が強い症例には減量での対応が良いかもしれない.
手術までのGS療法施行回数は,自験例が最も短く4コースで,他は13~21コースであった.手術に切り替えるタイミングとして決まったものはないが,Satoiら7)は初回の化学(放射線)治療後240日以降に手術を行った症例において良好な生存率が得られたと報告している.その理由として,十分な量の抗癌剤が投与されたことでPR/complete responseの割合が高くなり,適切な症例選択ができたためと結論付けている.自験例ではGrade 3の好中球減少を認め,長期間の化学療法継続が困難と判断し,手術適応外因子であった大動脈周囲リンパ節転移が消失したことから手術へのconversionを選択した.しかしながら,より良い予後を目指すためには他剤へ切り替えながら化学療法を継続し,240日以降に手術をするという選択肢を考慮すべきであった.
以上より,GS療法はGEM単剤と比べて有害事象が多いが奏効率が高く,切除不能からadjuvant surgeryを施行できた症例も報告されていることから,選択肢の一つになりうると考えられた.加えて,2013年12月に切除不能膵癌に対するFOLFIRINOX療法が保険収載された.今後,治療の選択肢が増えたことでadjuvant surgeryに移行できる症例も増えることが予想され,更なる生存率の向上が期待される.
利益相反:なし