2015 年 48 巻 8 号 p. 706-714
2015 年 48 巻 8 号 p. 706-714
症例は72歳の女性で,膵頭部膵管内乳頭粘液性腺癌および膵尾部膵管内乳頭粘液性腺腫に対しmiddle-preserving pancreatectomy(以下,MPPと略記)を行った.術前の造影CTでportal annular pancreas(以下,PAPと略記)Type III aの所見を認めたが指摘しえず術中に診断した.糖尿病の既往があり残膵量を多くするため膵頭側断端は2面となった.PAPを伴う症例に対する膵切除の報告はまれでありMPPを施行した報告はない.今回2,000例の造影CTを検証しPAPは2.05%の頻度であった.PAPはその存在が認識されずに手術が行われている可能性が高い.PAPの存在は切除部位や再建法,術後合併症の発生に大きく影響する.安全に手術を施行し術後合併症のリスクを軽減するためには,PAPの存在を知り術前に診断し,切除範囲や再建方法を熟慮することが重要である.
膵鉤部が上腸間膜静脈・門脈の後方を回り膵体部と癒合する膵奇形は,“portal annular pancreas(以下,PAPと略記)”や“circumportal pancreas”として報告されている.その膵切除症例の報告はまれであり1),middle-preserving pancreatectomy(以下,MPPと略記)を施行した報告はまだない.今回,我々はPAPの膵奇形をともなう膵頭部膵管内乳頭粘液性腺癌(intraductal papillary mucinous carcinoma;以下,IPMCと略記)および膵尾部膵管内乳頭粘液性腺腫(intraductal papillary mucinous adenoma;以下,IPMAと略記)に対し,MPPを施行した1例を経験した.PAPの膵奇形は腹部造影CTで診断可能で,膵手術における膵切離線や再建法に非常に大きく影響するが,術前に指摘しえた報告は少ない.PAPの膵奇形をともなう症例における,術前診断や術式決定の一助となると考えられたため報告する.
患者:72歳,女性
主訴:なし.
既往歴:幽門側胃切除(Billroth I法再建,胃ポリープ,36年前),虫垂切除,末端肥大症,糖尿病,拡張型心筋症,C型肝炎
家族歴:特記事項なし.
現病歴:2008年1月にC型肝炎の経過観察目的にMRIを行い,膵頭部分枝膵管型膵管内乳頭粘液性腫瘍を指摘された.その後,半年ごとに造影CTを行い経過観察されていた.2013年7月の造影CTで,膵頭部病変の増大と充実性病変の出現を認め,手術目的に当科へ紹介となった.
血液検査所見:CEA 1.1 U/ml,CA19-9 9 U/ml,Span-1抗原11.5 U/ml,DUPAN2抗原25.0 U/ml,ヘモグロビン8.8 g/dl,LDH 251 IU/l,HbA1c 7.0%,その他特記事項なし.
超音波内視鏡検査所見:膵頭部に最大径40 mmの囊胞性病変とその内部に壁在結節を認めた.一部で上腸間膜静脈との境界が不明瞭であり,浸潤性IPMCが疑われた.膵尾部は囊胞性病変のみであった.
内視鏡的逆行性膵管造影検査所見:膵管は膵頭部で拡張し蛇行しており,膵尾部に囊胞性病変を認めた.膵管内超音波検査で,膵頭部に乳頭状増殖をともなう多房性囊胞を認め,膵頭部の病変は門脈左縁まで及んでいた.
腹部造影CT所見:膵頭部に31 mm×24 mmの分葉状多房性囊胞を認め,内部には膵実質相で淡く造影される壁在結節を認めた(Fig. 1).膵尾部には26 mm×23 mmの囊胞性病変を認めた.明らかなリンパ節腫大や遠隔転移の所見は認めなかった.膵鉤部が門脈の後方を回り,脾静脈の頭側で完全に膵体部背側に癒合していた.拡張した主膵管は門脈の前方を走行し,門脈後方の膵実質内には明らかな膵管様の構造は確認できなかった(Fig. 2A~C).PAP Type III aの所見であったが,術前には指摘しえなかった.他の内臓奇形は認めなかった.
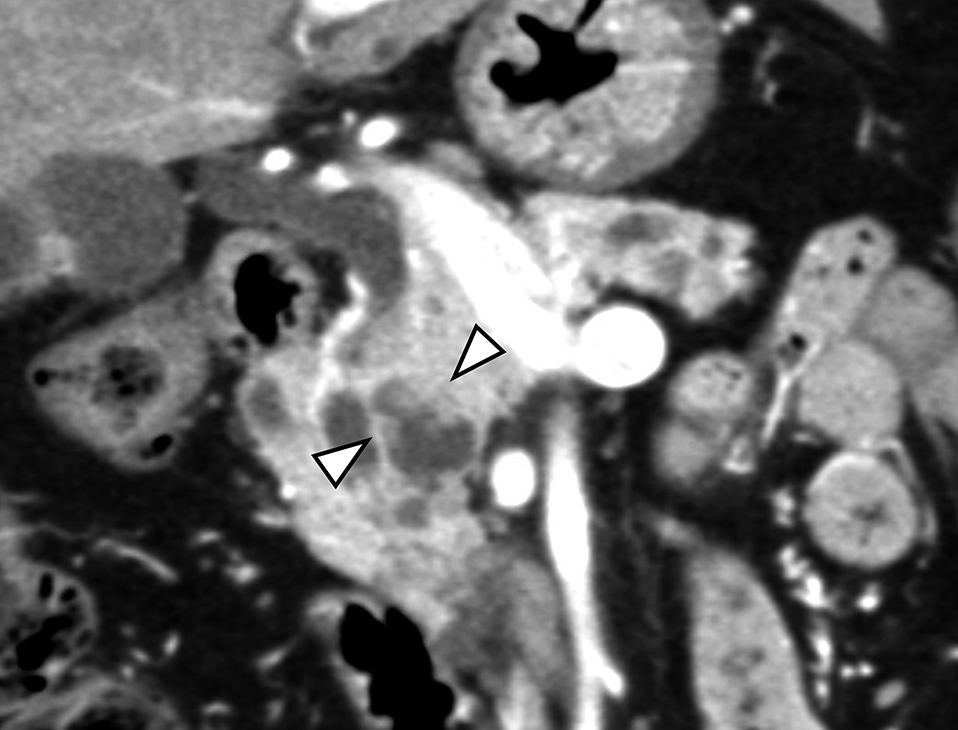
Coronal plane of enhanced CT. Enhanced solid lesion is detected in the cystic wall of the pancreas head (arrowheads).
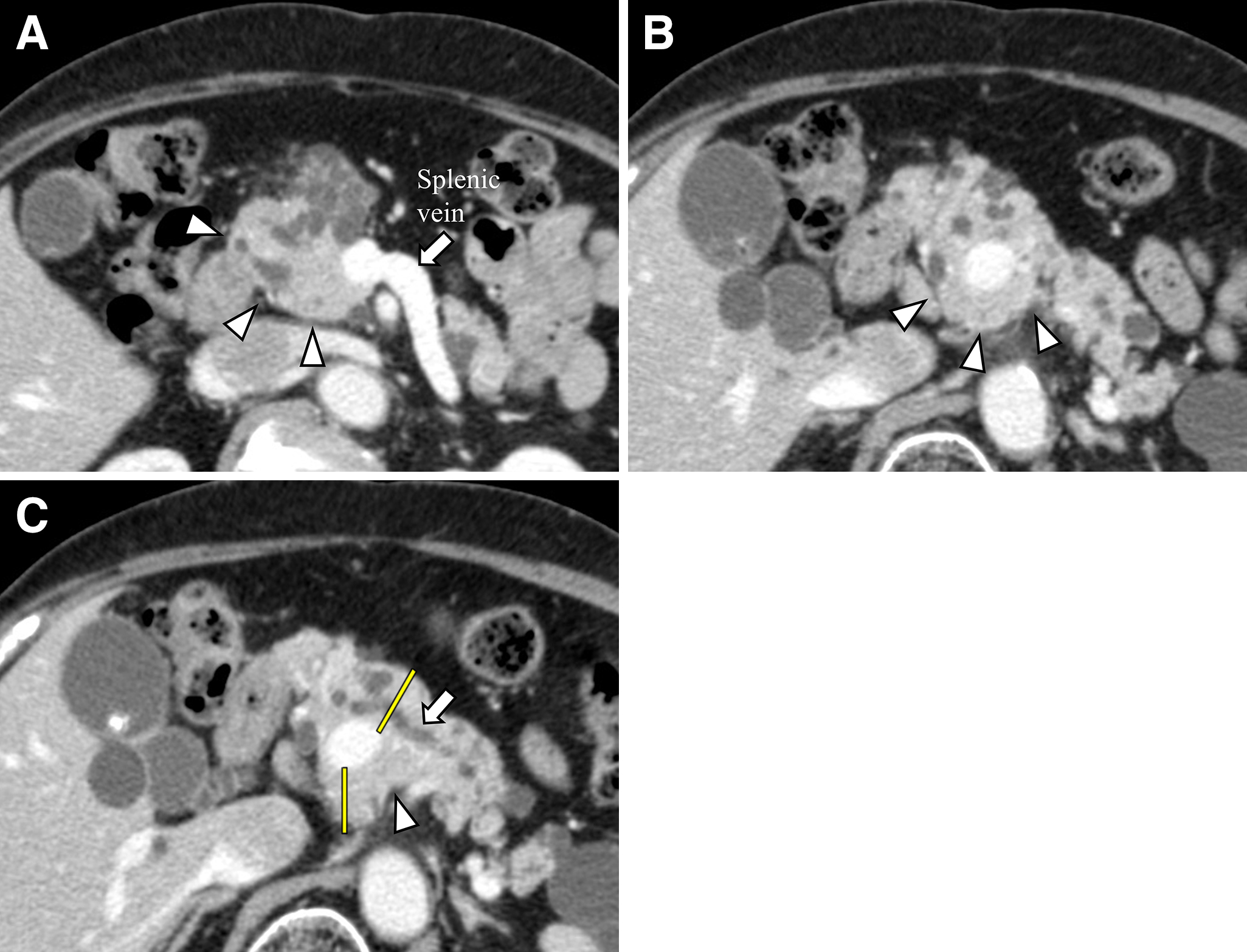
Transverse plane of enhanced CT. A, B: The uncinate process surrounds the portal vein annularly at the cranial side of the splenic vein (arrowheads). C: The main pancreatic duct (arrow) passes on the anterior side of the portal vein. The uncinate process connects with the pancreas body completely (arrowhead). The pancreas head was dissected at the yellow lines.
以上の所見から,膵頭部分枝膵管型IPMCおよび膵尾部分枝膵管型IPMAと診断し,2013年9月に手術を施行した.
手術所見:開腹すると,上腹部の癒着は著明であった.膵頭部病変切離は腫瘍伸展をエコーで確認し門脈左縁で行った.主膵管径は4 mmで軽度拡張を認めた.上腸間膜静脈への浸潤は認めなかった.上腸間膜静脈と門脈をテーピングして膵頭部を右側に牽引し,上腸間膜動脈周囲の処理を頭側に進めると,上腸間膜静脈と脾静脈の合流の頭側で膵鉤部が門脈後方を回り込み膵体部背側に完全に癒合していた(Fig. 3A, B).術前画像と術中エコー所見から,主膵管が門脈前方のみを走行することを確認し,PAP Type III aと診断した.門脈後方膵は門脈の背側で切離し,膵頭側の膵切離面は2面となった.門脈後方膵断端には明らかな膵管様構造は認めなかった.門脈後方膵断端の止血後,サージカルルーペを用いて膵断端を観察し,管腔構造が疑われる部位は微小膵管の可能性があると判断し,4-0合成非吸収糸でZ縫合をかけて処理を行った.背側膵動脈を温存し脾温存膵尾部切除を行い,膵尾側断端は主膵管を縫合閉鎖した.約70 mm長の膵臓が温存された.他の内臓奇形や脈管分岐の異常は認めなかった.膵頭側断面が2面のため,陥入法による膵胃吻合がより安全と考えられたが,幽門側胃切除術後であったため同法は困難であった.門脈前方膵と挙上空腸をBlumgart変法2)を用いて吻合し,IV A-1(Roux-en-Y)型で再建し,手術を終了した.術式はMPP(膵頭十二指腸切除術(D2郭清,Roux-en-Y再建)+脾温存膵尾部切除術)となった(Fig. 4).手術時間は9時間05分,出血量は1,230 mlで,術中に濃厚赤血球4単位の輸血を要した.
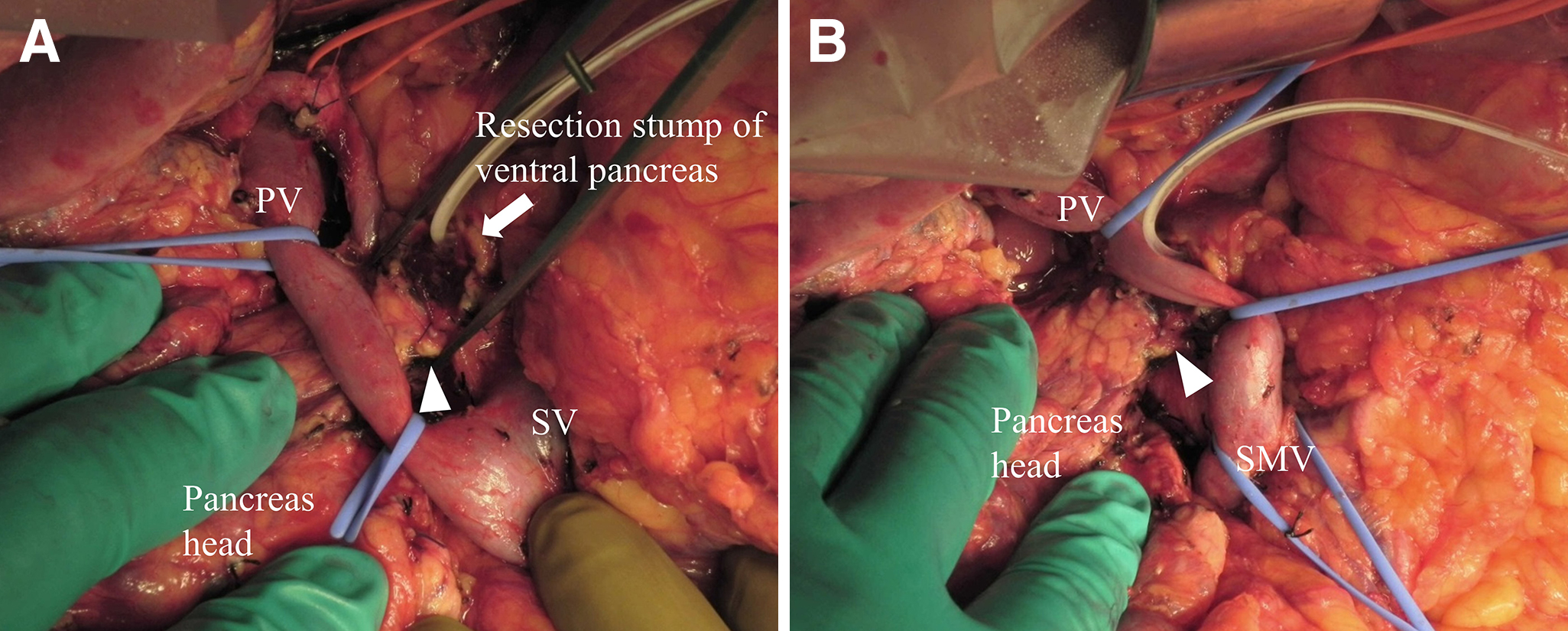
Intraoperative findings. A, B: The uncinated process connects with the pancreas body (arrowhead) at the cranial side of the splenic vein.

Reconstruction was performed in IV A-1 (Roux-en-Y) method.
摘出標本所見:主膵管は前方膵断端に認め,後方膵に明らかな膵管構造は認めなかった(Fig. 5).膵頭部では囊胞性病変と,主膵管内に乳頭状に増殖する充実性病変を認めた.膵尾部は囊胞性病変のみであった.

Formalin-fixed specimens of the pancreas head. Dilated main pancreatic duct is found at the cut end of the anterior pancreas (arrowhead). No structure similar to the pancreatic duct was found at the cut end of the posterior pancreas (arrow).
病理組織学的検査所見:膵頭部病変では膵管内で円柱上皮が乳頭状に増殖し,一部では膵実質に浸潤する所見を認め,浸潤性IPMCの診断で,膵癌取扱い規約(第6版補訂版)に従った進行度はpT1,pN0,M0,fStage Iであった(Fig. 6).膵尾部病変はIPMAであった.
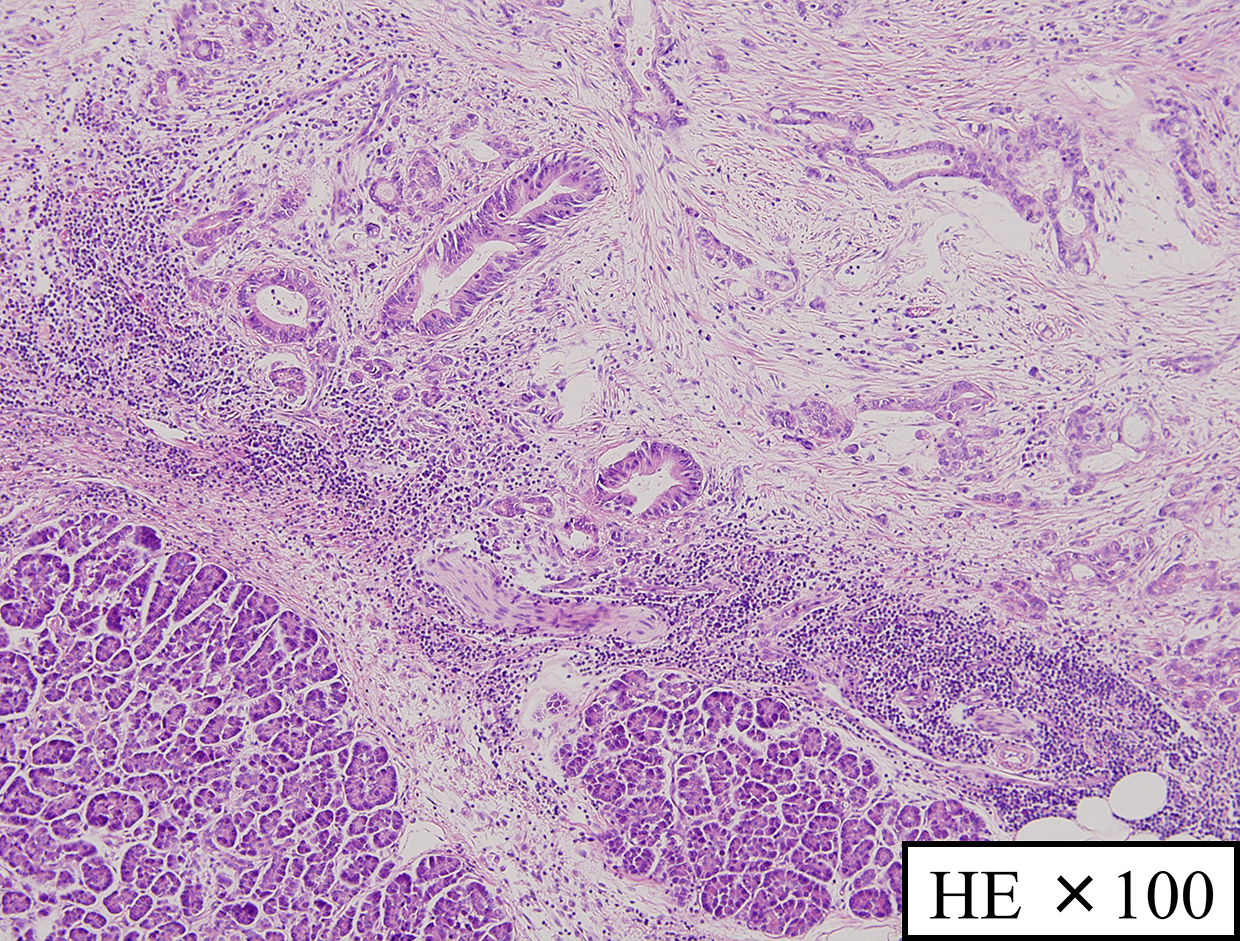
HE stain of the lesion in the pancreas head. It was diagnosed as invasive IPMC.
術後経過:膵空腸吻合部と膵尾側断端でInternational Study Group on Pancreatic Fistula分類Grade Aの膵瘻を来したが保存的に改善し,術後26日目に退院した.術後の耐糖能悪化は認めていない.
膵臓は腹側と背側の二つの膵原基が癒合することにより形成される3).他の臓器と比べてその発生過程は複雑で,輪状膵,異所性膵,膵体尾部欠損症,膵管癒合不全,膵胆管合流異常などの膵奇形が報告されている4).PAPは1.14~2.5%の頻度でみられるとされている5)6).しかし,医中誌Webで「門脈輪状膵」,「portal annular pancreas」,「circumportal pancreas」をキーワードに1977年から2014年までの対象期間で検索し,PubMedで「portal annular pancreas」,「circumportal pancreas」,「encasement of the portal vein」をキーワードに1950年から2014年までの対象期間で検索し,その参考文献も検索したところ,Sugiuraら7)の報告に始まり,膵切除を行った報告は自験例を含め20例のみであり,膵頭十二指腸切除を行った報告は17例のみと,極めてまれである(Table 1)1)5)~19).PAPはJosephら12)により膵管の走行でType I~IIIに分類され,Type IIIはさらに脾静脈と癒合部との関係でType III a~cに亜分類された(Fig. 7).
| No. | Author (Year) | Age/Sex | Disease | Operation | Type | Reconstruction | Preoperative diagnosis | Pancreatic fistula (Grade) |
|---|---|---|---|---|---|---|---|---|
| 1 | Sugiura7) (1987) |
51/F | nodular chronic pancreatitis | pancreatoduodenectomy | III b | P-J unknown |
No | No |
| 2 | Hamanaka8) (1997) |
59/M | carcinoma of the ampulla of vater | pancreatoduodenectomy | III c | unknown | No | unknown |
| 3 | Mizuma9) (2001) |
64/M | carcinoma of gallbladder | pylorus preserving pancreatoduodenectomy and subsegmental (S4/5) resection of the liver | III c | P-J invaginate |
Yes | Yes (unknown) |
| 4 | Marjanovic10) (2007) |
65/F | gastric cancer | subtotal gastrectomy, right hemicolectomy and pancreatic head resection | III c | P-J inosculate |
No | Yes (Grade B) |
| 5 | Hashimoto11) (2009) |
39/F | mucinous cystic adenoma with ovarian stroma and moderate dysplasia | distal pancreatectomy with splenectomy | I | — | Yes | Yes (Grade A) |
| 6 | Karasaki5) (2009) |
73/F | carcinoma of the bile duct | pylorus preserving pancreatoduodenectomy | III b | P-G invaginate |
Yes | Yes (Grade A) |
| 7 | Joseph12) (2010) |
51/M | periampullary carcinoma | pancreatoduodenectomy | II | P-J inosculate |
No | No |
| 8 | Matsumoto13) (2011) |
81/F | carcinoma of the ampulla of vater | pancreatoduodenectomy | II | P-J unknown |
Yes | No |
| 9 | Ishigami6) (2011) |
45/F | insulinoma of the pancreas head | pancreatoduodenectomy | unknown | unknown | No | No |
| 10 | Ishigami6) (2011) |
80/- | IMPN of the pancreas head | pancreatoduodenectomy | unknown | unknown | No | unknown |
| 11 | Ishigami6) (2011) |
65/M | carcinoma of the pancreas head | pylorus preserving pancreatoduodenectomy | unknown | unknown | Yes | No |
| 12 | Saikawa1) (2012) |
84/F | carcinoma of the bile duct | pancreatoduodenectomy | III b | P-J inosculate |
No | Yes (Grade A) |
| 13 | Muto14) (2012) |
45/F | insulinoma of the pancreas head | subtotal stomach preserving pancreatoduodenectomy | II | P-J unknown |
No | No |
| 14 | Shonaka15) (2012) |
53/M | neuroendocrine tumor of pancreas head | pylorus preserving pancreatoduodenectomy | II | P-G invaginate |
Yes | Yes (Grade A) |
| 15 | Jang16) (2012) |
71/M | IMPN of the pancreas head | pylorus preserving pancreatoduodenectomy | III a | P-J unknown |
Yes | Yes (Grade B) |
| 16 | Jang16) (2012) |
74/F | IMPC of the pancreas body | distal pancreatectomy with splenectomy | III c | — | Yes | Yes (Grade A) |
| 17 | Yamaguchi17) (2013) |
80/F | sarcoidosis of pancreas | distal pancreatectomy with splenectomy | I or II | — | No | No |
| 18 | Kobayashi18) (2013) |
61/F | carcinoma of the ampulla of vater | pancreatoduodenectomy | III a | P-J inosculate |
Yes | No |
| 19 | Fukuda19) (2014) |
60s/M | IMPA of the pancreas head | pancreatoduodenectomy | III a | P-J unknown |
No | No |
| 20 | Our case | 72/F | IPMC of the pancreas head and IPMN of the pancreas tail | middle-preserving pancreatectomy | III a | P-J inosculate |
No | Yes (Grade A) |
P-J: pancreaticojejunostomy, P-G: pancreatogastrostomy

Types of portal annular pancreas reported by Joseph et al. in 201012).
PAPの発生原因は明らかではない.膵臓は胎生6~7週に腹側膵原基が十二指腸の回転に伴い背側から左側に回転し,門脈として遺残する左卵黄静脈の右側で癒合し発生する3).過去の報告例や当院での41例の全てで,他の内臓奇形の合併を認めないことから,単純に腹側膵原基と背側膵原基の癒合の際に左卵黄静脈を挟み左右それぞれ2か所で癒合することで発生すると推測される.また,挟み込んだ左卵黄静脈の右側で腹側膵原基と背側膵原基の膵管の吻合が起こればWirsung管が門脈の前方を通るType IIIとなり,左卵黄静脈の左側で膵管の吻合が起こればWirsung管が門脈後方を通るType I/IIとなると説明できる.
PAPの診断は,造影CTで門脈を輪状に取り囲む膵組織を確認することにより容易である.しかし,まれな膵奇形であるため周知に至っておらず,術中所見で診断されることが多い.過去の報告例でも術前に診断しえた症例はわずか19例中9例で半数に満たず,自験例も術中にPAP Type III aと診断した.
Karasakiら5)は,腹部造影CTを受けた700例中8例(1.14%)でPAPを認めたと報告している.また,Ishigamiら6)は,肝移植ドナー317例中8例(2.5%)でPAPを認めたと報告している.今回,我々は2013年に当院で腹部造影CTを行った膵切除の既往のない症例をランダムに2,000例抽出し,PAPの頻度を検証した(Table 2).結果,2,000例中41例(2.05%)でPAPが疑われた.この頻度は過去の報告と一致するものであり,PAPは2%前後の頻度で存在すると思われる.日本消化器外科学会からの報告20)によると年間6,000例以上の膵頭十二指腸切除術が施行されており,100例以上のPAP症例が含まれている可能性がある.しかし,PAPの膵奇形をともなう膵切除の報告は自験例を含めて20例のみである.すなわち,そのほとんどの症例でPAPが指摘されることはなく,上腸間膜動脈周囲の郭清の際に門脈後方膵が集簇結紮により処理されてしまっていることが推察される.PAPという膵奇形を知り正確に診断することにより,無意識下での膵実質処理を避けることができ,結果として術後膵瘻やそれに起因する手術部位感染,ひいては術後出血や術死のリスクを減少させることが期待される.また,我々のデータでは,PAPが疑われる41例中,門脈後方膵に主膵管を認めるいわゆるPAP Type I/IIの症例は1例(2.44%)のみであり,Type III aが32例(78.05%)と最も多かった.過去の報告例においてType I/IIの頻度は16例中6例(37.5%)であり,我々のデータとは解離がある(Table 1).これは,門脈後方を主膵管が通過する場合は,門脈前方膵断端に主膵管構造を認めず術中にPAPの膵奇形に気付きやすく,報告の頻度が高くなっていると推測される.これは逆に,PAP Type IIIに気付かずに門脈後方膵を集簇結紮してしまっているという推察を裏付けるものでもある.
| Incidence of PAP | 41/2,000 (2.05%) |
| Sex | 16/25 |
| male/female | |
| Fusion site | 38/1/2 |
| suprasplenic/mixed/inflasplenic | |
| Main pancreatic duct | 35/1/5 |
| anteportal/retroportal/unknown | |
| Type | 1/32/2/1/5 |
| I or II/III a/III b/III c |
今回,我々はPAP Type III aの膵奇形をともなう膵頭部分枝膵管型IPMCおよび膵尾部分枝膵管型IPMAに対して,MPPを施行した.術前の造影CTでPAPの所見を認めたが指摘しえず,術中所見で診断した.膵頭側の膵切離線が癒合部より膵尾側であれば,膵切離面は一面となり術後膵瘻のリスクは減少する.さらにはPAPのいずれのタイプであっても安全に切離,再建が可能である.Matsumotoら13)もPAP Type IIに対する膵頭十二指腸切除術において,門脈前方膵の切離後に,膵管の合流部の膵尾側で膵臓を追加切除したと報告しており,PAPを伴う症例では癒合の膵尾側での膵切離が望ましいと考える.しかし,今回我々はMPPを予定しており,糖尿病の既往もあることから,残膵を極力多くする目的であえて追加切除は行わずに,膵切離面は2面とした.その結果,現在のところ耐糖能悪化は認めていない.また,MPPは主に良性の多発腫瘍に対して適応とされることが多い21).自験例では,膵頭部病変が微小浸潤までのIPMCであること,膵尾部病変がIPMAであることからMMPの適応とした.残膵への血流を温存することが重要であり,自験例でも背側膵動脈を確認し温存した.
PAPの膵奇形をともなう症例の膵切除の報告は非常にまれであるが,2%前後の頻度でPAPは存在し,決してまれではない膵奇形である.また,その存在は切除部位や再建法,術後合併症の発生に大きく影響する.術前造影CTでの指摘は容易であり,安全に手術を施行し術後膵瘻を含めた合併症のリスクを軽減するためには,この膵奇形の存在を知り術前に診断し,切除範囲や再建方法を熟慮することが重要である.また,MPPは良性の多発病変や微小浸潤性IPMCまでのIPMNに対する良い適応術式であり,残存血流を維持できれば積極的に行うべき術式であると考える.
利益相反:なし