2019 年 52 巻 5 号 p. 247-256
2019 年 52 巻 5 号 p. 247-256
症例は71歳の男性で,30年前に事故で胸部中部食道を損傷し,狭窄を生じていた.嚥下困難増悪の精査で,狭窄部に乳頭状腫瘍が指摘された.生検では炎症や癌が鑑別であったが,数回検査しても確定診断に至らなかった.CTでは不整な壁肥厚と,穿通による肺炎が認められた.癌が否定できず,通過障害や肺炎の原因であるため,手術を行った.腫瘍は浮腫状で柔らかく,胸腔洗浄細胞診,106recリンパ節の迅速診断は陰性であり,定型的な郭清は省略し胸部食道亜全摘を施行した.巨大な疣贅状の腫瘍で,HE染色では扁平上皮の層構造は比較的保たれていたが,粘膜下層に芽出様浸潤が見られた.免疫染色検査で基底層がp53,p63,Ki67強陽性で,核異型・核分裂があり,verrucous carcinoma(以下,VCと略記)と診断された.VCは,扁平上皮癌の亜型で,食道発生はまれである.長期経過をとった食道VCの1例を経験したので報告する.

A 71-year-old man who suffered esophageal damage due to an accident approximately 30 years previously complained of dysphagia. Endoscopic examination revealed a whitish papillary tumor in the esophagus. Biopsy results seemed to suggest an extremely well-differentiated squamous cell carcinoma or inflammation, but a definitive diagnosis could not be reached despite multiple inspections. Chest CT showed irregular thickening of the wall of the esophagus and pneumonia by penetration, and PET showed high trace accumulation in the affected area. We decided to operate on the patient due to the possibility of cancer, potential obstruction to the passage of food, and secondary pneumonia. Intraoperatively, the tumor was found to be soft and edematous, and since intraoperative diagnosis of pleural lavage fluid and the LN around the recurrent laryngeal nerve were negative, we performed thoracic esophagectomy without typical lymph node dissection, and reconstruction using a gastric tube. Gross examination of the tumor revealed a warty appearance. HE staining showed that the squamous laminar structure of the esophagus was maintained, although a slight variant form was present. Immunostaining revealed the tumor to be verrucous carcinoma (VC) with a positive reaction of basal layer to p53, p63 and Ki67 as biomarkers. VC is a subtype of squamous cell carcinoma that most commonly occurs in the mouth. We report a rare case of esophageal VC with a review of the literature of similar cases.
Verrucous carcinoma(以下,VCと略記)は,良悪性の判定が極めて困難な超高分化な扁平上皮癌である.口腔咽頭や外性器領域での報告が多く,食道領域のVCは非常にまれで,食道内容物の停滞や,human papilloma virus(以下,HPVと略記)感染などの慢性炎症が発生の要因として知られている1)~4).今回,食道損傷による狭窄から,粘膜白色肥厚,良性leukoplakiaを生じ,30年を経て巨大な食道VCを生じた1例を経験したので報告する.
患者:71歳,男性
主訴:嚥下困難
家族歴:特記すべきことなし.
既往歴:虫垂炎,高血圧症,高尿酸血症,脳梗塞
生活歴:喫煙 40本/日×47年間(67歳~禁煙).飲酒 2合/日×47年間(67歳~機会飲酒).
現病歴:1984年(41歳),転落事故にて胸部を打撲し,胸部中部食道を損傷し,保存的に治療された.その後,同部に狭窄を生じ,バルーン拡張術が度々施行された.1999年(56歳),狭窄部にヨード不染帯が認められたが,生検では正常扁平上皮と診断された.2001年(58歳)から,同部の粘膜白色肥厚が観察されていたが,2006年(64歳)の生検でも,正常扁平上皮と診断された.2014年2月(71歳時),嚥下困難感増悪のため当院内科を受診し,胸部中部食道に全周性の白色乳頭状腫瘍が指摘された.生検では確定診断には至らなかったものの,臨床的には悪性腫瘍の可能性は否定できず,また経時的に病変部の増悪も認められたため,手術目的に当科へ紹介された.
初診時血液検査所見:Alb 3.3 g/dl,Hb 10.8 g/dと軽度の低下を認めた.SCCは2.4 ng/mlと上昇していた.
上部消化管内視鏡検査所見:2006年9月:切歯より25 cmの胸部中部食道に白色の食道狭窄を認めた.通常スコープは通過せず,細径スコープで観察した.狭窄部近傍のヨード不染帯から生検され,通常の扁平上皮と診断された(Fig. 1a).2014年2月:切歯より25 cmの胸部中部食道に乳頭状の全周性隆起性病変があり,内腔は狭窄していた.この口側のヨード不染帯より生検を施行し,肥厚した重層扁平上皮が認められ,炎症による反応性変化,leukoplakia,papilloma,超高分化な扁平上皮癌などが鑑別とされた(Fig. 1b).2014年3月上旬:乳頭状病変の口側にピンホール状の小孔を認めた(Fig. 1c).2014年3月下旬:小孔は不明瞭となったが,隆起性病変は増大し,内腔狭窄が増悪した(Fig. 1d).経過から,悪性腫瘍を強く疑い,生検を度々行ったが,いずれもleukoplakiaに相当する肥厚した重層扁平上皮を認めたのみで,悪性の診断には至らなかった.3回目の生検では粘膜表層の角質内に細菌,真菌の浸潤が見られた.

Results of upper gastrointestinal endoscopy. a) Benign esophageal stenosis was detected in 2006. b) Papillary elevation was observed in half of the lumen in February 2014. c) A fistula, resembling a pinhole, was seen at the oral end of the papillary lesion in March 2014. d) There was worsening of the stenosis due to the submucosal protruding lesion a couple of weeks after the exam in Fig. 1c.
胸腹部造影CT所見:2014年2月:胸部中部食道から下部食道に造影効果を伴う不整な壁肥厚を認めた.明らかな周囲臓器への浸潤は認めなかった(Fig. 2a).2014年3月:食道の壁肥厚は浮腫を伴い増強し,右肺下葉へ穿通し,炎症を生じていた(Fig. 2b).

Chest CT. a, b) Chest CT showed irregular thickening of the wall of the esophagus. c, d) The wall thickness worsened, communicating through the lower lobe of the right lung, leading to pneumonia.
PET所見:食道にはSUV max 19.7の集積があり,悪性の可能性が高いと考えられた.肺への集積は淡く,炎症による反応の可能性が高いと思われた(Fig. 3).
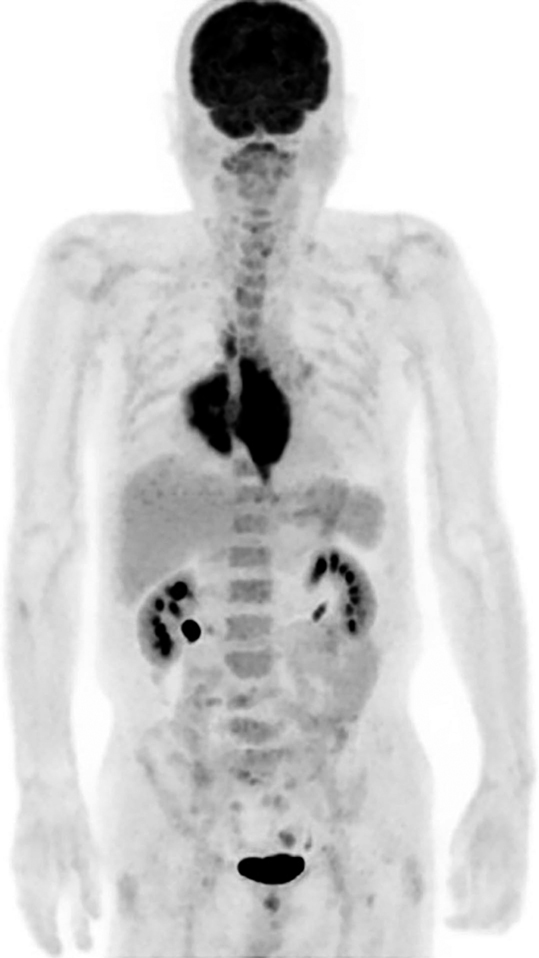
PET indicated the possibility of malignancy, according to the accumulation of tracer in the esophagus.
手術所見:食道は腫瘍状であるが,浮腫が主体で柔らかく,典型的な悪性腫瘍の所見とは異なっていた.胸腔洗浄細胞診,および106recリンパ節の迅速診断は陰性だった.下肺と縦隔は,特に肺への穿通部で強固に癒着していたが,炎症性と考え,癒着部の肺のみを合併切除した.定型的な郭清は省略し,胸部食道亜全摘を行い,細径胃管を胸骨後経路で挙上し,頸部吻合を行った.
切除標本肉眼所見:11.5×9 cm大の巨大な疣贅状腫瘍で,内腔は著しく狭小化していた.ヨードには濃染~淡染された(Fig. 4).

The resected specimen was found to be a verrucous papillary tumor that was mostly stained by iodine.
病理組織学的検査所見:食道壁の層構造は比較的保たれていたが,扁平上皮はびまん性に肥厚・増殖し,基底層には異型増殖が見られ(Fig. 5a),基底突起は粘膜下層に芽出状浸潤性に延長する,構造異型が認められた(Fig. 5b, Fig. 5c(=Fig. 6a)).免疫染色検査では,基底層がp53(Fig. 6b),p63(Fig. 6c),Ki67(Fig. 6d)に強陽性を呈し,核異型・核分裂が活発なことから,VCと診断された.粘膜下層には著明な繊維化や浮腫と毛細血管やリンパ管の増生,出血が見られ,上皮直下には著しいリンパ球や形質細胞浸潤を伴う肉芽性炎症が認められた(Fig. 5d).肺穿通部も炎症性変化が見られるが,悪性像は認められなかった.リンパ節転移はなく,pT1b(SM3),pN0,M0,Stage I(食道癌取扱い規約第11版)であった.HPVは陰性であった.
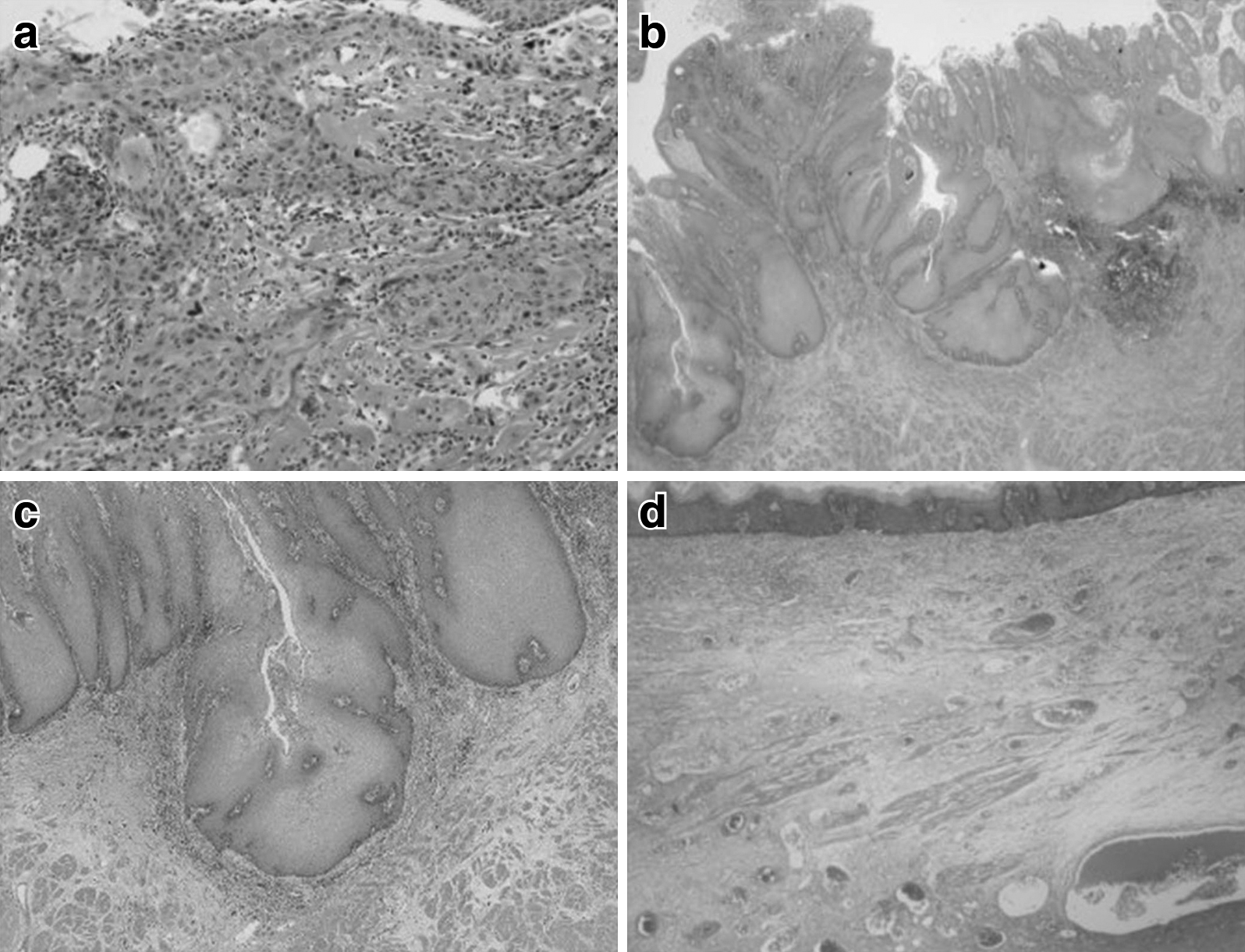
Histopathological findings. a) Localized atypical proliferation was detected (HE ×40). b, c) Exerted basal layer was also found (b: HE ×40, c: HE ×100). d) The laminar structure was retained, but the wall was diffusely thickened (HE ×10).
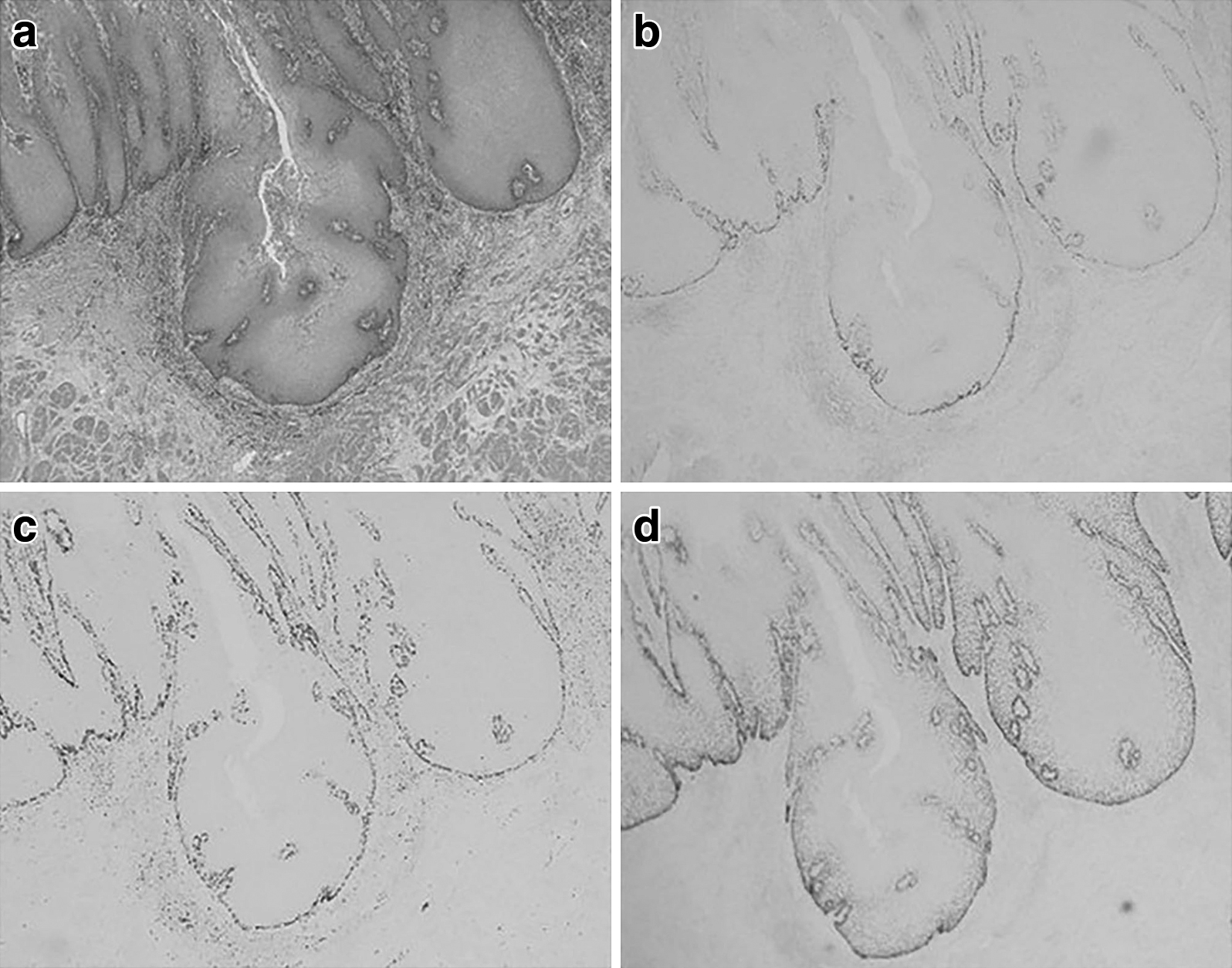
Observations of immunostaining (×100). a) The exerted basal layer stained by HE. b, c, d) The basal layer was deeply stained by p53 (b), p63 (c), and Ki67 (d) markers.
術後,縫合不全と重症肺炎を生じ,集中治療を要した.縫合不全は保存的に改善したが,吻合部狭窄を生じた.呼吸不全は遷延し,気管切開,胃瘻造設を行った.手術後1年8か月後に療養型病院へ転院した.
VCは,扁平上皮癌の1亜型で,白色調の疣状,乳頭状,カリフラワー様の外観を呈する腫瘍で,緩徐な発育と局所伸展を示し,遠隔転移を認めることはまれとされている.口腔領域や耳鼻科領域,外性器領域での報告が多く見られるが,食道領域のVCは非常にまれである1)~4).アカラシアや逆流性食道炎,食道狭窄(薬剤・外傷)など食道内容物の慢性的な停滞を来す背景や,HPV感染などが発生の要因として知られている.同様の背景から生じる良性leukoplakiaや乳頭腫,および悪性腫瘍との鑑別が必要である.角化が目立つ非常に高分化な腫瘍であり,深部への浸潤傾向を呈することから,生検では,粘膜表層のみではなく,深部まで採取しないと,病理診断は困難である.PubMed(1950年~2018年)および医学中央雑誌(1964年~2018年)で「esophagus」,「食道」,「VC」をキーワードにして検索したところ(会議録除く),59例の報告が見られた(Table 1)4)~44).病悩期間の長い症例が多く,診断に至るまでに,数か月から数年かけ複数回の生検を施行したり,より深層から検体を採取したり,生検検体を免疫染色したり,さまざまな試みがなされていた.悪性の所見が得られず,疑い診断で手術に臨み,術後病理組織検査でVCの診断となった報告もある.リンパ節転移が見られたのは1例のみで,遠隔転移の報告はない.本症例は事故による食道損傷後,狭窄を生じ,食道内容物が停滞しやすく,喫煙や飲酒による刺激も長年にわたって加わり,2001年(58歳)頃から食道粘膜の白色変化が生じていた.今回,56歳時と64歳時の生検標本を再検討したところ,いずれも異型や細胞分裂は乏しいが,基底細胞の増殖が認められ,免疫染色検査ではp53,Ki67がわずかに陽性であり,良性のleukoplakia(mild-moderate dysplasia)に合致する像であった.その後,定期フォローはされておらず,今回の手術材料でVCと診断された.Leukoplakiaが段階的にVCに変化したという報告は口腔領域において見られ,Ki67による免疫染色検査で,細胞増殖活性の高い細胞の悪性転化が裏付けられている45).食道においては,平坦な白色病変であったものが,時間経過とともに疣贅状となり狭窄が増悪し,癌の診断に至った報告例が多数ある.本症例でも同様に,慢性炎症により生じた良性leukoplakiaに,さらに炎症が持続的に加わることで,頻繁に細胞分裂を繰り返してVCに進展した可能性は十分に考えられる.VCは,リンパ節転移や遠隔転移を来すことが非常にまれであるため,治療としては局所の制御が重要となる.VCに対して,放射線治療や化学療法が奏効した報告も見られるが,非常に高分化な腫瘍であるため,感受性が乏しい場合や,放射線治療に伴うanaplastic transformationの懸念46)もあり,適応は慎重に選択すべきと考えられる.腫瘍のサイズが比較的大きく,多くの症例で手術が選択されており,根治治療となりえている.また,画像から予測されるより,深達度が浅いことが多いため,ESDで根治が得られた症例もある.本症例では,生検で確定診断には至らなかったが,著明な食道壁肥厚と通過障害,肺への穿通も生じたため,手術を施行した.典型的な悪性腫瘍の所見とは異なり,迅速診断をもとに系統的な郭清は省略したが,局所の制御は得られ,許容しうる治療となった.
| No | Author | Year | Age/Sex | Chief complaint | Imaging findings | Upper endoscopy | Diagnostic procedure | Time span | Treatment | Size (cm) | Stage Outcome |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | Minielly4) | 1967 | 58M | Dysphagia | Deformity of the esophagus | Fungating friable lesion | Biopsy 3 times VC |
Operation | 8.5×9 | POD13 Death | |
| 2 | Minielly4) | 1967 | 70F | Dysphagia Cough |
Large mass with proximal dilation | Warty reddish tumor | Biopsy VC |
8Y | Radiation | ||
| 3 | Minielly4) | 1967 | 70F | Dysphagia | Large mass with proximal dilation | Extensive polypoid necrotic lesion | Biopsy VC |
Radiation | 2M Death | ||
| 4 | Minielly4) | 1967 | 36M | Epigastralgia | Perforation to the large cavity | Moderate esophagitis Perforation couldn’t seen | Biopsy SCC |
10Y | Operation | 9×8 | N+ |
| 5 | Minielly4) | 1967 | 57M | Dysphagia Anorexia |
Obstruction of the lumen | Obstrution | Biopsy review VC |
4Y6M | Dilation | Death | |
| 6 | Parkinson5) | 1970 | 76M | Hematemesis | Complete obstraction with proximal dilation | ①Ulcerating lesion ②Cauliflower-like tumor |
Biopsy →Necropsy SCC →VC |
1Y6M | BSC | 7.5 | Sudden Death |
| 7 | Sridhar6) | 1980 | 54M | Dysphagia | 4 cm filling defect Lobulated surface | Not identified | Surgical specimen VC |
Operation | N0 | ||
| 8 | Sakurai7) | 1983 | 78F | Dysphagia | Large tumor extending to trachea and thyroid | Cauliflower-like grayish red tumor | Biopsy VC |
Bleomysis | 10×5 | Lost of following | |
| 9 | Agha8) | 1984 | 66M | Dysphagia Cough |
Pulmonary infiltrates with mediastinal abscess | Cauliflower-like tumor | Biopsy/ Cytodiagnosis VC |
BSC | |||
| 10 | Barbier9) | 1987 | 50F | Dysphagia | No invasion | Whitish thickening Cobblestone lesion |
Biopsy VC |
6Y | Operation | TisN0M0 Stage 0 | |
| 11 | Koerfgen10) | 1988 | 75M | Dysphagia | No invasion and metastasis | Cauliflower-like tumor | Repeated biopsy SCC |
4Y | Operation | N0 | |
| 12 | Koerfgen10) | 1988 | 54 | Dysphagia | Thickened wall No invasion and metastasis | Exophytic growth with polypoid offshoots | Repeated biopsy SCC |
1Y | Operation | 6.5×6.5 | N0 |
| 13 | Kojima11) | 1988 | 70M | Dysphagia | Lumen occupying tumor | 1/2 of the lumen Cauliflower-like tumor |
Biopsy Atypical SCC |
Operation | 6×5.5×2 | T3N0M0 Stage II | |
| 14 | Jasim12) | 1990 | 79M | Dysphagia Weight loss |
Long segment of irregular narrowing | Irregular stricture with nodular ulcerated surface | Autopsy VC |
6Y | Dilation | 9×6×2 | Death N0 |
| 15 | Biemond13) | 1991 | 76F | Dysphagia Cough Chest pain | Irregular stenosisn and bronchus fistula | Whitish papillary tumor | Autopsy VC |
6M | None | Death N0M0 | |
| 16 | Roach14) | 1993 | 67M | Dysphagia Chest pain |
Soft tissue mass No metastasis | ①Food residue ③Warty polypoid lesion |
Repeated biopsy VC Susp |
1Y8M | Dilation Radiation | 5M Death | |
| 17 | Garrard15) | 1994 | 51F | Dysphagia Epigastralgia |
Mucosal irregularity | ①Raised white plaque ②Irregular circumferencial lesion |
Biopsy SCC |
Operation | |||
| 18 | Takahama16) | 1995 | 73M | Epigastralgia | IIa+IIc Whitish elevation | Biopsy Atypical SCC |
Operation | 9.7×4.5 | T1aN0M0 Stage 0 | ||
| 19 | Malik17) | 1996 | 66M | Dysphagia Chest pain |
Large lumen-occluding mass | ①Erosion of mucosa ②Large friable tumor |
Surgical specimen VC |
2Y | Operation | 5×2 | N0 |
| 20 | Tajiri18) | 2000 | 40M | None (screening) | Elevated, 1 cm papillary lesion | Eleveted papillary lesion | Biopsy VC |
EMR | 0.6×0.8 | TisN0 Stage 0 | |
| 21 | Osborn19) | 2003 | 67M | Dysphagia Chest pain |
Thickened wall | ①White, villous, fungating lesion ②Thickened, whitish, polypoid lesion | Surgical specimen VC |
Operation | 8×8 | N0 | |
| 22 | Devlin20) | 2004 | 56F | Epigastralgia | No metastasis | ①Mucosal irregularity ②Nodular mucosa |
Biopsy 5 times VC |
10M | Operation | 2.7 | N0 |
| 23 | Petris21) | 2005 | 73M | Dysphagia Weight loss |
No metastasis | Stricture | Surgical specimen VC |
1Y2M | Operation | N0 | |
| 24 | Petris21) | 2005 | 58M | Dysphagia Weight loss |
Mass at the EGJ No metastasis | Poorly demarcated tumor Stricture |
Surgical specimen SCC |
6M | Operation | 6×5.5 | N0 |
| 25 | Mizutani22) | 2005 | 72M | Hematemesis Asitia |
Circumferential irregular tumor | Lumen occupying warty elevation | Biopsy SCC |
Operation | 8.0×7.0 | T3N0M0 Stage II | |
| 26 | Miyako23) | 2005 | 50M | Dysphagia | Circumferential thickened wall | Traverse whitish elevation | Biopsy 3 times SCC |
Operation | 3 2 spots |
T1bN0M0 Stage I | |
| 27 | Na24) | 2009 | 50M | Dysphagia Weight loss |
Thickened wall No metastasis | Papillary lesion | Biopsy 5times large biopsy/VC |
1Y | Operation | 7.5×4.8 | T2N0M0 Stage II |
| 28 | Oh25) | 2009 | 73F | Epigastralgia | Irregular and granular surface | 2/3 of the lumen Cauliflower-like whithish lesion |
Repeated biopsy Immunostaining/VC |
1Y5M | Refused Treatment | 3.5 | |
| 29 | Garcia26) | 2010 | 71F | Gastriesiphageal reflux | No metastasis | Exophytic, whitish, warty tumor stricture | Surgical specimen VC |
Dilation Operation | 3.9×2.5 | T2N0M0 Stage II | |
| 30 | Tonna27) | 2010 | 61M | Dysphagia Chest pain |
①Whitish plaque ②Nodular mucosa |
Surgical specimen VC |
11Y | Operation | 10 | M0 | |
| 31 | Munson28) | 2010 | 63F | Dysphagia Cough Chest pain | Intramucosal nodularity | ①Thickened, friable mucosa ②Circumferential tumor |
Biopsy SCC, VC |
1Y | CRT | 16 | cT3N1M0 Stage III |
| No | Author | Year | Age/Sex | Chief complaint | Imaging findings | Upper endoscopy | Diagnostic procedure | Time span | Treatment | Size (cm) | Stage Outcome |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 32 | Osawa29) | 2011 | 76F | Epigastralgia | Slight anomalia | 3/4 of the lumen 0-I+0-IIa |
Biopsy SCC |
Operation | 6.6×3.6 | T1aN0M0 Stage 0 | |
| 33 | Nishi30) | 2011 | 66M | Dysphagia Epigastralgia | Thickened wall LN swelling | Ulcerative and papillary lesion Stricture |
Surgical specimen VC |
Operation | 4.8×4.5 | T3N0M0 Stage II | |
| 34 | Taniyama31) | 2012 | 74M | Nausea | Thickened wall 7 cm in diameter | Many nodes | Biopsy 3 times deep layer/SCC |
11M | Operation | ||
| 35 | Vieira32) | 2013 | 58M | Dysphagia Weight loss |
No metastasis | Whitish pseudopolypoid lesion Stricture |
Surgical specimen SCC |
Dilation Operation | T2N0M0 Stage IIA | ||
| 36 | Ahmed33) | 2013 | 58F | Dysphagia | Soft tissue fullness | Large semi-pedunculated polype | Large biopsy VC Susp |
CRT Operation | |||
| 37 | Sweetser34) | 2014 | 61M | Dysphagia Weight loss |
Warty whitish lesion | 10Y | Operation CRT | T2N0M0 Stage II | |||
| 38 | Sweetser34) | 2014 | 73F | Dysphagia Odynophasia | Circumferential polypoid tumor | 6Y | CRT | ||||
| 39 | Sweetser34) | 2014 | 66M | Dysphagia Odynophagia | Multilobular, obstructing whitish polypoid tumor | 7Y | Operation | T1N0M0 | |||
| 40 | Sweetser34) | 2014 | 70F | Dysphagia Weight loss |
Superficial exophytic whitish lesion | FNA SCC |
3Y | Operation | T1N0M0 | ||
| 41 | Sweetser34) | 2014 | 71M | Dysphagia | Hemicircumferential polypoid tumor | 20Y | |||||
| 42 | Sweetser34) | 2014 | 57M | None | Villous shaggy tumor | ||||||
| 43 | Sweetser34) | 2014 | 75F | Dysphagia Weight loss |
Polypoid mucosa | 2Y | |||||
| 44 | Sweetser34) | 2014 | 62M | Dysphagia Weight loss |
Warty whitish tumor Stricture |
2Y | Operation | T3N0M0 Stage II | |||
| 45 | Sweetser34) | 2014 | 63F | Dysphagia | Circumferential whitish lesion Stricture |
2Y | CRT | ||||
| 46 | Sweetser34) | 2014 | 68M | Dysphagia | Exophytic polypoid tumor Thickened mucosa |
1Y | Operation CRT | T1N0M0 | |||
| 47 | Sweetser34) | 2014 | 62F | Dysphagia | Exophytic polypoid tumor Thickened white plaque |
1Y | Operation | T1N0M0 | |||
| 48 | Behrens35) | 2014 | 77M | Odynophagia | No metastasis | Circumferential irregular mucosa | Biopsy 2times VC |
6M | EMR | R1 (HM) | |
| 49 | Ramani36) | 2014 | 78M | Dysphagia Weight loss |
Long irregular stricture Some mediastinal LN |
Irregular intraluminal tumor | Repeated Biopsy deep layer/VC |
Dilation CRT | 5 | ||
| 50 | Brandalise37) | 2015 | 64M | Dysphagia Weight loss |
Thickened wall Obstruction of the lumen | ①Whitish plaque ②Growth of vegetation |
Surgical specimen VC |
Operation Radiation | 16 | T3N0M0 Stage II | |
| 51 | Egeland38) | 2016 | 67M | Dysphagia Weight loss |
Thickened wall | ①Candida infection ②Ulcer and protruding lesion |
Surgical specimen VC |
10M | Operation | ||
| 52 | Egeland38) | 2016 | 59M | Dysphagia | Whitish irregular mucosa Polypoid lesion |
Surgical specimen VC |
9M | Operation | T2N0M0 Stage II | ||
| 53 | Abe39) | 2016 | 68M | None (screening) | 1 cm polypoid lesion | ESD VC |
ESD | ||||
| 54 | Murawaki40) | 2016 | 60M | Asitia Epigastralgia | No paticular | ①Whitish mucosa ②Elevated lesion |
Repeated biopsy SCC |
1Y1M | ESD | 1.8×1.3 | T1a, ly0, v0 Stage 0 |
| 55 | Ogawa41) | 2016 | 77M | Epigastralgia | Cauliflower-like whithish lesion | Surgical specimen VC |
Operation | ||||
| 56 | Cox42) | 2017 | 62M | Dysphagia | No invasion and metastasis | Warty lesion Stricture |
FNA SCC |
10Y | Operation | 9.5 | N0 |
| 57 | Kakimoto43) | 2017 | 77M | Dysphagea | Circumferential Thickened wall | ①Warty whitish elevation ②Irregular erosion, and stricture |
Repeated biopsy SCC |
7Y | Operation | 4.5×3.1 | T3N0M0 Stage II |
| 58 | Hoffmann44) | 2018 | 61M | Dysphagia | No metastasis | Partially circumferential fungating tumor | VC Susp | Operation | |||
| 59 | Hoffmann44) | 2018 | 52F | Dysphagia | No metastasis | Fibrotic stricture | Biopsy VC Susp |
Dilation Operation | |||
| 60 | Our case | 71M | Dysphagea | Thickned wall Penetration to lung | ①Papillary circumferential elevation ②Growth of the elevation, and fistula |
Surgical specimen Immunostaining/VC |
13Y | Operation | 15×7 | T1bN0M0 Stage I |
SCC: squamous cell carcinoma, FNA: fine-needle aspiration, ESD: endoscopic submucosal dissection, EMR: endoscopic mucosal resection, BSC: best supportive care, CRT: chemoradiotherapy
VCはまれな疾患ではあるが,明らかな危険因子がある場合は,長期間にわたり定期的に経過観察をすることが必要と考えられる.また,VCを疑うにもかかわらず,悪性の診断に至らない場合は,より深部から検体を採取することが最も重要で,免疫染色検査や臨床所見を考慮して総合的に診断することが必要と考えられた.
利益相反:なし