Abstract
先天性代謝異常疾患である糖原病に肝細胞癌が合併することはまれである.今回,我々は肝切除後の術後管理に難渋した糖原病合併肝細胞癌の1例を経験したので報告する.症例は37歳の男性で,小児期に糖原病と診断されたが,成人を機にフォロー終了となっていた.CTで肝右葉を占める径11 cmの腫瘍を認め,造影動態から肝細胞癌と診断した.腫瘍は右,中肝静脈,下大静脈に広範に接しており,2回の肝動脈化学塞栓術を先行したところ,著明に縮小した.血管の圧排所見も改善したことから根治切除可能と判断し,肝右葉切除を施行した.画像上の全肝容積は2,805 mlと高度に腫大を認め,手術操作に難渋した(手術時間493分,出血量850 ml).術後は著明な乳酸アシドーシスを来したが,高濃度ブドウ糖点滴により改善した.術後6日目に左右下横隔動脈から出血し,動脈塞栓術により止血を得た.
Translated Abstract
It is extremely rare for hepatocellular carcinomas to occur in patients with glycogen storage disease. Here, such a case is reported. The patient, a 37-year-old man, was given a diagnosis of hepatocellular carcinoma occupying the right lobe, by CT. A diagnosis of glycogen storage disease had been given in his childhood. Because the tumor extended to the orifice of right, middle hepatic vein, and inferior vena cava, and was considered to be unresectable, he underwent transcatheter arterial chemoembolization. As a result, the size of the tumor was reduced from 11 cm to 7 cm. Right hepatectomy was performed. The volume of blood loss was 850 ml, and the operative time was 493 minutes. The patient experienced two postoperative complications possibly due to his glycogen storage disease. Severe lactic acidosis was treated with high concentration glucose administration on the 2nd postoperative day. Moreover, intraperitoneal bleeding from bilateral inferior phrenic arteries possibly due to the thrombocyte malfunction was stopped with transcatheter arterial embolization on the 6th postoperative day.
はじめに
糖原病I型はglucose-6-phosphatase(以下,G6Paseと略記)欠損により肝臓にglycogenが異常蓄積する疾患であり,20~60%が肝細胞腺腫を合併し,うち11%が悪性化するといわれている1).今回,我々は糖原病I型に続発した肝細胞癌に対し肝右葉切除を施行後に,乳酸アシドーシスと遅発性多発腹腔内出血を合併した1例を経験したため報告する.
症例
患者:37歳,男性
主訴:嘔吐,下痢
既往歴:糖原病I型(小児期に他院で診断され,成人を機にフォロー終了となっていた).
現病歴:嘔吐,下痢の精査のため前医で施行されたCTで偶発的に肝腫瘤を指摘され,当院に紹介された.
初診時現症:身長160.4 cm,体重50.6 kg.人形様顔貌を認めた.
初診時血液検査所見:HBs抗原(−),HCV抗体(−).腫瘍マーカーは,AFPは正常値だったが,PIVKA-IIは1,071 mAU/mlと高値であった.
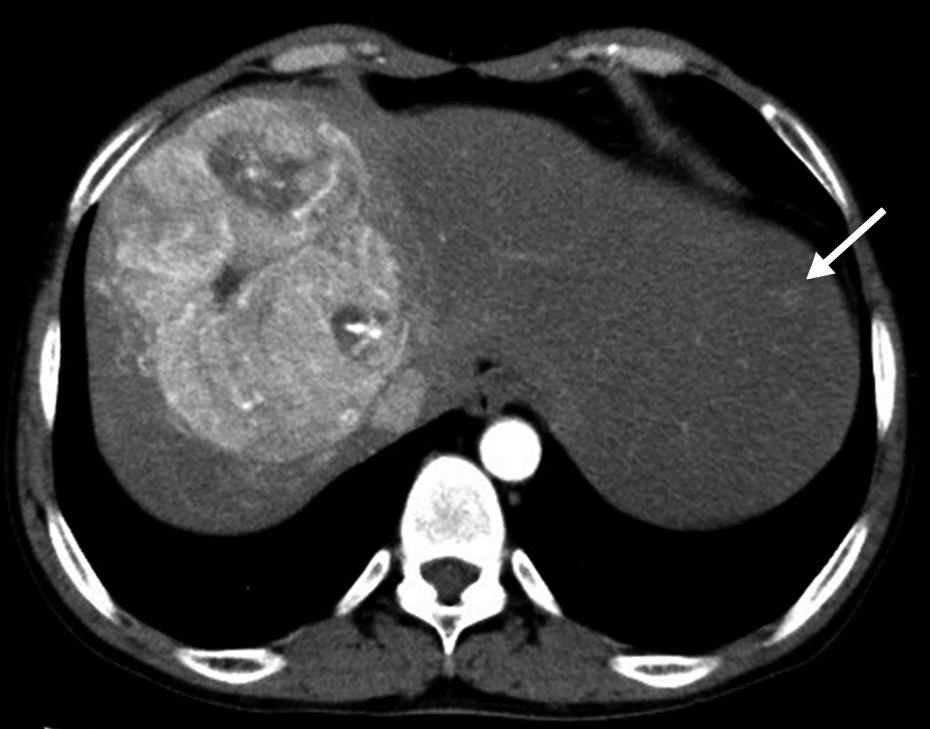
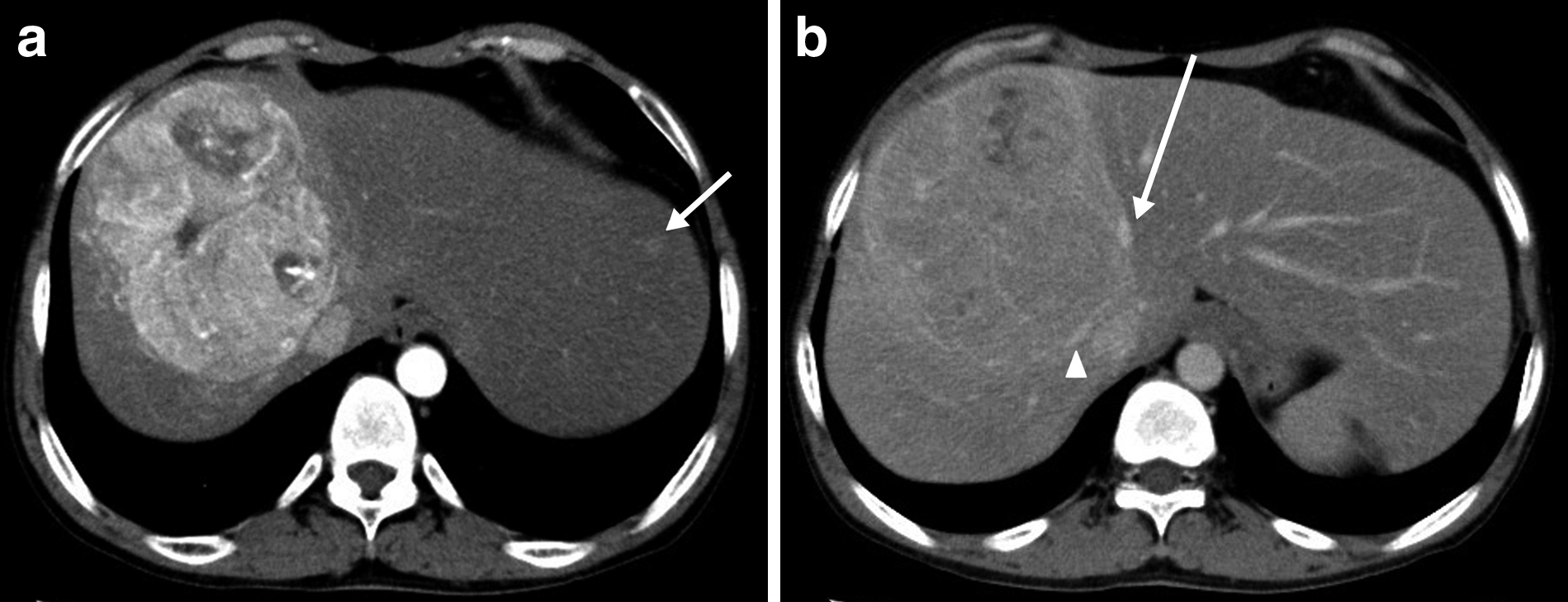
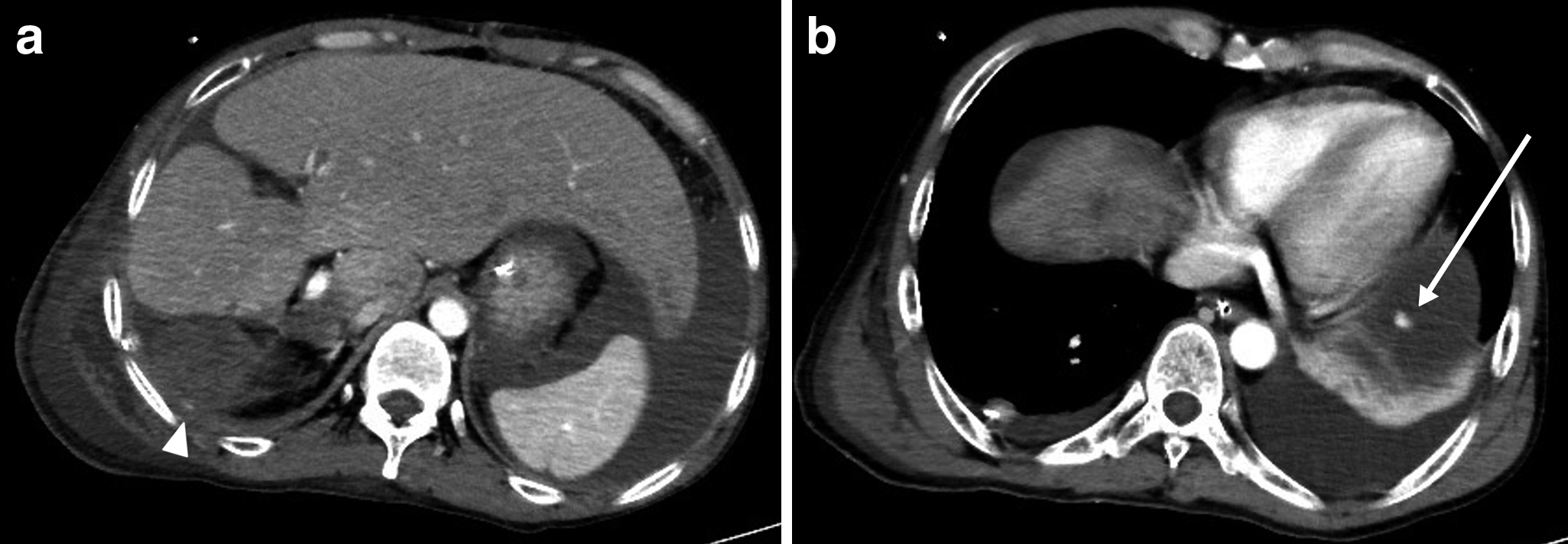
初診時CT所見:著明な肝腫大を認めた.肝右葉に,動脈相で早期濃染され,平衡相でwash outされる,径11 cmの腫瘍を認めた.肝S2にも動脈相で早期濃染される小病変を認めた(Fig. 1a).
以上より,肝細胞癌と診断した.主腫瘍は右肝静脈と中肝静脈を圧排しており,下大静脈にも広範に接していたため(Fig. 1b),肝動脈化学塞栓術(transcatheter arterial chemoembolization;以下,TACEと略記)を2回施行した.初回はシスプラチンを使用し,3か月後にシスプラチン,リピオドール®を使用して2回目のTACEを施行した.TACE後,腫瘍は径7 cmに縮小し,主要血管の圧排所見が改善したため,右門脈塞栓術(percutaneous transhepatic portal embolization;PTPE)の後に肝右葉切除を施行する方針とした.
術前血液検査所見:Alb 4.0 g/dl,Bil 0.5 mg/dl,PT活性値98.3%,ICGR15 3.3%であり,Child-PughはGrade A,肝障害度もGrade Aであった.腫瘍マーカーはPIVKA-II 115 mAU/mlであった.
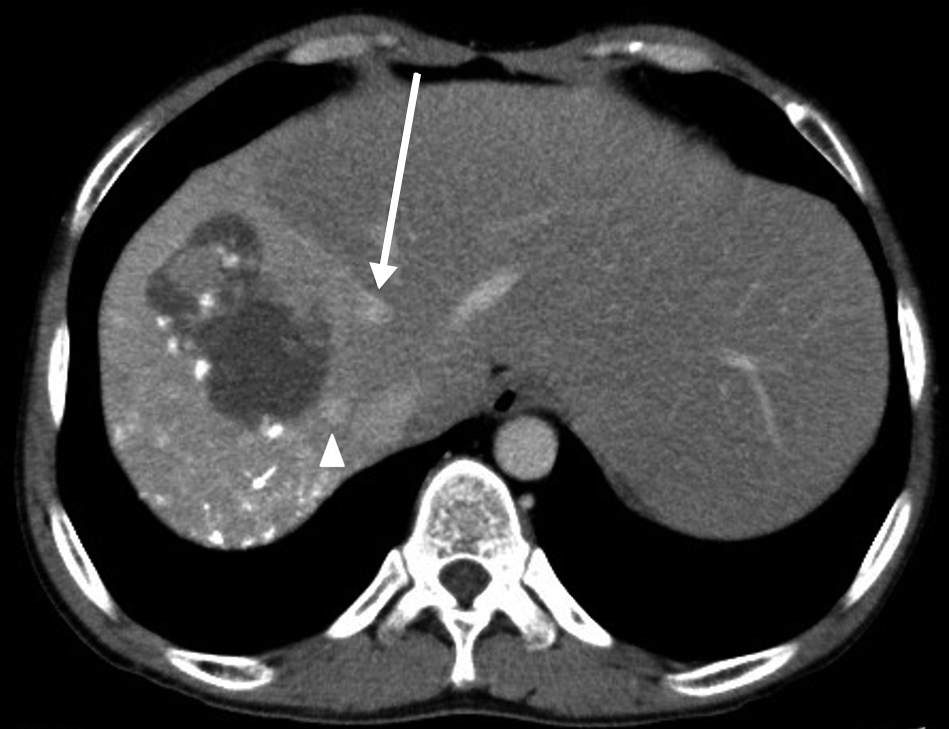
術前CT所見:腫瘍は径7 cmに縮小し,主要血管の圧排所見が改善した(Fig. 2).肝S2の小病変は画像上指摘できなくなった.全肝容積は2,805 mlと肝腫大を認めた.
手術所見:肝腫大が著明であったことから右葉の授動,肝離断に時間を要した.TACE前に指摘された肝S2の病変は,外側区域を授動したうえで,術中造影エコーを行うも同定できず,肝右葉切除のみを施行した.手術時間と出血量はそれぞれ493分,850 mlで,切除検体重量は948 gであった.
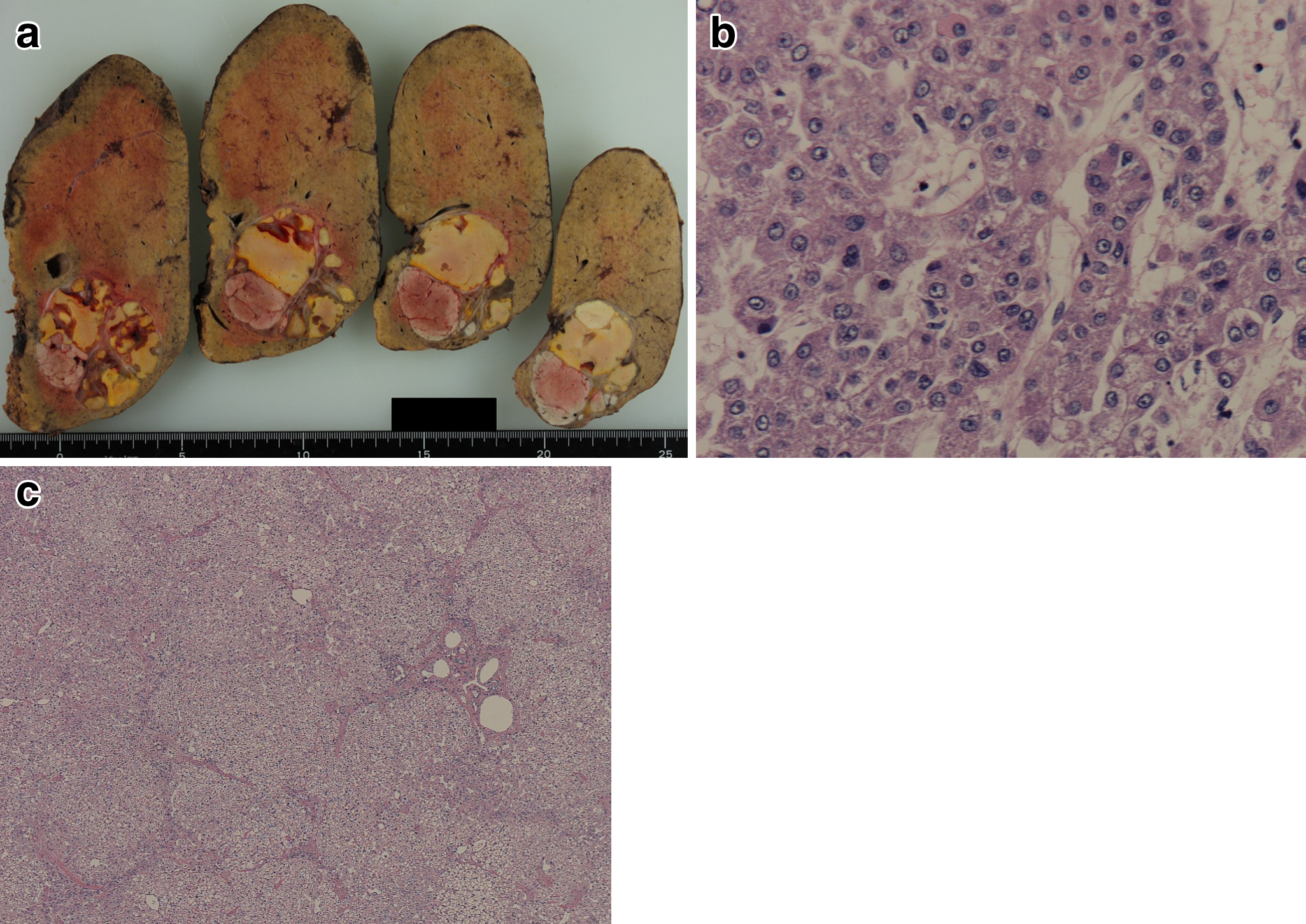
病理組織学的検査所見:最大径55×53 mmの多結節病変を認め(Fig. 3a),中分化型肝細胞癌(ypT2NXM0,ypStage II:UICC第8版)と診断された(Fig. 3b).腫瘍の60%程度に,術前治療によると考えられる壊死がみられた.また,背景肝の肝細胞には細胞質の澄明化,細胞境界の明瞭化がみられ,糖原病を示唆する組織像であった.脂肪化は軽度,線維化はF2であった(原発性肝癌取扱い規約 第6版)(Fig. 3c).
術後経過:術後1日目の動脈血液ガス分析で,pH 7.30,Base Excess −13.8,Lactate 16.86 mg/dlと著明な乳酸アシドーシスを認めた.腹部エコー検査では,門脈左枝および左肝動脈の血流は良好であった.高濃度ブドウ糖持続点滴(6.6 mg/kg/分)により,術後2日目にはpH 7.40,Base Excess −1.3,Lactate 3.62 mg/dlと改善した.
術後6日目未明に,突然の腹痛を訴えた.血圧108/64 mmHg,心拍数120回/分と,頻脈を呈し,血液検査でHb 4.4 g/dlと貧血を認めた.緊急腹部造影CTで,左右それぞれの下横隔動脈から,造影剤の血管外漏出像を認めたため(Fig. 4),血管造影検査を施行した.
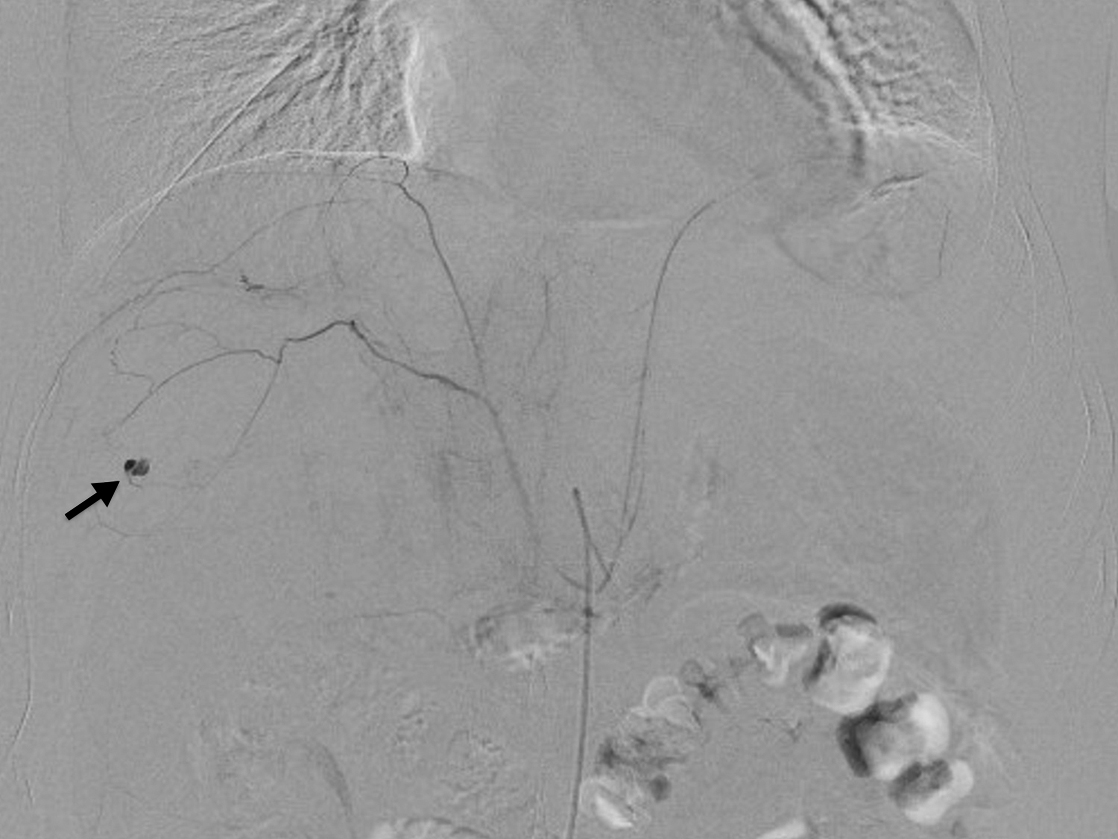
血管造影検査所見:右下横隔動脈からの出血を認め,塞栓術を施行した(Fig. 5).左下横隔動脈からの出血は認めなかったが,血管の攣縮による一時的な止血であり,再出血の可能性が高いと判断し,翌日に左も塞栓術を施行した.
塞栓術後の経過:術後21日目に軽快退院した.術後9か月現在,無再発で外来通院中である.
考察
糖原病I型はG6Paseの欠損により肝臓にglycogenが異常蓄積する常染色体劣性遺伝の先天性代謝異常症である.臨床的には,生後数か月から低身長,人形様顔貌がみられ,肝腎腫大,乳酸アシドーシスを伴う低血糖,また血小板粘着能低下による出血傾向がみられる2)3).発生頻度は10万~30万人に1人で4),20~60%が肝細胞腺腫を合併し,悪性化はそのうち11%とまれである1).医中誌Webにて1964年~2017年の期間で「糖原病」,「肝細胞癌」をキーワードとして会議録を除いて検索したところ,糖原病に合併した肝細胞癌に対し,肝切除術を施行したのは7例であった1)2)5)~9)(Table 1).本症例を含む8例全例が糖原病I型であり,肝細胞癌の発症年齢としては比較的若年であった.術後合併症について言及された報告は少ないが,腫瘍の急速な増大による在院死を1例,本症例と同様の代謝性アシドーシスを1例認めた.
Table 1
Reported cases of resected hepatocellular carcinomas in patients with glycogen storage disease in Japan
| No. |
Author |
Year |
Age |
Sex |
Type |
Preoperative treatment |
Operation |
Pathology |
Perioperative complication |
Outcome |
| 1 |
Sumimoto5) |
1988 |
29 |
F |
I |
none |
right hepatectomy, partial hepatectomy |
well |
none |
unknown |
| 2 |
Kuroda6) |
1995 |
34 |
M |
I |
none |
extended right hepatectomy |
well |
unknown |
unknown |
| 3 |
Wakabayashi7) |
1997 |
40 |
M |
I |
none |
left lateral segment hepatectomy |
mod |
none |
AWD |
| 4 |
Nakamura8) |
1997 |
40 |
M |
I |
none |
partial hepatectomy (S8) |
well |
unknown |
NED |
| 5 |
Kobayashi2) |
2002 |
33 |
M |
I |
TACE |
left lateral segment hepatectomy |
mod |
hospital death |
DOD |
| 6 |
Okuda1) |
2009 |
55 |
F |
I |
TACE |
partial hepatectomy (S2) |
por |
none |
NED |
| 7 |
Nishiyama9) |
2010 |
19 |
F |
I |
none |
subsegmental hepatectomy |
unknown |
metabolic acidosis |
unknown |
| 8 |
Our case |
|
37 |
M |
I |
TACE, PTPE |
right hepatectomy |
mod |
metabolic acidosis, intraperitoneal bleeding |
NED |
Type: glycogen storage disease type, TACE: transcatheter arterial chemoembolization, PTPE: percutaneous transhepatic portal embolization, well: well differentiated hepatocellular carcinoma, mod: moderately differentiated hepatocellular carcinoma, por: poorly differentiated hepatocellular carcinoma, AWD: alive with disease, NED: no evidence of disease, DOD: die of disease
糖原病に肝細胞癌が合併する原因については,①長期間の低血糖に起因する慢性的なグルカゴン刺激が肝細胞に増殖的変化を引き起こし悪性化を促す説,②脂肪酸代謝が亢進することにより,ペルオキシゾームでβ酸化された代謝産物である過酸化水素の産生が増加し,肝細胞の障害を引き起こし悪性化を促す説10),が挙げられるが,いまだに詳細は明らかでない.
糖原病の周術期には,手術操作や術後疼痛に伴うカテコラミンの増加や体温上昇によりグリコーゲンの分解が亢進するため,乳酸アシドーシスの増悪を来す9).本症例は,成人を機にフォローされていなかったこともあり,周術期の注意点について,事前の把握が不十分であった.17年間無治療で無症状であったが,侵襲の大きい手術のため,術後に著明な乳酸アシドーシスを来した.腹部エコー検査では門脈血流は良好であり,手術侵襲による糖原病の影響と考えられた.Oshitaら11)により,糖原病患者の肝切除後乳酸アシドーシスに対する高濃度ブドウ糖持続点滴(6.6 mg/kg/分)の有用性が報告されていたため,本症例でも術後1日目より開始したところ,術後2日目には乳酸アシドーシスは改善した.アシドーシスを予防するために,術中の高濃度ブドウ糖持続点滴(3.3~7.9 mg/kg/分)が有用という報告もある12)13).本症例のような高侵襲手術では,術中からの高濃度ブドウ糖持続点滴により,術後のアシドーシスを予防できた可能性がある.また,糖原病患者の周術期血糖管理については,経静脈的連続血糖モニタリングと人工膵臓を組み合わせた血糖管理が有用であったとする報告もあり14),今後の症例の集積が望まれる.
本症例は,術後6日目に左右下横隔動脈からの腹腔内出血を来した.いずれの出血点も,肝授動時の横隔膜との剥離面と考えられた.手術侵襲の大きさも一因であろうが,通常であれば術後6日目に多発腹腔内出血を来す可能性は低く,血小板粘着能低下を引き起こす糖原病の関与が示唆された.糖原病が血小板粘着能低下を引き起こす機序はいまだに明らかでないため,対応策を講じることは困難である.Reddyら15)による,糖原病I型合併肝腺腫に対する7切除例についての報告では,部分切除を施行した4例では術後出血を認めなかったのに対し,拡大右葉切除を施行した2例と,拡大左葉切除を施行した1例の計3例は,術後出血により再手術を要した.そのうち2例は多臓器不全となり,うち1例は術後死亡しており,糖原病患者に対する大量肝切除の適応は慎重であるべきと考えられる.本症例では,術前に外側区病変は不明瞭であったため,右葉切除のみとし,外側区の授動を行わなければ,肝授動時の横隔膜との剥離面からと考えられる出血を最小限にできた可能性がある.糖原病併存症例では,術後合併症を防ぐために侵襲をできるかぎり抑えるべきであり,今後,術前治療で病変が消失した可能性がある同様の症例に対する術式決定の一助となることを期待する.
糖原病は有病者数が少なく,周術期の詳細な報告例は乏しいが,今後は生存年数の延長に伴い,本疾患が併存する手術症例の増加も見込まれるため,本疾患に特異的な周術期合併症の認知が重要と考えられる.
利益相反:なし
文献
- 1) 奥田 悠季子, 太田 英夫, 三上 恒治, 長瀬 博次, 向井 亮太, 岡田 一幸,ほか.糖原病I型に合併した肝細胞癌の1例.癌と化学療法.2009;36:2362–2364.
- 2) 小林 規俊, 宮川 薫, 大川 伸一, 玉井 拙夫, 多羅尾 和郎, 杉政 往夫,ほか.糖原病に合併した肝細胞癌の1例.肝臓.2002;43:43–49.
- 3) 平井 律子, 中村 俊文, 北川 陸生, 竹平 安則, 山田 正美, 花島 一哲,ほか.糖原病1a型に合併した巨大肝細胞腺腫の1例.Liver Cancer.2000;6:126–130.
- 4) 藤田 賢司, 徳原 大介, 趙 有季, 濱崎 考史, 新宅 治夫.著明な高トリグリセライド血症を呈し,急性膵炎を繰り返した糖原病Ia型の1例.小児科臨床.2016;69:1623–1629.
- 5) Sumimoto S, Momoi T, Mikawa H, Honde H, Kobayashi N, Tanaka K, et al. Type Ia glycogen storage disease with multiple hepatic adenomas and a highly differentiated hepatic carcinoma: a case report and review of the literature. 小児科紀要.1988;34:47–55.
- 6) 黒田 誠, 笠原 正男, 赤座 香予子, 大隈 園美, 溝口 良順, 森浦 滋明.糖原病I型に合併した肝腫瘍の1例.病院病理.1995;13:62.
- 7) 若林 正夫, 花崎 和弘, 五十嵐 淳, 袖山 治嗣, 川村 信之, 宮崎 忠昭.糖原病I型に合併した肝癌の1例.日本消化器外科学会雑誌.1997;30:2019–2023.
- 8) 中村 俊文, 玉腰 勝敏, 北川 陸生, 竹平 安則, 山田 正美, 松下 雅広,ほか.糖原病I a型に合併した肝細胞癌の1例.日本消化器病学会雑誌.1997;94:866–870.
- 9) 西山 由希子, 大森 睦子, 倉迫 敏明, 熊田 雄太, 安積 さやか, 小倉 麻耶,ほか.肝切除術・噴門形成術の周術期管理を行ったVon Gierke病(糖原病Ia型)の一症例.姫路赤十字病院誌.2010;34:68–71.
- 10) 渡辺 明治, 峰村 正実, 高原 照美, 古井 啓, 土田 敏博, 桑原 芳弘,ほか.糖原病Ia型(von Gierke病)における肝発癌機構adenoma-carcinoma sequence.Pharma Medica.1994;12:141–154.
- 11) Oshita A, Itamoto T, Amano H, Ohdan H, Tashiro H, Asahara T, et al. Perioperative management of benign hepatic tumors in patients with glycogen storage disease type Ia. J Hepatobiliary Pancreat Surg. 2008;15:200–203.
- 12) 菱沼 典正, 鬼頭 剛, 水戸野 裕之, 白鳥 徹, 宮本 強, 廣井 威,ほか.2.5%ブドウ糖加酢酸リンゲル液を用いた糖原病I型2症例の麻酔管理.臨床麻酔.1998;22:695–697.
- 13) 若松 愛子, 岸田 朋子, 横山 幸三, 石神 哲郎, 椙山 加綱.甲状腺機能低下症と気管支喘息を合併した糖原病I型患者の麻酔経験.日本歯科麻酔学会雑誌.2002;30:203–208.
- 14) Yatabe T, Nakamura R, Kitagawa H, Munekage M, Hanazaki K. A case of perioperative glucose control by using an artificial pancreas in a patient with glycogen storage disease. J Artif Organs. 2016;19:100–103.
- 15) Reddy SK, Kishnani PS, Sullivan JA, Koeberi DD, Desai DM, Skinner MA, et al. Resection of hepatocellular adenoma in patients with glycogen storage disease type Ia. J Hepatol. 2007;47:658–663.