Abstract
症例は74歳の男性で,17年前に直腸癌に対し,低位前方切除術,D2郭清を施行した.病理診断はT2(MP),N0,M0,Stage Iであった.術後16年10か月,腸閉塞精査のためCT施行したところ,左下葉に腫瘍性病変を認め,血液検査で腫瘍マーカー上昇を認めた.上部・下部消化管内視鏡検査では悪性疾患を疑う所見はなかった.肺病変に対し胸腔鏡下左肺下葉切除術を施行し,病理組織学的検査で直腸癌からの転移と診断した.その後,肺転移再々発,脳転移を来したが,肺部分切除,ガンマナイフを施行し,初回肺転移からQOLを保ちつつ肺転移再発から2年2か月生存を得た.大腸癌術後5年以上経過してからの再発はまれであり,サーベイランス期間も5年が目安とされているが明確な基準はない.Stage I大腸癌においても術後10年以上の経過で再発する可能性があることを念頭に診療にあたる必要がある.
Translated Abstract
Herein, we report a case of synchronous brain and lung metastases after 17 years from the initial rectal resection of Stage I rectal cancer. A-74-year-old man, who had undergone low anterior resection for Stage I rectal cancer at the age of 57, was diagnosed with a lung tumor in the lower lobe of the left lung. He underwent left lower lobectomy, which was compatible with metastasis of the primary rectal cancer. Eight months later, he exhibited recurrent lung metastases with synchronous brain tumors, and underwent partial right lung resection, and subsequently gamma-knife treatment for the brain tumors. The patients died 2 years and 2 months after the initial lung resection. Brain metastases from colorectal cancer are extremely rare, particularly after more than 5 years since the initial resection. Multimodal therapy for colorectal cancer is effective enough to prolong the survival period and improving the quality of life, even if multiple metastases occur. However, after a long survival period with Stage I rectal cancer, there is a high probability of developing lung metastases with synchronous brain metastases.
はじめに
大腸癌の術後5年以上経過してからの再発はまれである.今回,我々はStage I直腸癌術後16年10か月で肺転移再発を来し,治癒切除を施行した1例を経験した.その後,肺転移再発に対し再肺切除,脳転移に対しガンマナイフ治療を行い,再発から2年以上の予後を得た.大腸癌術後15年以上の遠隔期に再発を来すことは極めてまれで,大腸癌術後症例の術後サーベイランス,再発後の治療選択などについて示唆に富む症例と考え報告する1)2).
症例
症例:74歳,男性
主訴:なし.
既往歴:2000年2月,直腸癌(Ra)に対して低位前方切除術,D2郭清を施行した.病理診断はtub1,T2(MP),N0,M0,ly1,v1,Stage I(大腸癌取扱い規約第6版)で,術後補助化学療法は施行しなかった.2006年8月(術後6年6か月)までは当院にてサーベイランスを行い,再発所見は認めなかった.
現病歴:2016年12月(術後16年10か月)に腸閉塞精査のために施行した胸腹部CTにて,左下肺野に5.7 cm大の腫瘤性病変を認めた.腹部には再発所見を認めなかった.上部・下部消化管内視鏡検査では,悪性疾患を疑う所見は認めなかった.
入院時現症:身長:157.5 cm,体重:68.5 kg,BMI 27.8.頸・胸部リンパ節腫大なし.胸部ラ音,心雑音なし.腹部はやや膨満.
血液検査所見:腫瘍マーカーの上昇(CEA 273.6 ng/ml,CA19-9 1,879.6 U/ml,DUPAN-2 2,400 U/ml,SPan-1 230 U/ml)を認めた.
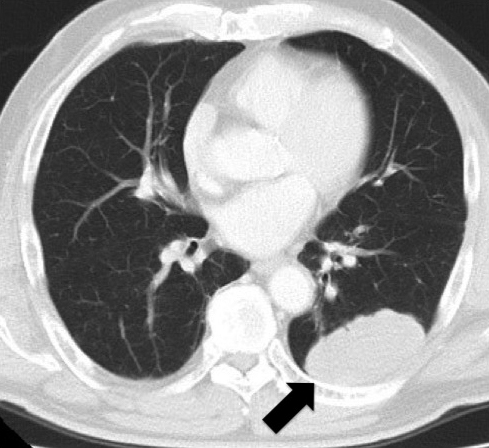
胸腹部CT所見:左下葉に57×34 mmの腫瘤性病変を認めた(Fig. 1).有意な縦隔リンパ節腫大なし.腹腔内には再発所見を認めず,癒着性イレウスと診断した.
頭部CT所見:転移を含め,特記事項なし.
以上より,原発性肺癌と診断したが,転移性肺腫瘍も除外診断として考慮した.
手術所見:2017年1月(術後16年11か月)胸腔鏡補助下左肺下肺切除,ND1aを施行した.迅速病理診断にて肺腫瘤は直腸癌転移と診断したが,左肺下葉の大部分を占居しており,部分切除は困難と判断し左肺下葉切除術を施行した.気管支断端も陰性であることを確認し,縦隔リンパ節郭清は施行しなかった.
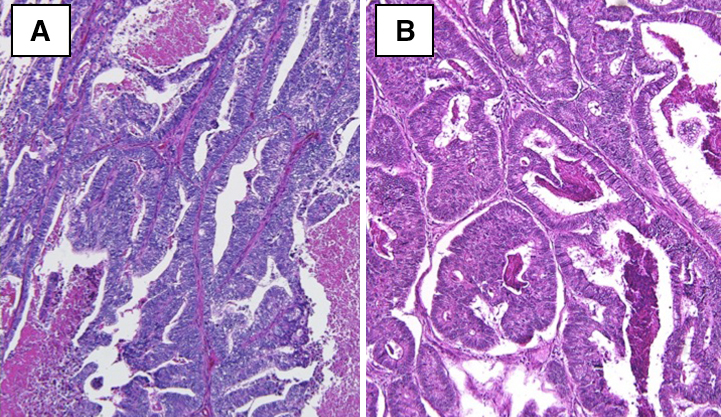
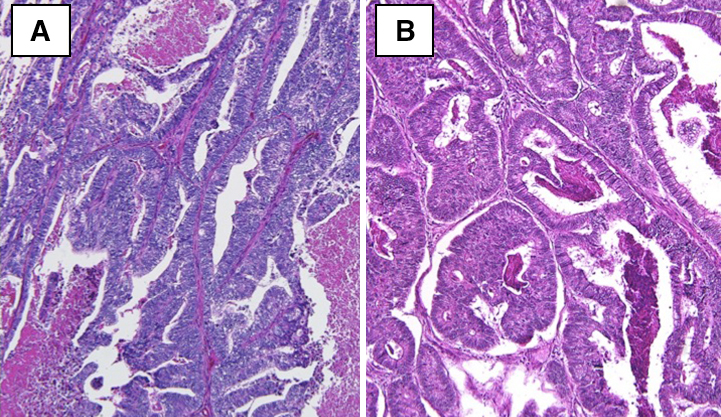
病理組織学的検査所見:比較的明瞭な異型腺管や癒合傾向を示す異型腺管を形成して浸潤性に増殖する腫瘍組織を認めた.構成細胞は高円柱状の核を有しており,核腫大と配列の乱れがみられ,tub2に相当する像を認めた(Fig. 2).既存の直腸癌の標本と形態は類似しており,免疫組織学的検討でTTF-1,NapsinAが陰性であること,CK7が陰性,CK20,CDX-2が陽性で,大腸癌の染色パターンを呈したことから,直腸癌の肺転移と診断した.
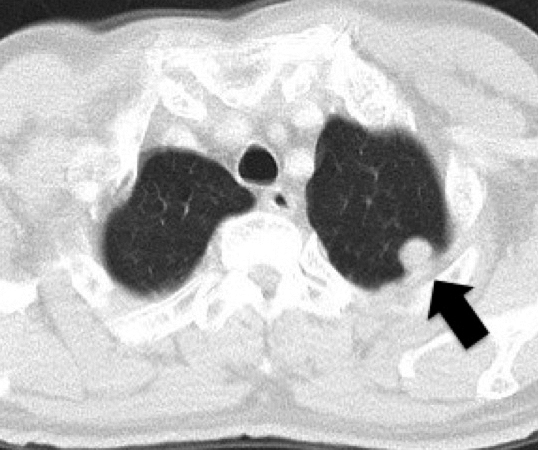
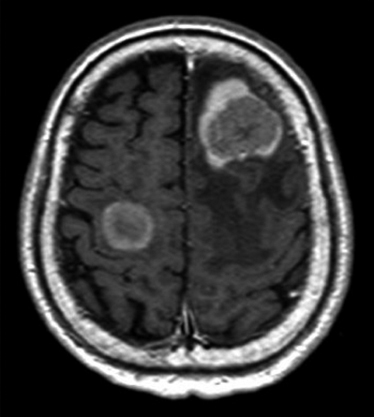
術後経過:術後補助化学療法は施行せず,1か月ごとに外来フォローを行った.2017年8月(術後17年6か月),胸部CTで左上葉に13 mmの円形腫瘤影を認め(Fig. 3),残肺再発と診断した.頭部CTを施行したが,脳転移の所見は認めなかった.2017年9月(術後17年7か月)に胸腔鏡下左上葉S1+S2腫瘍切除を施行した.病理組織学的検査で中心部に壊死を伴って癒合性の異型腺管を形成し,浸潤性に増殖する管状腺癌像を認めた.免疫染色検査では,初回肺手術と同様の染色パターンを示し,直腸癌の肺転移と診断した.2018年6月(術後18年4か月)CTで縦隔リンパ節腫大を認め,縦郭リンパ節転移と診断し,カペシタビンの投与を行った.2018年9月(術後18年7か月)よりふらつき,四肢の運動障害を認めるようになり,頭部MRIを施行したところ,多発脳転移(6か所)を認めた(Fig. 4).経過中に四肢麻痺や失語,嘔吐が出現したためカペシタビンは中止し,2018年10月(術後18年8か月)ガンマナイフ治療を行った.ガンマナイフ施行後より意識状態の著明な改善,右上下肢の筋力改善を認めた.自力での経口摂取可能,発語可能となりQOLの改善を認めたが,直腸癌手術から19年後,初回肺切除術より2年2か月後に癌死した.
考察
大腸癌治療ガイドラインに示されている統計では,大腸癌の再発は術後3年以内に85%以上,術後5年以内に95%以上が出現し,サーベイランス期間は術後5年間が目安とされている1).術後5年を超えてからの再発は,治癒切除症例全体の1%未満と報告されており2),大腸癌術後10年以上経過してからの再発例はまれである.自験例はStage I直腸癌術後17年目に肺転移再発と診断した.医学中央雑誌にて1964年から2019年9月までの期間で「大腸癌」,「再発」に「10年」「11年」…と順次年数をつけてキーワードに検索すると会議録を除き27例の報告があり3)~29),大腸癌術後15年以上経過しての再発は自験例を含め,3例と極めてまれといえる(Table 1).自験例を含めた28例を検討すると,原発巣は直腸癌13例(肛門管癌を含む),S状結腸癌4例,下行結腸癌2例,上行結腸癌9例と左側の症例が多かった.組織型ではtub1 11例,tub2 15例と分化型が目立ち,進行度はStage I 5例,Stage II 9例と半数がリンパ節転移を伴わない症例での遠隔期再発の症例が見られた点は特徴的である.再発部位は多様で,肺,肝臓,局所再発,十二指腸,回腸,肋骨,手術創,膵臓,脾臓,副腎,領域外リンパ節,腹膜再発とさまざまであるが発見時に複数臓器への再発を認めたのは3例のみで1臓器での再発が多く,基本的には治療方針として切除が選択されている.大腸癌治療ガイドライン2019年度版では,再発臓器が1臓器の場合,手術にて再発巣の完全切除が可能であれば積極的に切除を考慮する,とされている.肺切除の適応基準としては,①耐術可能,②原発巣が制御されているか,制御可能,③肺転移巣を遺残なく切除可能,④肺外転移がないか,制御可能,⑤十分な残肺機能,とされる.自験例では,2度の肺転移再発とも上記を満たし切除することで,初回肺切除から2年2か月生存を得ることが可能であった.ただ,直腸癌術後,17年の無再発期間であったが,再発後は初回肺切除後7か月に残肺再発,1年5か月に縦隔リンパ節再発,1年8か月後には脳転移再発を認め,再発後の比較的急速な病状の進行を認めた.初回肺切除時の胸部CT,頭部CTでその後の再発病巣の指摘は困難で,術後は1か月ごとにフォローを行い,初回肺切除後4か月の胸部CTでも残肺再発病変は認めなかったが,7か月後の胸部CTで再発病変を認めた.氷室ら30)は直腸癌術後の転移性肺腫瘍切除例の予後不良因子として,肺腫瘍最大径20 mm以上,肺切除前のCEA高値の二つの因子を報告している.自験例ではいずれの項目も満たしており,肺切除術後の再発リスクが高い状態であったと考えられる.遠隔転移巣切除後の補助化学療法は一定の見解は得られておらず,同ガイドラインでも弱く推奨する,にとどまっている.今回の検討でも,転移巣の切除後化学療法を行った記載が見られたのは8例のみであった.自験例のように再発リスクが高いと想定される場合は,術後化学療法の導入も考慮されるが,その妥当性は今後検討が必要である.
Table 1
Summary of cases of colorectal cancer recurrence more than 10 years after the first operation in Japan
| No. |
Author |
Year |
Primary site |
Histology |
T factor |
ly |
v |
N |
Stage |
Time to recurrence |
Recurrent site |
CEA |
Treatment |
Adjuvant chemotherapy |
Prognosis |
| 1 |
Suminaga3) |
1987 |
ascending colon |
mod |
SE |
— |
— |
1 |
IIIa |
10 |
local site |
normal |
opereation |
— |
— |
| 2 |
Nakamura4) |
1989 |
rectum |
well |
— |
— |
— |
— |
— |
10 |
lung |
— |
operation |
— |
— |
| 3 |
Yano5) |
1995 |
rectum |
well |
SM |
0 |
0 |
0 |
I |
10 |
liver |
6.1 |
operation |
— |
28M (live) |
| 4 |
Moriwaki6) |
1996 |
ascending colon |
mod |
SS |
2 |
1 |
0 |
II |
10 |
lung |
normal |
operation |
— |
14M (live) |
| 5 |
Ikenaga7) |
1996 |
sigmoid colon |
well |
SS |
1 |
1 |
1 |
IIIa |
10 |
duodenum |
normal |
operation |
none |
18M (live) |
| 6 |
Kawasaki8) |
1998 |
rectum |
well/mod |
— |
— |
— |
— |
— |
10 |
lung, liver, rib |
17.2 |
— |
— |
— |
| 7 |
Ishida9) |
1999 |
rectum |
well |
SS |
0 |
0 |
2 |
IIIa |
11 |
ope scar |
normal (2.9) |
operation |
— |
12M (live) |
| 8 |
Shimoda10) |
2002 |
rectum |
well |
SE |
0 |
0 |
0 |
II |
16 |
ileum |
normal (2.2) |
operation |
5'-DFUR |
37M (live) |
| 9 |
Yamaguchi11) |
2005 |
ascending colon |
well>mod |
SE |
1 |
2 |
2 |
IIIb |
10 |
spleen |
130.1 |
operation |
S-1 |
14M (live) |
| 10 |
Hiratsuka12) |
2005 |
ascending colon |
muc |
SS |
3 |
1 |
2 |
IV (LYM) |
10 |
lymph node |
14 |
chemotherapy |
— |
6M (death) |
| 11 |
Nakagawa13) |
2006 |
anal canal |
— |
A1 |
0 |
0 |
0 |
II |
10 |
lymph node (2) |
6.4 |
chemo., RT |
(UFT) |
12M (live) |
| 12 |
Tani14) |
2007 |
rectum |
mod |
A2 |
0 |
1 |
2 |
IV (H1) |
11 |
liver, pancreas |
60.1 |
operation |
UFT |
12M~ (live) |
| 13 |
Dabanaka15) |
2007 |
descending colon |
mod |
SE |
2 |
2 |
2 |
IV (P2) |
16 |
peritonaeum |
5.7 |
operation |
— |
live |
| 14 |
Hirama16) |
2007 |
ascending colon |
mod |
SS |
1 |
0 |
0 |
II |
11 |
peritonaeum |
18 |
operation |
UFT |
live |
| 15 |
Nakazaki17) |
2008 |
ascending colon |
mod |
SS |
1 |
1 |
1 |
IIIa |
10 |
liver |
6.7 |
operation |
none |
10M (live) |
| 16 |
Shimizu18) |
2009 |
ascending colon |
mod |
SE |
2 |
1 |
0 |
II |
11 |
lymph node |
31.7 |
none |
none |
live? |
| 17 |
Ide19) |
2009 |
ascending colon |
well |
SS |
0 |
0 |
0 |
II |
10 |
lymph node |
normal (3) |
operation |
none |
17M (live) |
| 18 |
Kuwada20) |
2011 |
sigmoid colon |
mod>well |
SM |
1 |
1 |
0 |
I |
10 |
lymph node |
16.2 |
operation |
UFT |
live |
| 19 |
Takeyama21) |
2011 |
sigmoid colon |
mod |
SS |
— |
— |
1 |
IIIA |
10 |
lung, adrenal gland |
102.1 |
operation |
none |
29M (live) |
| 20 |
Nishie22) |
2013 |
rectum |
mod |
A |
2 |
2 |
0 |
II |
10 |
local site |
16.6 |
operation |
none |
30M (live) |
| 21 |
Toshima23) |
2014 |
rectum |
mod |
SE |
2 |
1 |
2 |
IIIb |
12 |
lymph node |
7.2 |
operation |
none |
10M (live) |
| 22 |
Kanomata24) |
2015 |
rectum |
mod |
SS |
2 |
2 |
0 |
II |
11 |
liver |
8.7 |
operation |
none |
30M (live) |
| 23 |
Obara25) |
2015 |
rectum |
mod |
SS |
3 |
1 |
1 |
IIIa |
12 |
local site |
normal (2) |
operation |
none |
10M (live) |
| 24 |
Niitsuma26) |
2016 |
ascending colon |
well |
SS |
2 |
1 |
1 |
IIIa |
13 |
pancreas |
16.6 |
operation |
S-1 |
24M (live) |
| 25 |
Uno27) |
2016 |
sigmoid colon |
mod |
SS |
0 |
0 |
0 |
II |
11 |
liver |
6.3 |
operation |
none |
50M (death) |
| 26 |
Sakamoto28) |
2018 |
rectum |
well |
MP |
0 |
0 |
0 |
I |
10 |
local site |
15.9 |
RT |
— |
10M (live) |
| 27 |
Shirakawa29) |
2018 |
descending colon |
mod |
MP |
0 |
0 |
0 |
I |
12 |
liver |
71.5 |
operation |
— |
10M (live) |
| 28 |
Our case |
|
rectum |
well |
MP |
1 |
1 |
0 |
I |
17 |
lung |
273.6 |
operation |
none |
26M (death) |
自験例では腸閉塞の精査の際に再発病変を認め診断に至ったが,その時点で腫瘍径が約57 mmと比較的進行した段階であった.上記の氷室ら30)の報告に見られるように腫瘍径20 mm以下の早期の段階で再発が発見できればよりよい予後が得られた可能性がある.海外の報告では大腸癌再発例のうち,5年以上の晩期再発例は0.9~1.2%で,高分化型腺癌,リンパ節転移なし,初回術前CEA低値,左側結腸癌・直腸癌が多いと報告している31)32).今回の検討で初回術前CEAの検討は行えていないが,その他は同様の結果であり生物学的悪性度が低い腫瘍群と考えられる.発見することができれば初回手術後に長期間経過し再発する場合,発育速度が緩徐であると想定され,今回の検討でも記載のあった26例中22例で手術が選択されており,比較的予後良好である.我が国の大腸癌の新規罹患数が約15万人/年といわれ,遠隔期再発例が1%とすると1,500人余りは5年以降に再発しうる計算となり,無視できない数と考える33).5年以降も再発のリスクは考慮が必要であり,Frontaliら34)は直腸癌は5年以降も外来サーベイランスが必要としている.サーベイランスの方法としては,全例でCTを施行するのは医療経済面を考慮しても困難ではある.今回の検討で検索しえた範囲で24例中19例でCEAの上昇を認め,陽性率は約80%と高く,遠隔期再発の発見契機となる可能性が示唆された.腫瘍マーカーであれば診療所,かかりつけ医にて測定可能であることが多く,山口の報告によれば,かかりつけ医でのCEA上昇を契機に精査を行い,転移巣を発見し切除されている.病診連携を密に行うことで5年以降のサーベイランス,遠隔期再発の早期診断が可能になりうると考える.
今回,我々は大腸癌治癒切除後,17年目に肺転移,19年目に脳転移を認め,集学的治療を施行することで2年2か月の予後を得られた症例を経験した.大腸癌術後,15年以降の遠隔期再発は極めてまれではあるが,再発早期に発見,治療を行えば長期予後を得られる可能性があり,既往に大腸癌ある場合,再発を念頭に検査,治療を行う必要がある.
利益相反:なし
文献
- 1) 大腸癌研究会編.大腸癌治療ガイドライン医師用2019年版.東京:金原出版;2019. p. 49–52.
- 2) 小林 宏寿, 橋口 陽二郎, 上野 秀樹, 石黒 めぐみ, 望月 英隆.大腸癌術後再発に関するフォローアップ―大腸癌研究会プロジェクト研究「大腸癌術後のフォローアップに関する研究」の検討結果より―.日本大腸肛門病学会雑誌.2006;59:851–856.
- 3) 住永 佳久, 佐藤 知行, 宮田 道夫, 柏井 昭良, 金澤 暁太郎, 三浦 弘資,ほか.術後10年を経過して興味ある再発形式を呈した大腸癌の1切除例.日本外科学会雑誌.1987;88:349–353.
- 4) 中村 治彦, 橋本 雅史, 森山 浩, 永井 完治, 新妻 雅行, 雨宮 隆太,ほか.直腸癌術後10年を経て出現した空洞性肺転移巣の1切除例.日本胸部臨床.1989;48:796–798.
- 5) 矢野 秀朗, 小西 富夫, 根岸 征示, 渡辺 春子, 寺島 裕谷, 渡辺 俊之.大腸sm癌術後10年目に肝転移を来した1例.手術.1995;49:719–723.
- 6) 森脇 義弘, 山腰 英紀, 長堀 優, 今井 信介, 小林 俊介, 笠岡 千孝,ほか.上行結腸癌治癒切除10年後に発見された孤立性肺転移の1切除例.日本大腸肛門病学会雑誌.1996;49:1074–1079.
- 7) 池永 誠, 西 八嗣, 立石 晋, 榎本 拓茂, 荒井 義孝, 高野 康雄,ほか.大腸癌術後10年目に認められた転移性十二指腸癌の1例.日本臨床外科学会雑誌.1996;57:1635–1640.
- 8) 河崎 雄司, 安田 和人, 三上 真顕, 松本 慎吾, 星野 映治, 櫃田 豊,ほか.術後10年で肋骨へ転移し骨破壊像と硬化像の混合像を呈した直腸癌再発の1例.日本胸部臨床.1998;57:742–746.
- 9) 石田 雅俊, 濱路 政靖, 宮崎 知, 西田 幸弘.術後11年を経過して腹壁創瘢痕に孤立性再発をきたした直腸癌の1例.臨床外科.1999;54:706–708.
- 10) 下田 雅史, 齋藤 眞文, 上田 進久, 前浦 義市, 松永 征一, 岡本 茂.直腸癌術後16年目に発生した孤立性回腸転移の1例.臨床外科.2002;57:549–552.
- 11) 山口 智弘, 山下 哲郎, 小出 一真, 谷口 史洋, 塩飽 保博, 濱島 高志,ほか.大腸癌術後10年目に孤立性脾転移を来した1例.日本消化器外科学会雑誌.2005;38:1761–1766.
- 12) 平塚 研之, 角田 明良, 中尾 健太郎, 御子神 哲也, 山田 宏輔, 草野 満夫.術後10年でリンパ節再発をきたしたstage IV結腸粘液癌の1例.日本臨床外科学会雑誌.2005;66:673–679.
- 13) 中川 須美子, 天野 正弘, 山下 晋也, 西川 泰章, 檜垣 直純, 林田 博人,ほか.10年後に再発した肛門管癌に対して放射線化学療法を施行しQOLが得られた1例.癌と化学療法.2006;33:1977–1979.
- 14) 谷 直樹, 野口 明則, 竹下 宏樹, 山本 有祐, 伊藤 忠雄, 中西 正芳,ほか.直腸癌術後11年で認められた膵および肝転移の1切除例.日本消化器外科学会雑誌.2007;40:1536–1541.
- 15) 駄場中 研, 小林 道也, 岡本 健, 岡林 雄大, 吉岡 龍二, 花崎 和弘.Stage IV下行結腸癌術後16年で骨盤腔内腹膜外再発を認めた1例.日本臨床外科学会雑誌.2007;68:1821–1825.
- 16) 平間 知美, 下段 光裕, 足立 英明, 西田 睦夫, 平田 公一.上行結腸癌術後11年目のDouglas窩転移再発を治癒切除した1例.日本臨床外科学会雑誌.2007;68:1490–1495.
- 17) 中崎 隆行, 濱崎 景子, 清水 香里, 進藤 久和, 田村 和貴, 谷口 英樹,ほか.結腸癌原発巣切除後10年6ヶ月後に出現した肝転移の1例.日本臨床外科学会雑誌.2008;69:883–885.
- 18) 清水 久美, 数寄 泰介, 倉田 季代子, 若木 美佐, 竹内 健, 後藤 太一郎,ほか.術後11年で肺および肺門・縦隔リンパ節転移にて発見された大腸癌の1例.気管支学.2009;31:293–297.
- 19) 井手 佳美, 平松 和洋, 吉原 基, 鈴村 潔, 加藤 岳人.術後10年後にリンパ節再発した上行結腸癌の1切除例.日本臨床外科学会雑誌.2009;70:146–152.
- 20) 桑田 和也, 村岡 篤, 木村 圭吾, 國土 泰孝, 立本 昭彦, 津村 眞.ポリープ切除後10年目にリンパ節再発を認めたS状結腸ポリープ癌の1例.外科.2011;73:1249–1252.
- 21) 竹山 廣志, 鳥 正幸, 大森 健, 上島 成幸, 赤松 大樹, 西田 俊朗,ほか.大腸癌術後異時性両側副腎転移に対し両側副腎摘出術を施行した1例.日本消化器外科学会雑誌.2011;44:1319–1327.
- 22) 西江 尚貴, 稲田 涼, 母里 淑子, 近藤 喜太, 宇野 太, 永坂 岳司,ほか.直腸癌術後10年を経て発症した局所再発に対して治癒切除を施行した1例.癌と化学療法.2013;40:2585–2587.
- 23) 戸嶋 俊明, 濱田 円, 原野 雅生, 松川 啓義, 小島 康知, 塩崎 滋弘,ほか.直腸癌根治術後12年目に切除しえた,大動脈周囲リンパ節再発の1例.日本消化器外科学会雑誌.2014;47:410–418.
- 24) 鹿股 宏之, 牛窓 かおり, 立川 伸雄, 清水 芳政, 捨田利 外茂夫, 古内 孝幸.直腸S状部癌術後11年目に肝転移再発を認め切除した1例.臨床外科.2015;70:1151–1155.
- 25) 小原 恵, 大沼 忍, 唐澤 秀明, 渡辺 和宏, 工藤 克昌, 石田 晶玄,ほか.初回手術より12年後に診断された直腸癌局所再発に対し骨盤内臓全摘術を施行した1例.癌と化学療法.2015;42:2337–2339.
- 26) 新妻 徹, 浅井 浩司, 渡邉 学, 松清 大, 齋藤 智明, 石井 智貴,ほか.上行結腸癌術後13年後に認められた転移性膵癌の1切除例.日本消化器外科学会雑誌.2016;49:657–665.
- 27) 宇野 雅紀, 松永 和哉, 松崎 安孝, 神谷 里明, 松永 宏之, 川井 覚,ほか.結腸癌術後11年目に再発した胆管転移の1例.日本消化器外科学会雑誌.2016;49:15–21.
- 28) 坂本 一博, 河野 眞吾, 雨宮 浩太, 土谷 祐樹, 萩原 俊昭, 松澤 宏和,ほか.術後10年目に再発した下部直腸MP癌の1例.癌と化学療法.2018;45:1988–1990.
- 29) 白川 賢司, 前田 佳之, 坂部 龍太郎, 桑田 亜希, 田原 浩, 布袋 裕士.術後12年目に肝転移再発したStage I(T2)下行結腸癌の1例.日本臨床外科学会雑誌.2018;79:2103–2107.
- 30) 氷室 直哉, 南方 孝夫, 大島 穣, 片岡 大輔, 山本 滋, 門倉 光.結腸・直腸癌肺転移における肺切除後予後予測因子に関する臨床病理学的検討.日本呼吸器外科学会雑誌.2016;30:136–142.
- 31) Cho YB, Chun HK, Yun HR, Lee WS, Yun SH, Lee WY. Clinical and pathologic evaluation of patients with recurrence of colorectal cancer five or more years after curative resection. Dis Colon Rectum. 2007;50:1204–1210.
- 32) Seo SI, Lim SB, Yoon YS, Kim CW, Yu CS, Kim TW, et al. Comparison of recurrence patterns between ≤5 years and >5 years after curative operations in colorectal cancer patients. J Surg Oncol. 2013;108:9–13.
- 33) 国立がん研究センターがん対策情報センター.2019年のがん統計予測[Internet].国立がん研究センター;2019 Oct 23 [cited 2020 Feb 11]. Available from: https://ganjoho.jp/reg_stat/statistics/stat/short_pred.html.
- 34) Frontali A, Benichou B, Valcea I, Maggiori L, Prost À la Denise J, Panis Y. Is follow-up still mandatory more than 5 years after surgery for colorectal cancer? Updates Surg. 2020;72:55–60.