Abstract
症例は12歳の女児で,父方の祖父・母方の祖父が40歳,父が35歳で胃癌の既往あり.ふらつきを主訴に来院し上部消化管内視鏡検査で胃体部に3型病変および五つの0-IIc病変を認め,いずれからもpor-signet ring cell carcinomaが検出された.Helicobacter pylori(以下,HPと略記)感染陽性で,前庭部に鳥肌胃炎を認めた.cT2(MP)N0M0P0,cStage IBと診断し,胃全摘,D2郭清,Roux-en-Y再建を施行した.病理組織検査ではpor2,pT3(SS)pN0M0P0CY0,pStage IIAであり,Eカドヘリン染色陽性であった.S-1内服による術後補助化学療法を3クール行い無再発で5年2か月が経過している.HP感染に伴う鳥肌胃炎は若年胃癌のリスク因子であるが,家族性胃癌の診断基準を満たした未分化型癌が多発する症例はまれであり報告する.
Translated Abstract
Herein, we report a young surgical case of multiple gastric cancers on the background of nodular gastritis with Helicobacter pylori infection. A 12-year-old girl with a family history of advanced gastric cancer in young age in her paternal grandfather, maternal grandfather, and father, was admitted with anemia. Upper gastrointestinal endoscopy showed a type-3 advanced cancer and five 0-IIc type early cancers in the body of the stomach as well as nodular gastritis in the antrum. Histological examination of the biopsy samples detected poorly differentiated carcinoma and signet ring cell carcinoma in all six lesions. The type-3 gastric cancer was preoperatively diagnosed as cT2N0M0P0, cStage IB. The patient underwent total gastrectomy with Roux-en-Y reconstruction. The histopathological diagnosis of the resected specimen was pT3(SS)pN0M0P0CY0, pStage IIA. E-cadherin staining was positive in the tumor. Nodular gastritis with Helicobacter pylori infection was confirmed histologically. The patient received adjuvant chemotherapy with S-1, and no tumor recurrence was observed during 62 months follow-up after surgery. This is a rare case of multiple diffuse-type gastric cancers in a young patient, not only with the histological background of nodular gastritis with Helicobacter pylori infection, but also with a family history of diffuse-type gastric cancer.
はじめに
小児胃癌は非常にまれであり,また進行例が多く予後不良なことが多い1).家族歴を有することが多いが,本邦では多くがHelicobacter pylori(以下,HPと略記)感染による胃癌の家族内集積であり,遺伝性胃癌の頻度は少ない.鳥肌胃炎はHP感染若年女性に好発し,未分化型胃癌との関連が指摘されている.今回,鳥肌胃炎を背景として多発する小児多発胃癌の1切除例を経験したので報告する.
症例
患者:12歳,女性
主訴:黒色便,ふらつき,息切れ
既往歴:特記すべきものはなし.
家族歴:父(35歳時),父方の祖父(40歳時)および母方の祖父(40歳前後時)がびまん性胃癌(Fig. 1).
現病歴:生来健康であったが,10歳ごろから度々腹痛があった.2014年11月初旬ごろから上腹部痛と黒色便があった.ふらつき,息切れが出現し近医を受診した.血液検査にてHb 8.3 mg/dlと貧血を認め,上部消化管内視鏡検査にて出血性胃潰瘍と診断された.入院のうえ,プロトンポンプ阻害薬投与を受け症状は改善した.同年12月の上部消化管内視鏡再検にて胃に多発する陥凹性病変を認め,生検にてsignet ring cell carcinomaと診断され,精査加療目的に当科に紹介となった.
来院時現症:PS 0,身長153 cm,体重47 kg.
来院時血液検査所見:血算ではHb 13.5 g/dlと前医受診時と比べて貧血は改善した.生化学検査にて腎機能,肝胆道系酵素,電解質に異常は認めなかった.腫瘍マーカーはCEA 0.7 ng/ml,CA19-9 8 U/ml,CA125 9 U/ml,AFP 1.4 ng/mlといずれも正常であった.
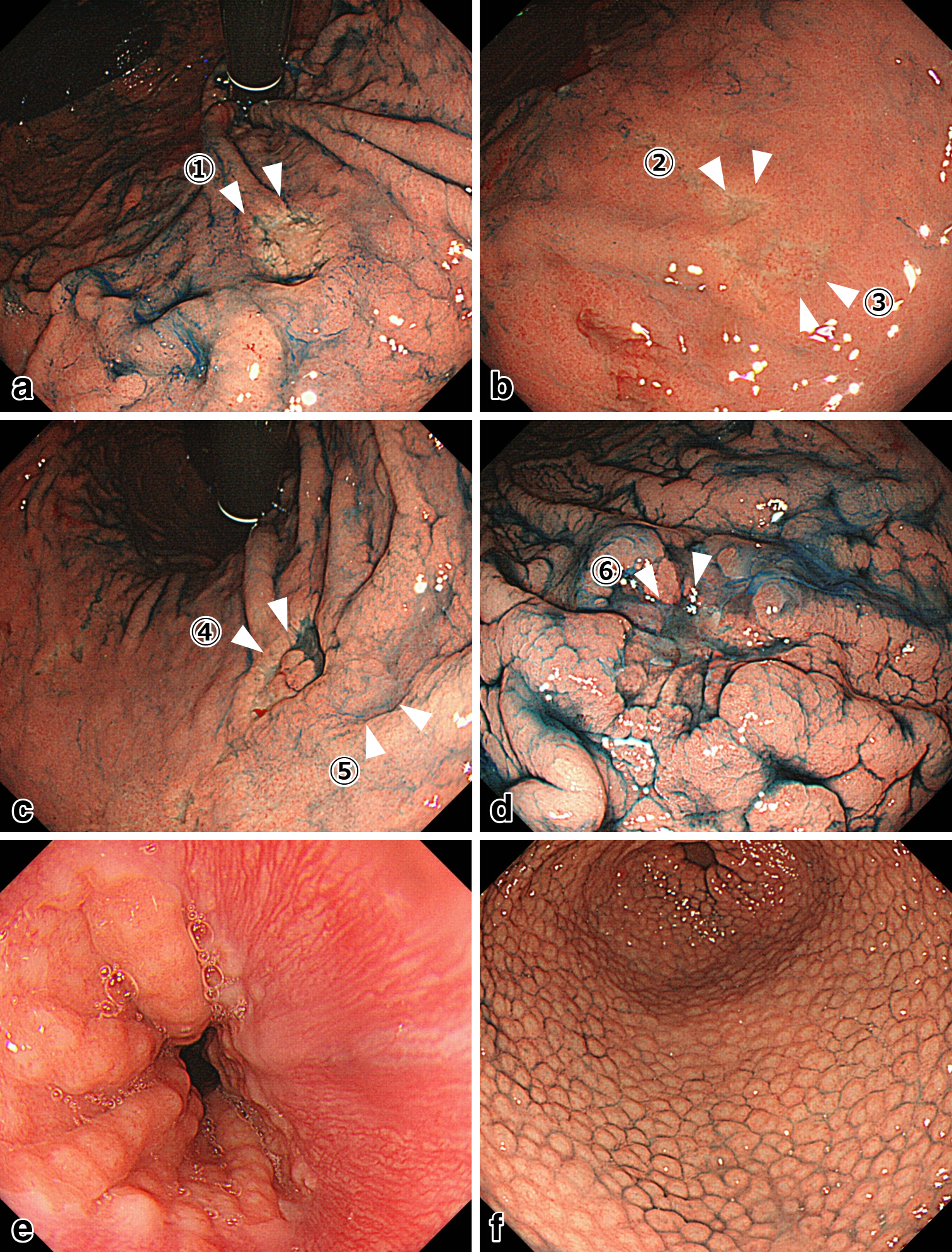
上部消化管内視鏡検査所見:胃体上部小彎(Fig. 2a),体中部小彎(Fig. 2b),体中部後壁(Fig. 2c)に合計五つの0-IIc病変を認め,体中部前壁にIII型病変(Fig. 2d)を認め,いずれの生検からもpor-signet ring cell carcinomaと診断された.また,噴門部(Fig. 2e)および幽門前庭部(Fig. 2f)に全周性に広がる鳥肌胃炎を認めた.
胸部・腹部造影CT所見:明らかな胃壁の肥厚やリンパ節腫大,遠隔転移を認めなかった.
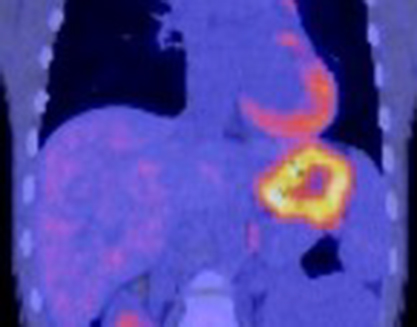
PET-CT所見:胃壁全体にSUV 6.5の集積亢進を認めた(Fig. 3).リンパ節転移や遠隔転移を示唆する所見は認めなかった.
以上より,多発胃癌,最も進行した体中部前壁病変について胃癌取扱い規約(第15版)によるcT2(MP)N0M0P0,cStage IBと診断した.
手術所見:開腹胃全摘,D2郭清,R-Y再建を施行した.郭清範囲内に有意なリンパ節の腫大は認めなかった.腹水はなく,腹膜播種や肝転移は認められなかった.
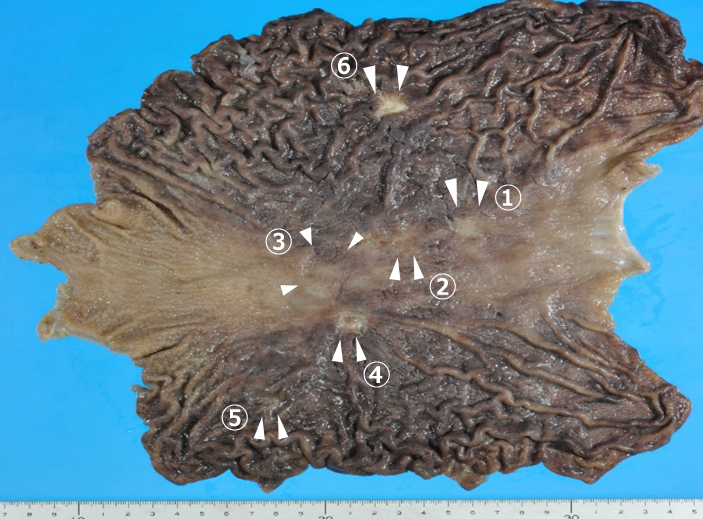
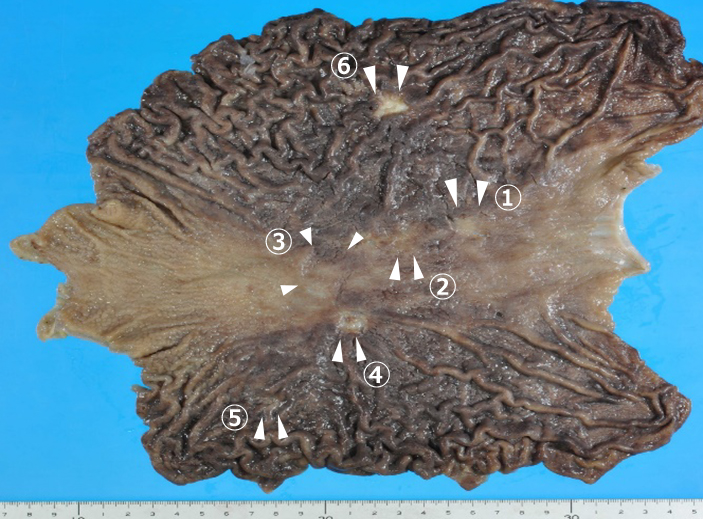
病理組織学的検査所見:摘出標本では胃体上部小彎に10×5 mmのごく浅い0-IIc病変(Fig. 4-①),体中部小彎に5×5 mmのごく浅い0-IIc病変(Fig. 4-②)および25×20 mmの0-IIc病変(Fig. 4-③),体中部後壁に15×15 mmの0-IIc病変(Fig. 4-④)および10×10 mmの0-IIc病変(Fig. 4-⑤),さらに体中部前壁に20×20 mmのIII型病変(Fig. 4-⑥)を認めた.
体中部小彎および後壁の0-IIc病変(Fig. 4-①,②,③,④,⑤)はsignet-ring cell carcinoma,pT1a(m)であった(Fig. 5a, b).同部では腸上皮化生は認めず,幽門前庭部から続く間質の炎症細胞浸潤とリンパ濾胞を伴っており鳥肌胃炎に合致する所見であり(Fig. 5a),また多数のHP感染を認めた.
体中部前壁のIII型病変(Fig. 4-⑥)はpor2>tub2,pT3(SS)であった(Fig. 5c).最も進行した病変に基づいて最終診断はpT3(SS)pN0(0/92)M0P0CY0,pStage IIAであった.III型病変の免疫組織化学染色では浸潤性増殖する癌細胞においてEカドヘリンの発現を認め(Fig. 5d),その発現強度は非癌部粘膜上皮と同等であった.Her2スコアは0であった.
術後経過:術後は良好に経過し,17日目に退院した.術後補助化学療法としてS-1(100 mg分2,4週投与2週休薬)を3クール施行し明らかな有害事象なく終了した.術後5年2か月が経過し,再発なく健康に生活を送っている.
考察
15歳以下の小児における胃癌の発生は極めてまれであり,全胃癌の約0.03%1),小児消化管悪性腫瘍の0.05%2)3)と報告されている.小児胃癌では未分化型かつびまん型(diffuse gastric carcinoma;以下,DGCと略記)が多く,進行が早いこと,発見が遅れがちであることから一般的に予後は不良であり,2年生存率は15.5%と極めて低い4).切除率も35.1%と低く,切除症例においても2年生存率は35.6%と報告されている1).初発症状としては腹痛が多く,初診時に胃十二指腸潰瘍と診断され,胃癌の診断が遅れる症例が散見される5).本症例においても出血性胃潰瘍の診断および治療後に再検の上部消化管内視鏡検査によって胃癌の診断へと至った.
小児胃癌においては家族歴を有することが多いが5),本症例においても父が35歳時,父方の祖父が40歳時,母方の祖父が40歳前後で胃癌を患っており,2015年に改訂された国際胃癌コンセンサスガイドライン6)の3項目のうち,1)第一度または第二度近親者に年齢を問わず2人以上のDGC患者を有する場合,および2)40歳未満のDGC患者である場合,の2項目を満たしており家族性胃癌と診断され,CDH-1遺伝子における生殖細胞変異の検索が推奨される.癌抑制遺伝子の一つであるCDH-1はE-カドヘリンをコードしており,欧米においてはCDH-1遺伝子の生殖細胞変異は常染色体顕性遺伝を呈する遺伝性びまん性胃癌の30~50%に関与している6).本邦においてもCDH-1変異による遺伝性胃癌が少数報告されている7)~9)ものの,胃癌罹患の多い本邦においては家族性胃癌に占める遺伝性胃癌の頻度は少なく,その多くがHP感染による胃癌の家族内集積と考えられている6)10).
本症例においては切除標本の免疫染色検査によって癌部非癌部ともにE-カドヘリンの発現を認めたもののCDH-1遺伝子変異を否定するものではない.そこで遺伝子診療部と協議したうえでCDH-1遺伝子の生殖細胞変異検索について遺伝子カウンセラーとともに両親への説明を行った.1)本邦ではCDH-1遺伝子変異の頻度が少ないこと,2)CDH-1遺伝子変異を認めた場合,胃癌に対して既に胃全摘術が行われており,今後は乳癌に対するスクリーニングが必要になること,3)CDH-1遺伝子変異を認めなかった場合も,CDH-1以外の腫瘍関連遺伝子変異の可能性は否定できず早期から癌検診を定期受診することが望ましいこと,4)間もなく18歳となる患者本人への説明と同意が必要であること,について説明したところ現時点での遺伝子検索には同意が得られなかった.今後,本人の同意が得られて遺伝子変異検索が行われた際には病因についてのさらなる検討が可能になるものと思われる.
一方,本症例においては多数のHP感染とともに噴門部および幽門前庭部に全周性の鳥肌胃炎を認めた.鳥肌胃炎は前庭部を中心に3 mm大の小結節隆起を均一に認め,組織学的には粘膜表層に多発するリンパ濾胞を特徴とするHP関連胃炎の1亜型と考えられている11).本症例においては内視鏡的に認識される小結節隆起部のみでなく胃全体にわたって大小のリンパ濾胞を認めており,PET-CTにおける胃壁全体の異常集積はHP感染による全胃炎を反映しているものと考えられた.
また,鳥肌胃炎はHP感染小児および若年女性に好発し,若年者未分化型胃癌のハイリスク所見といわれている11).塩谷ら11)による2002年から2012年の報告症例集計に日本医学中央雑誌にて検索しえた(鳥肌胃炎と胃癌で検索,会議録も含む)2013年から2018年の報告12)~16)を合わせると,鳥肌胃炎に合併した胃癌症例報告は合計67例であり,平均年齢38歳(15~69歳),女性が53例(79%),M領域が最も多く54例(81%),単発が66例(99%),多発(2病変)が1例のみ,0-IIc型が42例(63%),低分化型腺癌が31例(46%),印環細胞癌が34例(51%),早期癌が36例(54%)であった.HP感染は記載のあった66例中62例(94%)が陽性,2例(3%)が過去の除菌によって陰性化していた.家族歴や予後についてはいずれも記載がなかった.これらの結果と比較すると,本症例は鳥肌胃炎に伴う胃癌の典型的所見を多く有している一方,家族性胃癌の診断基準を満たし12歳と発症年齢が最も低く,胃内に多発している点において非常にまれで,初めての報告となる.家系内世代間で発症の若年化が進んでいることからも何らかの遺伝的素因は否定できず,HP感染に伴う鳥肌胃炎と遺伝的素因の相互作用によって発症した可能性が考えられる.
本症例はpT3(SS)N0M0,pStage IIAの進行癌であったが,D2リンパ節郭清を伴う胃全摘術とS-1内服による術後補助化学療法によって再発なく5年2か月が経過している.胃癌治療ガイドライン(2014年5月改訂第4版および2018年1月改訂第5版)においてはpT3(SS)N0とpT1を除くpStage II/IIIが術後補助化学療法の対象とされ,さらにpStage II胃癌に対しては1年間のS-1単独療法が推奨されている17)18).しかしながら,上記ガイドラインのエビデンスとなったAdjuvant Chemotherapy Trial of S-1 for Gastric Cancer(ACTS-GC試験)における年齢の適格基準は20~80歳であり小児胃癌は対象とされていない19).本症例においてはACTS-GC試験の対象外のstageおよび年齢であり,術後補助化学療法のエビデンスは存在しないものの,通常の胃癌よりも予後不良といわれる小児胃癌であることからS-1単独療法を行うことにした.ただし,妊孕性への影響を考慮して投与期間は3クールのみとし,有害事象なく終了した.非常に予後不良といわれる小児胃癌において良好な経過が得られており,引き続き慎重に経過観察の予定である.
今回,我々は鳥肌胃炎を背景として多発する小児胃癌の1切除例を経験した.小児の上腹部痛や胃の潰瘍性病変を認めた際には,家族歴を聴取しHP感染をチェックしたうえで,積極的に上部消化管内視鏡検査を行い胃癌や鳥肌胃炎の有無を検索する必要があると考えられた.
利益相反:なし
文献
- 1) 後藤 誠一, 池田 恵一, 中川原 章, 宮崎 澄雄, 石井 栄一, 藤岡 勝慶,ほか.7歳5ヶ月男児にみられた胃癌症例の経験及び本邦15歳以下小児胃癌の統計的観察.日本小児外科学会雑誌.1982 Oct;18(6):1159–1169.
- 2) Schwartz MG, Sgaglione NA. Gastric carcinoma in the young: overview of the literature. Mt Sinai J Med. 1984 Dec;51(6):720–723.
- 3) Goldthorn JF, Canizaro PC. Gastrointestinal malignancies in infancy, childhood, and adolescence. Surg Clin North Am. 1986 Aug;66(4):845–861.
- 4) 大塚 恭寛, 小澤 弘侑, 飯野 正敏, 木村 正幸, 岡住 慎一, 村岡 実,ほか.小児胃癌の1例.日本小児外科学会雑誌.1992;28(7):1403–1407.
- 5) Okuda M, Nomura K, Kato M, Lin Y, Mabe K, Miyamoto R, et al. Gastric cancer in children and adolescents in Japan. Pediatr Int. 2019 Jan;61(1):80–86.
- 6) van der Post RS, Vogelaar IP, Carneiro F, Guilford P, Huntsman D, Hoogerbrugge N. Hereditary diffuse gastric cancer: updated clinical guidelines with an emphasis on germline CDH1 mutation carriers. J Med Genet. 2015 May;52(6):361–374.
- 7) 吉村 美保, 永原 章仁, 飯島 克順, 芹沢 信子, 加藤 順子, 浅岡 大介,ほか.若年発症の同時性家族性多発胃癌の1例.Progress of Digestive Endoscopy.2006;68(2):110–111.
- 8) Yamada H, Shinmura K, Ito H, Kasami M, Sasaki N, Shima H, et al. Germline alterations in the CDH1 gene in familial gastric cancer in the Japanese population. Cancer Sci. 2011 Oct;102(10):1782–1788.
- 9) Yamada M, Fukagawa T, Nakajima T, Asada K, Sekine S, Yamashita S, et al. Hereditary diffuse gastric cancer in a Japanese family with a large deletion involving CDH1. Gastric Cancer. 2014 Oct;17(4):750–756.
- 10) 中島 健, 斎藤 豊.【知っておこう!遺伝性消化器疾患】遺伝性びまん性胃癌(解説/特集).消化器内視鏡.2018 Aug;30(8):1009–1013.
- 11) 塩谷 昭子, 鎌田 智有, 増山 仁徳, 春間 賢.若年者胃癌と鳥肌胃炎.日本臨床.2014 Jan;72(1):78–82.
- 12) 永田 豊, 江崎 幹宏, 前畠 裕司, 中村 昌太郎, 一瀬 理沙, 平橋 美奈子,ほか.鳥肌胃炎に合併した若年発症多発胃癌の一例.日本消化器内視鏡学会雑誌.2014 Apr;56(1):1222.
- 13) 安田 真弓, 岡本 健志, 永尾 未怜, 佐々木 翔, 西村 純一, 中村 宗剛,ほか.鳥肌胃炎に対するHelicobacter pylori除菌治療の6年後に発見された未分化型早期胃癌の1例.山口医学.2015 Feb;64(1):47–51.
- 14) 小田 丈二,水谷 勝,入口 陽介,山村 彰彦.鳥肌胃炎を伴った胃癌症例9例の臨床病理学的検討.第87回日本胃癌学会総会記事.2015 Mar. p.276.
- 15) 井上 貴博, 山崎 將人, 左近 龍太, 佐藤 俊, 中山 幹大, 小根山 正貴,ほか.鳥肌胃炎に合併した若年性胃癌の1例.日本臨床外科学会雑誌.2015 Oct;76:935.
- 16) 村尾 高久, 中藤 流以, 石井 学, 藤田 穣, 松本 啓志, 山中 義之,ほか.経鼻内視鏡にて発見された鳥肌胃炎除菌後未分化型早期胃癌の一例.日本消化器がん検診学会雑誌.2018 Mar;56(2):165.
- 17) 日本胃癌学会編.胃癌治療ガイドライン医師用.2014年5月改訂第4版.東京:金原出版;2014. p. 6, 28.
- 18) 日本胃癌学会編.胃癌治療ガイドライン医師用.2018年1月改訂第5版.東京:金原出版;2018. p. 6, 32, 75–77.
- 19) Sasako M, Sakuramoto S, Katai H, Kinoshita T, Furukawa H, Yamaguchi T, et al. Five-year outcomes of a ramdomized phase III trial comparing adjuvant chemotherapy with S-1 veresus surgery alone in stage II or III gastric cancer. J Clin Oncol. 2011 Nov;29(33):4387–4393.
 https://orcid.org/0000-0002-5270-7003
https://orcid.org/0000-0002-5270-7003