2019 年 26 巻 1 号 p. 7-13
2019 年 26 巻 1 号 p. 7-13
喫煙はさまざまながんの発生に関連していることが明らかであるにもかかわらず,がんと診断された後も喫煙を継続する患者がいる.しかし喫煙はがん患者のQOLに最も影響する“痛み”にも悪影響を及ぼす.喫煙者は非喫煙者に比較してがんに関連する痛みの頻度や程度が大きい.ニコチンは急性作用として鎮痛効果を有するが,喫煙者のような慢性的なニコチン摂取は痛みのプロセシングを変化させ,さらにニコチン摂取の中断による離脱症状で痛覚過敏が生じる.喫煙は創傷治癒を遅延させ組織損傷を助長する.また,さまざまな薬物と相互作用があり抗がん薬や鎮痛薬の作用を減じて痛みを増悪させるリスクもある.しかし痛みがあると喫煙欲求が増すため患者は痛みと喫煙の悪循環に陥る.よって,がんと診断された時点から痛み治療に並行して禁煙支援を行うことが,がん患者のQOL維持に重要である.
喫煙が肺がんをはじめとしてさまざまながん種(口腔がん,喉頭がん,咽頭がん,食道がん,胃がん,肝臓がん,すい臓がん,腎がん,膀胱がん,子宮頸がん,骨髄性白血病)の発生や進行と関連することがこれまでの報告で明らかとなっている1)が,がんと診断された後も喫煙を継続する患者は少なくない.がんの診断が禁煙の強い動機となることが示唆されている2)一方で,Nayanらの総説3)によると90年代の報告では頭頸部がんと診断されたうちの23~35%,肺がんと診断されたうち13~20%の患者が診断後にも喫煙を継続していた.わが国の報告では,がんと診断された時点での喫煙者168人中96人(57%)が診断後10年までの間に喫煙を継続しており4),また,当院における麻酔科管理の悪性腫瘍手術症例801人において,手術前日になっても喫煙していた患者が45人(6%)いた5).実際の臨床場面でも“がんになってしまったのだから今さら禁煙しても意味がない”と主張して喫煙を継続する患者と遭遇することがある.このようながん患者に禁煙をすすめていくためには,喫煙ががんの発生と関連するだけでなくがん治療成績や生存率,さらにはがん患者の生活の質(QOL)に悪影響を及ぼすことを,患者本人,家族,医療者に周知させる必要がある.近年はがん治療の成績が向上しており,さまざまながん種において患者の生存率は高くなり,生存期間も長くなっている.この現状から,がん患者のQOLを維持することの重要性がますます認識されつつある.
本稿では,がん患者のQOLに大きく影響する“痛み”と喫煙の関係について文献的に考察し,さらに受動喫煙による痛みへの影響についても言及する.
がん患者の経験する身体的な痛みは,①がんそのものによる痛み,②がんの治療に伴う痛み(手術,放射線治療,化学療法などによる痛み),③がんやがんの治療と直接関係のない痛み(二次的に生じた廃用症候群による痛み,新たに合併した帯状疱疹後神経痛,もともとある腰痛や関節痛など)の3つに分類される6).それぞれの痛みについて喫煙者と非喫煙者を比較した研究がなされている.喫煙状況の定義は研究によって異なるが,喫煙習慣がないものをnever smoker,現在喫煙習慣があるものをcurrent smoker,過去に喫煙習慣があったが現在は喫煙していないものをformer smokerとしている研究が多い.禁煙期間などの条件も統一されていない.
1. がんによる痛みと喫煙Gonzalezら7)は米国のCancer Care Outcome Research and Surveillance studyに登録された患者のうち,肺がん患者2,390人,大腸がん患者2,993人を抽出してがんと診断された4~6カ月後に電話によるアンケートを実施し,痛みの有無,痛みの程度,痛みに対する治療の有無を調査し,喫煙状況との関連を検討した.肺がん患者においてcurrent smokerはformer smoker(禁煙期間の規定なし)に比べて痛みを感じることの頻度が高く,痛みの重症度が有意に高かった.大腸がん患者ではcurrent smokerはnever smoker,former smokerよりも痛みと痛み治療を受けた頻度が高く,never smokerに比べて有意に痛みの程度が強かった.これらの結果から著者らはがん患者の禁煙の必要性を論じているが,同時に痛み経験が多い患者ほど禁煙が困難であった可能性もあると述べている.Ditreら8)は,外来がん化学療法を開始する18歳以上の患者224人(乳がん35%,肺がん33%,その他のがん32%)を対象として喫煙状況と,現在有する痛みの程度,日常生活障害度,つらさを調査した.その結果,current smokerはnever smokerに比べて有意に痛みの程度が強く,日常生活も障害されやすかった.former smoker(1カ月以上喫煙していない)とnever smokerとの間には有意差はみられなかった.自己申告された痛みの程度と禁煙期間には有意に負の相関(r=−0.26,P<0.01)がみられ,痛みによる障害度と禁煙年数も同様に負の相関(r=−0.24,P=0.01)がみられたことから,禁煙によりがん患者の痛みを軽減できる可能性が示唆された.痛みだけでなく,その他の症状に関してもcurrent smokerはnever smokerに比べて多いという報告がある.Novyら9)はMD Andersonがんセンターの痛み管理センターに受診した94人のcurrent smokerと392人のnon-smoker(喫煙歴は問わず,現在喫煙習慣がないもの)に対して比較を行ったところ,current smokerは痛みの強さ,倦怠感,抑うつ,不安が強く,オピオイドの誤用のリスク(short form of the screener and opioid assessment for patients with pain)が高かった.オピオイド使用者におけるサブグループ解析では6カ月間の治療期間にわたってオピオイド使用量には差がなかったがcurrent smokerはより強い痛みを訴えていた.
2. がんの治療に伴う痛みと喫煙がんの治療に伴う痛みにおいても喫煙の影響が報告されている.胃がんで幽門側胃切除術と胃十二指腸吻合術を受けた236人を対象にした調査10)では,喫煙者もほとんどが術前1カ月間の禁煙をしていたが,術後48時間までの経静脈的患者自己調節鎮痛法(IV-PCA)によるオキシコドンの消費量は生涯喫煙本数が100未満のnon-smokerで有意に少なかった.トロント総合病院のTransitional Pain Serviceに通院する術後患者239人を対象にした調査11)では,current smokerはnever smokerに比べて術後1カ月の痛み程度[数値評価スケール(numerical rating scale:NRS)]が高く,また術後3カ月での痛みの改善度が少なく,術後から使用されたオピオイドの減量率も低かった.さらに喫煙量が多いほど術後3カ月でのオピオイド消費量が減りにくいという結果を示した.これらの結果から喫煙は術後急性痛だけでなく,3カ月後の慢性期の痛みにも関連する可能性が示唆される.しかしながらこれらの報告は多くが単施設での後ろ向き研究であるため,今後多施設による前向き研究での検討が必要と考える.
痛みの研究ではないが,Pepponeら12)は全米の化学療法または放射線療法を開始するがん患者を対象に治療前,治療直後(2週間以内),治療後6カ月の時点でアンケート調査を行い,治療によって生じるおもな12症状(倦怠感,脱毛,記憶障害,嘔気,抑うつ,睡眠障害,痛み,集中力の低下,ほてり,体重減少,皮膚障害,息切れ)について検討した.患者背景で調整した結果によるとcurrent smokerは治療直後および6カ月後の症状の訴えが多く,6カ月経過時点での症状回復度も少なかった.Kawakamiらは,非小細胞肺がんに対するパクリタキセル–カルボプラチン療法を受けた50人を対象にした調査13)において76%に末梢神経障害が生じたが,多変量解析で低クレアチニンクリアランスと並んで喫煙量が末梢神経障害の発症に関連していた[ハザード比1.03,95%信頼区間(CI)1.01~1.05,P=0.005]と報告している.さらに米国,カナダ,英国の多施設において精巣がんに対する化学療法後1年以上経過した952人の有害な健康アウトカムを調査した研究14)では,喫煙状況と有害アウトカムに有意な関連があった.5つ以上の有害事象発生に対してcurrent smoker[オッズ比(OR)3.7,95%CI 1.2~11.5,P=0.02],former smoker(禁煙期間の規定なし,OR 1.8,95%CI 1.0~3.1,P<0.05)が危険因子となると報告している.前立腺がん外部照射療法を行って2~14年間追跡されている836人の調査では15),腹痛および便意切迫の発生率がcurrent smokerでそれぞれ18%,53%,never smokerで2%,20%と有意差がみられた.乳がんの放射線治療による皮膚障害の程度がcurrent smokerで強いという報告もある16,17).以上をまとめると,喫煙はがん治療による痛みや有害事象と関連し治療完遂の妨げとなり,さらには治療中だけでなく治療後長期にわたり患者のQOLに影響しうる.
3. がんやがん治療と直接関係しない痛みと喫煙がん患者に高率に合併しうる疼痛疾患として,帯状疱疹後神経痛(PHN)があげられる18).イタリアのペスカーラという地域の家庭医と病院ネットワークが行った前向き調査19)では,帯状疱疹と診断された患者441人のうち30%が3カ月後にPHNと診断されたが,帯状疱疹発症時の痛みの強さと喫煙には有意に関連(OR 2.0,95%CI 1.1~3.6,P=0.021)があり,さらに喫煙はPHNへの移行における予測因子の一つ(OR 2.1,95%CI 1.2~3.6,P=0.007)であった.また,喫煙と腰痛との関連はよく報告されており,2009年までに発表された40研究のメタ解析20)によるとcurrent smokerとformer smokerともにnever smokerに比べて腰痛の発生が約1.3倍であり,current smokerは慢性腰痛(OR 1.8,95%CI 1.3~2.5),日常生活に支障をきたす腰痛(OR 2.1,95%CI 1.1~4.1)と有意な関連があった.
ここまでの報告から喫煙は,痛みを生じやすく重症化させやすいと考えられるが,この現象はどのような機序で起こるのだろうか.また,“喫煙するから痛い”のか“痛いから喫煙する”のか,どちらが原因でどちらが結果なのかは前述の調査結果からは判断できない.
タバコは何千もの化学物質を含有しておりその多くが生理学的作用を有しているが,代表的な成分としてニコチンがあげられる.喫煙によって摂取されたニコチンはイオンチャネル型受容体であるニコチン性アセチルコリン受容体に結合する.この受容体は中枢神経および末梢神経に広く分布しており覚醒,睡眠,不安,認知,痛みなどに関係しているが,急性のニコチン受容体刺激は鎮痛効果を示すことが動物やヒトの実験で知られている.これは内因性のオピオイドシステムを介していると考えられている.ラットにおいてニコチンによる鎮痛作用はニコチン受容体拮抗薬だけでなくオピオイド受容体拮抗薬の投与でも抑制される.またノルアドレナリンの作用を介して下行性疼痛抑制系を促進させる作用もあるとされる21).
しかし,喫煙者にみられるような慢性的なニコチン曝露は受容体やその反応性にさまざまな変化をもたらす.喫煙者では脳内のニコチン受容体が増加する22)が,持続的なニコチン投与で受容体の脱感作と耐性が比較的早期に生じるといわれている.ニコチン耐性ラットでは神経障害性痛モデルでの機械刺激に対する痛覚過敏が増強し,これは脊髄でのダイノルフィン濃度の増加やサイトカイン産生が関与していると考えられている21).Hawkinsらの研究23)ではニコチンを慢性的に投与したラットでは脊髄三叉神経核や三叉神経節において炎症性サイトカインをはじめとした炎症シグナル伝達に関与するさまざまな蛋白の発現が増加し,アストロサイトやミクログリアの活性化マーカーの発現が増加しているのが観察され,同神経領域に機械的痛覚過敏が生じていることから,ニコチンの慢性的な曝露が侵害受容ニューロンの末梢性感作,中枢性感作に関与しているのではないかと推察している.さらに,慢性的な喫煙を中断したときのニコチン離脱症状としても痛覚過敏が生じる.ラットの実験では,持続投与したニコチンを中止すると機械的刺激や熱刺激に対する痛み閾値が低下する.この機序として脊髄ミクログリア機能の変化や24),扁桃中心体のコルチコトロピン放出因子受容体を介した反応25)などが考えられている.喫煙は神経内分泌系の反応も変化させる.喫煙の急性刺激はストレス反応(交感神経–視床下部–下垂体–副腎刺激)を促進し,この反応は痛み閾値を上げる.しかし慢性的な喫煙では圧受容体機能やβ-エンドルフィン濃度が低下し,ストレス反応は減弱化する.以上のように慢性的なニコチン曝露は痛みのプロセシング(処理)過程を変化させ,痛みを感じやすくしていると考えられている.喫煙が痛みの増強因子というだけでなく痛みの慢性化にも影響しうることを示唆する研究もある.ヒトのfMRIを用いた研究では26),亜急性期(4~12週)の腰背部痛患者68人を1年間追跡し,症状が改善した群と遷延した群で側坐核–内側前頭前野という,嗜癖行動に関連すると考えられている2領域間(NAc–mPFC)の活性と喫煙状況を調査している.この皮質線条体回路の活性が強いほど慢性痛への移行リスクが増加し,喫煙者の脳で非常に強くなっていた.また研究期間中に禁煙した患者の脳では同部位の活性は有意に下がっていた.
さらに喫煙は痛みの原因となる組織構造変化を生じさせる.喫煙は骨粗鬆症,腰椎椎間板症の危険因子として知られている.喫煙は微小血管障害や一酸化炭素ヘモグロビン濃度の上昇をきたすことで組織の酸素供給を障害し,外傷や術後の創傷治癒,骨治癒の遅延をもたらし組織の変性を促進すると考えられている.Akmalら27)はin vitroの実験でニコチンが椎間板の髄核細胞の増殖抑制や細胞構造破壊を起こし椎間板を変性させることを示している.こういった組織損傷・変性と治癒遅延もがん患者の痛みの一因となりうる.
次に,喫煙は鎮痛薬や鎮痛補助薬と相互作用を有することが知られている.タバコ煙にはニコチンだけでなく多環芳香族炭化水素(PAH)も含有されているがPAHは強力な薬物代謝酵素誘導作用をもっており,特にシトクロームp450(CYP)1A2やUDP–グルクロン酸転移酵素(UGT)2B7の誘導作用がある21).アセトアミノフェンやアミトリプチリン,デュロキセチン,チザニジンなどはCYP1A2の代謝を受け,モルヒネはUGTによって代謝される.小規模な研究であるが,喫煙者ではデュロキセチン血中濃度が低下するため約15%の増量が必要であるという報告がある28).このことから喫煙者では薬物相互作用によって鎮痛薬の期待された効果が得られない可能性がある.
ここまで“喫煙するから痛い”メカニズムについて考察してきたが,“痛みがあるから喫煙してしまう”メカニズムについてはどうであろう.Ditreらの研究29)によると喫煙者では実験的な痛み刺激を与えるだけで喫煙欲求が起こる.123人の,体に痛みのない喫煙者(1日20本以上の喫煙と呼気中の一酸化炭素が8 ppm以上)を対象として,痛みを与える(P)群では0~1℃の水に手を浸けるcold-pressor testを行い,我慢できなくなる時間と痛みの強さ,および喫煙欲求の強さと実際に喫煙するまでの時間を記録した.痛みを与えない(NP)群では室温の水に手を浸けて同様に記録した.その結果,P群ではNP群に比べて有意に喫煙欲求が大きく,喫煙するまでの時間も短かった.このように“痛いから吸う”機序として考えられるのは,ニコチン急性刺激としての鎮痛もしくはニコチン離脱症状としての痛みの緩和を期待しての行為(expectancy),または単に痛みを紛らわすための行為(coping)である.このような機序に対しては,喫煙に鎮痛効果がないというビデオを見せることや,痛み刺激中に他の作業をさせて痛みを紛らわせることで喫煙欲求度を低下させ,喫煙までの時間も延長できた30).
これまで紹介してきた研究は禁煙期間を明確に定めていないものが多く,痛みへの影響を正常化させるために必要な禁煙期間についての詳細はまだわかっていない.ニコチンの離脱症状だけが痛覚過敏の原因であれば2週間~1カ月の禁煙で正常化するはずだが,いくつかの疫学調査において1カ月の禁煙期間ではcurrent smokerと差がないと報告されている8,10).喫煙が痛みに影響する機序は多面的であるため,より長期の禁煙が必要になると思われる.禁煙期間と痛みの程度には負の相関がみられる8)ため,がん患者においてはがんと診断されたと同時に,早期から禁煙を指導することが理想である.
近年わが国を含めて全世界的に受動喫煙による健康被害が重要視されている.では受動喫煙と痛みはなにか関連があるのだろうか.Inter99というデンマークにおける心血管疾患予防のための臨床研究の一部として行われたアンケート調査(n=6,784)31)では,①物を持ち上げたときの腰痛,②下肢に放散する腰痛,③頸肩痛,④関節痛,⑤腹痛,⑥頭痛,それぞれが過去1年間でどのくらいの頻度であったかを調査し,“ほぼ毎日痛い”または“しばしば痛い”と答えた体の部位の合計と喫煙歴や受動喫煙の曝露時間との関連を検討した.喫煙者では喫煙開始が若年であるほど,また喫煙量が多いほど痛みの部位が多く,非喫煙者でも1日5時間以上受動喫煙する環境にある者では有意に痛み部位の合計が多い結果となった.Aydoganら32)は,子宮全摘術を受ける101人の女性を対象に,喫煙者,受動喫煙者,非喫煙者の3群で術後24時間までのIV-PCAでのフェンタニル消費量を比較した.喫煙者だけでなく受動喫煙者も非喫煙者に比べて有意にフェンタニル消費量が多かった.動物実験の報告では33),1日20本の受動喫煙をさせたラットで椎間板の遺伝子発現変化や組織変性が確認されており,受動喫煙であっても痛みや痛み関連疾患に少なからず影響することがわかった.
本稿では,喫煙とがん患者の経験する痛みとの関係について文献レビューを行い,そのメカニズムについて考察した.喫煙と痛みには密接な関係があり,喫煙は痛み増強の原因であることがわかったが,またその痛みによって喫煙欲求が生じるため禁煙が困難となり,さらに痛みが増強する(図1).この悪循環を絶つためには痛みの治療と禁煙指導を同時に行うことが重要と考える.2016年に日本ホスピス緩和ケア協会が,“ホスピス・緩和ケア病棟における喫煙対策の現状と受動喫煙防止対策の強化に関する要望”34)を厚生労働省へ提出している.協会加盟の311施設に対してアンケート調査を行い,回答が得られた199施設(回答率64%)のうち敷地内禁煙が84%,建物内全面禁煙6%,喫煙室などの設置7%であったが,ホスピス・緩和ケア病棟では約3割の施設がなんらかの形で患者の喫煙習慣に配慮して喫煙許可を出していた.この現状をふまえて同協会は,ホスピス・緩和病棟には生命予後の短いがん患者が多数入院するため,原則として建物内禁煙(喫煙室設置可)とするよう要望している.しかしながら,すでに大半の施設は敷地内禁煙となっており,またたとえ病棟内に喫煙室を設けることが許可されても,ニコチンの半減期は約2時間35)と短いため,入院患者がその離脱症状を消失させられるほど頻回に喫煙できる環境にはなりえない.むしろ今まで述べてきたように喫煙・離脱によって痛みが増強しQOLが障害されるリスクが生じ,さらに患者のケアを担当する家族や医療従事者の受動喫煙も問題となる.ホスピス・緩和ケア病棟へ入院する段階はいわゆる終末期の状況の患者が多いと思われるが,そのような患者は痛みをはじめとした身体症状を多数有しており,その段階での禁煙は困難が予想される.よってがん患者の痛みコントロールやQOL維持のためには,より早期に禁煙指導を行うことが重要である.“がんと診断されたときからの緩和ケア”だけでなく“がんと診断されたときからの禁煙支援”が,多くの患者や医療従事者に周知されるべきと考える.
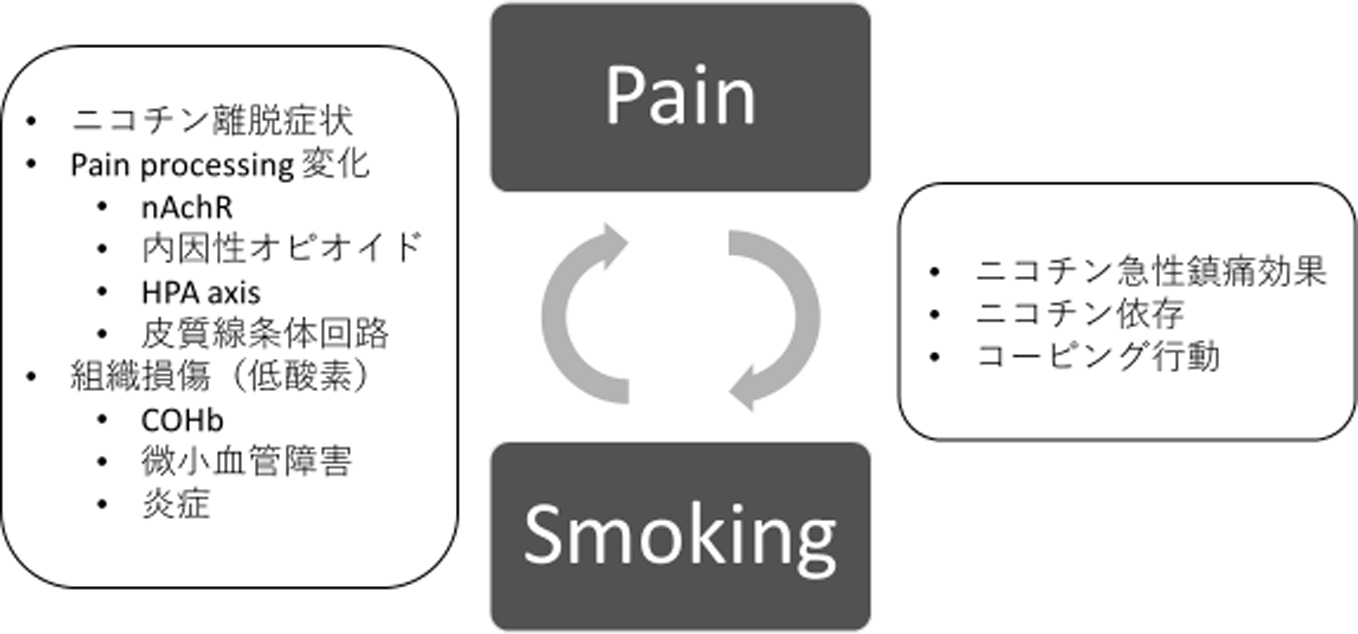
喫煙と痛みの密接な関係(possible mechanisms)
nAchR:ニコチン性アセチルコリン受容体,HPA:視床下部–下垂体–副腎髄質,COHb:一酸化炭素ヘモグロビン
この論文の要旨は,日本ペインクリニック学会第51回大会(2017年7月,岐阜)において発表した.