要旨
リンパ系システムは水分バランスの調整に於いて重要な役割を担っている.従来リンパ系システムの重要性は認識されてきたが,臨床的にリンパ系システムの画像化が困難であり,インターベンションによる治療介入も他の脈管系と比較して遅れをとってきた.しかし近年発達してきた鼠径部リンパ節からのリンパ管造影やMR lymphangiographyは新たな画像診断とインターベンションへのへの門戸を開いた.リンパ系システムの異常はリンパ浮腫とリンパ漏に大別される.この中で,リンパ漏れまれであるが重篤になり得る状態である.術後リンパ漏はリンパ漏の原因では頻度が高く,乳び胸水や腹部リンパ漏に代表される.適切な画像診断を行い,漏れを描出することでインターベンションにて治療可能となる.本稿では,総括的に臨床に重要なリンパ管解剖,リンパ管造影,適切なリンパ管造影の選択や様々なリンパ漏に対するインターベンションによる治療戦略を概説する.
Abstract
One of the crucial functions of the lymphatic system is maintenance of fluid balance. However, due to a lack of clinical imaging and interventional techniques, the lymphatic system has remained under the radar of the radiology community. The recently developed intranodal lymphangiography and MR lymphangiography have opened the door for lymphatic imaging and intervention.
Lymphatic disorders include lymphedema and lymphorrhea. Among them, idiopathic or secondary lymphatic leakage is a rare condition but can become potentially life-threatening. Postoperative lymphatic leakage is the leading cause of traumatic lymphatic leakage and can arise anywhere within the lymphatic system. Therefore, an appropriate lymphangiography technique is essential for identifying the leakage point.
Recently, interventional radiology has become available for the treatment of lymphatic leaks represented by chylothorax and abdominal lymphatic leakage associated with surgery. In the field of pediatrics, plastic bronchitis and protein losing enteropathy associated with congenital heart disease are also reported to be associated with lymphatic leakage, which can be treated by intervention.
This article comprehensively reviews the clinically relevant lymphatic anatomy, lymphangiography techniques and criteria for their selection, and treatment strategies for various kinds of lymphorrhea.
はじめに
リンパ系システムは免疫制御,代謝物の輸送,水分バランスの調整に於いて重要な役割を担い,体液循環において組織からの過剰な液体をリンパ管静脈吻合を介して静脈系に還流している.数世紀にわたりリンパ系システムの重要性は認識されてきたが,リンパ系の病態生理は十分に理解されてこなかった.同様に臨床的にもリンパ系システムの異常は画像化が困難であり,治療介入も他の脈管系と比較して遅れをとってきた.
リンパ系システムの異常はリンパ浮腫とリンパ漏に大別されるが,近年,リンパ系の画像化が進んだことにより,リンパ漏に関しては,リンパ管損傷部位を正確に同定することが可能となってきており,様々な領域でinterventional radiology(以下IVR)による治療が可能となってきた.
この中で,重要な役割を果たしてきたのがリンパ節内リンパ管造影(intranodal lymphagiography; IL)である.以前は古典的な足背リンパ管造影(pedal lymphangiography; PL)のみが直接リンパ管を造影する方法であったが1),近年ではILが報告されたことにより,劇的にIVRによる治療の幅が広がった2,3).現在では肝内リンパ管造影4–6)や腸間膜リンパ管造影7)も報告され,全身のリンパ漏の治療が可能となってきた.さらには先天性心疾患に関連する鋳型状気管支炎やタンパク漏出性胃腸症等の疾患もリンパ漏が原因の一つであることが解明され,これらに対するIVRも徐々に報告をされてきている8,9).本稿では日進月歩であるリンパ漏に対するリンパ管造影とIVRの現状について広く概説を行う.
リンパ系解剖と治療
リンパ系システムは前述の如く,免疫制御,代謝物の輸送,水分バランスの調整などに於いて重要な役割を担っている.このため,これらの成分が多量に漏れ出すリンパ漏は重篤になり得る病態である.体腔内に漏れる乳び胸腹水や腹部リンパ漏以外にも乳び尿やタンパク漏出性胃腸症,鋳型状気管支炎等もリンパ漏が関連する疾患である.このためこれらがどのような経路でリークを来すのかを理解し,さらに治療のためのアクセスルートを検討する上で,リンパ系の解剖を理解することが重要である.このため,治療を行う際に必要なリンパ系のマクロ解剖についてまず概説を行う.
胸管は人体最大のリンパ管であり,成人では40 cmにも及ぶ.主に骨盤,小腸,肝臓からのリンパ液を静脈に還流する.両側の下肢からのリンパ流が合流した左右の腰リンパ本幹,小腸からのリンパ管が合流した腸リンパ本幹,そして肝臓からのリンパ管が合流して乳び槽を形成する(Fig. 1).乳び槽は第12胸椎から第2腰椎レベルに位置し,胸管は乳び槽から始まり椎体の右腹側,下大静脈背側を頭側に走行し,横隔膜の大動脈裂孔を介して後縦隔に入る.第5胸椎レベルで左側に変位して走行し,その後食道背側から左側にでて上行した後に,左静脈角近傍で静脈に流入するが,多くのバリエーションが存在する(Fig. 2:文献5),Fig. 3a–gから引用,改変).胸管には肺や気管支,腎臓等からもリンパ液が還流する(Fig. 1).
小腸リンパ系は微絨毛中の毛細リンパ管から腸間膜のリンパ管を経て,腹部乳び槽に合流する.小腸リンパ液には小腸上皮細胞から吸収された脂肪がカイロミクロンとなり含有されているため,外観がミルクのような乳白色の乳びとなり特徴的である.このため胸管領域でのリンパ漏には乳びが含まれるため,乳び胸水や乳び心嚢液となる.一方で,腸間膜由来や胸管由来の腹部のリンパ漏は乳びとなる一方で,腰リンパ本幹や肝からのリンパ液は透明であるため,臨床上は小腸からリンパ流が関与した乳び漏とは容易に鑑別が可能である.
以上により腹部のリンパ漏は透明なリンパ液の漏れにも乳び漏にもなり得る上に,さらに無色透明なリンパ漏では,腰リンパ流のみならず,肝臓からのリンパ液による肝性リンパ漏の可能性があることも重要である4–6).さらに尿路系へのリンパ漏は胸管からの逆流であり,乳び漏となることが知られている.
以上により腹部のリンパ漏はリンパの解剖とリンパ液の性状や既存の手術内容を考慮することでリンパ管を損傷した部位をある程度予想し治療方針をたてることが可能となる.リンパ流の解剖を理解することで腰リンパ領域からの漏れは,鼠径部からのリンパ管造影でリーク部を描出できることが多く,比較的治療が容易である5).しかし腹部でのリンパ管の合流パターンはバリエーションが多く11),乳び腹水はしばしば鼠径部からのリンパ管造影ではリークが描出できず治療が困難である10).
リンパ管造影の歴史
リンパ管造影の歴史は,Kinmonthらが,1952年に足背リンパ管造影(PL)を報告したことで幕を開けた12).その後,悪性腫瘍のリンパ節転移の診断のためにリンパ管造影は行われたが,CTなどの画像診断の発達よりに,この目的のリンパ管造影は行われなくなった.一方でリピオドールが粘稠で,かつリーク部で炎症を惹起することでリンパ管造影自体がリンパ漏に対して,治療効果があるため,術後のリンパ漏に対して施行はされてはいた1).しかし現在ではより簡便に行える超音波ガイドに鼠径部のリンパ節を穿刺して行うリンパ節内リンパ管造影(IL)がルチーンに行われている.これらの技術を応用して,肝内リンパ管造影や鼠径部以外のリンパ節からのリンパ管造影,逆行性リンパ管造影も報告されている4–6).
1. 古典的足背リンパ管造影
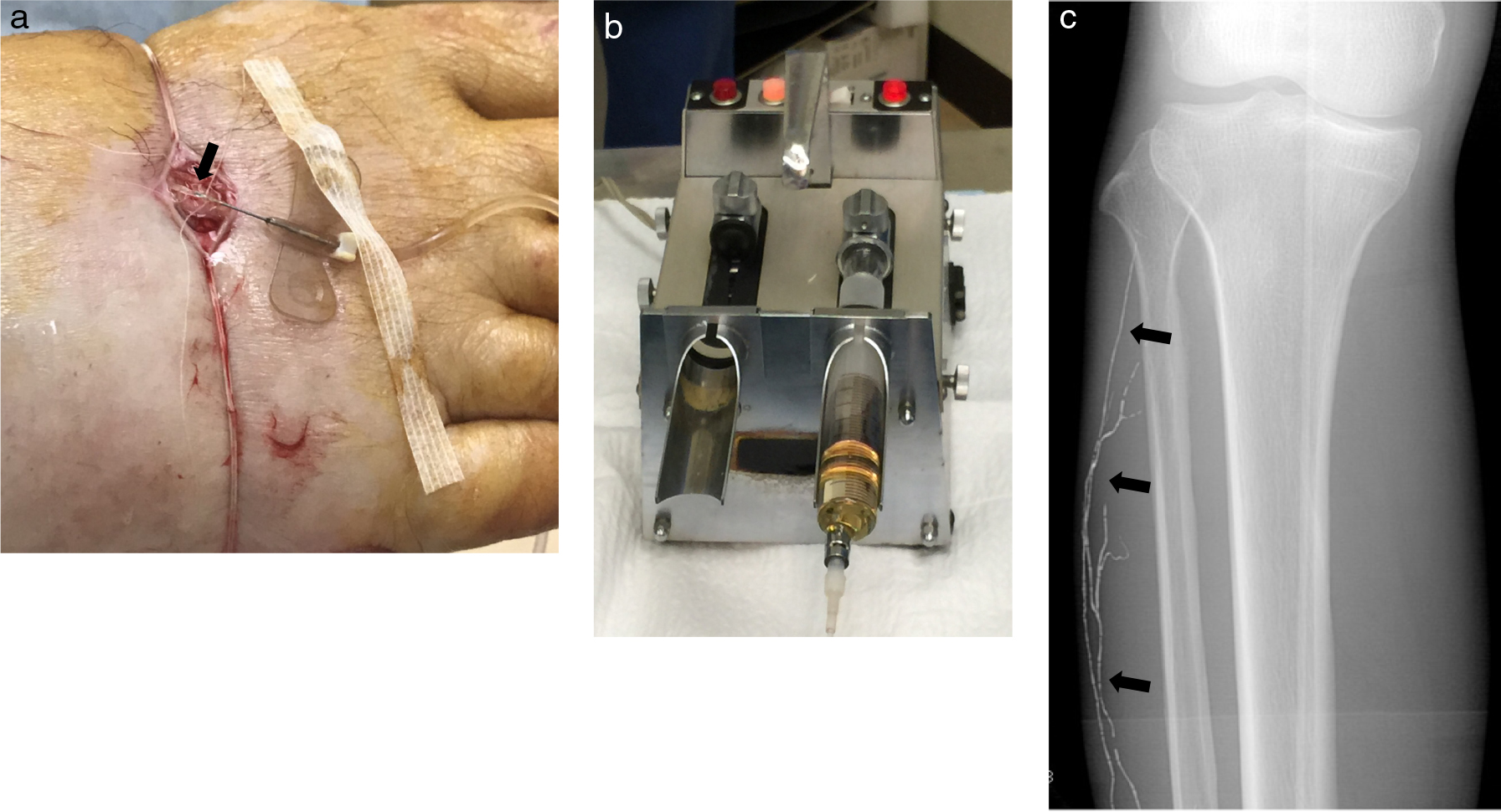
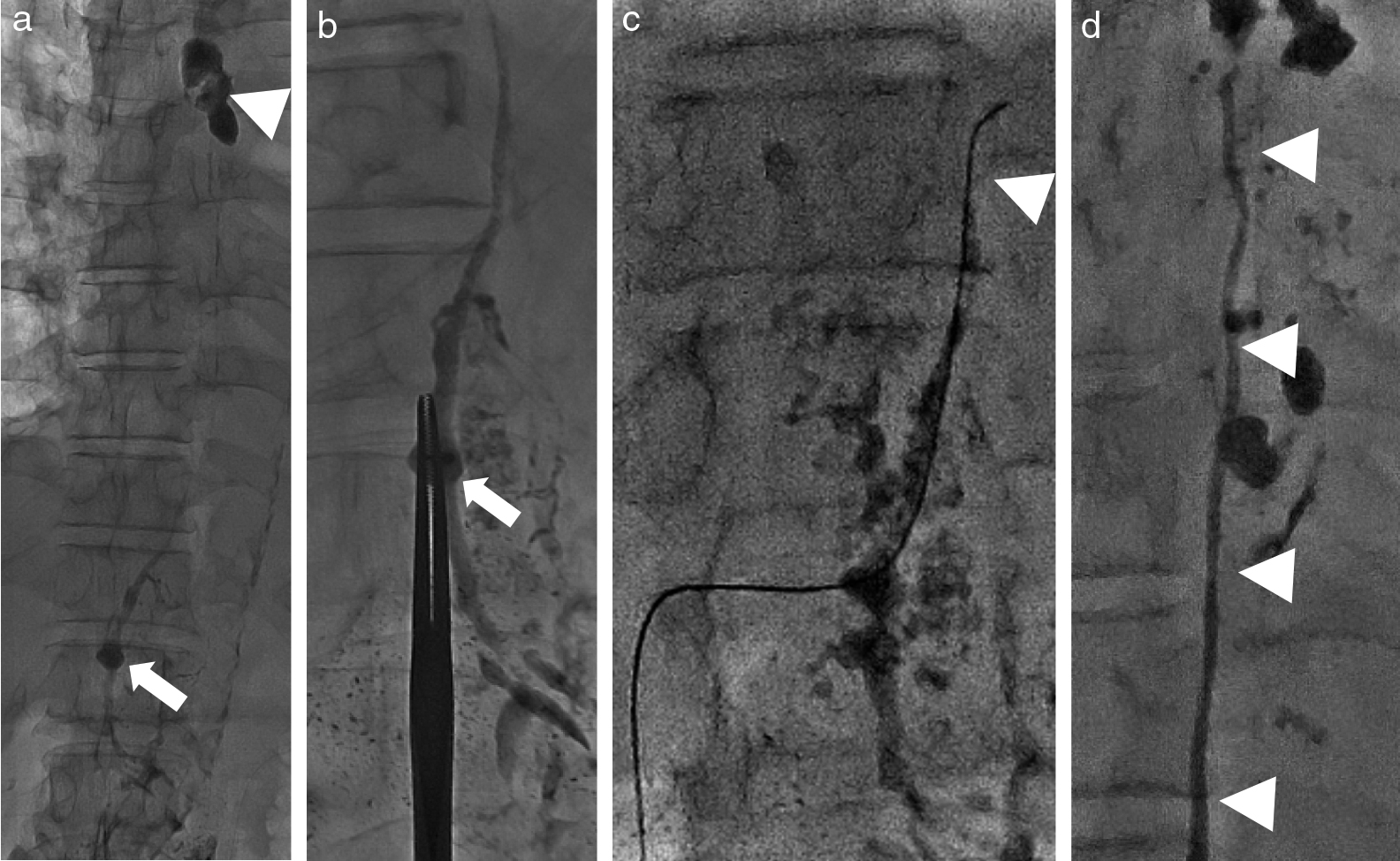
現在PLが施行される頻度は少ないが,下肢のリンパ漏の診断,治療の際には必要となる.血管造影の寝台上で仰臥位にて手技を行う.足部を消毒し,第1趾と第2趾の間の足背部に1 cm程度の縦切開を入れ,両側に糸をかけ開創する.微細なリンパ管を同定し,周囲組織から慎重に剥離し,生理食塩水で満たした1 mlシリンジを接続した29~30G翼状針にて穿刺を行う(Fig. 3a).前もって皮下に,1%リドカインとインジゴカルミンを1:1で混和したものを,ツベルクリン針でそれぞれ0.5 mlずつ皮下に注射することで皮下のリンパ管が青く染まり,目視できるようになる.その後,自動注入器にて緩徐にリピオドールを注入していく(Fig. 3b, c).
2. リンパ節内リンパ管造影
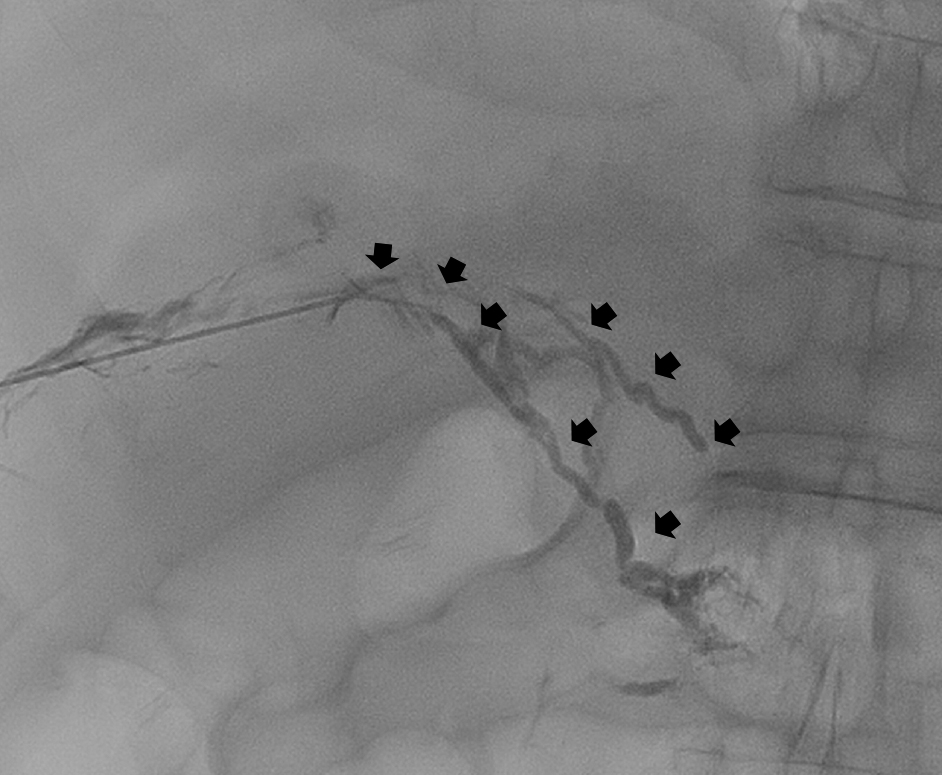
鼠径部の剃毛後,消毒を行う.表在用のリニア型高周波プローブ(8~10 MHz)にてフリーハンドで鼠径部リンパ節穿刺を行う.ロック付き1 ccシリンジを接続した50 cmのエクステンションチューブを23Gカテラン針に接続して穿刺を行っている(Fig. 4a).リンパ節は容易に移動するので,貫通しないように注意が必要である(Fig. 4b).穿刺後に用手的に緩徐にリピオドールを注入していく事でリンパ節の後に数珠状のリンパ管が描出されてくる(Fig. 4c).
3. 逆行性胸管造影
胸管は通常左静脈角近傍で,鎖骨下静脈に合流するため,逆行性に鎖骨下静脈からカニュレーションが可能である.しかし合流部には弁が存在するため,鎖骨下静脈造影では胸管は造影されない.このため鼠径部からILを行い胸管と鎖骨下静脈の吻合部を同定する(Fig. 5a).この情報を参考に左肘部皮下静脈経由で5Frカテーテルを鎖骨下静脈まで挿入し,透視下に弁の部分にカテーテルを押し当てる.その状態からマイクロカテーテルで胸管を選択することで直接胸管の造影が可能である(Fig. 5b).この方法を用いて,マイクロカテーテルを逆行性に胸管内に進めてIVRを行うことが可能である.しかし胸管と静脈の合流部は様々であり,解剖学的に選択が困難な症例も存在する5).
4. 肝内リンパ管造影
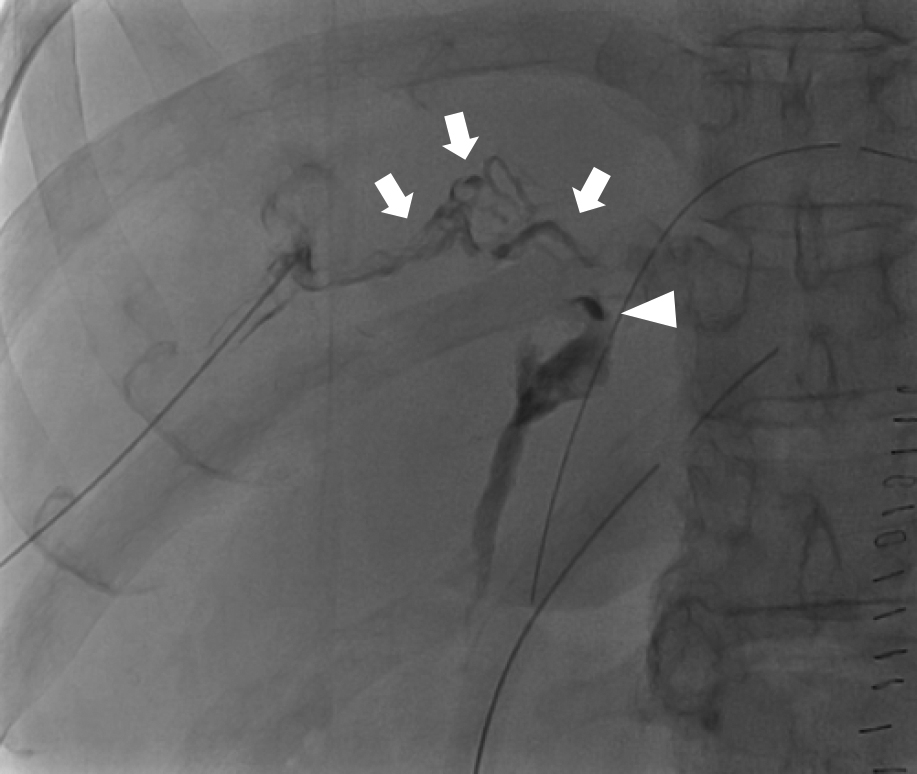
肝臓が産生するリンパ液は複数の経路で肝外に流出していくが,その中でグリソン鞘内の門脈周囲のDisse腔を走行するリンパ管が臨床的に重要である.このリンパ管は肝門部のリンパ節を経由して,肝十二指腸間膜内のリンパ管を通り,乳び槽に流入する.このため,肝十二指腸間膜リンパ管損傷に伴ったリンパ漏は肝臓由来の可能性がある10–12).また先天性疾患患者のタンパク漏出性胃腸症も肝臓からのリンパ液が十二指腸に漏れ出すことが原因の一つであることが報告されている9).これらの肝性リンパ漏の診断と治療には肝内リンパ管造影が必須である.肝内リンパ管は.超音波ガイドにグリソン鞘に針を進めて造影することで描出可能である.我々は,22G PTBD針を用いて,肝内リンパ管造影を行っている(Fig. 6).
MR lymphangiography
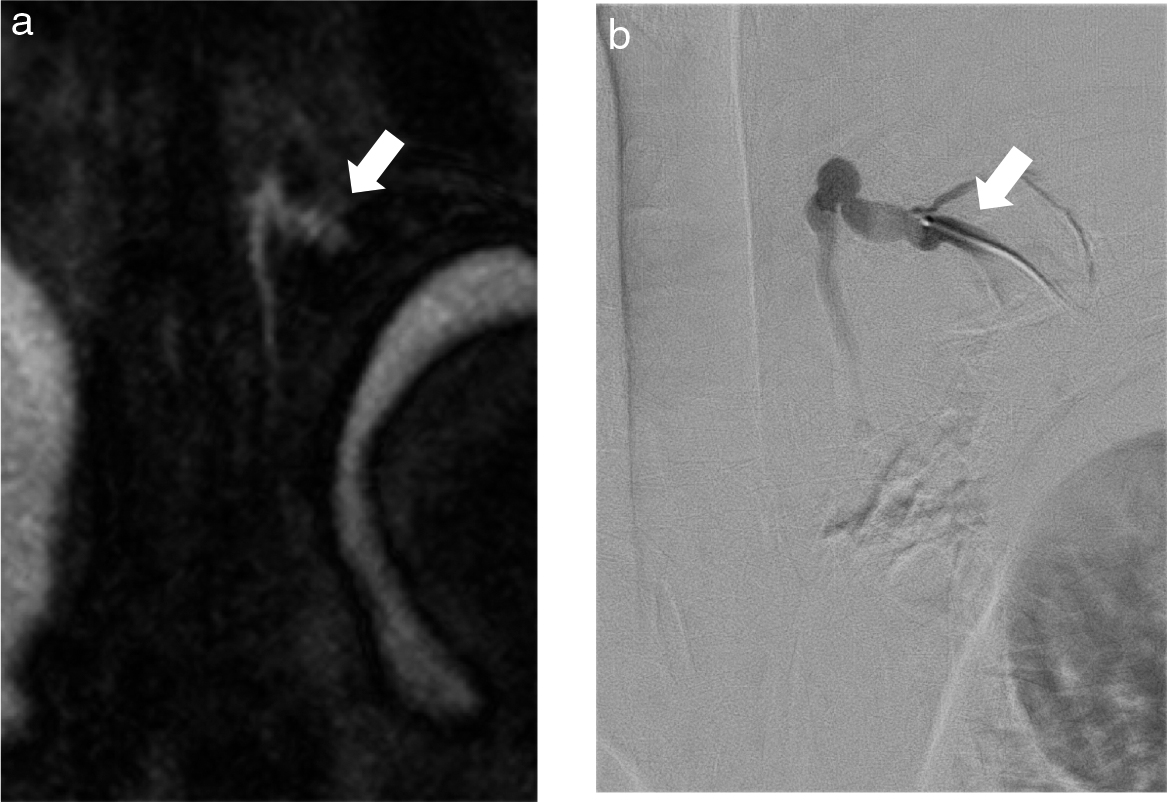
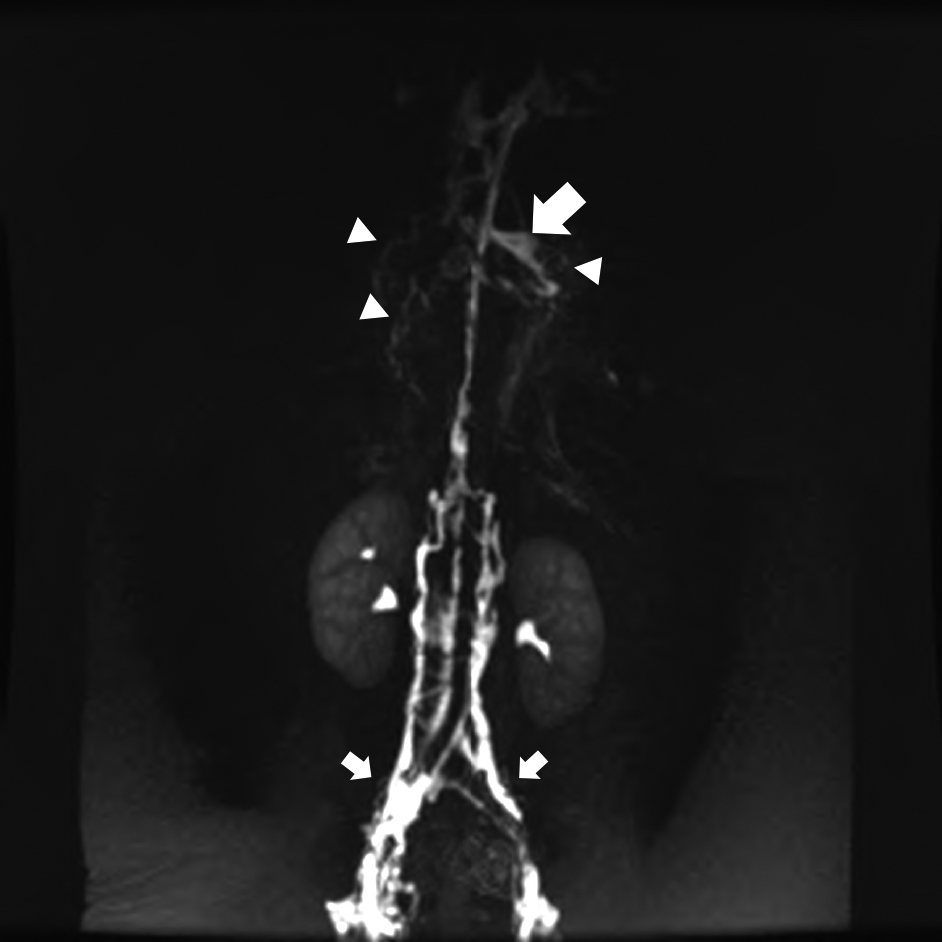
近年注目されているMRIによるリンパ管イメージング法として,非造影のMR lymphangiography(MRL)/MR thoracic ductography(MRTD)がある.基本はheavy T2イメージであり,これにより非侵襲的にリンパ管解剖の把握が可能でありIVR前の評価として重要である.胸管静脈吻合部も症例によっては描出が可能である(Fig. 7a, b).また適応外使用となるが,鼠径部のリンパ節を穿刺してガドリニウムを注入しながら行うダイナミックMRLは先天性心疾患のFontan術後の患者での術前評価,機能評価の面でも極めて有用である(Fig. 8)(Maxim Itkin先生提供:Neours/Dupont Children’s Hospital/Penn Medicine, Perelman School of Medicine, Hospital of University of Pennsylvania).
リンパ漏に対するIVR
大きくリンパ漏はリンパ管損傷,過剰産生,逆流,リンパ管奇形,先天性心疾患関係,特発性.その他のNoonan症候群等に大別される.比較的臨床で遭遇する頻度が高いのは術後のリンパ漏であり,IVRにて治療が可能なケースが増えてきている.しかし依然として治療が困難なリンパ漏も多く存在する.本稿では典型的なリンパ漏に対するIVRを紹介する.
1. 塞栓物質
リンパ管を塞栓する際は,液体状塞栓物質であるNBCA(N-butyl-2-cyanoacrylate)を用いる.NBCAは微量の水分あるいは陰イオンと接触すると重合を起こしてポリマーを形成して硬化する.これを用いてリンパ管を鋳型状に塞栓をする.通常,油性造影剤であるリピオドールと混和して重合時間を調整しつつ透視下で可視化して使用する.NBCAは薬事法上,皮膚欠損用創傷被覆材の一種として「医療用品(4)整形用品」に類別される.すなわち皮膚損傷のみへの適用が承認されているに過ぎず,血管内投与については禁忌・禁止項目に列挙されており現状ではNBCAのリンパ管内投与は適応外使用として医師の裁量の下で使用されているに過ぎない.このため充分なインフォームドコンセントのもとにIVRを施行する必要がある.
2. 乳び胸水に対する胸管塞栓術
乳び胸水が多量である場合は蛋白や脂肪の低下,脂溶性ビタミンの欠乏による低栄養,リンパ球喪失による血中リンパ球の減少などの代謝,免疫機能の低下,循環不全などの重篤な病態へと進行する可能性がある.このため保存的治療に反応しない難治性乳び胸水や排液量が1000 ml/日以上の乳び胸水が対象となる1,13).
手技:
a.術後乳び胸水に対する経腹的胸管塞栓術
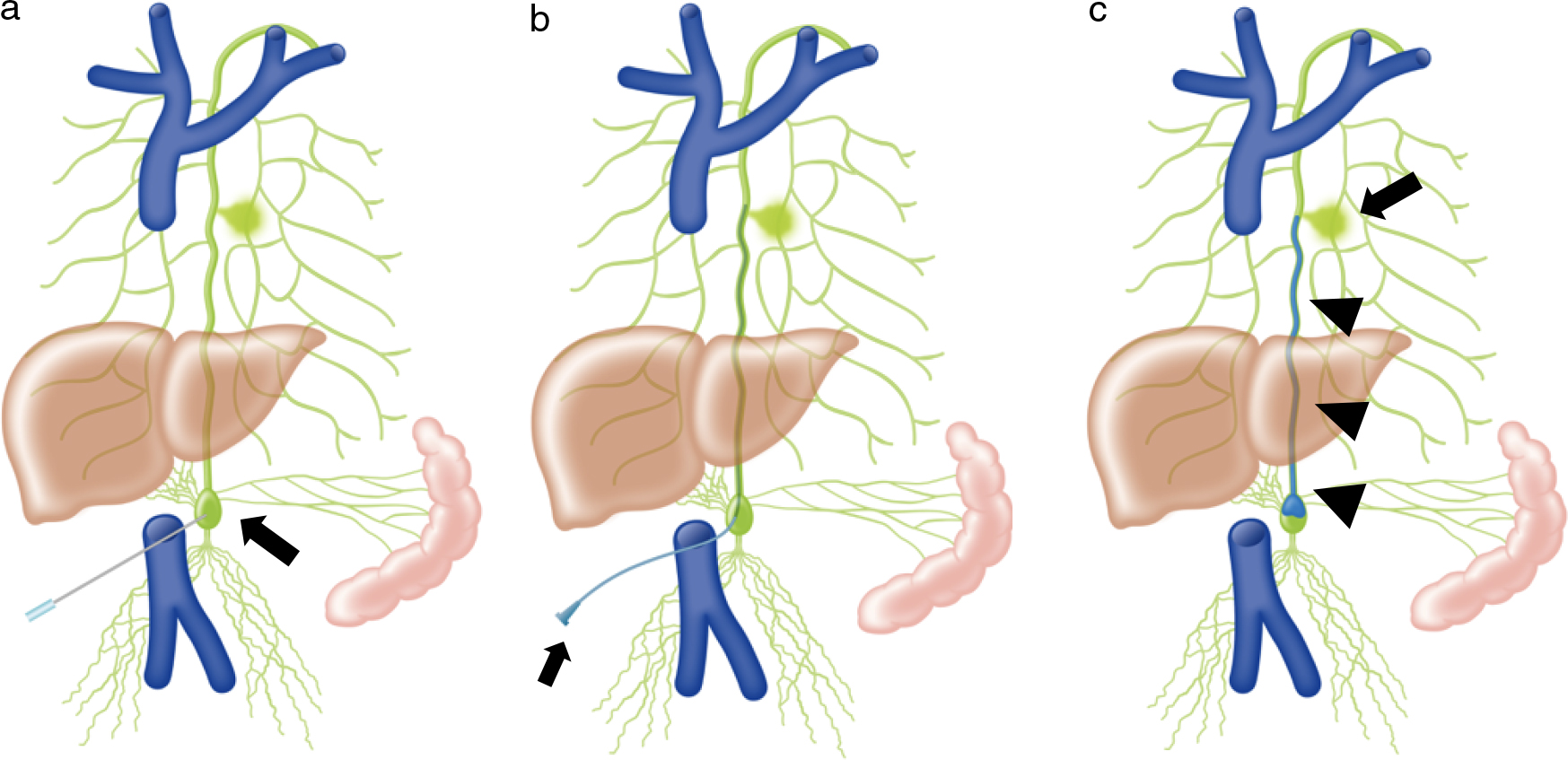
胸管塞栓術の歴史は古く1990年代にはCopeらが動物実験にて安全性を検討した後に臨床での初期経験を報告している14).その後現在までに安定した成績が報告されている15,16).リンパ管造影後に,透視下に経皮的に乳び槽を穿刺して塞栓を行う.手技の一連の流れをFig. 9(文献5)のFig. 2a–cより改変,引用)に提示すると共に,症例も供覧する(Fig. 10).
b.術後乳び胸水に対する逆行性アプローチによる胸管塞栓術
静脈角からの逆行性アプローチにより,胸管のカニュレーションを行う方法である5).前述の逆行性胸管造影と同様の方法で,胸管のカニュレーションを行う.胸管には弁があるためガイドワイヤーで慎重に弁を突破してマイクロカテーテルを進めていく.胸管分枝損傷による乳び胸水では,逆行性に分枝までマイクロカテーテルを進めて,塞栓を行うことが可能である(Fig. 11).
c.Fontan術後の鋳型気管支炎に対する塞栓術
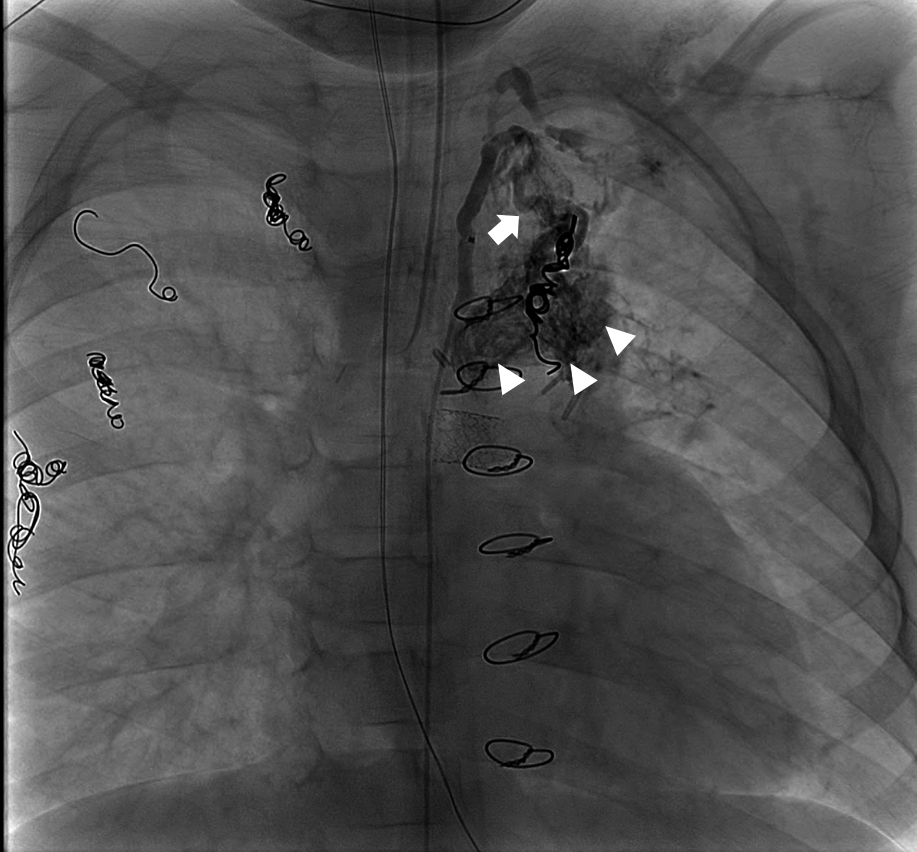
鋳型状気管支炎(plastic bronchitis; PB)は蛋白漏出性胃腸症(protein losing enteropathy; PLE)と同様にFontan術後の遠隔期合併症の一つとして重要である8).Fontan術後数年で18%に生じるとも言われ,様々な治療法が試みられるが確立された治療法はなく,気管支鋳型粘液栓を喀出し,気道閉塞のため致死的な経過をとる可能性がある16).近年,経皮的胸管塞栓術の手技を応用して胸管から気管支へのシャント塞栓を行うことで治療が可能であることが報告されている8,17)(Fig. 12:Maxim Itkin先生のご厚意により提供:Neours/Dupont Children’s Hospital/Penn Medicine, Perelman School of Medicine, Hospital of University of Pennsylvania).
3. 腹部リンパ漏に対する塞栓術
腹部のリンパ漏は大きくは腰リンパ系,肝リンパ系,小腸リンパ系に大別される術後症例ではリンパ管の損傷部位によって,リンパ漏,乳び漏,肝性リンパ漏が起こりえる.他にも稀なものとして,特発性乳び尿や先天性心疾患に伴ったタンパク漏出性胃腸症もリンパ漏が関連する.紙面の都合上,腰リンパ漏,肝性リンパ漏,蛋白漏出生胃腸症の症例を提示する.
a.腰リンパ漏
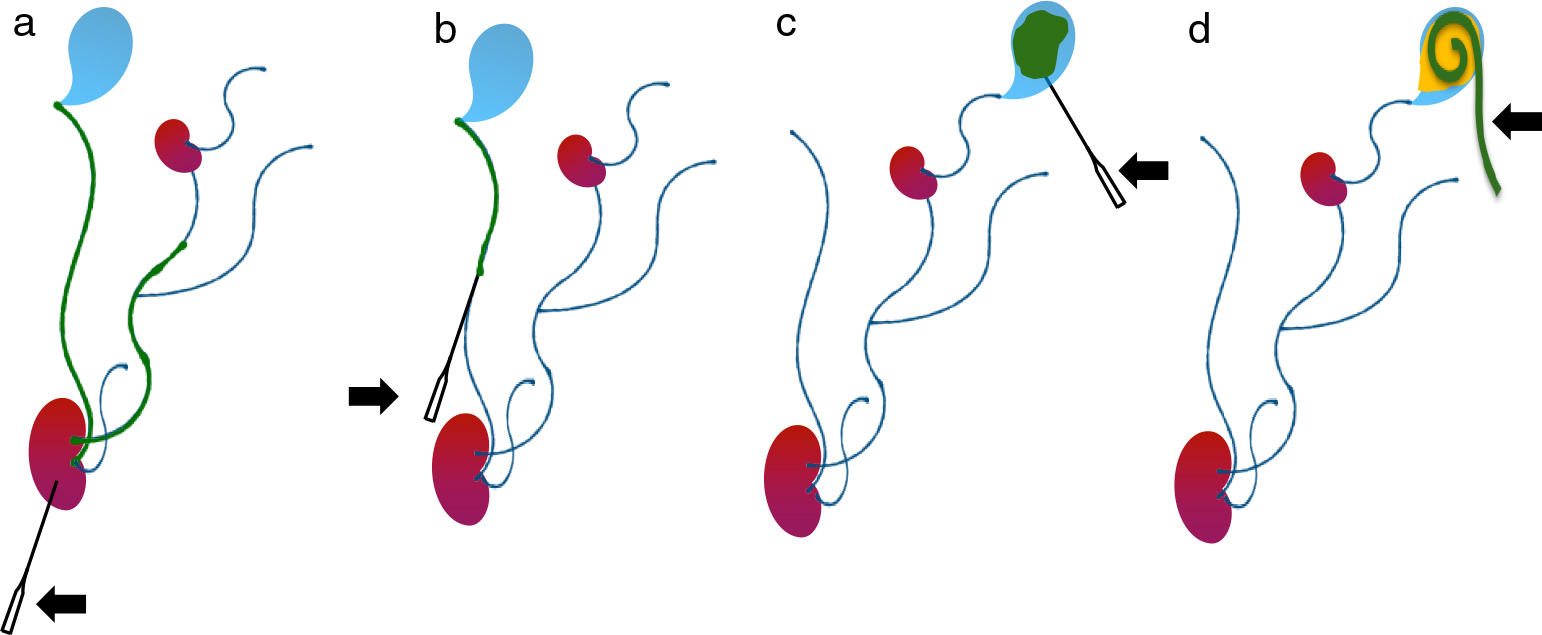
通常鼠径部からILにてリーク部が描出可能であり,腹部~骨盤領域のリンパ節郭清後,鼠径部のカットダウン後などに報告されている.Hurら18)は腹部領域のリンパ漏に対するNBCAによる塞栓術を報告し,リーク部の限局した小さな液体貯留腔(lymphopseudoaneurysm)を穿刺してNBCAを注入する方法,漏出部の上流のリンパ管(upstream lymphatic vessels)を塞栓する方法,漏出部の上流のリンパ節(upstream lymph node)から塞栓する方法を報告している.これに加えて硬化療法も有用である(Fig. 13).基本的な治療方法として,卵巣癌術後の骨盤リンパ節郭清による大量腹水を鼠径リンパ節(upstream lymph node)からNBCAを直接注入して治療した症例を提示する(Fig. 14).
b.肝性リンパ漏に対する塞栓術
肝臓は胸管を流れるリンパ液のうち,20~40%程度のリンパ液を産生する臓器である.肝内リンパは浅在性と深在性に大別され,深在性リンパはさらに肝静脈に沿ったリンパ流と門脈に沿ったリンパ流に分類される19).門脈に沿った肝内リンパ管は肝門部から肝十二指腸間膜内のリンパ管を介して乳び槽に合流する.このため肝十二指腸間膜のリンパ管損傷では術後に大量の肝性リンパ腹水をきたす可能性がある.IVRには肝内リンパ管造影が重要である4–6)(Fig. 15).
c.蛋白漏出生胃腸症の塞栓術
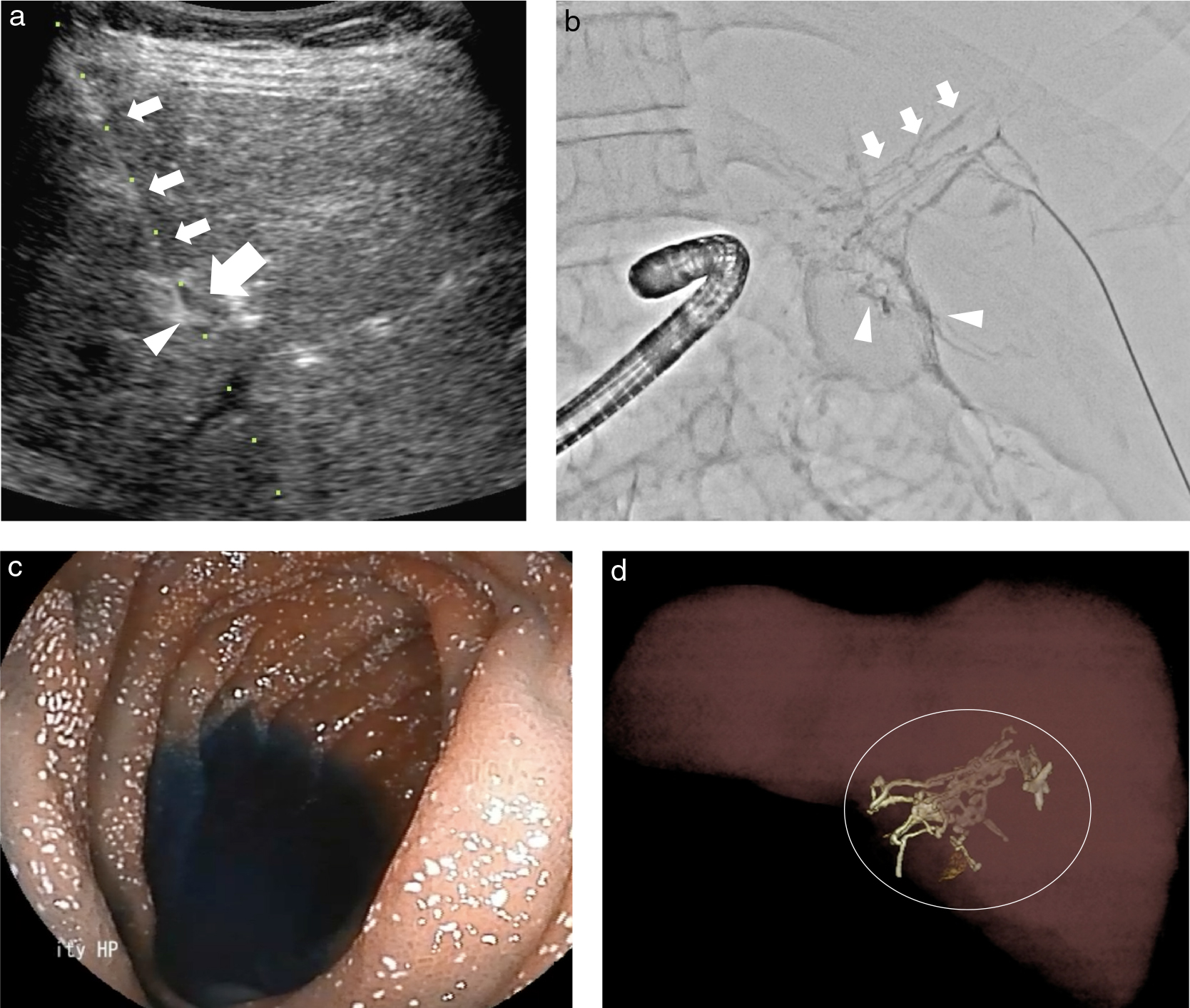
PB同様に蛋白漏出性胃腸症(protein losing enteropathy; PLE)はFontan術後の遠隔期合併症の一つとして重要である.Fontan術後,数年で3%程度に生じるとも報告されている16).様々な治療,管理法が試行されているが,治療法は確立されておらず,PLE 発症からの期間経過とともに血清タンパクやアルブミンの正常値の維持は困難となる.近年,肝臓由来のリンパ液が十二指腸に流出することが原因の一つであることが明らかとなった.このため肝内から十二指腸の周囲の肝十二指腸間膜のリンパ管塞栓を行うことで,治療が行えることが報告されている9).しかし長期の成績はまだ不明であり,自験例では再発も経験をしている(Fig. 16).
まとめ
紙面の許す限り,リンパ系IVRの現状について広く解説した.現状では本邦でのこれらのリンパ系IVRの認知度は低いと言わざるを得ないが,今後さらに新たな治療法や知見が得られていく可能性がある領域であると思われる.本稿が,日常診療においてリンパ系IVRに興味がある医師の一助になれば存外の喜びである.最後に,現時点でリンパ系IVRはどこの施設でも行える状況にはないため,もし治療適応等含めて質問があれば筆者に気軽に連絡をしていただければ幸いである.
連絡先:inomasa1130@gmail.com
謝辞
本論文の作成にあたり,貴重な症例を提供してくださったMaxim Itkin先生に感謝致します.
文献
- 1) Kawasaki R, Sugimoto K, Fujii M, et al. Therapeutic effectiveness of diagnostic lymphangiography for refractory postoperative chylothorax and chylous ascites: Correlation with radiologic findings and preceding medical treatment. Am J Roentgenol 2013; 201: 659–666.
- 2) Rajebi MR, Chaudry G, Padua HM, et al. Intranodal lymphangiography: Feasibility and preliminary experience in children. J Vasc Interv Radiol 2011; 22: 1300–1305.
- 3) Nadolski GJ, Itkin M. Feasibility of ultrasound-guided intranodal lymphangiogram for thoracic duct embolization. J Vasc Interv Radiol 2012; 23: 613–616.
- 4) Matsumoto S, Mori H, Tada I. Successful demonstration of post-operative lymphatic fistula by percutaneous transhepatic lymphography. Clin Radiol 2000; 55: 485–486.
- 5) Inoue M, Nakatsuka S, Yashiro H, et al. Lymphatic intervention for various types of lymphorrhea: Access and treatment. RadioGraphics 2016; 36: 2199–2211.
- 6) Hasegawa T, Tsuboi M, Fukushima K, et al. Refractory hepatic lymphorrhea: Percutaneous transhepatic lymphangiography and embolization with n-Butyl-2-cyanoacrylate glue. Cardiovasc Intervent Radiol 2021; 44: 1127–1130.
- 7) Lee H, Kim SJ, Hur S, et al. The feasibility of mesenteric intranodal lymphangiography: Its clinical application for refractory postoperative chylous ascites. J Vasc Interv Radiol 2018; 29: 1290–1292.
- 8) Dori Y, Keller MS, Rome JJ, et al. Percutaneous lymphatic embolization of abnormal pulmonary lymphatic flow as treatment of plastic bronchitis in patients with congenital heart disease. Circulation 2016; 133: 1160–1170.
- 9) Itkin M, Piccoli DA, Nadolski G, et al. Protein-losing enteropathy in patients with congenital heart disease. J Am Coll Cardiol 2017; 69: 2929–2937.
- 10) Nadolski GJ, Chauhan NR, Itkin M, et al. Lymphangiography and lymphatic embolization for the treatment of refractory chylous ascites. Cardiovasc Intervent Radiol 2018; 41: 415–423.
- 11) Loukas M, Wartmann CT, Louis RG Jr, et al. Cisterna chyli: A detailed anatomic investigation. Clinical Anatomy 2007; 20: 683–688.
- 12) Kinmonth JB. Lymphangiography in man: A method of outlining lymphatic trunks at operation. Clin Sci 1952; 11: 13–20.
- 13) Itkin M, Kucharczuk JC, Kwak A, et al. Nonoperative thoracic duct embolization for traumatic thoracic duct leak: Experience in 109 patients. J Thorac Cardiovasc Surg 2010; 139: 584–590.
- 14) Cope C, Salem R, Kaiser LR. Management of chylothorax by percutaneous catheterization and embolization of the thoracic duct: Prospective trial. J Vasc Interv Radiol 1999; 10: 1248–1254.
- 15) Schild HH, Pieper CC. Where have all the punctures gone? An analysis of thoracic duct embolizations. J Vasc Interv Radiol 2020; 31: 74–79.
- 16) Sharma VJ, Iyengar AJ, Zannino D, et al. Protein-losing enteropathy and plastic bronchitis after the Fontan procedure. J Thorac Cardiovasc Surg 2021; 161: 2158–2165.
- 17) Dori Y, Keller MS, Rychik J, et al. Successful treatment of plastic bronchitis by selective lymphatic embolization in a Fontan patient. Pediatrics 2014; 134: e590–e595.
- 18) Hur S, Shin JH, Lee IJ, et al. Early experience in the management of postoperative lymphatic leakage using lipiodol lymphangiography and adjunctive glue embolization. J Vasc Interv Radiol 2016; 27: 1177–1186.
- 19) Tanaka M, Iwakiri Y. The hepatic lymphatic vascular system: Structure, function, markers, and lymphangiogenesis. Cell Mol Gastroenterol Hepatol 2016; 14: 733–749.