2021 年 29 巻 3 号 p. 369-376
2021 年 29 巻 3 号 p. 369-376
呼吸器疾患患者を診療するうえで,各種モニタリングは欠かせない.特に呼吸不全を呈している患者のケアでは,安静時の低酸素血症や高二酸化炭素血症,労作時や運動時の低酸素血症や運動耐容能,さらに睡眠時の無呼吸・低呼吸や低換気などを正確に知るために,動脈血ガス分析,SpO2モニタリング,経皮CO2モニタリング,睡眠ポリグラフ検査などが臨床で実施されている.特に酸素療法や非侵襲的換気療法の導入時には,これらを積極的に用いて患者の病態を正確に把握し,また治療効果を確認することが重要である.睡眠時のモニタリングによって,慢性呼吸不全患者においては,REM睡眠時を中心に低換気をしばしば生じていることが分かってきており,この有無がCOPDの増悪回数や肺高血圧などと関係することが明らかになってきている.ここでは,各種モニタリングについて解説するとともに,睡眠時低換気の検出方法およびその意義についても述べたい.
普段,呼吸器疾患患者を診療するうえで,各種モニタリングは欠かせない.特に呼吸不全を呈している患者のケアにおいては,その病状を正確に把握するためのモニタリングは必須となる.具体的には安静時の低酸素血症や高二酸化炭素血症,労作時や運動時の低酸素血症や運動耐容能,さらに睡眠時の無呼吸・低呼吸や低換気などをできるだけ非侵襲的かつ正確に知ることが重要になってくる.
その手段として普段用いられるものとしては,動脈血ガス分析,SpO2モニタリング(スポット,終日,睡眠時など),6分間歩行などの運動負荷時のモニタリング,経皮CO2モニタリング,睡眠ポリグラフ検査などが挙げられる.
当科では,慢性呼吸不全患者に対して在宅酸素療法(HOT)や非侵襲的換気療法(NPPV)を導入する際には原則として教育入院を行っている.これらの際に行っているモニタリングについて述べる(図1).

HOT・NPPV導入に必要なベッドサイド検査
呼吸不全患者を診る際には,まず動脈血ガス分析を行う.室内気吸入時の動脈血酸素分圧(PaO2)が60 Torr(mmHg)以下となる呼吸障害,あるいはそれに相当する呼吸障害を呈する異常状態を「呼吸不全」と呼ぶ.PaO2はパルスオキシメータによる経皮的動脈血酸素飽和度(SpO2)で推測することは可能である(図2).しかし,PaCO2の測定には動脈血ガス分析が不可欠である.PaCO2の正常範囲は35 Torrから45 Torrであり,肺胞換気量に反比例する.通常は,呼吸中枢によってPaCO2が正常範囲になるように換気は厳格にコントロールされている.
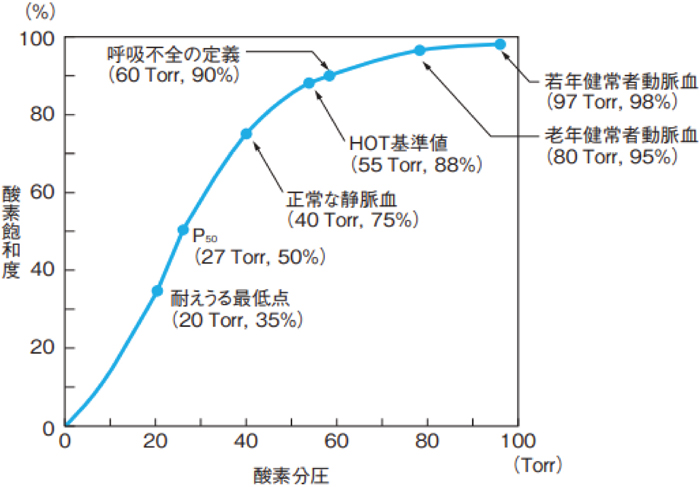
標準酸素解離曲線
体温37°C,pH 7.4の条件下での動脈血の酸素分圧(PaO2)と酸素飽和度(SpO2)の関係を示している.目安としてPaO2 60 TorrがSpO2 約90%に相当する.pHなどで曲線は変化する.
日本呼吸ケア・リハビリテーション学会 酸素療法マニュアル作成委員会・日本呼吸器学会 肺生理専門委員会編集 酸素療法マニュアル 2017から引用
PaCO2が正常範囲あるいはそれ以下の呼吸不全をI型,正常範囲を超えている場合をII型呼吸不全と区別している.PaCO2が45 Torrを超える場合には,極端な代謝性アルカローシスの場合を除き,換気が低下している,すなわち換気不全の状態と考えられる.II型呼吸不全の患者に不用意に高濃度の酸素を投与すると,PaCO2が急上昇し,CO2ナルコーシスを来す恐れがある.よって,呼吸不全患者に酸素を投与する場合には,I型かII型かをまず見極めることが重要である.もしI型かII型かが不明の場合は,少量の酸素流量から開始するべきである.
パルスオキシメータの登場により医療現場で低酸素血症を把握することは容易になった.ただし,その測定値であるSpO2は,日常生活において大きく変動することがあることを常に頭に入れておく必要がある.よってある一時点のSpO2の値だけでHOTを導入することは危険であり,また治療すべき低酸素血症を見落とす可能性も高い.
当院において,労作時の息切れや呼吸促拍などから呼吸不全を疑った場合には,SpO2を持続的に測定・記録できるパルスオキシメータを用いて,終日あるいは終夜のモニタリングを行う.外来でも,パルスオキシメータを患者に持ち帰ってもらうことで自宅生活における労作時あるいは夜間の低酸素血症の有無を確認することができる.これにより飲酒や睡眠導入薬の影響をみることも可能である.このモニタリングで大切なことは,日誌にできるだけ詳細な行動内容を記載してもらうことである.これにより,日常労作と低酸素血症との関係が明確になってくる.最近では,加速度センサーを内蔵しているパルスオキシメータも開発されつつあり,労作強度と低酸素血症との関係を検討することも可能になっている.また,防水仕様のパルスオキシメータも開発され,入浴中の低酸素血症を把握することが可能となった.
SpO2の終夜モニタリングを行うことで,睡眠時無呼吸症候群の合併をスクリーニングすることができる(図3).また,睡眠時に間欠的に強い低酸素血症が持続する現象を認めることがある.トイレなどの労作中でなければ,後述のREM睡眠時関連低換気の可能性がある(図4).
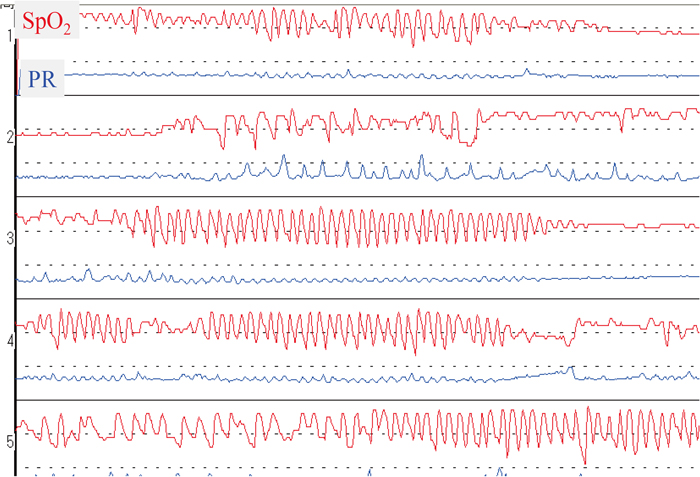
夜間SpO2モニタリングの1例
睡眠時無呼吸症候群を疑う.
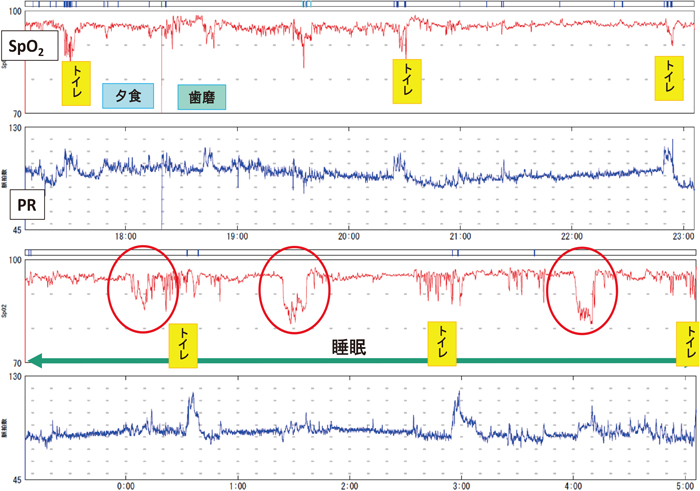
SpO2モニタリングの1例
石綿肺,両側気胸の患者.トイレの際に労作時低酸素血症を認める.また,睡眠中に間欠的に強い低酸素血症を認める.
なお,労作時の低酸素血症は,パルスオキシメータを装着したうえで6分間歩行などの運動負荷を行うことで容易に把握することができる.一定の負荷をかけるという意味では重要な検査であるが,在宅における日常労作時の低酸素血症を把握し,それをHOTなどで是正するという意味では,SpO2の終日モニタリングの方が臨床的に役立つこともある.
動脈血ガス分析の項でも述べたが,PaCO2は肺胞換気量と反比例することから,その変動を知ることで換気量の変化を推定することができるが,動脈血ガス分析を連続的に行うことは難しい.そこで開発されたのが,経皮CO2モニタである.皮膚を40度以上に温めて末梢血を動脈血化し,皮膚に装着したセベリングハウス型電極で二酸化炭素分圧を経皮的に測定する.その計測値PtcCO2は実際のPaCO2との間に平均6.1 Torrの差があり,20%以上の症例では差が10 Torrを超えるという報告もある1).しかしながら,PaCO2変動をみることで,換気量の変化を知ることは可能である.
呼吸不全患者においては,たとえ日中に高二酸化炭素血症を認めなくても,睡眠中にしばしば換気が低下していることが知られており2),夜間の経皮CO2モニタリングはその換気の変化・低下を明確にとらえることができる.特に,PtcCO2がベースラインから5 Torr以上,5分以上にわたって間欠的に上昇する現象にしばしば遭遇する.室内気では同時にSpO2低下も伴う.我々はこれを間欠的夜間高二酸化炭素血症(episodic nocturnal hypercapnia: eNH)と呼んでいる3)(図5,6).後述するが,この現象はREM睡眠時の低換気にほぼ一致する.
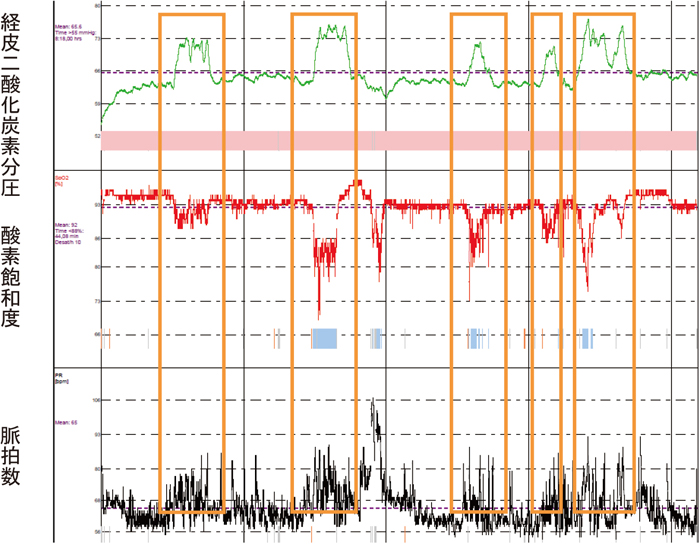
経皮CO2モニタリングの1例
夜間に周期的に低酸素血症および高二酸化炭素血症が繰り返し生じている.
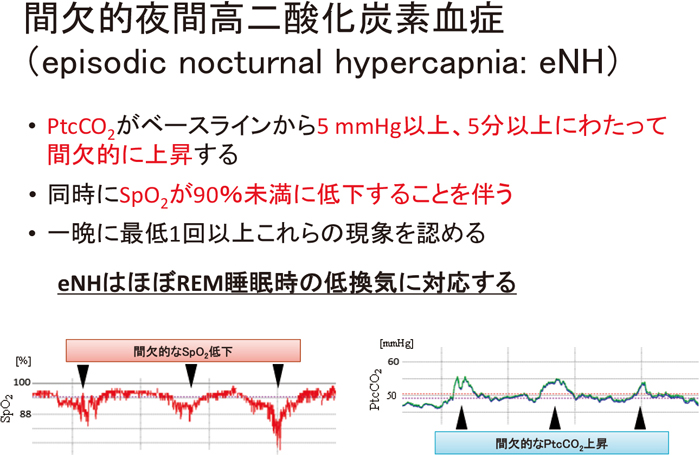
間欠的夜間高二酸化炭素血症(episodic nocturnal hypercapnia: eNH)の定義
Kitajima T et al., Int J COPD 2018; 13: 843から引用
PSGは,睡眠呼吸異常を非侵襲的に検出するために,一晩の脳波,筋電図,胸部・腹部の呼吸運動,SpO2,心電図などを同時に測定・記録する.特に睡眠時無呼吸症候群の確定診断に用いられている(図7).COPDに睡眠時無呼吸症候群が合併することをOverlap syndromeと呼び,予後不良因子の一つと言われている.慢性呼吸不全の治療に加えてこの睡眠時無呼吸症候群のコントロールを行うことが大切である4).最近では,NPPVの治療機器に睡眠時無呼吸を感知して自動的にEPAP圧を変動させる機能(AutoEPAP)が搭載されるようになってきている.
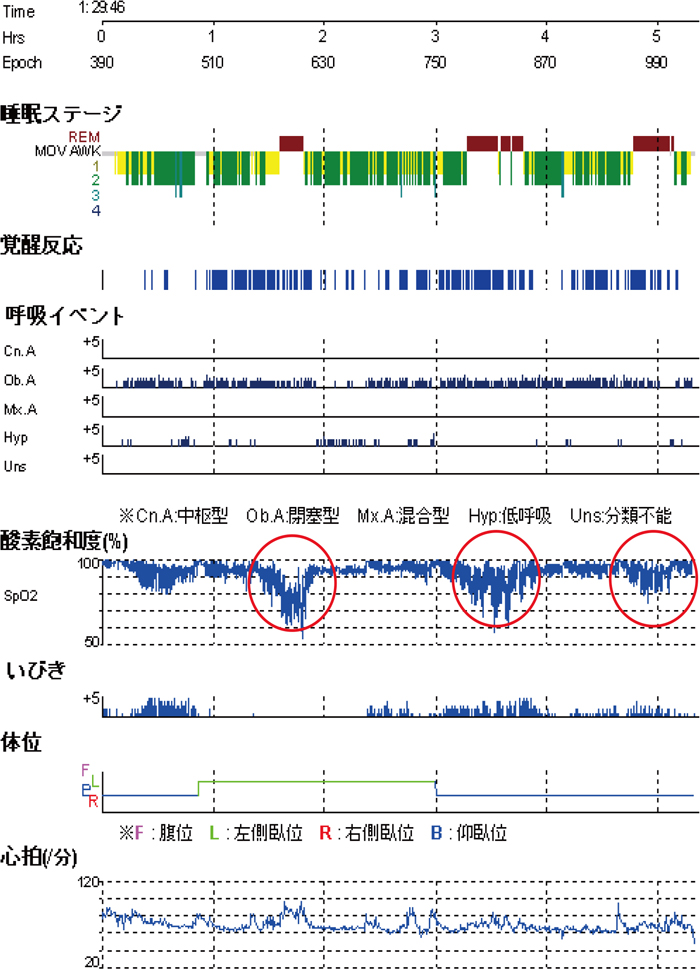
睡眠ポリグラフ検査の1例
重症睡眠時無呼吸症候群.特にREM睡眠時に著明な低酸素血症を伴う.
このPSGは慢性呼吸不全患者の睡眠呼吸異常を検出するためにも有用である.特に,経皮CO2モニタリングとPSGを併用すると,睡眠時の低換気を正確に把握することが可能となる(図8).前述のeNHはPSGを併用することでREM睡眠時に生じていることが明らかになった(REM睡眠関連低換気)3).
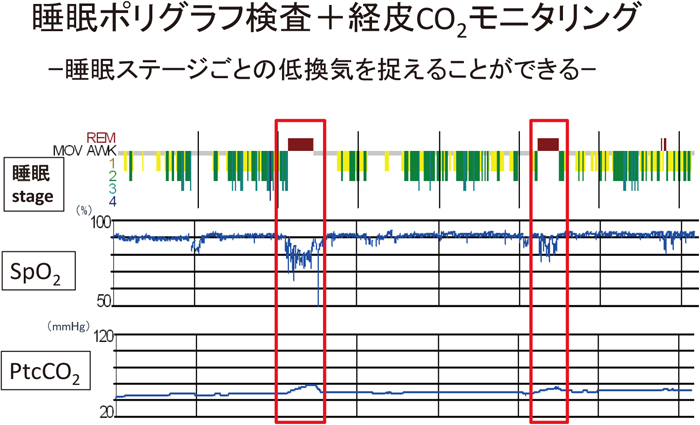
睡眠ポリグラフ検査+経皮CO2モニタリング
REM睡眠時の低換気で間欠的な低酸素血症・高二酸化炭素血症を来していることが明らかである.
健常人でも睡眠中には換気が低下することが知られている5).これは睡眠中に代謝が低下することや上気道抵抗の上昇,化学受容体の感受性が低下することなどが理由に挙げられている.特にREM睡眠時には肋間筋や呼吸補助筋などの骨格筋の換気への寄与が減少し,横隔膜の関与が高まることが知られている6).さらに低酸素血症や高二酸化炭素血症に対する化学感受性も低下すると言われている7)(図9).COPDなど閉塞性障害の患者に加え,結核後遺症・後側弯症など拘束性障害の患者,また,横隔神経麻痺や神経筋疾患などの患者でも,REM睡眠時に換気が大きく低下することが知られている8).そして日中の低換気,すなわち高二酸化炭素血症が明らかでない段階でもすでにこの睡眠時低換気を認める.たとえば,重症COPD患者においては,日中の著明な高二酸化炭素血症(PaCO2>55 Torr)を認めなくても,約半数にこのREM睡眠時低換気を認める3).すなわち,呼吸不全は夜にはじまるのである2)(図10).これを知るためには夜間のモニタリングが不可欠である.
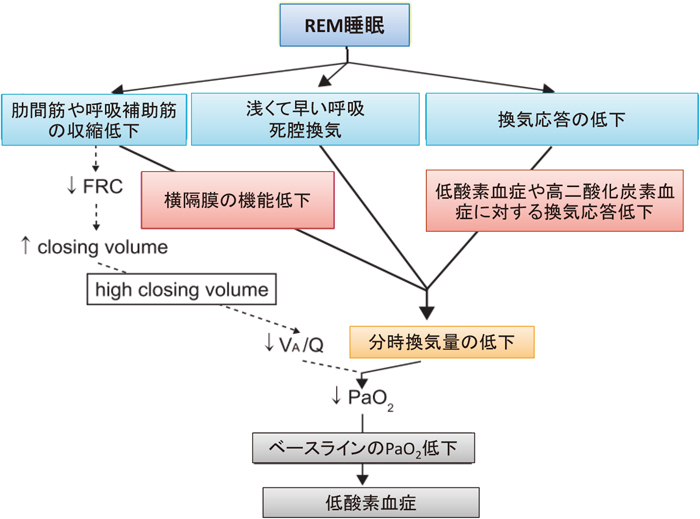
REM睡眠時に低換気となるメカニズム
Marrone O et al., Int J COPD 2006,1: 363. から引用・改変.
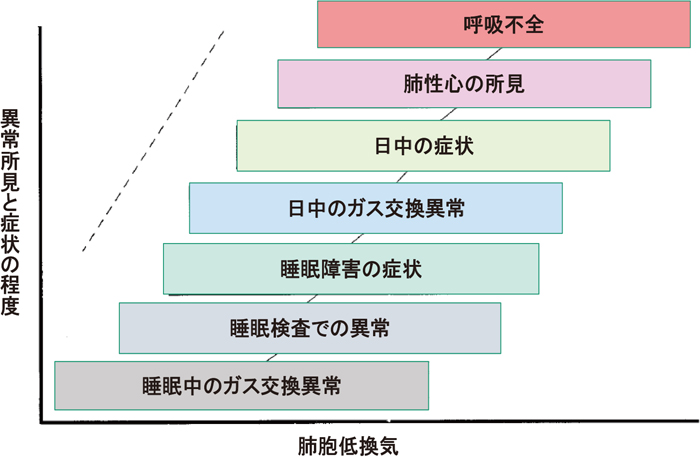
睡眠時低換気の症状は夜から昼へ
CHEST 1999, 116: 521–534から引用・改変
夜間の経皮CO2モニタリングでeNHを認める,すなわちREM睡眠関連低換気を伴う進行期COPD患者は,そうでない患者に比べて過去1年間の増悪回数や推定肺動脈収縮期圧が有意に高く,低アルブミン血症を伴うことが明らかになった3)(図11).これらの患者に,NPPVを導入してこのeNHを解消する,すなわちREM睡眠時の低換気を改善することで増悪回数は有意に低下することを我々は明らかにした3).
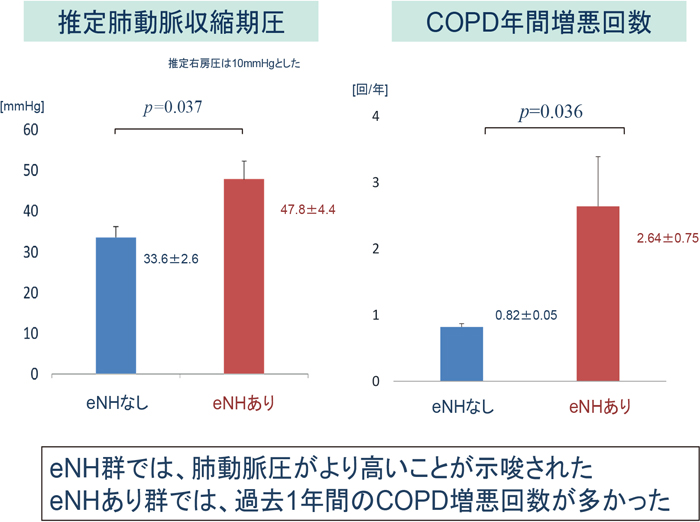
eNHと肺高血圧,COPD増悪回数との関係
Kitajima T et al., Int J COPD 2018, 13: 843.から引用
一方,eNHを伴う慢性呼吸不全患者に安易に夜間酸素投与を行うと,一見低酸素血症は改善したようにみえるが,PtcCO2はかえって増加し,頻脈などを伴うことが明らかになってきている.FletcherらはREM睡眠中心に低酸素血症を伴う患者は予後不良で,酸素投与によって予後が改善しないことも報告している9).よってeNHを伴う呼吸不全患者に対して夜間の酸素投与は慎重に行う必要がある.
慢性呼吸不全患者は,HOTやNPPVを導入することによって予後は明らかに改善し,また在宅で生活することが可能となった.しかしながら,その導入に際して上述の各種モニタリングを行い,正確な病態把握を行っている施設はまだまだ少なく,日中のある一時点の動脈血ガス分析やSpO2の値のみでこれらの在宅呼吸ケアを導入しているところが多い.しかしこれでは労作時の低酸素血症や睡眠中の睡眠時無呼吸症候群や睡眠時低換気の合併を把握することは困難である.各種モニタリングを積極的に行うことで患者の病態に応じた適切な酸素流量の設定やNPPVの機器設定が可能となる.これはひいては患者のQOLや予後改善につながると思われる.特に経皮CO2モニタリングを積極的に導入するために診療報酬上の後押しなどが必要であると思われる.
本論文発表内容に関して特に申告すべきものはない.