2025 年 37 巻 1 号 p. 57-66
2025 年 37 巻 1 号 p. 57-66
陸上植物の有性生殖において、配偶子(生殖細胞)として雌側では卵、雄側では精子(精細胞)をつくる過程が必須であり、その形成様式は進化の過程でダイナミックに変遷してきた。コケ植物や小葉植物、シダ植物では配偶体世代の器官として、多細胞でできた造卵器や造精器といった配偶子器(配偶子嚢)が発生し、卵や精子がつくられる。ほんの約十年前まで、配偶子器の発生に関しては、解剖学的な知見に留まっており、発生を制御する分子機構は未解明であった。近年、モデルコケ植物のタイ類ゼニゴケにおいて、研究基盤が整い、分子遺伝学的な理解が進んできたことで、配偶子器の発生の分子機構に関しても目覚ましく研究が進展している。著者らは、配偶子器発生制御因子としてBZR/BES転写因子MpBZR3を見出し、研究を進めてきた。本稿ではゼニゴケを中心に、コケ植物の配偶子器発生研究を取り巻く最新状況をレビューする。
In the sexual reproduction of land plants, the production of female gamete egg and male gamete sperm is an essential process. These processes have drastically changed through plant evolution. In bryophytes, lycophytes, and monilophytes, multicellular gametangia develop as reproductive organs during the haploid generation. Egg and sperm are produced in the female and male gametangia, archegonia and antheridia, respectively. Until a decade ago, knowledge about gametangium development was largely limited to anatomical observations, and the molecular mechanisms underlying their development remained poorly understood. Recently, however, the establishment of research tools for the model bryophyte Marchantia polymorpha has enabled significant progress in uncovering the molecular genetics of gametangium development. In our research, we have focused on gametangium development and identified a BZR/BES transcription factor MpBZR3 as a key regulator of this process. This article will provide an overview of recent research advancements in understanding gametangium development in bryophytes.
陸上植物は、大きな雌性配偶子である卵と小さな雄性配偶子の精子(精細胞)という異型配偶子による有性生殖を行なう共通した特徴を持つ。陸上植物とその姉妹群である車軸藻植物を含むストレプト植物において、その共通祖先は同型配偶子による生殖をしていたと推測されている(Mori 2015)。一方で、陸上植物やシャジクモ藻類などの一群は、異型配偶子による生殖を行なう。つまり、陸上植物が誕生するまでの過程で異型配偶子は獲得されたとされている。しかしながら、陸上植物とシャジクモ藻類の卵細胞と精子を生み出すシステムが同一起源かどうかも未だ議論の中にあるなど、植物進化の過程で同型配偶子から異型配偶子への転換という大きなイノベーションがいつ、どのようにして起きたのかは植物進化の大きな疑問である。さらに、配偶子形成の様式は、陸上植物の進化過程で大きく変遷してきた(Bowman 2022)。約5億年前に植物が陸上化した後、最初に登場したと考えられているコケ植物の系統では、主な生活世代が単相(n)の配偶体であり、造卵器(Archegonium)や造精器(Antheridium)と呼ばれる器官 [これらをまとめて配偶子器(gametangium)と呼ぶ] が発生する。造卵器と造精器の中で配偶子である卵と精子がそれぞれ分化する(Bowman et al 2022)。同様の様式は、小葉植物やシダ植物でもみられるが、配偶体世代が優位な生活環から、胞子体世代を生活世代の主とした生活環への転換に伴い、造精器や造卵器の細胞数の退縮が進む(Hackenberg and Twell 2019, 長谷部 2020)。さらに被子植物において、雌性配偶体である胚嚢、雄性配偶体である花粉は数細胞で構成されており、多細胞性の造卵器や造精器は消失する(Berger and Twell 2011)。これまで配偶子形成の研究は、モデル被子植物を中心に進められてきたが、このような系統間の多様性や進化過程を理解するには多様な植物種での知見が鍵となる。コケ植物タイ類ゼニゴケMarchantia polymorphaがモデル植物として確立されたことにより(Ishizaki et al. 2016, Bowman et al. 2017, Bowman et al 2022)、ここ数年でゼニゴケの配偶子形成過程、造卵器や造精器の発生過程を制御する分子メカニズムの理解が急速に進んできている(Hisanaga et al. 2019b, 山岡ら 2019, Kohchi et al. 2021, Bowman et al. 2022)。本稿では、我々の研究成果を含めながら(Furuya et al. 2024b)、ゼニゴケの配偶子器の発生における研究状況の現状をまとめ、今後の研究の展望について議論する。
配偶子器発生の解説に先立ち、前提となるゼニゴケの生活環および性決定・性分化に関して簡単に触れる。ゼニゴケは、他の陸上植物同様、世代交代型の生活環をもつ(図1, 嶋村 2012, Shimamura 2016, Kohchi et al. 2021)。複相世代の胞子体内で減数分裂を経て生じた単相の胞子は、発芽後に多細胞性の配偶体組織である葉状体を形成し、主な生活を送る。葉状体はその頂端にあるノッチと呼ばれるくぼみの中央に位置する頂端幹細胞を含む幹細胞領域(Stem cell zone)と、そこを中心とした分裂分化細胞領域(Dividing and differentiating cell zone)を起点に、3次元的な組織分化を伴いながら、成長していく。栄養成長期から有性生殖期への相転換に伴い、生殖枝の発生が始まる(図1)。ゼニゴケは雌雄異株であり、雌株はU染色体、雄株はV染色体と呼ばれる性染色体をそれぞれ持つ(Yamato et al. 2007, Bowman et al. 2017, Iwasaki et al. 2021)。栄養成長期の葉状体では、基本的に雌雄の形態的な差異は見られないが、生殖成長期に移行すると、雌株では雌器托(Arhcegoniophore)、雄株では雄器托(Antheridiophore)と呼ばれる形状の異なる生殖枝が形成される(Shimamura 2016, Kohchi et al. 2021)。雌器托は、その頂端に9から10本の指状突起をもつ雌器床を形成し、その下側の付け根に造卵器が配置される。一方で、雄器托では、造精器を内包する円盤状の雄器床が形成される。このような生殖器官の性的二形は、常染色体上にあるMYB転写因子をコードするFEMALE GAMETOPHYTE MYB (MpFGMYB)とその遺伝子座のアンチセンスにあるlong non-coding RNA SUPPRESSOROF FEMINIZATION(SUF)が性分化スイッチとして働くことで制御されている(Hisanaga et al. 2019a, Kajiwara et el. 2024)。雄株ではSUFが発現することにより、MpFGMYBの発現は抑制されている。この抑制にはSUFがアンチセンス側で転写されること自体が重要であり、雄株でSUFの転写を止めるとMpFGMYBの発現が生じ、雄株にも関わらず雌器托と卵細胞分化が不完全な造卵器を形成する。一方で、雌株側では、SUFの発現は顕著に抑えられており、MpFGMYBの転写が活性化されている。雌株のMpfgmyb機能欠損変異体は、雄器托構造が発生し、精子構造に異常が見られるものの造精器ができる。このようにMpFGMYBは雌の性分化制御において重要な役割を有しており、雄株でMpFGMYBとSUFがともに機能を失っても造精器発生は通常に進行することから、ゼニゴケの配偶体発生は雄がデフォルトであると考えられる。先述のように、この性分化スイッチの人為的な転換によって誘導される性染色体と一致しない性表現を示す配偶子器では、配偶子分化が正常には生じない(Hisanaga et al. 2019a)。このことから、卵および精子の適切な分化には、それぞれU染色体、V染色体上に座乗する遺伝子が必須であると考えられている。偶然にもU染色体とV染色体の両方を持つゼニゴケは雌型の性分化が生じることから、雌のU染色体上に雌性化因子(フェミナイザー)の存在が示唆されていた(Haupt 1932, Iwasaki et al. 2021)。性染色体のゲノム解析に基づいた研究から、BPC転写因子をコードするU染色体上のBASIC PENTACYSTEINE ON THE U CHROMOSOME(BPCU)がフェミナイザーとしてはたらく性決定因子であることが判明した(Iwasaki et al. 2021)。雌株においてBPCUはSUFの発現を抑制しており、MpFGMYBの転写が活性化することで雌の性表現が現れる。このように、生殖枝および配偶子器の形態、発生的な雌雄差は、性染色体を起点とする分子メカニズムを背景に持つが、生殖成長期への相転換に伴う初期発生には共通する部分が多い。雌雄に関わらず相転換には、光環境、日長感受が重要な要因となる(Kubota et al. 2014, Inoue et al. 2019)。実験室環境下では、長日条件の白色光に遠赤色光を補光することで相転換を誘導することが可能である(Chiyoda et al. 2008)。このような生殖誘導環境下において、葉状体のノッチ付近の表皮細胞が雌では造卵器始原細胞(archegonium initial cell)、雄では造精器始原細胞(antheridium initial cell)へと分化する。これら配偶子器始原細胞(gametangium initial cell)では、共通してsubfamily VIIIa bHLH転写因子MpBONOBO(MpBNB)を発現する(Yamaoka et al. 2018)。Mpbnb機能欠損変異体では、生殖誘導環境下でも生殖枝および配偶子器の発生が観察されず、一方で人工的にMpBNBの活性化を誘導すると非誘導環境下でも生殖枝、配偶子器が発生する(Yamaoka et al. 2018)。したがって、MpBNBは有性生殖発生のマスター制御因子としてはたらいており、その発現制御が相転換の起点となる。配偶子器始原細胞の分化において、MpBNBは、subfamily XI bHLHs LOTUS JAPONICUS ROOTHAIRLESS LIKE/DEFECTIVE REGION OF POLLEN(MpLRL)とヘテロ二量体を形成し、MpBNBの安定化および機能にMpLRLは必須である(Saito et al. 2023)。このように、生殖成長の初期過程では、生殖枝の形成に先立ち配偶子器発生が開始する(Yamaoka et al. 2018, Yamaoka et al. 2021, Saito et al. 2023, Cui et al. 2023)。そして、発生中の配偶子器を巻き込む形で、頂端ノッチ周辺が形態変化することで、生殖枝原器が形成されていく(Yamaoka et al 2021, Cui et al. 2023)。興味深いことに、この生殖枝形成の初期においてすでに雌雄の差が見られる(Cui et al. 2023)。雄株では多数の造精器始原細胞および初期造精器が散発的にみられ、そのまま雄器托原器の表面に散らばって分布していく。一方で雌株では、少数の造卵器始原細胞および初期造卵器のみが観察され、雌器托原器の周縁に局在していく。雌株で見られるこのような特徴は、Mpfgmyb機能欠損によってかなり初期の段階から雄株同様になることから、MpFGMYBが雌性分化の、マスター制御因子であることが支持される。このようにゼニゴケでは、栄養成長から生殖成長への相転換の過程で、配偶子器とそれに伴う生殖枝の発生、さらには性分化という複雑で多層的な発生イベントが適切に制御されている。

図1 ゼニゴケの生活環の概略。コケ植物タイ類ゼニゴケは、単相の配偶体世代において葉状体と呼ばれる形態で栄養成長する。主に光環境依存的に、栄養成長期から生殖成長期へ相転換する。この際にbHLH転写因子MpBNBが鍵制御因子として重要な役割を持つ。生殖成長期には雌株では、造卵器を付随した雌器托、雄株では造精器を内包する雄器托が形成される。雌雄の生殖器官の形態、発生は性分化を制御する性分化モジュールにより決定づけられる。造精器で分化した運動能をもつ精子が水中を遊泳し、造卵器にある卵に到達し、受精する。受精卵は胞子体となり、減数分裂を経て胞子が形成される。図はFuruyaら(2024b)を引用、改変した。
造精器の発生は、造精器始原細胞の分化から始まる((図2, Yamaoka et al 2021, Cui et al. 2023)。雄器托形成前には頂端ノッチ周辺の表皮細胞が造精器始原細胞へと分化し、雄器托の発生の進行に伴って、雄器床周縁の翼部の表皮細胞からも継続的に分化する(Durand 1908, 荒木 2012, Shimamura 2016, Yamaoka et al. 2018, Cui et al. 2023)。造精器始原細胞は最初に頂端側の造精器本体母細胞(antheridium proper mother cell/outer antheridial cell)と基部側の柄母細胞(stalk mother cell/basal antheridial cell)に分裂し、造精器本体母細胞は複数回の縦横分裂により4つの造精器細胞(antheridial cell)が複数段積み重なった構造を形成する(荒木 2012, Shimamura 2016)。その後、並層分裂により内側の精原始祖細胞(spermatogenous cell progenitor)、外側の外被(ジャケット)始祖細胞(jacket cell progenitor)が生み出される。外側に位置する外被(ジャケット)始祖細胞は、一層の外被(ジャケット)細胞(wall cell/jacket cell)の系譜として維持され、分裂しながらジャケットを形成する。一方の内側の精原始祖細胞は、精原細胞(spermatogenous cell)となり、同調的に細胞分裂を繰り返し、最後から2番目の分裂を終えると精母細胞(spermatid mother cell)となる。1つの精母細胞は一度だけ斜め分裂を行ない2つの精細胞(spermatid)が生み出され、最終的に精子(spermatozoid)が形成される。造精器始原細胞の分化には、先述のようにMpBNB-MpLRLヘテロ二量体がマスター制御因子として働いている(Yamaoka et al. 2018, Saito et al. 2023)。興味深いことに、MpBNBの発現は、初期の造精器において、精原細胞の系譜となる並層分裂後の精原始祖細胞でみられるものの、後期の精原細胞や外被(ジャケット)細胞では発現が見られない(Yamaoka et al. 2018)。造精器発生初期に発現する遺伝子として、plant homeodomain (PHD) fingerタンパク質コードするGERMLINE IDENTITY DETERMINANT/MALE STERILITY1(MpGLID/MpMS1)が見出されてきた(Higo et al. 2016, Ren et al. 2024)。MpGLIDは造精器始原細胞というよりはむしろ、初期の造精器原器で発現している(Higo et al. 2016, Ren et al. 2024)。Mpglid機能欠損変異体では、雄器托の形成および造精器の発生開始には影響がみられないが、並層分裂後の内側の細胞群が生殖細胞系譜である精原細胞として分化しない(Ren et al. 2024)。MpGLIDの異所発現は、葉状体の形態へ影響するとともに、葉状体内側の柔細胞を精原細胞様の細胞群に分化させた。同様の表現型はMpBNB過剰発現において見られるが、Mpglid変異体背景では生じなくなる。加えて、MpGRIDの発現はMpBNBにより直接的に制御されることが示されている。これらより、MpGLIDはMpBNBの下流因子として生殖細胞系譜の分化に働くと考えられる(Ren et al. 2024)。造精器発生の後期では精原細胞から精母細胞、さらには精細胞への分化が進行する。MYB転写因子をコードするDUO POLLEN1(MpDUO1)は、精母細胞と精細胞で特異的に発現する(Higo et al 2018)。Mpduo1機能欠損変異体では、精母細胞における最後の斜め分裂は見られるものの、精細胞の分化に異常が生じ、不稔となる。実際に、Mpduo1変異体では、造精器特異的に発現するチューブリン遺伝子MpTUA5やMpTUB4、精子形成に寄与することが予想されるダイニン構成要素やプロタミン様タンパク質をコードするDYNEIN LIGHT CHAIN 7(MpLC7)やPROTAMINE-LIKE(MpPRM)の発現レベルが低下していた。加えて、シロイヌナズナDUO1の下流で働くDUO1-ACTIVATED ZINC FINGER1(DAZ1)とDAZ2のホモログ遺伝子MpDAZ1の発現も低下しており、ゼニゴケにおいてもMpDUO1-MpDAZ1モジュールが保存されていることも示されている。このように、MpDUO1は精細胞分化過程の進行に必須の役割を持つ(Higo et al 2018)。RWP-RK転写因子をコードするRWP-RK domain(MpRKD)とMINUS DOMINANCE (MpMID/MpRWP2)も発生中の造精器で発現している(Higo et al 2016, Koi et al. 2016, Rovekamp et al. 2016)。MpRKDの発現はMpDUO1に先立って見られるが、Mprkd変異体においてもMpDUO1は発現し、一部の細胞からは稔性のある精子がつくられる(Koi et al. 2016, Higo et al 2018)。しかしながら、Mprkd変異体では、精原細胞分裂や精子形成が同調しない特徴がみられ、部分的に精原細胞分化に異常が観察された(Koi et al. 2016)。MpMID/MpRWP2はMpDUO1と同時期に発現しているが、Mpmid変異体はこれまでのところ顕著な表現型は見出されていない(Higo et al 2018)。ここまで、造精器の発生、精子細胞系譜の確立を中心にまとめてきた。詳細は割愛するが、その後の精子分化過程は細胞内小器官の大規模な再構築がおこる興味深いプロセスであり(Shimamura 2016, Minamino et al. 2022, Norizuki et al. 2022)、さらに精子放出や精子運動に関しても研究が進みつつある(Cao et al. 2024, Yamamoto et al. 2024)。
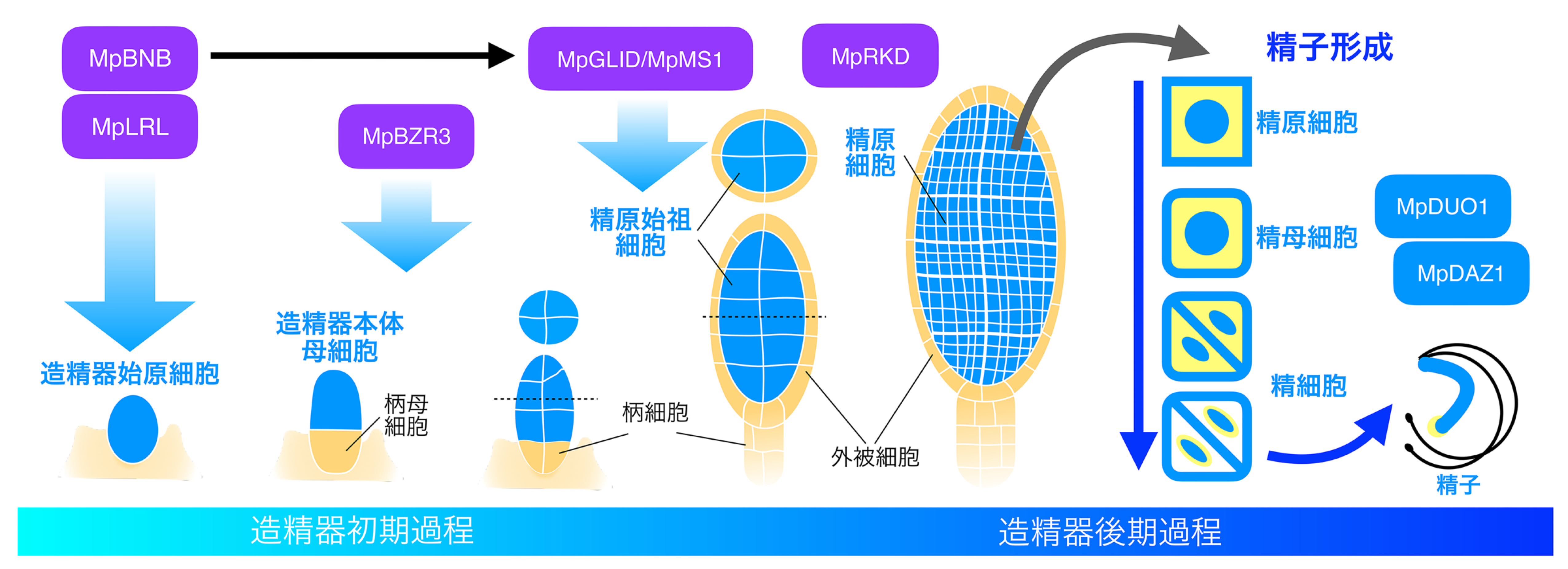
図2 ゼニゴケ造精器発生の模式図。発生初期において、造精器始原細胞は縦横方向の分裂を繰り返し、その後、並層分裂を経て、外側の外被(ジャケット)始祖細胞と内側の精原始祖細胞が生じる。精原始祖細胞は、精原細胞となり、分裂を繰り返したのち、最終的に精子へと分化する。それぞれの過程で機能する制御因子を示す。紫色の因子は造精器、造卵器発生で共通して機能するもの、青色の因子は造精器発生に関わるもの。図はFuruyaら(2024b)を引用、改変した。
造卵器は、雌器床における指状構造の下部側の付け根付近で継続的に発生する(図3, Yamaoka et al 2021, Cui et al. 2023)。表皮細胞に由来する造卵器始原細胞は、造精器始原細胞と同様に、まず頂端側と基部側に分ける細胞分裂が起こる(Durand 1908, Shimamura 2016, Sokoloff and Remizowa 2021)。基部側の細胞は造卵器基部母細胞/柄母細胞(basal archegonial initial cell)となり、頂端側に位置する細胞は造卵器本体母細胞(outer archegonial initial cell)となる。造卵器本体母細胞では、連続的に縦方向に3回の非対称分裂が起こり、3つの一次周縁細胞(primary peripheral cell)に囲まれつつ、遠位端の細胞表面が外部に露出した一次軸細胞(primary axial cell)が生じる。この細胞が内外を分ける分裂をすることで、造卵器原器の頂端に位置する外側の一次栓細胞(primary cover cell)と内側の一次卵母細胞(primary central cell)となる。卵原細胞は造卵器の成長に伴い先端基部軸に垂直方向の分裂し、卵前駆細胞である二次卵母細胞(secondary central cell)と一次頸溝細胞(primary canal cell)となる。基部側の二次卵母細胞は非対称分裂を経て、卵(egg)と腹溝細胞(ventral canal cell)に分化し、頂端側の一次頸溝細胞は、4個以上の頸溝細胞(neck canal cell)に分裂する。結果として、基部側から卵、腹溝細胞、頸溝細胞群が1列に配置され、分化に伴い細胞壁が喪失する。卵細胞は成熟の過程で著しく体積が増加し、細胞質に富み、小さな液胞と脂肪滴が周縁部に蓄積する。最終的に、頸溝細胞と先端の栓細胞は崩壊し、腹溝細胞は退縮することで、造卵器頸部の中央に精子が遊泳できる通路がつくられる。このように造卵器の発生は最初の頂端基部軸に沿った水平方向の分裂以降、造精器とは大きく異なった細胞分裂・分化パターンで形成される。造卵器始原細胞の分化においてもMpBNB-MpLRL複合体が制御因子としてはたらく(Yamaoka et al. 2018, Saito et al. 2023)。初期の造卵器発生過程において、MpBNBの発現は非対称分裂が生じるたびに、卵を生じる側の系譜で維持され、最終的に卵細胞に限定される(Yamaoka et al. 2018, Bao et al. 2024)。シロイヌナズナ胚嚢発生において、ヒスチジンキナーゼCYTOKININ-INDEPENDENT 1 (CKI1) は、下流の二成分制御系を構成するhistidine-containing phosphotransfer proteins (HPTs)とtype-B response regulators (RRBs) を介して、中央細胞の分化に重要なはたらきを持つ(Yuan et al. 2016)。ゼニゴケのCKI1オーソログMpCKI1の機能欠損変異体Mpcki1の造卵器初期発生の詳細な観察では、造卵器始原細胞の最初の分裂は起こるものの、その後の造卵器本体母細胞における非対称分裂の縦方向への分裂が生じず、代わりに最初の分裂面と並行した分裂面が生じることが示されている(Bao et al. 2024)。つまり、Mpcki変異体では一次卵母細胞が生じず、そこに由来する卵、腹溝細胞、頸溝細胞が形成されない。加えて、野生株ではこれら細胞分裂のたびに、卵を生じる側の系譜のみに収束していくMpBNBレポーターのシグナルが、Mpcki変異体では、造卵器始原細胞から水平方向に2回に分裂が生じた後、3つの細胞全てで喪失する。これら造卵器の発生過程においてMpCKI1が機能するには、MpHPTとMpRRBで構成される二成分制御系が必須であり、それらの変異体でも同様の表現型が見られる。したがって、MpCKI1-MpHPT-MpRRB経路は、造卵器発生初期過程において生殖細胞系譜を規定する非対称分裂に必須であり、また生殖細胞系譜アイデンティティーを確立するためにMpBNBの蓄積を限定するはたらきを持つと考えられる(Bao et al. 2024)。造精器発生において生殖細胞分化に関わるMpGLIDは、造卵器発生においても発現し、卵の成熟とともに減少する(Ren et al. 2024)。雌株のMpglid機能欠損変異体では、一次卵母細胞は適切に形成されるものの、分裂後に基部側細胞の二次卵母細胞が分化せず、それに由来する卵や腹溝細胞の形態的特徴が生じない。またもう一方の頂端側の細胞も分裂し、頸溝細胞群のような細胞列は構成されるものの、その後も継続的に無秩序な細胞分裂が起こり、形態の乱れた造卵器となる。このように、MpGLIDは造卵器発生においても生殖細胞形成のために、二次卵母細胞の分化を制御していると思われる。分化し成熟した卵は受精が起こるまで細胞分裂を停止する必要がある。造精器においても発現が見られるMpRKDは、二次卵母細胞が分裂し形成された卵において顕著な発現が見られ、成熟した卵でも維持されるが、受精の後では検出されない(Koi et al. 2016)。Mprkd変異体およびamiRNAによるMprkdノックダウン変異体では、卵前駆細胞、腹溝細胞、頸溝細胞が形成されるが、成熟した卵への分化および細胞分裂の休止が正常に起こらず、代わりに、分裂を伴いながら、大きな液胞と細胞壁をもつ細胞群が生じる(Koi et al. 2016, Rovekamp et al. 2016)。このようにMpRKDは卵の分化、成熟過程で重要な役割を持つとともに、分裂を抑制し、静止状態を維持することに寄与することを示している。また興味深いことに、Mprkd変異体において腹溝細胞や頸溝細胞、栓細胞の崩壊は適切に生じるにもかかわらず、精子の誘因が見られなくなる(Koi et al. 2016)。卵成熟が起こらないMprkd変異体を用いたトランスクリプトーム解析から、成熟した卵細胞で特異的に発現するThree-Amino-Acid-Loop-Extension (TALE) ホメオドメイン転写因子をコードするKNOTTED1-LIKE HOMEOBOX1(MpKNOX1)が見出された(Hisanaga et al. 2021)。MpKNOX1は、他のTALEホメオドメイン転写因子MpBELL3、MpBELL4、およびMpBELL2とともに受精卵の活性化、胚発生の制御をしていることが示されている(Hisanaga et al. 2021, Dierschke et al. 2021)。このように、造卵器発生は特に初期段階において、MpBNBやMpGLIDのような造精器と共通した制御因子が重要な機能を持っており(Yamaoka et al. 2018, Ren et al. 2024)、実際に比較的共通した遺伝子発現プロファイルを示す(Flores-Sandoval et al. 2018)。一方で、発生的には初期から大きく異なった分裂パターンを示す(Durand 1908, Shimamura 2016)。雌雄の配偶子器発生の差を生み出す背景には、先述した性決定・性分化の分子モジュールが大きな貢献をしているだろう(Hisanaga et al. 2019, Iwasaki et al. 2021, Cui et al. 2023)。雌分化のマスターレギュレーターであるMpFGMYBの機能欠損変異体では、造精器への転換が生じるため、MpFGMYBの造卵器発生へ寄与も不明であり、今後の解明が待たれる(Hisanaga et al. 2019)。

図3 ゼニゴケ造卵器発生の模式図。発生初期において、造卵器始原細胞は、非対称分裂を繰り返し、内部に位置する一次卵母細胞が形成される。一次卵母細胞に由来する細胞は、最終的に基部側から、卵、腹溝細胞、頸溝細胞群へと分化する。造卵器の成熟に伴い、腹溝細胞、頸溝細胞群は崩壊し、精子が遊泳可能な頸部が形成される。それぞれの過程で機能する制御因子を示す。紫色の因子は造精器、造卵器発生で共通して機能するもの、赤色の因子は造卵器発生に関わるもの。図はFuruyaら(2024b)を引用、改変した。
ここまでに記してきたように、ここ数年の間に、急速にゼニゴケの配偶子器発生に関わる制御因子が見つけ出されてきている。私たちも同時期に新たな制御因子としてBRASSINAZOLERESISTANT 1/BRI1-EMS-SUPPRESSOR 1(BZR/BES)転写因子MpBZR3に着目し、その解析を進めてきた(Furuya et al. 2024b)。ここでは、MpBZR3を中心に、他の制御因子との関連についても議論したい。MpBZR3は、ゼニゴケの組織別トランスクリプトームをもとに、雌雄の有性生殖器官で共通して顕著に発現する遺伝子として見出されてきた(Flores-Sandoval et al. 2018, Furuya et al. 2024b)。MpBZR3が属するBZR/BES転写因子ファミリーは、被子植物において、植物ホルモンのブラシノステロイドのシグナル伝達経路におけるマスター転写因子としてよく知られており、植物の発生において重要な役割を持つ(Nolan et al. 2020, Wang et al. 2002, Yin et al. 2002, Furuya et al. 2024a)。近年のゲノム解析の進展に伴い、幅広い植物種を用いた系統解析が可能となった結果、BZR/BES転写因子ファミリーは大きく3つのサブグループに分類できることがわかってきた(Jiao et al. 2020, Mecchia et al. 2021, Furuya et al. 2024b)。私たちはそれぞれのサブグループをtype A、type B、type Cと名付けた(Furuya et al. 2024b, 古谷 2024)。よく研究されてきているシロイヌナズナが持つ6つのBZR/BES転写因子はすべてtype-Aサブグループに属していた。ゼニゴケは3つBZR/BES転写因子を持ち、それらはそれぞれのサブグループに1つづつ含まれていた。Type-Aサブグループに属するMpBZR2/MpBES1は、シロイヌナズナのBES1との類似性が示されており、ゼニゴケでは葉状体の細胞分裂と分化のバランスを制御している(Mecchia et al. 2021)。私たちが着目したMpBZR3は、これまでにほとんど研究されていないtype-Bサブグループに属していた。MpBZR3を過剰発現するゼニゴケを作出したところ、雄株では造精器、雌株では造卵器に類似した構造が異所的に発生した(Furuya et al. 2024b)。このような表現型は他の、type-Aサブグループに属するMpBZR2/MpBES1、type-CサブグループのMpBZR1の過剰発現体では観察されず、type-BサブグループのMpBZR3に特有の機能であることが示唆された。雄株において、MpBZR3過剰発現により誘導される造精器様構造体では、核の凝縮が起こらず完全な精子形態形成は見られないものの、部分的な鞭毛は観察され、鞭毛関連の遺伝子群の発現も観察された。一方で、雌株において見られた構造体は、造卵器で発現するMpBELL5等の遺伝子群の発現は検出されたが、形態的には造精器と比較すると不完全であった。MpBZR3-Citrine knock-inレポーター株を用いて、MpBZR3の配偶子器発生における発現パターンを観察したところ、造精器発生では、造精器始原細胞においてすでにシグナルが見られ、その後、精原細胞、外被(ジャケット)細胞いずれの系譜でも発現が維持されたが、発生後期にはシグナルが喪失した(Furuya et al. 2024b)。造卵器側でも、造卵器始原細胞からシグナルは見られ、その後も造卵器のいずれの細胞系譜でも検出されるが、卵細胞では分化後も他の細胞群と比較して強いシグナルが維持された。配偶子器始原細胞の確立に重要なMpBNBの機能欠損変異体背景ではMpBZR3の発現は見られなくなることから、MpBZR3はMpBNBによる配偶子器始原細胞の確立後に発現すると考えられる。またMpBZR3過剰発現による造精器、造卵器様構造体はMpbnb変異体背景でも誘導されたが、その形態は野生型背景で誘導されたものよりも不完全であった。このことはMpBZR3はMpBNB非依存的に配偶子器様構造体を誘導することができることに加え、MpBNBが配偶子器始原細胞の分化だけでなく、配偶子器の発生過程にも寄与することを示唆している。このMpBNBのはたらきにはMpGLID/MpMS1の発現制御も含まれるだろう(Ren et al. 2024)。さらに、Mpbzr3機能欠損変異体は、雄雌ともに生殖枝の発生は正常であった。このことより、MpBZR3は、MpBNBによって制御される配偶子器始原細胞の確立とそれに伴う生殖枝発生を引き起こす相転換自体には寄与しないと考えられる(Furuya et al. 2024b)。Mpbzr3機能欠損変異体における造精器発生を観察すると、Higo et al 2016で定義されている雄器托の発生ステージによって表現型が異なることがわかってきた(Furuya et al. 2024b)。雄器托発生初期のstage 1や2において野生型ではある程度発生が進んでいる造精器が観察されるが、Mpbzr3変異体では、数細胞からなる造精器原器様の構造は見られるものの、その分裂パターンは異常であり、発生も停止している様子が観察された。実際に、遺伝子発現レベルでも、Mpbzr3変異体ではMpBNBの発現は野生型と同程度であったが、MpGLID/MpMS1の発現は低下していた。このことはMpBZR3が造精器始原細胞の確立以降の初期発生プロセスにおいて重要な役割を持つことを示唆している。一方で、雄器托発生後期のstage 3や4ではMpbzr3変異体いおいても正常な造精器発生が進行し、稔性をもつ精子が分化していた。このことは雄器托の発生が進むに伴い、MpBZR3非依存的な造精器発生が起こることを示している。このような雄器托発生のステージによる違いがどのように生じているのかは不明であり、MpBZR3による造精器発生制御における分子機構の解明が待たれる。一方、造卵器発生において、Mpbzr3変異体では、造卵器発生の初期過程では卵の分化が観察され、顕著な異常は見られなかったが、その後、造卵器の形態異常と卵の崩壊が観察され、稔性も失われていた(Furuya et al. 2024b)。したがって、Mpbzr3変異体では卵が一度分化した後に維持できなくなっていると思われる。このようなMpbzr3変異体の表現型は、卵の分化が適切に起こらずに細胞分裂が進行するため卵が維持できないMprkd変異体とも異なっており(Koi et al. 2016, Rovekamp et al. 2016)、MpBZR3がMpRKDよりも遅いタイミングで卵の分解を防ぐことで維持に寄与していると考えられる。実際に、雌器托のトランスクリプトーム解析において、Mpbzr3変異体と野生株の間でMpRKDの発現レベルに顕著な影響は見られていない(Furuya et al. 2024b)。同様の傾向は、より初期の発生に関わるMpBNB、MpCKI1、MpGLIDでも同様である(Furuya et al. 2024b, 一部未発表)。MpBZR3の発現は、Mpbzr3変異体において影響が見られる発生段階よりも広域で観察されており、MpBZR3がどのように卵の維持を制御しているのかは未解明である。このようにMpBZR3は造精器発生、造卵器発生のいずれにおいても重要なはたらきを持つが、その役割はそれぞれで異なっていることが考えられる。今後、それぞれの配偶子器の発生における相互作用因子の特定や、直接的な下流標的遺伝子の解析が進むことで、MpBZR3の機能メカニズムの解明が期待される。
ここまで、コケ植物タイ類ゼニゴケにおける配偶子器発生の最新の知見をまとめてきたが、コケ植物に限って見ても、造精器、造卵器の発生過程は系統や種によって多様であると考えられる(Kofuji et al. 2018, Frangedakis et al. 2020, 小藤と嶋村 2021, Sokoloff and Remizowa 2021)。ここではゼニゴケ同様、モデルコケ植物として研究基盤が整い、知見が蓄積されてきているセン類のヒメツリガネゴケの配偶子器発生について簡単に議論する。ヒメツリガネゴケは雌雄同株であり、低温、短日環境で配偶子器発生が開始されると、まず茎葉体の頂端幹細胞とその隣接した細胞が造精器始原幹細胞へと分化する(Landberg et al., 2013, Kofuji and Hasebe 2014, Hiss et al., 2017, Kofuji et al., 2018, Landberg et al. 2021)。造精器始原幹細胞は、造精器頂端幹細胞を継続的に生み出し造精器をクラスター状に発生していく。このように造精器の発生が進むと、葉を一枚挟んで隣接する茎部分において、造卵器頂端幹細胞が生み出され造卵器が発生する。このように造精器頂端幹細胞や造卵器頂端幹細胞を確立し、そこを起点に発生が起こる点は、ゼニゴケと大きく異なっている。ヒメツリガネゴケでは、植物ホルモンのオーキシンの生合成および応答性が、造精器、造卵器の形態形成に寄与することが明らかになっている(Landberg et al., 2013, Landberg et al. 2021)。被子植物においてジベレリン応答遺伝子として知られるMYB転写因子をコードするPpGAMYB1およびPpGAMYB2の機能欠損変異体では、造精器がつくられる部分で、造卵器が形成されることからPpGAMYBは造精器の発生運命を制御すると考えられる(Aya et al. 2011)。ゼニゴケにおいて特に造卵器において卵の分化・維持に関わるMpRKDのオーソログPpRKDの機能欠損変異体では、造卵器発生が起こらない(Yoro et al. 2024)。一方で異所的な発現誘導により、造精器の発生が抑制され、造卵器の発生パターンに類似した造卵器様器官が形成されてくることから、ヒメツリガネゴケにおいて、PpRKDは雌化を促進する性分化制御因子として機能することが示された(Yoro et al. 2024)。このようにゼニゴケとヒメツリガネゴケでは性分化の制御様式が異なっているとともに、RKDのはたらきにも違いが見られる。ゼニゴケでは配偶子器発生の開始を制御するMpBNBのヒメツリガネゴケにおけるオーソログPpBNB1およびPpBNB2のはたらきにも違いが見られる(Sanchez-Vera et al. 2022)。これらの二重変異体では造精器と造卵器の発生は開始するが、その後、精子前駆細胞である精原細胞や卵前駆細胞の分化が見られず原器全体の分裂パターンに異常が見られる。このことはゼニゴケにおいて、MpBZR3を過剰発現した際にMpbnb変異体背景では造精器、造卵器の発生がより不完全になることとも類似しており(Furuya et al. 2024b)、ゼニゴケにおいてもヒメツリガネゴケ同様にMpBNBが配偶子器の発生過程にも影響することをサポートする。また、ゼニゴケでのMpBNBの配偶子器始原細胞の確立という重要な役割は、ヒメツリガネゴケでは保存されていないと思われる。このようにRKDやBNBの機能に大きな違いが見られている一方で、ゼニゴケMpGLID/MpMS1のヒメツリガネゴケオーソログPpMS1とPpMS2のはたらきは比較的類似している(Landberg et al. 2022, Ren et al. 2024)。これらの二重変異体において、造精器発生において内外を分ける並層分裂後、内側の精子前駆細胞(精原細胞)の分裂が停止し、機能的な精子形成が起こらない(Landberg et al. 2022)。造卵器発生において、二重変異体の影響は比較的少なく、造卵器の発生は後期まで進行したが、頸溝細胞等の分解が適切に起こらず、精子が遊泳する通路の形成が阻害されることに加え、卵のサイズが小さくなっており、稔性も失われていた(Landberg et al. 2022)。このような共通性と差異は、配偶子器発生の核となるプログラムの存在と多様性をつくりだす要因になっているのではないだろうか。
本稿は、令和6年度平瀬賞の受賞に伴い、受賞対象となった論文(Furuya et al. 2024b)の背景と内容、さらには同時期に発表された最新の知見をふまえてまとめたものです。平瀬賞選考委員の皆様に深く感謝を申し上げます。また対象論文は、近藤 侑貴博士(大阪大)、荒木崇博士(京都大)、福田裕穂博士(秋田県立大)、笠原賢洋博士(立命館大)、山岡尚平博士(京都大)、三枝菜摘氏(京都大)、冨田由妃博士(京都大)、南野尚紀博士(熊本大)、河内孝之博士(京都大)、深城英弘博士(神戸大)、上田貴志博士(基生研)、石崎公庸博士(神戸大)、西浜竜一博士(東京理大)、丹羽優喜博士(グランドグリーン)、井上佳祐博士(京都大)、山本千愛博士(筑波大)、元村一基博士(立命館大)、島津舜治博士(大阪大)との共同研究の成果です。加えて、本稿作成にあたり、荒木崇博士(京都大)には、語句の監修も含め多大なるお力添えをいただき、近藤侑貴博士(大阪大)、島津舜治博士(大阪大)には多くのアドバイスをいただきました。厚く御礼申し上げます。