2025 年 37 巻 1 号 p. 9-18
2025 年 37 巻 1 号 p. 9-18
真核細胞を支えるオルガネラは個々の機能を発揮するだけでなく、複数のオルガネラ機能を必要とする制御系を形成し、様々な生物学的プロセスを担う。例えば、多くの代謝系はオルガネラ間で代謝産物を受け渡す必要があるため、時空間的に制御されたオルガネラ間相互作用が必要となる。ペルオキシソームは、脂肪酸代謝や活性酸素種の除去、光呼吸やジャスモン酸の生合成など様々な機能をもち、これらの機能が低下すると、植物では種子の発芽不全、個体の矮性化、生殖異常、胚発生致死などが引き起こされる。光呼吸は、ペルオキシソーム、葉緑体、ミトコンドリアから構成される代謝系で、この3つのオルガネラが光依存的に相互作用し、その時にはペルオキシソームの形態変化や葉緑体との接着面の増加が引き起こされる。また、脂肪性種子の発芽時には、オイルボディに蓄積されたトリアシルグリセロールからリパーゼにより切り出された脂肪酸がペルオキシソームへ輸送され、この場合はペルオキシソームとオイルボディが相互作用する。このオルガネラ間相互作用は膜接触部位を介して行われ、その際にはオルガネラ間で脂質輸送も行われることが明らかになりつつある。本稿では、ペルオキシソームと他のオルガネラの相互作用の分子機構について、主にシロイヌナズナの研究を中心に概説する。
Organelles in eukaryotic cells not only perform individual functions but also form regulatory systems that require coordinated interactions among multiple organelles to carry out various biological processes. For example, many metabolic systems depend on spatiotemporally regulated organelle-organelle interactions to facilitate the exchange of metabolites between organelles. Peroxisomes, which are ubiquitously present in eukaryotic cells, play key roles in processes such as fatty acid metabolism, reactive oxygen species (ROS) detoxification, photorespiration, and the biosynthesis of jasmonic acid. Defects in these functions can lead to seed germination failure, dwarfism, reproductive abnormalities, and embryonic lethality. Photorespiration, a metabolic pathway involving peroxisomes, chloroplasts, and mitochondria, requires the light-dependent interaction of these three organelles. During this process, changes in peroxisome morphology and increased adhesion to chloroplasts occur. Additionally, during the germination of oilseed plants, fatty acids produced by lipase-mediated hydrolysis of triacylglycerol in the oil body are transported to peroxisomes, where direct interaction between peroxisomes and oil bodies takes place. It is now clear that these organelle-organelle interactions occur via membrane contact sites, facilitating lipid transport between organelles. This review focuses on the molecular mechanisms underlying the interactions between peroxisomes and other organelles, with a particular emphasis on studies in Arabidopsis thaliana.
真核細胞を構成する細胞小器官(オルガネラ)は、個々の機能を発揮するだけでなく複数のオルガネラ機能を必要とする制御系を形成し、様々な生物学的プロセスを担う。例えば、多くの代謝系や生合成系はオルガネラ間で中間代謝産物を受け渡すために、各オルガネラが適切な時空間配置をとるだけでなく、オルガネラ同士の相互作用が正確に行われる必要がある。このオルガネラ間相互作用は静的でなく、生きた細胞内ではオルガネラは活発に運動を行って細胞内の位置を変えるほか、光をはじめ温度や塩ストレスなど外界のシグナルや成長段階や組織に対応した様々な動態を示す (Oikawa et al. 2019, Koenig et al. 2023)。このオルガネラ間相互作用が正常に行われないと、細胞機能、ひいては個体の機能に異常を来すことから、細胞や個体の機能維持には、一つのオルガネラ機能だけでなく、性質の異なる複数のオルガネラ間の相互作用による制御が必要であり、その分子基盤の解明が行われている。植物細胞内は動的な環境にあるため、複数のオルガネラ機能を必要とする代謝系において、代謝産物を単純拡散により偶発的に受け渡しするよりは、オルガネラ同士が互いに近接している方が、代謝産物を効率的に移動させることが可能となる。動物や酵母などでは、オルガネラ同士が膜接触部位(Membrane contact site: MCS)を介して数十ナノメートルに近接し、脂肪酸代謝やカルシウム調節、脂質輸送を行っていることが報告されている (Helle et al. 2013)。MCSは、全てのオルガネラ間で観察されており、オルガネラは少なくとも 1 つ、もしくは複数のMCSを形成する(Valm et al. 2017, Shai et al. 2018, Baillie et al. 2020)。植物においても、脂肪酸合成における葉緑体と小胞体 (Block and Jouhet 2015) や、脂質代謝におけるオイルボディとペルオキシソームの直接的相互作用が観察されている (Hayashi et al. 2001, Cui et al. 2016)。
単膜系オルガネラのペルオキシソームは、植物だけでなく動物や酵母など、全ての真核細胞に必須なオルガネラである。直径約1.0〜1.5 µmの大きさで、独自のオルガネラゲノムをもたないため、構成タンパク質は全て核ゲノムにコードされている。ペルオキシソームは、組織や器官、個体の生育環境に応じて、機能や数、形態が変わる (Mano and Nishimura 2005)。様々な機能をもっており、脂肪酸代謝や活性酸素種の除去などは、植物、動物、酵母のペルオキシソームに共通の機能である。一方、動物では胆汁酸合成やコレステロールの生合成、酵母ではアルコール資化、植物では光呼吸やジャスモン酸の生合成など、生物種に特化した機能ももつ。これらの機能が低下すると、細胞や個体の正常な機能が異常となり、植物では種子の発芽不全、個体の矮性化、生殖異常、胚発生致死などが引き起こされる (Mano and Nishimura 2005, Goto-Yamada et al. 2014)。これらの植物の機能には、ペルオキシソームと他のオルガネラとの相互作用が必要であり(図1)、葉緑体、ミトコンドリア、オイルボディ、小胞体などとの相互作用についての分子基盤が解明されつつある。
本稿では、ペルオキシソームと葉緑体、オイルボディの相互作用、そしてオルガネラ間の脂質輸送について、筆者らが進めてきたシロイヌナズナの研究を中心に紹介する。
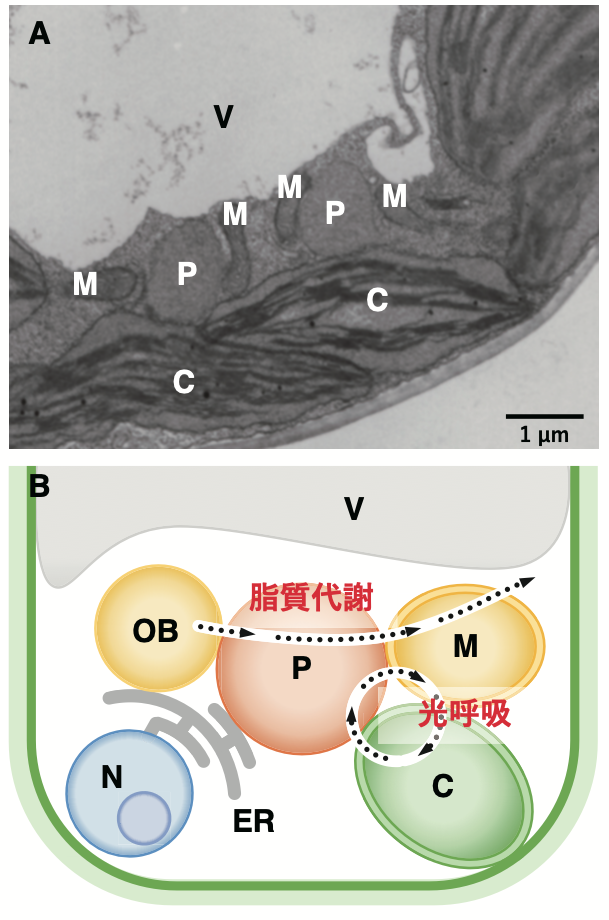
図1 植物細胞におけるペルオキシソームとのオルガネラ相互作用。(A) シロイヌナズナ緑葉の電子顕微鏡写真。(B) ペルオキシソームと他のオルガネラとの相互作用。光呼吸時にはペルオキシソーム、葉緑体、ミトコンドリアと相互作用が、貯蔵脂質の代謝時にはオイルボディ、ペルオキシソーム、ミトコンドリアとの相互作用が観察される。C, 葉緑体;ER, 小胞体;M, ミトコンドリア; N, 核; OB, オイルボディ; P, ペルオキシソーム; V, 液胞。
緑葉組織の葉肉細胞内の葉緑体周辺を観察すると、多くのオルガネラが葉緑体と物理的に相互作用し、接着と解離を繰り返している (Oikawa et al. 2015, Baillie et al. 2020, Hall et al. 2024)。その中でも特にペルオキシソームは葉緑体と高頻度で相互作用を行っている(図2)。
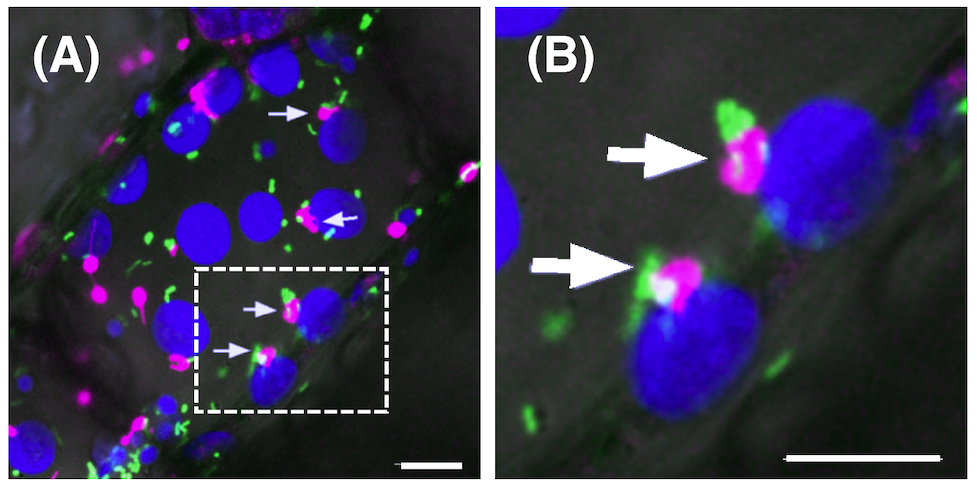
図2 ペルオキシソーム、ミトコンドリア、葉緑体間の相互作用。(A-B) シロイヌナズナ葉肉細胞内の葉緑体(青)、ペルオキシソーム(マゼンタ)、ミトコンドリア(緑)の共焦点レーザー顕微鏡画像。3つのオルガネラ相互作用を白矢印で示した。(B) は (A) の点線で囲んだ部位の高倍率像。 Bars = 5 µm。
緑葉組織において、ペルオキシソームと葉緑体が近接している様子は、半世紀ほど前から、ペルオキシソーム酵素の生化学的解析とともに、キュウリやカボチャなどの緑化芽生えの緑葉組織を用いた透過型電子顕微鏡解析で示されていた(図1A、Frederick and Newcomb 1969, Trelease et al. 1971, Nishimura et al. 1986)。また、ミトコンドリアも葉緑体近傍に局在している様子が示されており、これらのオルガネラの相互作用の意義として、異なる性質のオルガネラ間機能を必要とする代謝(光呼吸、ジャスモン酸の生合成など)との関連性が示唆されてきた(図1B、Frederick and Newcomb 1969, Trelease et al. 1971, Nishimura et al. 1986, Hayashi and Nishimura 2006, Kaur et al. 2009, Pan et al. 2020, Bittner et al. 2022)。
しかしながら、このペルオキシソーム、ミトコンドリア、葉緑体間の物理的相互作用の分子機構や、3者の相互作用の真の意義(代謝との関連性)に関しては未解明な部分が多い。筆者らは、緑葉組織の葉肉細胞内のペルオキシソームと葉緑体との相互作用についてイメージング解析を行い、光依存的な制御機構があることを明らかにした (Oikawa et al. 2015)。ペルオキシソームは、暗所では球形で運動性が乏しい状態であるが、適切な白色光下では活発な運動を伴い、楕円形やアメーバ状に形態を変化させながら接着領域を増大させることで、葉緑体との相互作用を強化することが明らかとなった。異なる光波長の照射や光合成阻害剤を用いた解析、加えて、光合成ができない班入りの領域を葉にもつシロイヌナズナ変異体yellow variegated 2用いた解析から、このペルオキシソームと葉緑体の相互作用は、光合成により誘導されることが明らかになった (Oikawa et al. 2015)。さらに、アクチン重合阻害剤を用いてペルオキシソームの運動を阻害しても、ペルオキシソームと葉緑体は相互作用することから、相互作用自体にはアクチン繊維は介在しない。また、葉緑体に相互作用しているペルオキシソームの経時観察では、葉緑体とペルオキシソームの相互作用が基盤となり、そこにミトコンドリアが捕捉される様子も観察された。また、白色光による光合成誘導条件下においては、光呼吸に関連する酵素活性が高く、オルガネラ相互作用と光呼吸の代謝との相関性が示唆された (Oikawa et al. 2015)。しかしながら、葉緑体間を移動するペルオキシソームがどのように葉緑体に捕捉され、ペルオキシソームと葉緑体の相互作用が開始されるのかは不明であった。そこで、葉緑体の表層に着目したイメージング解析を行った結果、葉緑体の表層から突起状の膜構造体が頻繁に形成され、その突起状の構造にペルオキシソームが補足されることが明らかとなった(図3A)。興味深いことに、その突起構造は時間が経つに従いストロミュール様の構造体にも変化した(図3B)。葉緑体の突起構造は、高温や塩などのストレスにより誘導されることが、報告されている (Holzinger et al. 2007)。また、ストロミュールは、病害応答や活性酸素種(Reactive oxygen species : ROS)などにより誘導される(Hanson and Conklin 2020)。筆者らが観察した葉緑体上の突起構造が、既存の報告例と同一のものであるかは現時点では不明であるが、葉緑体を介したオルガネラ相互作用の関連性を強く示唆するものである。
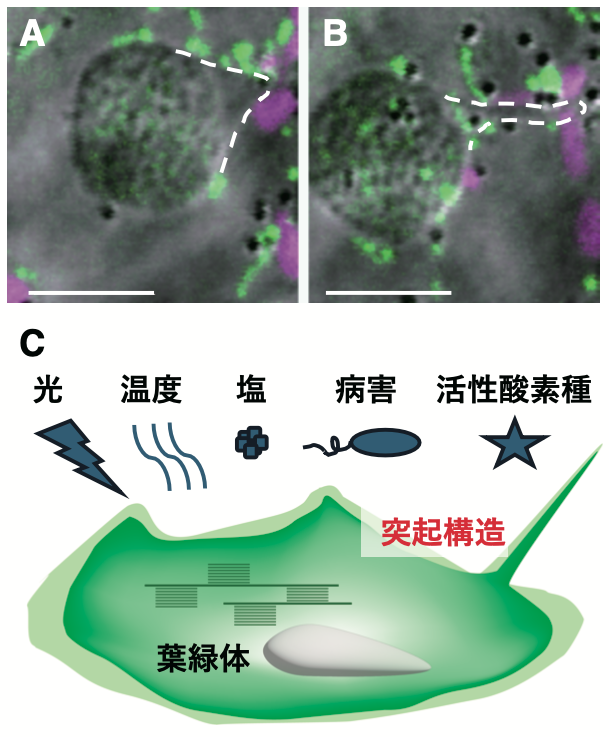
図3 ペルオキシソームと葉緑体膜構造との相互作用様式。 (A-B) 葉緑体(灰色)の膜構造である突起構造(A: 白点線)、ストロミュール(B:白点線)とペルオキシソーム(マゼンタ)、ミトコンドリア(緑)間の相互作用。Bars = 5 µm。 (C) 葉緑体膜の構造変化。光、温度、塩、病害、活性酸素種などに反応し、葉緑体表面から様々な膜構造が形成される。
現在のところ、葉緑体とペルオキシソームの相互作用に関する分子機構は、ほとんど明らかになっていない。ペルオキシソーム形成因子で、ペルオキシソーム膜に局在するPeroxin 10 (PEX10) の部位変異型タンパク質を過剰に蓄積させると、ペルオキシソームの形態異常に加え、ペルオキシソームと葉緑体との相互作用にも異常を生じ、光呼吸にも影響を与えることが報告されている (Schumann et al. 2007)。しかし、PEX10がどのようにペルオキシソームと葉緑体との相互作用を制御しているかは明らかになっていない。筆者らのこれまでの解析から、葉緑体とペルオキシソームとの相互作用を誘導する因子の一つは光であることが明らかとなっているが、その他にも温度やROSなどの関与も示唆されている(図3C)。下記の「オルガネラ相互作用の解析方法」に示したような、先端技術の解析機器や手法を組み合わせることで、相互作用因子の同定とその機能解析が進めば、葉緑体とペルオキシソームとの相互作用機構の分子機構が明らかとなることが期待される。
シロイヌナズナなどの脂肪性種子は、発芽時において、オイルボディ(リピドボディやリピドドロプレットと呼ばれることもある)に蓄積した脂質を分解して最終的にショ糖を合成し、幼植物体が光合成能を獲得するまでの生長エネルギーとして利用する。この時、オイルボディのトリアシルグリセロール(TAG)からリパーゼにより切り出された脂肪酸が、ペルオキシソーム(この時期のペルオキシソームは特にグリオキシソームとも呼ばれる)へと輸送され、ペルオキシソーム内でさらに代謝された後、ミトコンドリアを介してショ糖が合成される (図1B、Mano and Nishimura 2005)。この発芽時におけるオルガネラの細胞内の空間配置として、以前よりペルオキシソームとオイルボディが近接して存在することが、主に電子顕微鏡観察から報告され、これは、脂質分解系における中間代謝産物を効率的に輸送するためであると考えられていた (Trelease et al. 1971, Frederick et al. 1975, Nishimura et al. 1986)。そして、このペルオキシソームとオイルボディが直接相互作用していることが、シロイヌナズナのperoxisome defective 1 (ped1) 変異体の解析から明らかにされた (Hayashi et al. 2001)。ped1変異体は、ペルオキシソームの脂肪酸β酸化の最終段階を触媒する3-Keto acyl-CoA thiolase酵素をコードする遺伝子が欠損した変異体である (Hayashi et al. 1998)。ped1変異体では、オイルボディに脂質を蓄積させることはできるものの、その代謝が正常に行われずショ糖を合成できないため、発芽時においてショ糖要求性を示す (Hayashi et al. 1998)。ped1変異体の発芽時の子葉の免疫電子顕微鏡観察を行ったところ、ペルオキシソームが巨大化して、ペルオキシソーム膜が内部に陥入していること、その陥入部位にオイルボディが直接接着していることが明らかとなった (Hayashi et al. 2001)。これらの結果は、ペルオキシソームとオイルボディとの直接的な相互作用が、脂質の分解中に生成される中間代謝産物の輸送に重要な役割を果たしていることを示唆している。
筆者らは、オイルボディ膜タンパク質の1つOleosinとGFPとの融合遺伝子を発現させたシロイヌナズナ形質転換体(以降、OleGと呼ぶ)を作製した。OleG形質転換体では、オイルボディがリング状の構造物として可視化される (Cui et al. 2016)。このOleG形質転換体を親株として変異処理を行い、GFPの蛍光パターンが親株と異なる変異体をスクリーニングしたところ、ペルオキシソームとオイルボディの相互作用に異常を示す変異体が単離され、SUGAR-DEPENDENT 1 (SDP1) 遺伝子に変異をもつことが明らかとなった (Cui et al. 2016)。SDP1は、リパーゼ活性をもつオイルボディ膜に局在するタンパク質で、オイルボディに蓄積したTAGから、脂肪酸を切り出す役割を担っている (Eastmond 2006, Kelly et al. 2011)。sdp1変異体は、オイルボディが凝集体となる表現型を示すが、このsdp1変異体においてペルオキシソームを可視化させると、ペルオキシソームとオイルボディとの相互作用が観察された (Cui et al. 2016)。興味深いことに、この相互作用はショ糖依存性を示し、ショ糖を含まない培地ではオイルボディ凝集体とペルオキシソームの相互作用が引き起こされるが、58 mMショ糖を含む培地では相互作用は弱まることが明らかとなった(図4、Cui et al. 2016))。野生型のシロイヌナズナを、ショ糖を含む培地で発芽させると、オイルボディに蓄積された脂質分解が抑制されることから、ショ糖がペルオキシソームとオイルボディの相互作用を解離させることにより、脂質の分解を負に制御していることが明らかとなった。
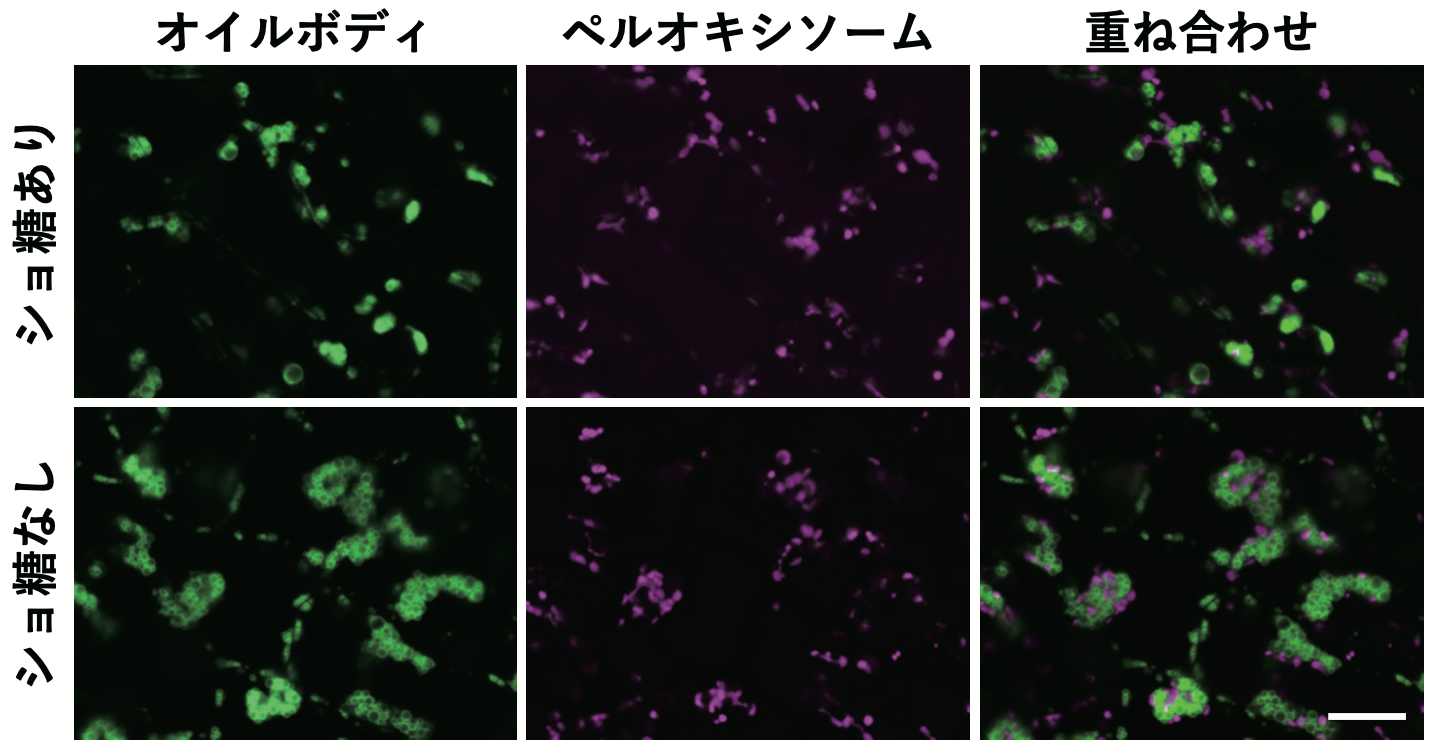
図4 種子発芽時におけるオイルボディとペルオキシソームの相互作用。オイルボディをGFP、ペルオキシソームをRFPで可視化させたシロイヌナズナsdp1変異体の種子を、58 mMショ糖を含む培地と含まない培地で発芽させ、5日目の子葉を共焦点レーザー顕微鏡で観察した。Bar = 10 µm。
どのような因子がオイルボディとペルオキシソームの相互作用を制御しているのであろうか?筆者らは、sdp1変異体に様々なペルオキシソーム変異を導入し、ショ糖を含まない培地におけるオイルボディとペルオキシソームの相互作用を解析した。その結果、sdp1 ped3二重変異体では、1 mMのショ糖存在下(ped3変異体はショ糖要求性を示し、0 mMでは解析できないため1 mMショ糖培地を使用)でも、オイルボディとペルオキシソームの相互作用が弱まることが明らかとなった (Cui et al. 2016)。PED3(別名CTS/PXA1)はペルオキシソーム膜に存在するATP Binding Cassette (ABC) 輸送体で、脂肪酸をペルオキシソーム内へ輸送することが明らかとなっている (Zolman et al. 2001, Footitt et al. 2002, Hayashi et al. 2002)。脂肪酸輸送体が、ペルオキシソームとオイルボディの相互作用因子として機能するのは大変興味深い。オイルボディ側の因子としては、マウスと線虫を用いた研究から、オイルボディの膜上に局在するAdipose triglyceride lipase(ATGL)が関与することが報告されている (Kong et al. 2020)。また、HeLa細胞とU-2 OS細胞では、オイルボディの膜上のM1 Spastinタンパク質が、ペルオキシソーム膜上のABCD1(PED3と同様のABC輸送体)と相互作用することが明らかにされている (Chang et al. 2019)。植物のオイルボディ膜上には、先述したSDP1に加え、Monoacylglycerol lipase 8 (MAGL8) が存在し、これら2つのタンパク質がリパーゼ活性によるTAGの分解だけでなく、ペルオキシソームとの相互作用に関わっていることが示唆されているが、現時点ではまだ相互作用因子は同定されていない。興味深いことに、SDP1はオイルボディ膜に局在するものの、発芽が進むにつれて、ペルオキシソームに輸送されることが明らかとなっている (Thazar-Poulot et al. 2015)。つまり、発芽の初期にはオイルボディとペルオキシソームの相互作用が、効率的な脂質代謝に必要であるものの、成長が進み光合成によりエネルギー獲得ができるようになると脂質分解によるショ糖合成の必要性が低下するため、オイルボディとペルオキシソームの相互作用も弱まり、そのためSDP1がオイルボディから除去されると予想される。現時点では、その分子機構や、なぜ移動先がペルオキシソームなのかといった意義も明らかになってはいない。また、SPD1、MAGL8、PED3/CTS/PXA1が直接相互作用するのか、あるいは他の因子を介しているのかもわかっておらず、今後の解析が待たれる。
細胞内には多様な脂質分子種が存在し、生体膜の構成、シグナル伝達、タンパク質の修飾などの役割を担っている。生体膜は主にグリセロ脂質、スフィンゴ脂質、ステロールで構成されるが、各オルガネラによって膜の脂質組成には特徴があり、この組成変化がオルガネラの形態や機能発現に影響することがわかっている (Hagio et al. 2000, Aronsson et al. 2008, Pan et al. 2014)。生体膜脂質の生合成は複数のオルガネラに渡って行われ、合成された脂質は必要とされるオルガネラ膜へと輸送される必要がある。先述したMCSの機能は、オルガネラ間を係留するタンパク質やタンパク質複合体によって多岐にわたり、その機能の1つにオルガネラ間の脂質輸送があげられる(図5A)。細胞内の脂質輸送は小胞経路または非小胞経路によって行われるが、脂質の種類に非選択的な小胞輸送に比べてMCSにおいて行われる非小胞輸送では脂質の選択性や特異性が高く、生体膜脂質組成の恒常性維持にも重要な役割を果たすと考えられる。この項目では、オルガネラ間相互作用におけるMCSを介した脂質輸送について概説する。
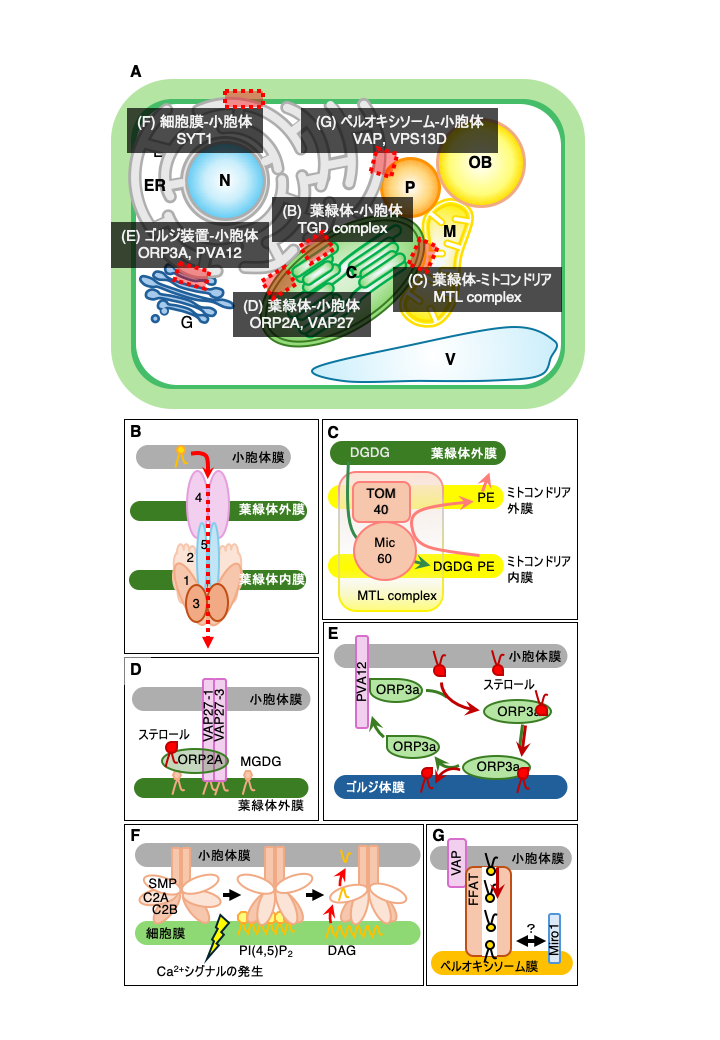
図5 植物細胞内のMCSを介した脂質輸送 (A) MCSを介した脂質輸送例。図中の6つの例について、(B)〜(G) として概要を示す。N: 核、ER: 小胞体、G: ゴルジ装置、OB: オイルボディ、C: 葉緑体、P: ペルオキシソーム、M: ミトコンドリア、V: 液胞。(B) 葉緑体−小胞体の接触部位におけるホスファチジン酸輸送。TGD複合体は、二量体のTGD1、TGD3、TGD4、TGD5、八量体TGD2から構成され、脂質前駆体を、小胞体からストロマに輸送する。TGD5は、外膜のTGD4と内膜のTGD1、TGD2、TGD3輸送複合体を橋渡しする。Wangら (2012) は、TGD4タンパク質の一部の領域が小胞体と葉緑体の膜のMCSに局在し、脂質を小胞体から葉緑体膜に輸送する役割を果たすと提唱している。図はFanら(2015)より引用・改変した。(C) 葉緑体−ミトコンドリア接触部位におけるPEとDGDGの輸送。MTL複合体にはTOM複合体とMICOS複合体のサブユニットであるMic60が含まれている。Pi 欠乏時にTom40と相互作用したAtMic60はミトコンドリアの外膜と内膜の係留を促進し、ミトコンドリア膜からのPEの輸送と葉緑体からのDGDGの輸送に関与している可能性が示唆されている。図はMichaudら(2016)より引用・改変した。 (D) 小胞体−葉緑体接触部位におけるステロール輸送。小胞体に局在するVAP27-1と27-3は、葉緑体外膜のMGDGとの相互作用によって小胞体と葉緑体外膜を係留する。ORP2AはMGDGとの結合およびVAP27との相互作用で小胞体−葉緑体膜接触部位に存在する。また、ORP2A はステロールとも結合することができる。VAP27-ORP2A複合体が欠損すると、葉緑体でのみ特異的に植物ステロールの含有量が上昇することから、ORP2Aを介して葉緑体からのステロールを引き抜き、他の区画に輸送している可能性が示唆されている。(E) 小胞体−ゴルジ装置接触部位におけるステロール輸送。ORP3aはPVA12との相互作用によって小胞体に局在している。ステロールとの結合により構造が変化したORP3aはPVA12との相互作用が阻害され、小胞体から分離する。ステロールと結合したORP3aはゴルジ装置で結合したステロールを分離し、再度PVA12と相互作用することで小胞体にリサイクルされる。(F) 小胞体−細胞膜接触部位における脂質交換。SYT1は2量体を形成し、N末端の疎水性領域を介して小胞体に固定され、C末端のC2Bドメインを介して細胞膜に結合する。非生物的ストレスによってCa2+シグナルが発生すると細胞膜にPI(4,5)P2が蓄積する。Ca2+依存的にSYT1のC2Aドメインが細胞膜へ結合した後に細胞膜に蓄積したPI(4,5)P2からホスホリパーゼCによって生じたDAGが、SMPドメインによって細胞膜から引き抜かれ小胞体に輸送される。 (G) 小胞体−ペルオキシソーム接触部位における膜脂質輸送。哺乳類のVPS13Dは疎水性の溝を持つ細長いチューブ状の構造をしている。ペルオキシソーム膜局在型Miro1と、VPS13DのFFAT様モチーフを介した相互作用により、脂質が小胞体からペルオキシソーム輸送される。図はGuillén-Samanderら(2021)より引用・改変した。
(1) 葉緑体−小胞体の接触部位におけるホスファチジン酸輸送(図5B)植物におけるグリセロ脂質の生合成は葉緑体と小胞体で行われている。葉緑体内で合成された脂肪酸(FA)は、葉緑体脂質(ホスファチジルグリセロール:PG、モノガラクトシルジアシルグリセロール:MGDG、ジガラクトシルジアシルグリセロール:DGDG、スルホキノボシルジアシルグリセロール:SQDG)の合成に使用されるか、小胞体へ輸送されて葉緑体外のリン脂質(ホスファチジルイノシトール:PI、ホスファチジルコリン:PC、ホスファチジルエタノールアミン:PE、PG)とTAGの合成に使用される。小胞体由来のリン脂質前駆体は葉緑体に戻り、MGDG、DGDG、SQDGの合成に使用される (Michaud et al. 2017)。
葉緑体での糖脂質(MGDG, DGDG, SQDG)合成のために、小胞体から葉緑体へ輸送される脂質候補としてはジアシルグリセロール(DAG)、PC、リゾPCなどが提唱されているが、ホスファチジン酸(PA)が関わる可能性も示唆されている (Xu et al. 2005, Awai et al. 2006, Wang et al. 2012)。現在までに、小胞体から葉緑体への脂質前駆物質の供給は5つのTRIGALACTOSYLDIACYLGLYCEROL(TGD)タンパク質(TGD1〜5)が関与していることが明らかになっている(Xu et al. 2003, Awai et al. 2006, Lu et al. 2007, Xu et al. 2008, Fan et al. 2015)。TGD1、TGD2、および TGD3 は葉緑体内膜に存在し、ABCトランスポーター複合体を構成する (Roston et al. 2012)。ホモ二量体を形成するTGD4は葉緑体外膜に存在する膜貫通脂質輸送タンパク質で、一部は小胞体と物理的に接触している可能性が示唆されている。TGD5はTGD1、TGD 2、TGD 3で構成されるABCトランスポーター複合体とTGD4を架橋することで、葉緑体外膜から内膜への脂質の移動を促進する巨大な複合体を形成させることが示唆されている (Fan et al. 2015)。この巨大なタンパク質複合体では、TGD4のN末端領域が小胞体からのPAを認識後、C末端領域のβバレルチャネルを介して葉緑体膜の膜間面にPAを転送する。続いて、TGD2がPAを受け取り、GD1、TGD 2、TGD 3から構成されるABCトランスポーター複合体により、ATPを加水分解しながら内膜を介してPAを転送すると考えられている(Wang et al. 2012)。
(2) 葉緑体−ミトコンドリア接触部位におけるPEとDGDGの輸送(図5C)リン酸(Pi)欠乏時の植物細胞では、膜脂質の広範なリモデリングが観察されている (Härtel and Benning 2000, Jouhet et al. 2003)。このリモデリングに必要なPiはリン脂質(主にPEとPC)の分解から供給されるが、それに伴って欠乏する膜脂質はDGDGで補われる。DGDGは葉緑体外膜で合成され、Pi欠乏時に葉緑体とミトコンドリアとの相互作用により、DGDGをミトコンドリアに移動することが示されている (Jouhet et al. 2004)。近年、ミトコンドリア膜貫通リポタンパク質(MTL; Mitochondrial transmembrane lipoprotein)複合体がこの輸送に関わることが報告された。MTL複合体はTOM複合体とMICOS複合体のサブユニットであるMic60を含む。Tom40と相互作用したAtMic60はミトコンドリアの外膜と内膜の係留を促進し、ミトコンドリア膜からのPEの輸出と葉緑体からのDGDGの輸入に関与している可能性が示唆されている (Michaud et al. 2016)。
(3) 小胞体−葉緑体接触部位におけるステロール輸送(図5D)Syntaxin-like vesicle-associated membrane protein-associated proteins (VAP) 27-1とVAP27-3は小胞体の特定のサブドメインに局在し、葉緑体外膜に存在する脂質(MGDG)との相互作用により小胞体と葉緑体外膜を係留する。また、MGDGとの結合を介して葉緑体外膜に局在するOxysterol-binding protein (OSBP) related protein (ORP) 2AはVAP27複合体と相互作用する。vap27-1、vap27-3、orp2aの単一および多重変異体では、VAP27-ORP2A複合体の欠損により、MGDGおよびPGのアシル組成がわずかに変化すること、葉緑体でのみ特異的に植物ステロールの含有量が上昇することから、これら2つの因子は小胞体-葉緑体膜接触部位で植物ステロールの恒常性を維持する役割を果たすと考えられる。またORP2Aを介して葉緑体からのステロールを引き抜き、他の区画に輸送している可能性も示唆されている (Renna et al. 2024)。
(4) 小胞体−ゴルジ装置接触部位におけるステロール輸送(図5E)ORP3aはVAP33ファミリータンパク質であるPVA12と直接相互作用して小胞体に局在するが、ドナー膜とアクセプター膜間のステロールキャリアとして小胞体とゴルジ装置の間を移動することも示されている (Yan and Olkkonen 2008)。ステロールと結合することでORP3aの構造変化が引き起こされ、その結果PVA12との相互作用が阻害され、ドナー膜(小胞体)から解離する。ステロールと結合したORP3aはアクセプター膜(ゴルジ装置)で結合したステロールを降ろし、再度PVA12と相互作用することでドナーコンパートメント(小胞体)にリサイクルされると予測されている (Saravanan et al. 2009)。
(5) 小胞体−細胞膜接触部位における脂質交換(図5F)Synaptotagmin 1(SYT1)はN末端の疎水性領域、SMPドメイン、C末の2つのC2ドメインで構成される。N末端の疎水性領域を介して小胞体に局在し、C末端のC2Bドメインを介して細胞膜に結合する。非生物的ストレスによってCa2+シグナルが発生すると、細胞膜ではPhosphatidylinositol 4,5-bisphosphate(PI(4,5)P 2)が蓄積し、細胞膜に蓄積したPI(4,5)P 2はホスホリパーゼCによってDAGへと分解される。このDAGはSYT1のC2AドメインがCa2+依存的に細胞膜へ結合した後に、SMPドメインによって細胞膜から引き抜かれ小胞体に輸送される (Benavente et al. 2021)。
(6) 小胞体−ペルオキシソーム接触部位における膜脂質輸送(図5G)酵母や哺乳類のVacuolar Protein Sorting 13 (VPS13) は、全長にわたって疎水性の溝を持つ細長いチューブ状の構造をしており、オルガネラ間の接着部位で脂質がチューブ内を通ってオルガネラ膜に輸送されることが示唆されている (Lees and Reinisch 2020, Li et al. 2020a)。哺乳類においては、ミトコンドリア膜タンパク質のMitochondrial Rho GTPase 1(Miro1)のスプライスバリアントがペルオキシソーム膜に輸送されることが報告されている。哺乳類のVPS13Dは、FFAT (two phenylalanines (FF) in an acidic tract (AT))様モチーフを介して、小胞体膜上のVAPタンパク質とペルオキシソーム膜局在型Miro1と相互作用することで、小胞体からペルオキシソームへの脂質の輸送に関わることが示された (Baldwin et al. 2021, Guillén-Samander et al. 2021)。しかしながら、ペルオキシソーム膜局在型Miro1とVPS13Dとの相互作用などの分子機構については明らかにされていない。
オルガネラ間の脂質輸送の分子機構については、まだ一部しか明らかにされておらず、今後さらなる解析によって詳細な機能同定が行われることが期待される。
近年、蛍光タンパク質を用いて、葉緑体やペルオキシソーム、ミトコンドリアなどのオルガネラを可視化した形質転換体の作出が可能となり、生細胞でのイメージング解析が容易になった (Goto-Yamada et al. 2022, Koenig et al. 2023, Hall et al. 2024)。先述したペルオキシソームと葉緑体、ミトコンドリアとの相互作用や、ペルオキシソームとオイルボディとの相互作用解析もイメージング技術なしでは成し得なかった。また、ペルオキシソームやミトコンドリアがアクチン繊維上を移動する様子や、同時に複数のオルガネラの動態や局在、相互作用の様子などをイメージング解析することも今では困難でなくなっている。オルガネラの形態は、環境により変化する。例えば、ROSや紫外線、温度変化によるペルオキシソーム膜構造の変動がライブイメージングにより捉えられている (Sinclair et al. 2009, Midorikawa et al. 2023)。このように、環境変化や外部刺激に対するオルガネラ動態をイメージング技術により捉え、オルガネラ機能から細胞機能、最終的には植物個体の機能を理解することが可能となっている。
オルガネラ相互作用を定量的に評価する方法についても開発が進んでいる。フェムト秒レーザーは、集光点の微小領域に爆発現象を生じさせ、衝撃波と応力波を伝搬し、周辺の微小物体に衝撃力を作用する (Hosokawa et al. 2011)。このフェムト秒レーザーを葉緑体に接着しているペルオキシソーム近傍(5 µm内)に集光させ、葉緑体から剥離するペルオキシソームの様子を撮像し、ペルオキシソームと葉緑体の接着力を算出する系が開発された (Oikawa et al. 2015, Hosokawa et al. 2016)。この系では、レーザー出力と原子力間顕微鏡のカンチレバーの振れ幅とバネ定数より力学的数値を計算するもので、明所でのペルオキシソームと葉緑体との接着力は暗所の約2.5倍、アクチン細胞骨格を破壊した細胞では7倍近く増加していることが明らかとなった (Oikawa et al. 2015)。
光ピンセットは、照射光と異なる屈折率をもつ物質に生じた放射圧を利用して、物質を集光点に補足して操作する光技術である。この技術を応用して、タバコ表皮細胞内の葉緑体に接着するペルオキシソームを剥離する実験が行われ、葉緑体とペルオキシソームの接着強度が測定されている (Gao et al. 2016)。
走査型電子顕微鏡で接着領域をより詳細に解析する手法として、近年FIB (Focused Ion Beam)-SEM法や連続切片SEM法が用いられている。この解析によりイネや、シロイヌナズナ葉肉細胞内の葉緑体の微細構造やオルガネラの配向性がより詳細に三次元で視覚化されている (Midorikawa et al. 2022, Yamane et al. 2022)。葉緑体運動の解析では、古くから顕微鏡をカスタマイズして、マイクロビームを用いた光照射解析が行われてきた (Wada 2016) が、観察ステージを改変して、温度変動性の解析に適した顕微鏡などが開発され、高温や低温にシフトする過程で葉緑体やペルオキシソームの形態変化する様子が観察されている (Holzinger et al. 2007, Midorikawa et al. 2023)。
顕微鏡で撮像した画像データーをImaris (https://imaris.oxinst.jp) やImageJ (https://imagej.net/ij/) などの市販ソフトウェアやオープンソースの画像解析ツールを用いて、オルガネラ相互作用を定量解析する方法も開発されている (Oikawa et al. 2022b, Midorikawa et al. 2023)。また、AIによるオルガネラ自動認識技術が開発されていることから (Li et al. 2020a, Feng et al. 2023)、今後、これを応用したオルガネラ相互作用を自動で追尾することも可能となろう。加えて、Split-GFPを用いたオルガネラ間相互作用因子同定法 (Baillie et al. 2020, Li et al. 2020b) や、免疫沈降法、プロテオーム解析などの生化学的手法を組み合わせることにより、オルガネラ相互作用に関わる新たな制御因子の同定など、オルガネラ間相互作用の分子基盤の理解が進むと期待される。
本稿では、オルガネラ間相互作用の研究において、ペルオキシソームと葉緑体、ペルオキシソームとオイルボディとの相互作用、MCSを介した脂質輸送について、現在明らかにされている分子機構について紹介した。ペルオキシソームには、他にも多くの機能が存在し、他のオルガネラとも相互作用する。また、不活性化したペルオキシソームは、選択的オートファジーの一種であるペキソファジーによって分解される (Shibata et al. 2014)。この時、オートファゴソーム膜とペルオキシソームが相互作用してペキソファゴソームが形成される (Oikawa et al. 2022a)。これも広義にはオルガネラ間相互作用の一つと捉えられることができるだろう。もちろん、ペルオキシソーム以外のオルガネラや、輸送小胞、細胞骨格などのほとんどの細胞内構造物も相互作用して細胞機能を支えており、それが植物個体を支えている。これらのオルガネラ間相互作用は、動物細胞や酵母細胞でも観察される (Schrader et al. 2015, Joshi 2021)。オルガネラ相互作用の可視化や定量化を可能とする新技術も開発されており、これらを用いることで、多様な生物におけるオルガネラ間相互作用の分子機構が明らかとなり、生物種間の共通性、あるいは種特異性に迫ることが期待できる。
本稿は、日本植物学会第 88 回大会シンポジウム「植物 / 微生物 / オルガネラの相互作用とイメージングで解き明かす」の講演内容を中心にまとめたものである。オーガナイザーの豊岡公徳先生(理化学研究所)と永田典子先生(日本女子大学)には、この場を借りてお礼申し上げます。本稿の内容は、基礎生物学研究所の西村幹夫先生が主宰された高次細胞機構研究部門に、筆者らが在籍していた時から継続されてきたオルガネラ研究内容の一部であり、西村幹夫先生をはじめとする多くの高次細胞機構研究部門メンバーによって遂行された研究成果である。また、プラスミドや形質転換植物などの実験材料も多くの方からご提供いただいた。この場を借りて感謝申し上げます。本稿およびシンポジウムに関する研究は、JSPS科研費(22120007、26440157、17K07457)の助成を受けて実施されたものである。