2025 Volume 145 Issue 5 Pages 461-468
2025 Volume 145 Issue 5 Pages 461-468
Durotep®MT Patch (DMTP) (Janssen Pharmaceutical K.K., Tokyo) is a systemically acting narcotic patch containing fentanyl. It is applied transdermally and removed 72 h after applying. The range of effective serum fentanyl concentrations is very narrow (0.3–3 ng/mL). Therefore, analysis of the absorption kinetics (ABK) is especially important. We studied ABK for fentanyl from DMTP 16.8 mg. There are 5 analytical methods to obtain ABK: The estimated mean absorbed rate at steady state (EMARSS) obtained using the residual method (standard value), absolute bioavailability method, Wagner–Nelson method, 3-compartment model Loo–Riegelman method (3LR), and SPLINE–Deconvolution method (SDecon), yielding results of 0.104, 0.119, 0.114, 0.109, and 0.103 mg/h respectively. EMARSS for 3LR and SDecon were nearly equal to the standard value. The absorbed rate for fentanyl with elapsed time by SDecon indicated an amplitude of 3 times with about a 20 h period at 10.7–72 h and the increase in the absorption rate began before the increase in the serum concentration when DMTP was applied transdermally. This phenomenon indicates that the mean absorption rate was constant; thus, an absorption steady state was reached. The actual mean absorption rate during this period was 0.0924 mg/h (range: 0.0594–0.131). The cumulative absorption ratio increased gradually with only a small amplitude, and bioavailability was 44.2%. From our results, SPLINE–Deconvolution is the most suitable method to assess fentanyl absorption kinetics of DMTP.
麻薬性鎮痛剤であるフェンタニルの全身作用型貼付剤の1つとして,デュロテップ®MTパッチ(ヤンセンファーマ株式会社,東京)がある.デュロテップ®MTパッチは72 h毎に貼り替えて使用する.フェンタニルを経口投与すると絶対的バイオアベイラビリティは約30%であり,1)ほとんど吸収されないため,初回通過効果を受けない経皮吸収は有効な手段である.静脈内投与での術後疼痛の有効血中濃度は0.6–3 ng/mLである.2)術後のモルヒネの必要量の減少で判定すると,定速静注のフェンタニル0.1 mg/hの投与速度で得られる血中濃度(平均±標準偏差:1.37±0.28 ng/mL)で鎮痛効果有効性が高まるという報告がある.3)狭い有効血中濃度を維持するために,貼付剤からフェンタニルの全身への吸収は,定速静注のような安定した速度に近づくのが望ましい.デュロテップ®MTパッチの場合,貼付後72 hで剥離するまでフェンタニルの血中濃度は,Lag timeを経て上昇し,その後上下に一定の振れ幅をもって維持され,下降していくことが報告されている.4)フェンタニルをBolus投与による負荷投与後,定速静注を行い,定常状態に到達後の血中濃度は一定に保たれることが報告されている.5)したがって,貼付剤からの全身に吸収されるフェンタニルの血中濃度は吸収速度の変化に応じて上下に変動していると考えられ,有効血中濃度を維持する投与設計を行ううえで,貼付剤からの吸収動態を解析することは重要である.
全身作用型貼付剤の吸収動態の解析には,残渣法,絶対的バイオアベイラビリティ法,Wagner–Nelson法,6) Loo–Riegelman法,7) 3-コンパートメントモデルLoo–Riegelman法8)及びデコンボリューション法9,10)がある.しかし,これらの方法を用いて,デュロテップ®MTパッチのような全身作用型フェンタニル貼付剤に関して吸収動態,すなわち,吸収量,バイオアベイラビティ,吸収速度及び累積吸収率の経時的変化を詳細に解析した報告はない.吸収速度の目安として,残渣法により得られた吸収量を貼付時間で除して得られる“定常状態における推定平均吸収速度”が一般的に便宜上用いられている.しかし,“実際に観察される吸収速度”を把握することは臨床的に重要である.実際の吸収速度の変化を解析できるのは,SPLINE関数を用いたデコンボリューション法(SPLINE–デコンボリューション法)11)である.
本研究において,全身作用型フェンタニル製剤であるデュロテップ®MTパッチに関して,残渣法,絶対的バイオアベイラビリティ法,Wagner–Nelson法,6) 3-コンパートメントモデルLoo–Riegelman法8)及びSPLINE–デコンボリューション法11)の比較検討を行い,吸収動態の解析におけるSPLINE–デコンボリューション法の有用性の検討を行った.
フェンタニルの全身作用型貼付剤であるデュロテップ®MTパッチの貼付時の薬物動態の情報を,また,フェンタニルクエン酸塩の静脈内投与の薬物動態の情報収集を行った.デュロテップ®MTパッチの情報,すなわち,フェンタニルの血中濃度推移及びarea under the concentration curve(AUC),maximum serum concentration(Cmax),terminal elimination half-life(t1/2)及びtime of maximum observed serum concentration(tmax)等の薬物動態のパラメータは,添付文書,インタビューフォーム,新医薬品の「使用上の注意」の解説及び関連論文から得た.静脈内投与のデータに関しては,健常成人に関する論文の中から,投与しているフェンタニルがクエン酸塩であることが明記されているVasishtらの報告(2010)12)を用いた.
薬物動態解析のために必要な貼付剤であるデュロテップ®MTパッチのフェンタニルの血中濃度推移は,健常成人(日本人)40例において16.8 mg貼付剤1枚を72 h単回貼付時のデータ4)を用いた.一方,静脈内投与の血中濃度推移は,健常成人(外国人)12例にフェンタニルクエン酸塩0.2 mg(フェンタニルとして0.127 mg)をBolus投与した時のデータ12)を用いた.両者の血中フェンタニル濃度推移から,Webアプリケーションのグラフの数値化ツールであるWebPlotDigitizer 4.5(WPD, USA)(http://automeris.io/WebPlotDigitizer/)13)を用いて,フェンタニルの血中濃度の読み取ったデータを抽出した.
In vitroの方法として残渣法があり,そのほか4つの方法はin vivoの方法である.In vivoの方法は,いずれも,静脈内投与のデータが必要である.Bolus投与のデータに関しては,Vasishtらが報告した血中濃度推移(Ref. 12,Fig. 1)からWPDにより求めた読み取ったデータに関して,Napp(Ver. 3.071β)を用いて解析を行い,3-exponentialのEq.(1)でフィッティングを行った.
 | (1) |
Bolus投与時の3-コンパートメントモデルをFig. 1に示した.このモデルに基づいて,Napp(Ver. 3.071β)を用い解析を行い,k及びVpを求めた.

デコンボリューションの式はEq.(2)で表される.9,10)
 | (2) |
ここで,式中のCtd及びCivから逆に吸収速度及び累積吸収率を求めた.Civは3-exponentilalのEq.(1)を用いた.解析はTinyBasic(Ver.1.5.1)上で,DECONプログラム9–11)をBasicで組み,そのプログラムを用いて行った.デュロテップ®MTパッチ72 h単回貼付投与後と静脈内投与後の血中濃度の測定時間を一致させる必要がある.本製剤の貼付時のサンプリングポイント(t時間における血中濃度)はスパースなため,各ポイント間の区間補正をすることにより,静脈内投与の連続データに合わせることができる.スパースなデータを補間して解析する方法の報告はない.貼付投与のグラフから抽出したスパースな血中濃度値を,R(Ver.4.2.2)のSPLINE関数を用いて補間を行った.なお,補間の間隔が大きいと,真の値から離れることが報告されているため,14)Δt=0.01 hに設定した.
残渣法は,パッチ中の剥離後の残存フェンタニル量を測定し,使用前の量(規格値: 16.8 mg)との差により放出量を求める方法である.デュロテップ®MTパッチの残渣法で得られたフェンタニルの体内への放出量に関しては,ヤンセンファーマ株式会社のデータ15)と藤田らの報告16)との2つのデータがあった.
絶対的バイオアベイラビリティ法の式は,Eq.(3)で表される.絶対的バイオアベイラビリティFを求め,吸収量はDosetd×Fにより求めた.
 | (3) |
Wagner–Nelson法の式は,Eq.(4)で表される.
 | (4) |
Eq.(4)のAT及びA∞は,各々Eq.(5)及びEq.(6)で表される.
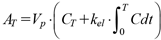 | (5) |
 | (6) |
Eq.(5)は,実際のATを求めるための計算式である.一方,Eq.(6)は,A∞を求めるために1-コンパートメントモデルを仮定して,一般的に使われる式である.この仮定により,Vp・kel=CLivが成立する.
3-コンパートメントモデルLoo–Riegelman法で,AT/Vpを算出する式は,Eq.(7)で表される.
 | (7) |
一般的に便宜上使われている定常状態における推定平均吸収速度は,吸収量を貼付時間で除して求められる.したがって,デュロテップ®MTパッチの場合貼付時間は72 hであるため,各々の方法で得られた吸収量を貼付時間72 hで除すことにより求めた.
表皮に残存する量として,放出量と吸収量の差から求めた.藤田らの報告は患者のデータ16)であるのに対してヤンセンファーマ株式会社の値は健常人のデータ15)である.したがって,ヤンセンファーマ株式会社の放出量7.46 mg15)を基準にして求めた.
なお,本文中の略語とその内容を下記に示した.
A, B, C, α, β, γ: Hybrid定数,A∞: 総吸収量,Ai: iコンパートメントの薬物量,AIC: 赤池の情報量基準,AT: 0からT時間までの薬物吸収量,AUC: 血中薬物–時間曲線下面積,AUC∞及びAUC0→∞: 時間0から無限大時間まで外挿して得られた血中薬物–時間曲線下面積,AUCiv: 静脈内投与後のAUC, AUCt1→t2: 時間t1から時間t2までの血中薬物–時間曲線下面積,AUCtd: 経皮投与後のAUC, Civ(t): 入力関数(単回静脈内投与時の血中薬物濃度),CLiv: totalクリアランス(iv時),Cmax: 最高血中薬物濃度,CT: T時間の薬物血中濃度,Ctd(τ): 出力関数(単回経皮投与時の血中薬物濃度),Doseiv: 静脈内投与時の投与量,Dosetd: 経皮投与時の投与量,F: 絶対的バイオアベイラビリティ,F(θ): 重み関数(薬物の吸収速度),Fa: T時間までのみかけの薬物吸収率,k(k12, k21, k13, k31, kel): 1次速度定数,T: 投与後の時間,t1/2: 消失相の半減期,tmax: 最高血中薬物濃度到達時間,Vp: セントラルコンパートメントの分布容積.
12人の健常人に投与量0.2 mgのフェンタニルクエン酸塩(フェンタニルとして,0.127 mg)をBolus投与した時の血中濃度推移(Ref. 12,Fig. 1)をEq.(1)にフィッティングして得られたHybrid定数を用いてシミュレーションカーブを作成し,そのカーブにWPDで抽出した11個の読み取ったデータをプロットした(Fig. 2).Damping–Gauss–Newton法(Weight: 1/Cp2)により,3-exponential Eq.(1)で良好なフィッティングを示した(AIC=−50.36).得られたHybrid定数A, α, B, β, C, γをEq.(1)で示すと下記のようになった.
 |
一方,3-コンパートメントモデルの解析で得られた速度定数k12, k21, k13, k31及びkelは各々,3.436, 3.513, 2.090, 0.682及び1.236 h−1であり,分布容積Vpは,31.58 Lであった.

The solid line shows the best fit of the 3-exponential equation to the measured data.
In vivoによる方法はいずれも静脈内投与のデータが必要となる.デュロテップ®MTパッチは日本人のデータ(n=40),4)フェンニルクエン酸塩の静脈内投与のデータは外国人のデータ(n=12)12)である.そこで,デュロテップ®MTパッチ16.8 mgを72 h単回貼付したときの日本人4)と外国人17)のtmax, Cmax, t1/2, AUC0→120 h及びAUC0→∞をTable 1に示した.外国人の値に対する日本人の値の比を求めて各パラメータについて比較を行った.tmaxは,一般的にそれ自身のばらつきが大きく,デュロテップ®MTパッチの場合,比は1.31と大きな値を示した.一方,Cmax, t1/2, AUC0→120 h及びAUC0→∞について,各々,1.05, 1.08, 1.07及び1.09とほぼ1であった.したがって,フェンタニルの薬物動態には人種差がないことが示唆された.
| Race | Japanese (A) | non-Japanese (B) | (A)/(B) | |||
|---|---|---|---|---|---|---|
| n | 40 | 33 | ||||
| mean | S.D. | mean | S.D. | |||
| Tmax | (h) | 30.8 | 12.2 | 23.6 | 10.4 | 1.31 |
| Cmax | (ng/mL) | 3.31 | 1.34 | 3.15 | 1.08 | 1.05 |
| t1/2 | (h) | 21.4a) | 5.8 | 19.9b) | 5.8 | 1.08 |
| AUC0→120 h | (ng·h/mL) | 189.5 | 58.7 | 176.8 | 52.5 | 1.07 |
| AUC0→∞ | (ng·h/mL) | 202.0 | 61.1 | 185.4 | 55.8 | 1.09 |
Pharmacokinetic parameters of Japanese and non-Japanese data were selected from an interview form for Durotep®MT patch at p. 20 and p. 21, respectively. Numbers a) and b) are 36 and 32, respectively (Tmax is time of maximum observed serum concentration, Cmax is maximum serum concentration, t1/2 is terminal elimination half-life, AUC is area under the concentration curve, AUC0→120 h is AUC from time zero to 120 h, AUC0→∞ is AUC from time zero extrapolated to infinite time).
デュロテップ®MTパッチ4.2, 8.4, 12.6及び16.8 mgを72 h単回貼付したときのCmaxと貼付用量は,正の相関(p<0.0001)を示した(n=31).したがって,デュロテップ®MTパッチにおいて,用量4.2–16.8 mgにおいて線形性が確認された.
4. デュロテップ®MTパッチ72 h単回貼付時の血中濃度推移と吸収速度の経時的変化SPLINE–デコンボリューション法により得られたデュロテップ®MTパッチ16.8 mgを72 h単回貼付後の血清フェンタニル濃度推移(点線)と吸収速度の時間推移(実線)をFig. 3に示した.得られた血清フェンタニル濃度推移上に読み取ったデータをプロットすると,良好なフィッティングが得られた(Fig. 3).血清中フェンタニル濃度推移をみると,定常状態における範囲は1.59–2.98 ng/mL(平均2.32 ng/mL)であり,術後鎮痛に必要である0.6–3 ng/mL2)の範囲内であった.SPLINE–デコンボリューション法により得られた吸収速度は,Lag time 0.26 hを経て急激に上昇し,10.7 hから剥離する72 hまで約20 hの周期で一定の振れ幅を持って上昇・下降を3回繰り返した後で,急激に下降し0.0141 mg/hとなり剥離後再度上昇したが,その後緩徐に減少した.吸収の定常状態における吸収速度の範囲は0.0594–0.131 mg/h(平均0.0924 mg/h)であった.一方,同時にプロットした血清フェンタニル濃度推移と吸収速度を比較すると,血中濃度は,吸収速度が先に上昇し,その後を追って上昇し,3つの振幅を経て,剥離後は吸収速度と比較するとゆっくり減少した.

Durotep®MT Patch was removed at 72 h. Serum fentanyl concentrations interpolated using the SPLINE function are shown as the dotted line, and measured data are plotted on that line. AR obtained by SPLINE–Deconvolution is shown as the solid line.
SPLINE–デコンボリューション法により得られたデュロテップ®MTパッチ16.8 mgを72 h単回貼付後のフェンタニルの吸収速度(実線)と累積吸収率(破線)の経時的変化を同時にプロットした(Fig. 4).吸収速度はLag timeを経て定常状態になり3つのピークがあるが,累積吸収率は剥離した72 hまでごくわずかな揺れはあるものの一定の割合で増加し,最終解析時間120 hまで持続的なゆるやかな上昇がみられた.貼付開始後120 hにおける累積吸収率,すなわちバイオアベイラビリティは44.2%であった.

Durotep®MT Patch was removed at 72 h. CAR is shown as the dashed line and AR is the solid line. CAR and AR were obtained by SPLINE–Deconvolution.
残渣法により求められた放出量,放出率及び定常状態における推定平均吸収速度をTable 2に示した.放出量は,ヤンセンファーマ株式会社の報告値は平均7.46 mg(健常成人,n=12)15)であった.一方,藤田らの報告値は,平均9.77 mg(患者,n=5)16)であり,放出率はヤンセンファーマ株式会社の報告値15)及び藤田らの値16)は,今回解析に用いたデュロテップ®MTパッチの規格値16.8 mgを基準にすると,各々44.4及び58.2%であった.ヤンセンファーマ株式会社の報告値15)及び藤田らの報告値16)から求めた定常状態における推定平均吸収速度は各々0.104及び0.136 mg/hであった.
| Method | Delivered amount (mg) | Absorbed amount (mg) | Delivered ratio or bioavailability (%) | Estimated mean absorption rate at steady state (mg/h) | |
|---|---|---|---|---|---|
| Residual method | Janssen Pharmaceutical K.K. Data15) (Healthy volunteer) | 7.46 | 44.4 | 0.104 | |
| Fujita S., et al.16) (Patient) | 9.77 | 58.2 | 0.136 | ||
| Absolute bioavailability method | 8.59 | 51.1 | 0.119 | ||
| Wagner–Nelson method6) | 8.22 | 48.9 | 0.114 | ||
| 3-Compartment model Loo–Riegelman Method8) | 7.88 | 46.9 | 0.109 | ||
| SPLINE–Deconvolution method9) | 7.43 | 44.2 | 0.103 | ||
Estimated mean absorption rate at steady state is calculated by absorbed or delivered amount divided by 72 h, which is the removal time. Explanation of precautions for use of new drugs for Durotep®MT Patch at pp. 75 (2010), Janssen Pharmaceutical K.K.15) Fujita S., et al., Jpn. J. Pharm. Palliat. Care Sci., 10, 47–52 (2017).16) Wagner J. G., et al., J. Pharm. Sci., 53, 1392–1403 (1964).6) Wagner J. G., J. Pharm Sci., 72, 838–842 (1983).8) Yamaoka K. and Tanigawara Y., “MyCom ni yoru yakubutu sokudoron nyumon,” Nankoudou Press, Tokyo, 1983, pp. 91–112.9)
算出したパラメータをTable 2に示した.ATすなわちA0→120 hはEq.(5)及びEq.(7)よりWagner–Nelson法及び3-コンパートメントモデルLoo–Reigelman法では各々8.13及び7.79 mgである.したがって,採血時間はパッチ剥離後45 h(貼付開始から120 h)と十分経過しているため,Bolus投与時の消失速度を使用し外挿によるAUC120 h→∞を求めて加えて計算すると,A∞(総吸収量)は各々8.22及び7.88 mgであった.一方,Eq.(3)及び(6)より求めた総吸収量は8.59 mgであった.バイオアベイラビティは,デュロテップ®Mパッチの規格である16.8 mgに対して求めると,各々,51.1, 48.9, 46.9及び44.2%であり,ヤンセンファーマ株式会社の値44.4%と近い値を示したのは,SPLINE–デコンボリューション法で得られた値であった.ヤンセンファーマ株式会社の放出量より求めた定常状態における推定平均吸収速度は0.104 mg/h,吸収量より算出した定常状態における推定平均吸収速度は,絶対的バイオアベイラビリティ法,Wagner–Nelson法,3-コンパートメントモデルLoo–Riegelman法及びSPLINE–デコンボリューション法の場合,各々,0.119, 0.114, 0.109及び0.103 mg/hであった.
8. フェンタニルの表皮層への残存放出量と吸収量の差は,表皮に残存する量となる.健常人のデータであるため,ヤンセンファーマ株式会社の放出量7.46 mg15)を基準にすると,その差は,絶対的バイオアベイラビリティ法,Wagner–Nelson法,3-コンパートメントモデルLoo–Riegelman法及びSPLINE–デコンボリューション法の場合,各々−1.13, −0.70, −0.01及び0.03 mgであった.皮膚への残存率は,負の値を除くと7.46 mgに対して0.4%であり,皮膚への残存はほとんどないことが示唆された.
SPLINE–デコンボリューション法により得られたデュロテップ®MTパッチ16.8 mgを72 h単回貼付後のパッチからのフェンタニルの吸収速度並びに累積吸収率の経時的変化をプロットした(Fig. 4).貼付後10.7 hから72 hの間,すなわち吸収の定常状態における吸収速度の3つの約20 h周期の上下の変動の要因として,膏体からのフェンタニルの放出の変動が考えられる.また,フェンタニルの貼付剤からの体内への吸収後に起きる腸肝循環,あるいは,その体内動態の日内変動による可能性が考えられる.大塚ら19)は,ラットに3H-フェンタニルを皮下注したとき,48 hまでの放射能胆汁中排泄率は50%で,そのうち73%が再吸収され腸肝循環に由来する可能性を示唆している.ヒトでの腸肝循環を検討した報告はない.ヒトにおいて,Bolus投与による負荷投与後,定速静注を行い定常状態になった後の血中濃度は,24 h一定に保たれることが報告されている.5)この際,腸肝循環において特徴的な血中濃度の上下の変動がみられない.また,吸収速度の変動に伴って変化する血中濃度が24 hにわたり一定であることから,日内変動の可能性は低いと考えられた.
デュロテップ®MTパッチを貼付後72 hで剥離した後の吸収速度の上昇がみられる.皮膚へのフェンタニルの蓄積に着目すると,貼付が終了してから最終採血時間120 hにおいて,SPLINE–デコンボリューション法により計算された吸収量とヤンセンファーマ株式会社の放出量の差は0.03 mgと計算された.したがって,最終的にはほとんど皮膚での残存がないと考えられる.もうひとつの要因として,SPLINE関数による採血ポイントの補間が良好でないことが影響する可能性があげられる.デュロテップ®MTパッチの場合,補間により得られた3次SPLINE曲線は,各データ点で急激な曲がり方が変化することもなく,滑らかに全データ点がつながっている曲線であることがわかる(Fig. 3).したがって,SPLINE関数による補間は適切であり,吸収速度の変化は,72 hに剥離後に生じた上昇も含め,得られた血中濃度の補間曲線に対応したものであることが示唆された.一方,剥離後に変曲点がみられない血中濃度推移の緩やかな下降を示すβ1遮断剤であるビソプロロールの経皮吸収剤ビソノ®テープ(トーアエイヨー株式会社,東京)の読み取ったデータの解析により,SPLINE関数による採血ポイントの補間が,剥離後の吸収速度の上昇にどの程度影響するか検証を行った.静脈内投与20)(t1/2; 10.3 h)及び貼付剤24 h単回貼付時(t1/2; 18.06 h)21)の血中濃度推移のデータを基にSPLINE–デコンボリューション法で解析を行うと,SPLINE関数による適切な採血ポイントの補間が確認され,それに対応して求められる吸収速度はほとんど上昇を示さなかった(Fig. 5).

Bisono®Tape was removed at 24 h Plasma bisoprolol levels interpolated using the SPLINE function are shown as the dotted line, and measured data are plotted on that line. AR obtained by SPLINE–Deconvolution is shown as the solid line [IV Data: Leopold G., et al., J. Clin. Pharmacol., 26, 616–621 (1986).20) Transdermal Data: Iwao Y. and Minami K., NIPPON GOMU KYOKAISHI, 87, 422–427 (2014)].21)
健常成人のBolus投与時のフェンタニルの消失半減期は,Vasishtらの報告12)の読取りデータより3.53 h, McClain DAらの報告値は3.65 h22)であった.デュロテップ®MTパッチの剥離後の消失半減期は,21.4 h4)であった.デュロテップ®MTパッチの場合,消失半減期が長くなるのは,フェンタニルの皮膚での分布が要因であると考えられる.佐藤ら23)は,パッチ製剤コンパートメントと血液コンパートメントとの間に,皮膚コンパートメントを置き,デュロテップ®MTパッチ2.1 mgを72 h単回貼付した時の薬物動態解析を行っている.得られたパラメータを用い,デュロテップ®MTパッチ2.1 mgを貼付時の,パッチ製剤と皮膚コンパートメントのフェンタニル量及び血液コンパートメントの血清フェンタニル濃度の変化をシミュレーションしている.皮膚コンパートメントのフェンタニル量の変化から,皮膚における蓄積は低いことが推測される.一方,剥離後のパッチ製剤のフェンタニル残存量は,シミュレーションカーブより,0.273 mgと算出される.ヤンセンファーマ株式会社の報告におけるデュロテップ®MTパッチ2.1 mgを単回貼付したときのパッチ製剤中フェンタニル残存量1.05 mg(n=12)15)と比較すると,シミュレーションデータで得られた残存量は実測値の26%であり,大きな差が認められた.また,今回の吸収速度の解析により,デュロテップ®MTパッチの吸収速度が一定でないため,体内への吸収速度を1次速度と仮定できない.したがって,用いられたフェンタニル貼付製剤のモデル解析には問題があると考えられた.皮膚でのフェンタニルの分布の今後の検討が必要と考えられる.
吸収量に関して,ヤンセンファーマ株式会社は健常成人で7.46 mg,15)藤田らの報告では,実際の患者からの剥離パッチで9.77 mg16)であり,比較的大きな差がある.その差の要因として,対象者の皮膚の温度差,脱水状態の程度の違いなどが考えられる.また,製剤のフェンタニルの残存量の測定時の問題,すなわち,測定法の違い並びに抽出率の違いなどがあげられる.全身作用型貼付剤であるビソノ®テープでは,皮膚の角層水分量と吸収量に関して,相関関係があったことが報告されている[相関係数:r=0.964(n=5)].24)薬物の性質にもよるが,フェンタニルの場合にも皮膚の乾燥の度合いに差に原因があるかもしれない.実際に患者の方がデュロテップ®MTパッチからのフェンタニルの放出量が大きかったため,フェンタニルの血中濃度測定は重要であると考えられる.
In vitroの方法での放出率,放出量,定常状態における推定平均吸収速度及びin vivoの方法により求めた吸収率,吸収量,並びに定常状態における推定平均吸収速度をTable 2に示した.吸収動態を解析するうえで,経時的変化を把握することは重要である.残渣法と絶対的バイオアベイラビリティ法は,最終的な吸収量及び吸収率を算出することはできるが,吸収速度の経時的変化を追うことができない.吸収量は,SPLINE–デコンボリューション法,Wagner–Nelson法及び3-コンパートメントモデルLoo–Reigelman法で,各々,7.43, 8.22及び7.88 mgであり,解析方法により差が認められた.この差が生じる要因として,Wagner–Nelson法及び3-コンパートメントモデルLoo–Reigelman法において,AUCの算出において用いる台形法が使われており,その計算結果の誤差が挙げられる.一方,デコンボリューション法の結果により吸収速度の上下の変化があることが示されたため,吸収が1次速度であるという仮定は成り立たない.したがって,デュロテップ®MTパッチに関して,Wagner–Nelson法及び3-コンパートメントモデルLoo–Reigelman法によるモデル解析は適さないと考えられる.また,モデルに関しては,フェンタニルは,3-コンパートメントモデルの挙動を示すことが報告されている.22) Wagner–Nelson法は1-コンパートメントモデルを仮定しているため,6)誤差が大きくなったと考えられた.3-コンパートメントモデルLoo–Reigelman法は3-コンパートメントモデルを仮定しているため,モデルによる誤差は相対的に少なかったと考えられた.
臨床上,目安として使われている定常状態における推定平均吸収速度について,最終的に得られた吸収量より算出すると,デュロテップ®MTパッチの場合,3-コンパートメントモデルLoo–Riegelman法及びSPLINE–デコンボリューション法の場合,吸収量から算出すると各々0.109及び0.103 mg/hであった.実際には,貼付後10.7–72 hの間の実際にみられた吸収の定常状態における平均吸収速度は0.0924 mg/hであった(Fig. 3).フェンタニル定速静注の投与速度は0.100 mg/hで有意な鎮痛効果を示すことが知られている.2,3)
SPLINE–デコンボリューション法は経時的に吸収速度並びに累積吸収率の経時的変化という重要な情報を得ることができる.また,徐放性製剤,吸入薬,坐薬などの体内への吸収動態の解析への応用も可能であると考える.したがって,SPLINE–デコンボリューション法は,吸収動態を解析するうえで今後更に重要な位置付けになると考えられる.
開示すべき利益相反関係はない.