2018 年 60 巻 7 号 p. 1353-1359
2018 年 60 巻 7 号 p. 1353-1359
当院では大腸憩室出血に対してEndoscopic Band Ligation(EBL)で治療を行ってきた.今までの経験から治療のポイントをお伝えする際に,治療全体をA:責任憩室の同定,B:EBL手技,C:治療後のマネージメントについて分けて説明する.
A:責任憩室の同定では,腸管蠕動が強まる前に責任憩室を同定することが重要である.また活動性の出血(Active Bleeding:AB)のみならずNon-Bleeding Visible Vessel(NBVV)やAdherent Clot(AC)といったStigmata of recent hemorrhage(SRH)を同定することが求められる.
B:EBL手技では効果的なマーキングクリップを行うため,2つのクリップを鳥居状に配置する事が重要である.バンドが不成功であった際にはクリップやボスミン局注を憩室の開口部の大きさをみて選択する.
C:治療後のマネージメントでは早期再出血への対応,少数例ながら本邦で報告されている穿孔例について情報を共有したい.
われわれは憩室出血に対してEndoscopic band ligation(EBL)での治療を行ってきた 1),2).EBLをA:責任憩室の同定,B:EBL手技,C:治療後のマネージメントに分けてそれぞれのポイントを説明する(Figure 1).

EBL法フローチャート.
●背景 大腸憩室について
●当院での緊急下部消化管出血プロトコール
本邦においては大腸憩室保有率が増加し,大腸憩室出血は増加傾向にある.下部消化管出血の原因として憩室出血は最大のものであり,当院で2009年1月から2013年9月に施行された緊急下部内視鏡検査のうち,51%(333例/654例)は憩室出血によるものであった.憩室出血の自然止血率は75-80%と高く,全例で内視鏡止血術が必要となる訳ではない 3).内視鏡治療が必要となるのは出血源であることを強く示唆するHigh risk stigmata of recent hemorrhage(SRH)を有する憩室である 4).High risk stigmata of recent hemorrhageとはActive Bleeding(AB),Non-bleeding visible vessel(NBVV),Adherent Clot(AC)である(Figure 2~4) 5).当院で2004年1月から2016年9月までの間に施行された憩室出血に対する初回緊急下部内視鏡検査370例中,明らかな責任憩室を同定できたdefinite diverticular hemorrhageは145例,SRHを有する憩室を指摘できなかったpresumptive diverticular hemorrhageが225例であった.145例のSRHに関しては ABが48例(33%),NBVVが42例(29%),ACが52例(36%),分類不能3例であった.活動性の出血のみを探そうとするのではなく,前処置をかけた状態で数ミリの露出血管を探す気持ちで慎重な観察を行う事が望ましい.出血源同定のためには,water jet scopeの使用や先端アタッチメントの装着が有用とされている 6).
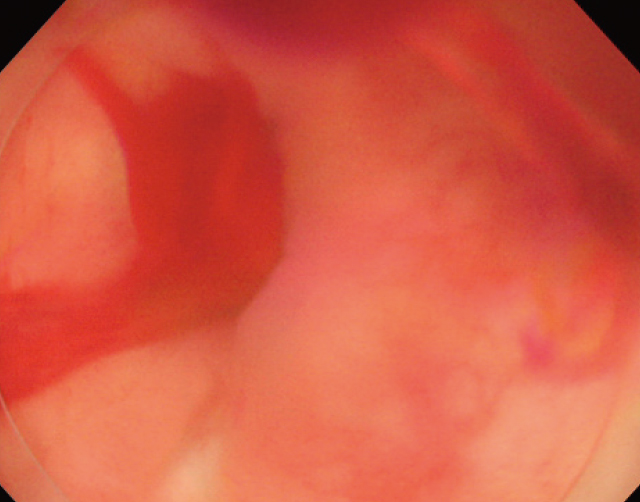
Active Bleeding(AB).
憩室から活動性出血を認める.
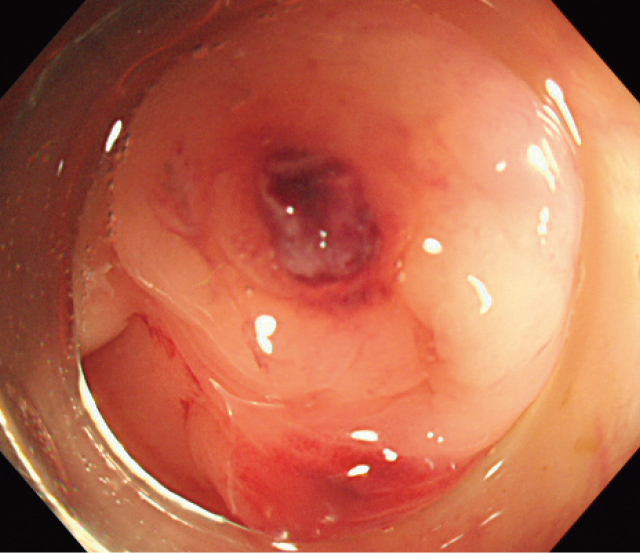
NonBleeding Visible Vessel(NBVV).
憩室内部をアタッチメントを装着したスコープで吸引し翻転させることでdome内の露出血管が確認された.

Adherent Clot(AC).
他の憩室にはみられない,強く付着した血餅を認める.凝血塊を洗浄で剥がすことで活動性出血を来す事や,露出血管が確認されることがある.
以下に当院での緊急下部内視鏡検査実施におけるプロトコールを示す(Figure 5).

緊急下部消化管出血.
バイタルが安定している下部消化管出血症例では,24時間以内に経口洗浄液を使用した前処置をかけて緊急下部内視鏡検査を施行する.明確な基準はないが,十分な補液によっても頻脈及び血圧低下が改善しない症例や輸血を要しその後も出血が継続している症例では,前処置をかけずに緊急下部消化管内視鏡検査を行う.
また被爆の問題は残るが,当院では出血源同定のために同意がとれた症例では全例造影CT検査を下部消化管内視鏡検査前に施行している.CT検査によって憩室出血以外の腫瘍等による出血や右側・左側等の憩室分布を把握した上で下部内視鏡検査を行うことが出血源同定率をあげると考え実施している.
●責任憩室の同定について
出血時には凝血塊が多く視野も悪い.いわゆる軸保持法での挿入は難しく,自然にループ形成を伴うケースも多い事からスコープは主に細径のOlympus PCF-H290Iを使用している.前処置を施行した症例では先端にアタッチメント(Olympus D-201-12704)を装着している.前処置が行えないケースでは凝血塊や憩室便がフード内に入り込むことが多くあえてアタッチメントを装着せずに挿入している.
強い腸管蠕動が起る前に責任憩室を同定できるかがポイントとなる.鎮痙剤が使用可能なケースではブチルスコポラミンやグルカゴンを検査時に使用する.ひとたび蠕動が強く起ると憩室自体が観察しづらくなるため,通常の半量を検査前に投与し,蠕動が強まった際に再度追加で投与するようにしている.Water jet scopeを使用しているが,凝血塊が非常に多く水洗のみでは剥がれないケースも多い.経口洗浄液をwater jet scopeから出し洗浄を行い対応している.しかしながらwater jet scopeからの大量の水洗を行う事は強い蠕動を誘発することにも繋がる.責任憩室を疑うエリアに到着後は洗浄チューブ(Olympus PW-1V-1)を用いて愛護的に憩室内の凝血塊を剥がす様にしている(Figure 6-a,b).

洗浄チューブを用いた観察.
a:アタッチメント先端を腸管壁に付着させ憩室内を水で満たすことで微小な露出血管も同定しやすくなる.
b:EBLを施行し憩室が翻転することでより露出血管が明瞭となった.
本邦で多いとされる右側の大腸憩室出血では左側と比し出血量が多く,出血源の同定や止血処置に難渋するケースが多い. Tamariらが報告したstep-clipping methodは初回下部消化管内視鏡検査で出血源を同定できなかった症例において有用と考えられる 7).当院においてもStep-clipping methodとは異なるが,初回観察時SRHを有する憩室か確証が得られなかったケースではマーキングクリップを積極的に施行している.憩室近傍にマーキングクリップを施行しておく事で次回の出血時に造影CT及び内視鏡検査で責任憩室を同定しEBLを施行可能であった例も多い(Figure 7~10).
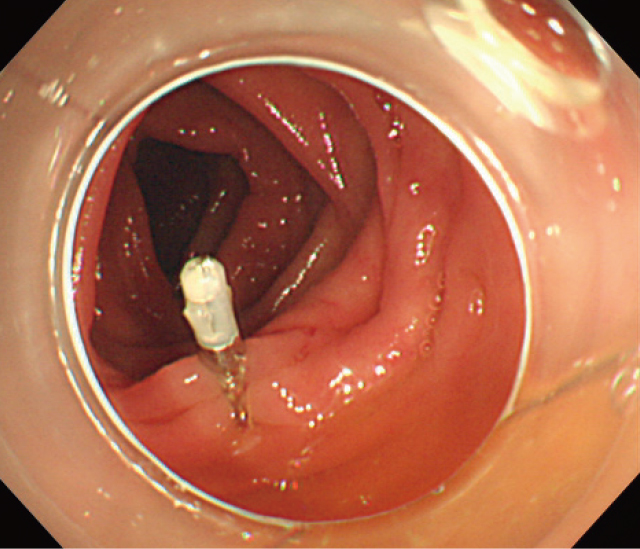
責任憩室か確証が得られなかった憩室へのマーキングクリップ.
初回観察時には自然止血されており,他の憩室と比較し凝血塊がやや多い程度の印象であった.

初回検査後に再出血を来たし施行したCT.
マーキングクリップが施行されている位置にextravasationを認め責任憩室と同定.

再検査時の活動性出血.
マーキングクリップ施行部位から活動性出血を認めEBLを施行.

EBL施行により止血.
翻転した憩室に露出血管を認めマーキングクリップを施行した憩室が責任憩室であったことが確認された.
造影CTでextravasationが不明な場合は一旦深部挿入し責任憩室の同定を開始する.挿入時にACやNBVVか判断に迷い確証がない憩室があった際には,マーキングクリップを施行し一旦全体の観察を優先している.実際にEBLを施行する際には後述するようにマーキングクリップの本数を増やすため,再挿入時にも責任憩室であるかは判断できる.造影CTでextravasationがあった際には,疑わしい部位からの観察にうつり蠕動がおこらないうちに責任憩室の同定を目指す.water jet scopeからの洗浄も行うが,憩室内部の観察時は洗浄チューブを使用して愛護的に血餅を除去する様に努める.先端アタッチメントと憩室内部を洗浄水で満たす事で露出血管の同定が行いやすくなる.
Scopeを再挿入する事から所用時間がかかるのではないかと指摘を頂く事も多いが,マーキングクリップを施行後は平均10-15分程度で処置が終了している 8).
当院で施行したEBL手技を動画で示す(電子動画 1).
電子動画1
責任憩室を同定後にマーキングクリップを留置する.同定時に止血されていたとしても再度出血を来すケースも多い.マーキングクリップは鳥居状に責任憩室の左右に行う(Figure 11).視野が狭くなるEBLデバイス挿入後に鳥居状のクリップ中央にスコープ先端が入ると自然に吸引操作に移る事が可能となる.再挿入時はデバイスにより視野が狭くなり,デバイスの先端は長くクリップ施行時とは内視鏡画面が異なる印象となる.憩室が多発している症例では,マーキングクリップにより事前に責任憩室ではない周囲の憩室を巾着状に縫縮し,責任憩室の誤認を防ぐ場合もある.活動性の出血で視野が保てない際にはボスミン1Aを生理食塩水 19mlで希釈した2万倍希釈ボスミン液を数ml局注することで一時止血が得られる事が多い.マーキングクリップの留置後は素早く内視鏡を抜去し,EBLデバイスとして食道静脈瘤治療に用いるデバイス(住友ベークライト MD-48710)を装着し再挿入する.デバイス内に憩室を十分に吸引できたことを確認しO-ringをリリースする.責任憩室がスコープ表面と直交するのであれば,自然に憩室が中央となる形で吸引しやすい.屈曲部では周囲の粘膜のみが吸引され憩室が翻転しづらいことがあるため,体位変換で憩室を吸引しやすい位置を探る.リリース後は愛護的に水洗することでスコープ先端を徐々に翻転した憩室から離す.無理にスコープを動かさず,アングル操作を避けることでO-ringがかかった部位が傷つかないようにする.止血が確認されたら,送気を最低限にしてスコープを抜去する.

鳥居状のマーキングクリップ.
EBLデバイス挿入後は視野が狭くなる.
責任憩室を見失わないために2つのクリップを憩室と同レベルで左右に留置する.
憩室が非常に多く硬い粘膜等ではバンドがかからず弾かれる事がある.当院の検討でも約5%程度の症例で憩室にバンドがかからずクリップ法や局注法を要した.開口部が大きい憩室でバンドがかからない際には,露出血管が確認出来る事が多くクリップで血管を把持する.開口部が小さく露出血管が視認できない場合,前述した2万倍希釈ボスミン液の局注で止血を試みる.右側の出血量が多い憩室でボスミン局注後に再出血した際には,血管塞栓術や外科的治療も考慮する.外科的な治療に移行することも考慮して,ボスミン液には少量の墨汁を混ぜて点墨を同時に行う.
早期再出血
EBL施行後30日以内の出血を早期再出血と定義している.EBL後には約10%程度の早期再出血がみられる.われわれは治療後の早期再出血を潰瘍底の種類から5つに分類している.①バンドの脱落②露出血管を有する潰瘍③露出血管が無い潰瘍④黄色/黒色の壊死組織⑤別の憩室からの出血である.対応は潰瘍底によって異なりバンドの脱落に対しては再度EBLを試みる.露出血管が視認できるケースではクリップを追加する.露出血管が無い潰瘍や黄色の壊死組織に対しては保存的な加療で経過観察が可能であった(Figure 12).治療後平均2日程度で再出血を来す事が多いが,特に1日以内の再出血はバンドの脱落を考慮して早期の内視鏡検査を行う 9).

早期再出血時の対応.
早期再出血時にはEBL後の潰瘍底により対応が異なる.
晩期再出血
EBL施行後30日移行の出血を晩期再出血と定義している.EBL施行後に潰瘍底は瘢痕化し憩室は消失する.しかしながら晩期再出血に関してはクリップ等での治療を行った際と出血率は概ね変わらない.当院のデータでは2004年1月から2014年11月までに施行した61例のEBL症例のうち21例に晩期再出血を来たした.同期間中にクリップ法で治療を行った39症例中26例に晩期再出血があり治療によって憩室が瘢痕化するEBLと再出血の率に優位差はみられなかった 10).治療後にも別の部位から再出血を来す事がある旨を患者にお伝えすることはクリップ法と変わらず重要な事である.
憩室炎
当院で施行した145例のEBL施行症例のうち1例に憩室炎を来した.幸い抗菌薬を使用した保存的な加療で手術を避けられたが治療後の腹痛時には後述する穿孔にも留意した経過観察が望ましい 11).
穿孔
当院では積極的に行っているEBLではあるが,残念ながら他施設より穿孔の報告例もある.左側結腸では比較的腸管壁が厚くEBL時に筋層が結紮されず,右側結腸では筋層も結紮されると報告されていた 12).しかしながら当初2例続いた穿孔報告は左側結腸に対してEBLを施行した基礎疾患を有するステロイド内服症例であった 13),14).創傷治癒が遷延することにより穿孔に繋がる可能性があると考慮されていたが,新たに他院からの報告で特に基礎疾患がない左側の若年者症例で穿孔を来した報告がなされた 15).全国でのEBL施行件数から考慮すると穿孔を来す率が高いとは言えないが,特に手技に問題が無いと考えられる症例でも穿孔に至った事が現時点では課題と言える.2017年12月現在ではデバイスは保険収載されておらず各施設で倫理委員会等の承認を受けて患者に十分な説明の元,治療にあたって頂きたい.
本論文内容に関連する著者の利益相反:なし