2019 年 61 巻 10 号 p. 2346-2352
2019 年 61 巻 10 号 p. 2346-2352
症例は13歳の健常男児.主訴は発熱,胸痛,食欲不振.上部消化管内視鏡検査にて,中部食道に境界明瞭な円形潰瘍を,下部食道に融合傾向を伴う縦走潰瘍を認めた.生検では,核腫大,核のスリガラス状変化を認め,抗単純ヘルペスウイルス(HSV)抗体による免疫染色が陽性であった.来院時血清抗HSV-IgG抗体は陰性であったが,回復期には抗HSV-IgG抗体が陽転化した.以上より,HSV初感染によるヘルペス食道炎と診断した.一般的にヘルペス食道炎は免疫不全患者にHSVの回帰感染によって発症し,初感染によるヘルペス食道炎の報告は本邦にはない.また,早期の抗ウイルス療法が著効し,内視鏡像も改善した.
ヘルペス食道炎は,単純ヘルペスウイルス(herpes simplex virus;HSV)による感染症で,悪性腫瘍や免疫不全などの基礎疾患を有する患者に多いとされ,その発生機序は,知覚神経節に潜伏感染するウイルスの再活性化による回帰発症が主と考えられている 1),2).健常人にも稀ながら発症することが知られている 3)が,本邦においてHSV初感染時にヘルペス食道炎を発症した報告はない.今回,単純ヘルペスウイルス初感染の健常小児に生じたヘルペス食道炎を経験したので報告する.
症例:13歳,男性.
主訴:発熱,食後の胸痛,食欲不振.
既往歴:虫垂炎手術(11歳).アレルギー疾患なし.
家族歴:父が喘息,祖父が脳卒中と糖尿病.
生活歴:喫煙なし,飲酒なし,ペットの飼育歴なし.
現病歴:生来健康.1カ月前から乾性咳嗽が出現し,1週間前から持続する発熱と食後の胸痛のため近医受診.気管支炎を疑われ,セフカペンピボキシル塩酸塩水和物錠(100mg)3錠/日を投与されるも胸痛改善せず,食事摂取困難となり,当科紹介受診となった.
身体所見:身長153.0cm,体重45.0kg.血圧126/74mmHg,脈拍96/分整,体温36.8℃.意識清明.口唇に異常所見なし.咽頭軽度発赤あり,扁桃腫大なし.心肺に異常なし.腹部は平坦軟で,圧痛を認めず.皮疹なし.表在リンパ節触知せず.
臨床検査成績:CRPの軽度上昇を認めた.血清抗HSV-IgM抗体は9.0(陰性:0.8未満)と陽性で,抗HSV-IgG抗体は陰性であった.抗サイトメガロウイルス(cytomegalovirus;CMV)-IgM抗体は陰性で,抗CMV-IgG抗体は5.9(陰性:2.0未満)と陽性であった(Table 1).

入院時臨床検査成績.
胸腹部CT:異常所見は認めず.
症状が強いため,上部消化管内視鏡検査について十分な説明を行い,患者も家族も同意されたため小児科医による鎮静下で検査を施行した.鎮静は,ミダゾラム0.1mg/kgを初回静脈投与し,検査中に適宜1mgずつ追加を行い,計9mgを使用した.検査中,血圧や呼吸状態は安定しており,良好な鎮静が得られた.
上部消化管内視鏡所見:中部食道の切歯列より26cmの7時方向に3mm大の小びらん,28cmの5時方向に5mm大の辺縁隆起を伴う境界明瞭な浅い円形潰瘍を認め,下部食道に融合傾向を伴う縦走潰瘍を複数認めた(Figure 1).下部食道の縦走潰瘍と食道胃接合部の間には正常粘膜が介在していた.中部食道の小びらん辺縁,円形潰瘍辺縁,下部食道の縦走潰瘍辺縁,潰瘍底より計4カ所生検を行った.
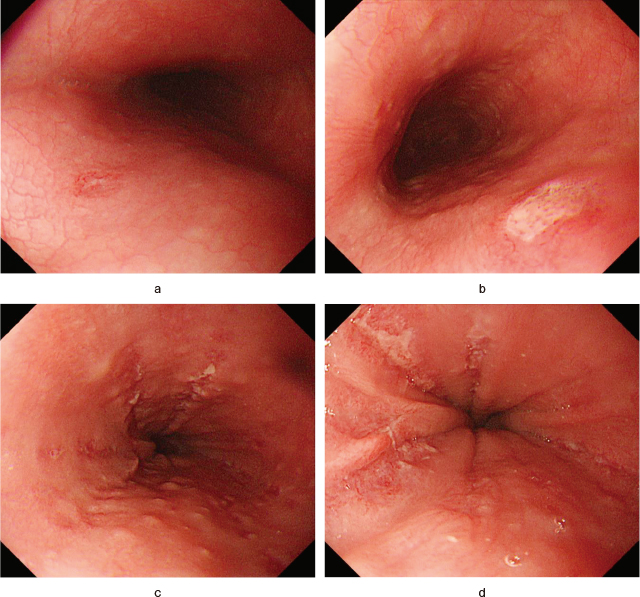
上部消化管内視鏡所見(第1病日).
a:中部食道(切歯列より26cm,7時方向)に3mm大の小びらんを認める.
b:中部食道(切歯列より28cm,5時方向)に5mm大の辺縁隆起を伴う境界明瞭な浅い円形潰瘍を認める.
c,d:下部食道に融合傾向を伴う縦走潰瘍を複数認める.
生検病理組織所見(下部食道の縦走潰瘍辺縁より採取):HE(ヘマトキシリン―エオジン)染色にて,核腫大と,スリガラス状の核内封入体(full型)を伴う扁平上皮細胞を複数認めた(Figure 2-a).抗HSV抗体による免疫組織化学染色では核に陽性所見を認めた(Figure 2-b).以上よりヘルペス食道炎と診断した.

生検病理組織所見.
a:核腫大と,スリガラス状の核内封入体(full型,矢印)を伴う扁平上皮細胞を複数認める(HE染色,×600).
b:抗HSV抗体による免疫組織化学染色では核に陽性所見(矢印)を認める(HSV免疫染色,×600).
臨床経過:胸痛による食欲不振,体重減少を認めるなど症状が非常に強く,内視鏡所見よりHSVあるいはCMVによる食道炎を疑い,血清抗体価や病理結果を待たずに内視鏡検査当日(第1病日)よりバラシクロビル塩酸塩錠1,000mg/日を7日間経口投与した.第4病日には症状は消失し,第14病日の血液検査ではCRPは陰性化した.内視鏡検査では,すべての潰瘍の白苔は消失し,完全な上皮化には至っていないが,一部びらんを混じた発赤調粘膜状態を呈していた(Figure 3).ペア血清において抗HSV-IgM抗体は11.37と更に上昇を認め,抗HSV-IgG抗体は7.3と陽転化しており,本症例はHSV初感染によるヘルペス食道炎であると診断した.抗HSV1-IgG抗体が4(陰性;4未満)と陽性であり,抗体HSV2-IgG抗体が4未満(陰性;4未満)と陰性であったことからHSV-1型による感染と考えられた.治療終了後も症状の再燃なく,経過良好である.

上部消化管内視鏡所見(第14病日).
a:中部食道.
b:下部食道.
すべての潰瘍の白苔は消失し,完全な上皮化には至っていないが,一部びらんを混じた発赤調粘膜状態を呈している.
感染性食道炎の三大原因病原体として,カンジダ,HSV,CMVが挙げられ,HSVやCMVによる食道炎は免疫不全状態でみられることが多く,カンジダによる食道炎に比して日常診療にて遭遇することは比較的稀である 4).
HSVによる感染症は不顕性感染から皮膚粘膜の限局性病変,中枢神経感染症,全身感染症に至るまで非常に多彩な病態を示す 5).HSVは1型と2型があり,HSV-1はおもに三叉神経節,HSV-2は腰仙骨神経節に潜伏する.潜伏感染したHSVは宿主の状態により再活性化し,回帰発症を引き起こす 5).
ヘルペス食道炎は,悪性腫瘍,後天性免疫不全症候群(AIDS),糖尿病,腎不全,重症熱傷,慢性閉塞性肺疾患,心血管障害,類天疱瘡などのさまざまな基礎疾患を有する免疫不全状態の患者や臓器移植後あるいは免疫抑制剤やステロイド投与中にHSV再活性化に伴う回帰発症としての報告が多い.本症例は,生来健康であり,治療後も良好な健康状態であることから免疫不全を呈する基礎疾患の存在は否定的である.発症1カ月前から乾性咳嗽があり,気管支炎等により体力低下していた可能性はあり,また,部活動での飲料の回し飲みが発症の原因の可能性はあるが推測の域を出ない.
ヘルペス食道炎は,HSV-1型によるものが多いが,稀ながら2型による報告もある 6),7).本症例では,回復期(第14病日)の抗体検査の結果よりHSV-1型による感染と考えられた.HSV-1型の初感染像の多くは,歯肉口内炎,ヘルペス疱疹,ヘルペス角結膜炎であり,健常人のHSV初感染時にヘルペス食道炎を発症した本邦報告例はない.
海外ではRodriguesら 8)が健常小児のヘルペス食道炎の6症例を報告しており,本症例と同様に,当初,抗HSV-IgM抗体陽性,抗HSV-IgG抗体陰性で,後に抗HSV-IgG抗体が陽転化したことで全例が初感染であったことを確認している.6例は1歳〜9歳(平均年齢4歳)で,発熱,体重減少を全例に,嚥下痛を5例に(残り1例は1歳のため評価不能),胸骨後痛を4例に,嘔吐を3例に認め,食道の粘膜傷害部の免疫組織学的検査によりHSV-1型による感染を証明している.Ramanathanら 3)は,小児例を含む38例の健常人発症のヘルペス食道炎報告例を検討し,8例(21.1%)でHSV初感染であり,健常人でのヘルペス食道炎ではHSV初感染例が相当数含まれると報告している.
初感染によるヘルペス食道炎と診断するためには,発症早期に内視鏡検査と血清抗体検査を行う必要がある.欧米と異なり,本邦で初感染のヘルペス性食道炎の報告がない理由としては以下が考えられる.成人の場合は,本邦において内視鏡検査の施行は容易であり,内視鏡所見よりヘルペス食道炎を疑う機会はあるものの,HSV初感染を疑われることが少なかった可能性がある.一方で,HSV初感染の機会が多いと考えられる小児においては,内視鏡検査を施行される機会が少なかったのかもしれない.欧米では小児消化器病専門医が小児の消化器内視鏡検査を行う体制となっているが,本邦では小児内視鏡の専門医は少ない.今後,小児内視鏡検査がより普及すれば初感染のヘルペス性食道炎の報告が増加する可能性はある.
一般的に,ヘルペス食道炎の症状は,嚥下痛,胸骨後痛,発熱が多く,嚥下障害,吐血や貧血,食欲不振などの重篤な症状を呈する例もある.健常人では対症療法のみで自然治癒することがほとんどとされる 9).本症例では,当初は発熱と咳などの軽度の症状であったが,食後の強い胸痛による高度の食欲不振を呈するようになり,感染性食道炎を疑い,内視鏡検査並びに血清抗体検査を施行した.
ヘルペス食道炎の内視鏡所見の特徴としては,病変は中部食道から下部食道に多く,初期には小水疱を形成し,水疱が潰れて上皮が脱落すると,発赤した辺縁隆起を伴う境界明瞭な潰瘍を形成する.潰瘍の形態から「火山口様」(volcano-like appearance)と表現されることもある.そして,進行すると潰瘍辺縁の粘膜上皮が白濁し,次第に融合し地図状となり,食道全体に広がる 10),11).本症例でも,中部食道には辺縁隆起を伴った境界明瞭な浅い潰瘍を認めた点では特徴的な像であった.下部食道に認めた縦走潰瘍は必ずしも特徴的所見ではなかったが,潰瘍が融合傾向であるという点はヘルペス食道炎の特徴を示していた.下部食道に認めた縦走潰瘍と食道胃接合部の間には正常粘膜が介在しており,逆流性食道炎の合併は否定的であった.
CMVによる食道炎も同様に中下部食道に潰瘍を形成し,ヘルペス食道炎との鑑別を要するが,一般に初期から地図状,蛇行状のびらんを認め,潰瘍がより大きく,ヘルペス食道炎の潰瘍に見られる辺縁隆起は認められない 10).このように,ヘルペス食道炎とCMVによる食道炎は内視鏡所見である程度鑑別可能であり,本症例においても中部食道で辺縁隆起を伴う小潰瘍を認めたことから,よりヘルペス食道炎を疑った.ただし,混合感染例も報告 4)されており,注意が必要である.
ヘルペス食道炎の病理所見では,表層性のびらんまたは粘膜下層にまでにとどまる浅い潰瘍で,潰瘍辺縁の扁平上皮細胞は風船様腫大や多核巨細胞化を認めることを特徴とする.ウイルス感染に特徴的な核内封入体は,full型(核のスリガラス状変化)やCowdry A型(周囲にhaloを伴った多数の核内封入体)であり 12),本症例ではfull型封入体を認めた.ヘルペス食道炎の特徴的な病理所見を得るためには,感染した扁平上皮を採取する必要があり,内視鏡検査時の生検は潰瘍底からではなく潰瘍辺縁から施行する必要がある 10).一方で,CMVは線維芽細胞と内皮細胞に感染するため,CMVによる食道炎を疑う場合は潰瘍底から生検を施行する必要がある 10).ヘルペス食道炎の診断のための生検は複数行う必要があり,本症例においても,特徴的な病理所見が得られたのは,縦走潰瘍辺縁からの生検のみであった.
ヘルペス食道炎の確定診断のためには,生検組織を用い,免疫組織化学染色によるHSV抗原の検出,PCR法によるウイルスDNAの検出,ウイルス培養等による病変局所におけるウイルスの証明が最終的には必要である.
本症の治療法としては,免疫不全状態の患者に対しては,アシクロビルの有用性が確立されているが,健常人では自然治癒することが多く,対症療法のみで6〜42日(平均17.5日)で改善すると報告されている 9).一方で,健常人のヘルペス食道炎に対してアシクロビルを投与した9例の検討では,8例が24〜72時間で治療への反応があり,全例4〜14日(平均9.3日)で合併症なく症状消失したという報告 13)があり,アシクロビル投与の臨床的有効性は高いと思われる.
健常人のヘルペス食道炎疑い患者に対し,対症療法あるいはPPI投与 14)で経過観察とするか,抗ウイルス薬投与を選択するかは現時点で明確な基準はない.臨床的には,ウイルス性食道炎の確診度と患者の症状での判断とならざるを得ない.本症例では,健常小児であり自然治癒の可能性はあったが,胸痛による食事摂取不可の状態であり,内視鏡所見よりHSVまたはCMVによる食道炎を強く疑ったためバラシクロビル塩酸塩錠を投与した.その結果,薬剤投与72時間後には症状は完全に消失した.健常人に対する抗ウイルス療法の有用性や適切な投与量あるいは投薬期間については,今後の更なる検討が必要である.
最近,海外においてヘルペス食道炎と好酸球性食道炎が併存したとする報告が増加している.Fritzら 15)は,健常小児におけるヘルペス食道炎において約半数に好酸球性食道炎を併発し,その多くにアレルギー疾患を有していたと報告している.併発するメカニズムに関しては,未治療の好酸球性食道炎が食道粘膜のバリア機能を破綻させHSVの易感染性を生ずるという説,逆に,ヘルペス食道炎が組織傷害と食道粘膜のバリア機能の破壊を引き起こし,強い免疫応答により好酸球性食道炎を引き起こすとする説がある 16).本症例では,初診時の内視鏡検査における食道粘膜生検にて有意な好酸球の浸潤を認めなかった.更に,抗ウイルス剤のバラシクロビル塩酸塩錠投与のみで症状の完全消失と食道病変の著明な改善が得られたこと,治療後内視鏡検査にて好酸球性食道炎を疑う所見を認めなかったこと,アレルギー疾患を有していなかったことから好酸球性食道炎の併発は考えにくく,侵襲性も考慮し治療後の内視鏡時には生検を施行しなかった.その後も症状の再燃なく,経過良好である.
健常小児に発症したHSV初感染に伴うヘルペス食道炎の症例を経験し,早期の抗ウイルス治療が奏効した.早期診断と適切な治療選択の観点からも内視鏡所見を熟知することが重要である.
本論文内容に関連する著者の利益相反:なし