2019 年 61 巻 2 号 p. 156-162
2019 年 61 巻 2 号 p. 156-162
症例1は51歳の男性で,メトロニダゾール(MNZ)治療抵抗性のため,近医より当院に紹介となった.症例2は53歳の男性で,当院にてアメーバ性大腸炎と診断された.両症例ともMNZを2コース投与したが,いずれも大腸内視鏡(CS)にて大腸に潰瘍の残存を認めた.MNZに続きパロモマイシン(PRM)の内服を行い,CSで治癒を確認した.両症例とも嚢子の残存がMNZ抵抗性の原因と考えられた.これまでの報告と今回の経験からMNZ治療終了2~3カ月にCSを行い,潰瘍が残存している場合はMNZ抵抗性と診断し,MNZとPRMの併用治療を行うのが良いと考えられた.
アメーバ性大腸炎は通常メトロニダゾール(metronidazole;MNZ)の内服で治癒が可能である.しかし,稀にMNZの内服でも治癒が得られない症例がみられる.その原因として,MNZの効果が不十分 1)や,嚢子の残存 2)などが考えられる.今回われわれは,MNZ投与にて治癒が得られなかった症例をMNZ抵抗性と定義し,自験2例を報告し,文献的考察を加える.
症例1:51歳,男性.
主訴:下痢,血便.
現病歴:当院を受診する約6カ月前から下痢を認めたため近医を受診した.大腸内視鏡(colonoscopy;CS)を施行され過敏性腸症候群と診断された.その4カ月後に下痢と血便を認めたため前医を受診し,CSを施行したところアメーバ性大腸炎と診断された.MNZ 750mg/日の内服を2週間行ったところ血便は消失した.しかし,下痢が持続するためMNZの内服終了約3カ月後に再度CSを施行したところ,盲腸に潰瘍の残存を認め,生検組織でアメーバの虫体が確認されたため,治療目的に当院に紹介となった.
初診時現症:発熱や腹痛は認めなかった.
血液検査所見:Hb 9.1g/dlと貧血を認めたが,CRPや白血球の異常は認めなかった.血中のアメーバ抗体は800倍と高値であった.
CS所見(Figure 1):盲腸から上行結腸中部まで白苔を伴うびらんを認める.特に盲腸は浮腫が強く,白苔を伴う易出血性のびらん・潰瘍が多発していた.
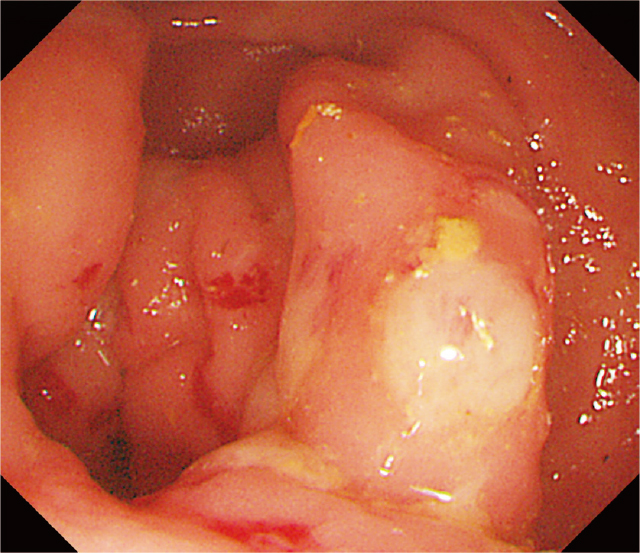
自験例1の当院での初回のCS.
盲腸:浮腫状であり,白苔を伴う易出血性の潰瘍・びらんが多発していた.
経過:病変部の白苔の鏡検にて,アメーバの栄養体と嚢子を確認したため,アメーバ性大腸炎と診断した.Comercial sex worker(以下CSW)との接触もなく,男性間性交渉者(以下MSM;men who have sex with men)でもないとのことであった.再感染を予防するため,感染経路を十分に説明した上で,MNZ 1,500mg/日を14日間投与した.治療後は下痢の改善を認めたが,治療終了約2カ月後に施行したCS(Figure 2)では,前回より改善はあるものの,盲腸から上行結腸にびらん・潰瘍は残存しており,生検組織でアメーバの栄養体を認めた.再感染の可能性は低くMNZ抵抗性と診断し,MNZ 750mg/日を10日間投与後に,パロモマイシン(paromomycine;PRM)1,500mg/日を10日間投与した.治療終了約2カ月後に施行したCS(Figure 3)で,内視鏡的に瘢痕がみられ治癒と診断した.
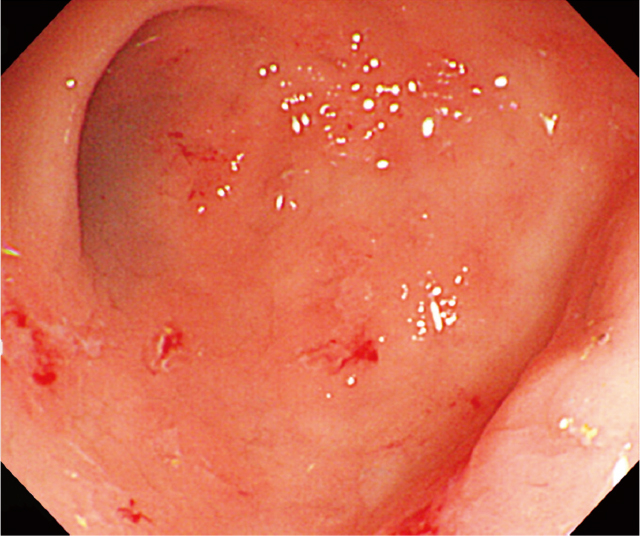
自験例1の当院での2回目のCS.
盲腸:前回より改善はあるものの,潰瘍,びらんは残存していた.
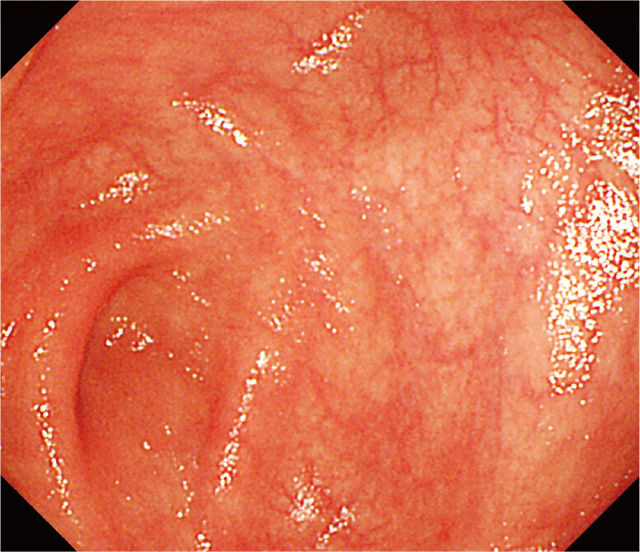
自験例1の治癒時のCS.
盲腸:びらん,潰瘍は瘢痕化しており,治癒を確認できた.
症例2:53歳,男性.
主訴:下腹部違和感,下痢.
現病歴:当院を受診する約1カ月前から下腹部違和感と下痢を認めていたため,精査目的に当院を受診した.
初診時現症:発熱や腹痛は認めなかった.
血液検査所見:WBC 14,730/mm3,CRP 1.46mg/dlと炎症反応の上昇,TP 6.1g/dl,Alb 2.7g/dlと低蛋白・低アルブミン血症を認めた.
CS所見(Figure 4):周囲に紅暈を伴う,白苔の付着するたこいぼ様の潰瘍を多数認めた.病変は全大腸に比較的均等に認められた.
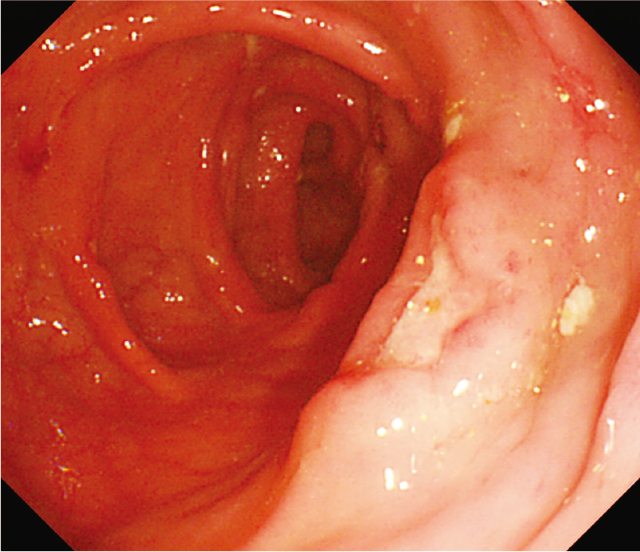
自験例2の当院での初回のCS.
上行結腸:周囲に紅暈を伴う,白苔の付着するたこいぼ様の潰瘍を認めた.
経過:CS時の白苔を鏡検にて,アメーバの栄養体が確認されたためアメーバ性大腸炎と診断した.CSWとの接触もなく,MSMでもないとのことであった.MNZ 750mg/日,10日間の内服を行ったところ,自覚症状の改善を認め臨床的に治癒と判断した.しかし,治療終了約2カ月後に再度下痢症状が出現し,同時期に施行したCS(Figure 5-a,b)では,全大腸に易出血性で粘液も付着する白苔を伴うびらん・潰瘍が多発していたことから,アメーバ性大腸炎と診断した.再感染の可能性も考え,感染経路を十分に説明した上で,患者と女性パートナーの両者にMNZ 750mg/日,10日間の治療を行った.その後は症状の再燃なく経過し,治療終了約3カ月後に治癒の確認目的にCSを施行した.盲腸には白苔を伴うたこいぼ様の潰瘍を多数認め(Figure 6-a),上行結腸と直腸(Figure 6-b)にも一部同様の病変を認めた.その他の部位には病変は認めなかった.以上より,再感染の可能性は低いと考え,MNZ抵抗性アメーバ性大腸炎と診断した.MNZ 1,500mg/日を10日間投与後にPRM 1,500mg/日の投与を行ったところ,治療終了約2カ月後のCSにて治癒を確認した(Figure 7).
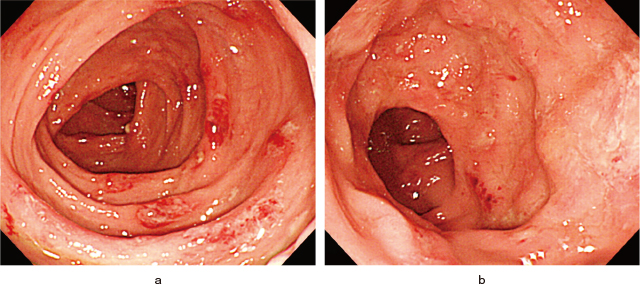
自験例2の当院での2回目のCS.
a:横行結腸.
b:直腸.
全大腸に易出血性で粘液も付着する白苔を伴うびらん・潰瘍が多発していた.
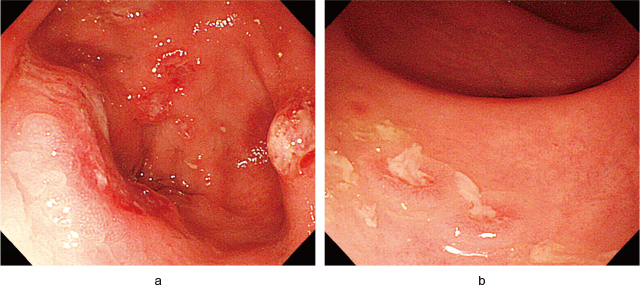
自験例2の当院での3日目のCS.
a:盲腸 白苔を伴うたこいぼ様の潰瘍を多数認めた.
b:直腸 直腸にも一部同様の病変を認めた.
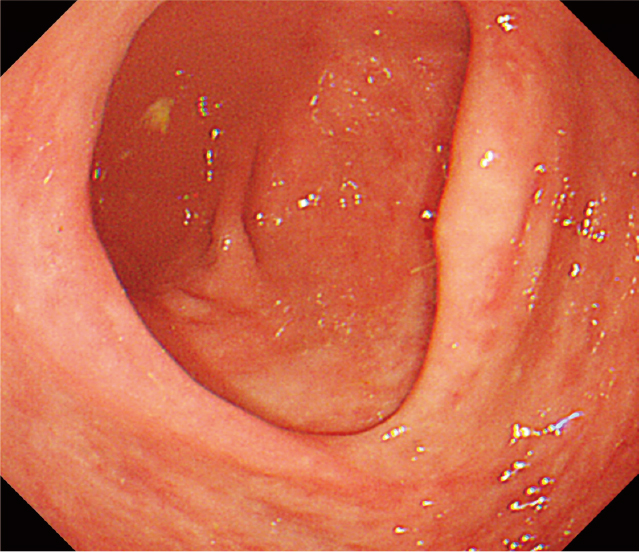
自験例2の当院での4回目のCS.
盲腸:びらん・潰瘍は瘢痕化していた.
赤痢アメーバ症の疫学は,最近の10年程で大きな変化が起こっている 3).男性の性的感染経路は,以前は同性間接触が多かったが,2008年には異性間接触が同性間接触を初めて上回った.2010年と2013年の比較では,無症候例が6%から19%に,CSで診断された症例が65%から73%に増加した.無症候例はCSで診断される症例が大部分であった 3).
アメーバ性大腸炎は,以前は法定伝染病に指定されてきたために,専門施設で隔離され治療されてきた.1999年には4類感染症となり隔離の必要がなくなり,2003年には5類感染症となり,7日以内に最寄りの保健所への届け出が義務付けられるのみとなった.これらを機に,それまで専門施設でのみ行われていた本症の治療は,多くは診断した施設において外来で行われることになった.
アメーバ性大腸炎はEntamoeba histolyticaの嚢子を経口摂取することにより感染する.嚢子は下部小腸で脱嚢して栄養体となり,その後は分裂を繰り返しながら大腸に到達する.盲腸でさらに分裂・増殖するが,組織内に侵入することで潰瘍を形成する.まず盲腸で潰瘍を形成し,さらに増殖して下行し,他の部位に潰瘍を形成すると考えられる.栄養体の一部は嚢子となり,糞便中に排泄されて感染源となる.病変が進行すると下痢や血便などの症状を引き起こす.直腸に病変があれば下痢がなくても血便を来すことが多い.一方,盲腸に限局している場合は無症状のことが多い 4).
大腸にEntamoeba histolyticaが定着した後,感染者の9割は無症状もしくは薬物治療を要さない極めて軽症の下痢を呈した後,自然軽快する.これらを無症候持続感染者と呼ぶが,多くは感染が持続し,10~20%が数カ月~数年以内に腸炎や肝膿瘍などの侵襲性アメーバ性大腸炎を発症すると報告されている 5).最近本邦では,便潜血検査陽性が理由で行うCSや人間ドックのCSで発見される無症候性持続感染者の報告が増加している 6).その大部分は盲腸に限局した潰瘍性病変である 4),7),8).これらの症例では,糞便検査で嚢子を認めることは稀であり,非侵襲的検査による診断は困難である 5).渡辺らは,無症候性持続感染者は数カ月~数年にわたり断続的に嚢子を排泄するとしている 5).
嚢子は厚い壁で覆われており,ヒト体外の環境中で長期間生存することが可能である.一方,栄養体はヒト体外環境中では長く生存できないが,腸管内で定着し増殖することができる.感染様式には2つあり,発展途上国では嚢子に汚染された水や食物を介してヒトへの感染拡大が起こる.一方先進国では,MSMやCSWとの接触が多くを占め,ヒト体外環境を介さない感染拡大が起こっている 5).
MNZは腸管から吸収され,栄養体に効果を示すが,嚢子には効果がない.一方,PRMは便中への嚢子の排出をとめる薬剤(luminal agent)であり,栄養体には効果を示さない.MNZ抵抗性アメーバ性大腸炎には,栄養体に対する効果が不十分であるものと,栄養体は消滅させるが嚢子の残存のためアメーバ性大腸炎が治癒しないものがある.前者のなかで,最初から症状が消失しないものは明らかであるが,症状が消失するが効果が不十分で潰瘍が残存するものと後者の鑑別はCSを行わないと不可能である.
医学中央雑誌で『アメーバ性大腸炎,再発』『アメーバ性大腸炎,難治』『アメーバ性大腸炎,MNZ抵抗性』をキーワードとして用いて1976年から2016年まで検索したが,会議録を除くと本邦ではMNZ抵抗性は2例であった.自験例含めた4例のなかで,一旦症状が軽快した再発例は3例であった(Table 1) 1),2).
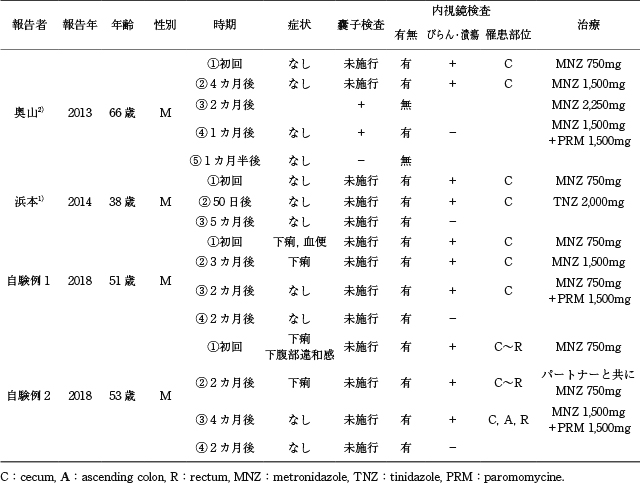
MNZ抵抗性アメーバ性大腸炎の本邦報告例.
奥山らの報告した症例Aは 2),MNZ1回目投与4カ月後のCSにて盲腸のびらんを認めた.次いでMNZ2回目の投与2カ月後の便検査で嚢子を認めた.MNZ3回目投与1カ月後のCSで盲腸のびらんは消失したが,便検査で嚢子は残存していた.その後MNZとPRMの併用により嚢子の消失を確認し治療を終了した.本例では1回目のMNZ投与の4カ月後では嚢子による潰瘍の再発と考えられた.一方,3回目のMNZ投与の1カ月後では潰瘍は治癒しており,その後に嚢子による再発が起こったと推測された.このことより嚢子による再発を確認するためには治療終了1カ月後の観察では短すぎると考えられた.
浜本らが報告した症例Bは 1),MNZ750mg/日を10日間投与した約50日後にCSを行ったところ,盲腸の潰瘍が残存し,チニダゾール2,000mg/日を10日投与後に治癒した.本例はMNZに抵抗性であったと考えられるが,増量により効果があった可能性も否定できない.チニダゾールで治癒していることより,嚢子の関与はなかったものと考えられる.
自験例1は当院での1回目の治療では,3カ月後のCS施行前から自覚症状があり,内視鏡でも盲腸に潰瘍を認めた.2回目の治療では2カ月後にCSで潰瘍を認めたが,自覚症状はなかった.自験例2は1回目の治療では2カ月後のCS施行前から自覚症状があり,CSでも潰瘍を認めた.2回目の治療では4カ月後CSにて潰瘍を認めたが,症状はなかった.自験2例とも,治療後に無症候性持続感染の状態となっており,その後治療しなければ時間の経過とともに症状が出現したと思われる.2症例ともに最終的にMNZとPRMの併用で治癒したことから,嚢子の残存による再発と考えられた.
再発部位に関しては,CSで病変を確認できた全例で盲腸に病変がみられた.このことより内視鏡による治癒判定では全大腸内視鏡検査を行うことが必要と考えられた.盲腸に病変が認められた理由としては,残存した嚢子が盲腸で増殖して潰瘍を作った可能性が考えられ,元々便が貯留しやすい部位であることも関係していると考えられた.
本邦における治癒判定は,MNZ治療終了後1~2週で糞便検査を行い原虫が陰性 9),あるいは治療後2~3カ月以上臨床的再発がなく,糞便検査で原虫が陰性 10)とされている.糞便中に嚢子が残存している場合にPRMを用いるとしている.しかし,専門施設以外でアメーバ原虫の便検査はほとんど行われていない.便検査は37℃に保ちながら速やかに鏡検の必要があり,判定にも熟練を要する.感度も40〜50%程度であり偽陰性が多い 11).感度を高めるためには新鮮便の3日間の検査が推奨されているが,外来ではほぼ不可能である 10).そのため多くの病院ではCSでの治癒の確認,あるいは症状の消失で治癒と判定している.CSを勧めても症状が治れば拒絶する患者も比較的多く,CSも行われないことが多いのが実情である.そのため,実際の再発率は不明である.しかし,今回のような再発例の報告は少ないため,多くは1コースのMNZの投与で治癒している可能性が高い.
臨床症状が軽快しても,治癒したとは限らない.例えば盲腸に潰瘍が残存し,その後時間が経過して臨床症状がでる場合もあり得るため,再発と再感染の区別がつかないからである.これを区別するには治療後できるだけ短期間でCSにて治癒を確認することが望ましい.CSによる潰瘍の治癒時期に関しては短いものでは1〜2カ月という報告が多い 12),13).自験例1と自験例2はともに嚢子による再発と考えられたが,自験例1では3カ月後と2カ月後に,自験例2では2カ月後と4カ月後にCSで潰瘍がみられた.一方,症例Aでは4カ月後には嚢子による潰瘍再発は認めたが,1カ月後では潰瘍再発はみられなかったが嚢子はみられた.以上のことから治療終了2~3カ月後にCSをすればMNZ抵抗性の診断はほぼ可能と推測された.
本邦ではPRMは保険収載されて間もなく,使用経験は少ない.本邦においては,多くの症例がMNZ内服1コースの治療で治癒するため,全例にPRMを併用する必要はないと考えられる.嚢子の便検査が難しい一般施設では,前述したようにMNZ治療終了2~3カ月後にCSを行い,MNZ抵抗性と診断した場合にMNZとPRMの併用療法を行えば良いと考えられた.今後,このような症例を蓄積することでMNZ抵抗性の実態も明らかになると思われる.
MNZに続きPRMの内服を行い,治癒せしめたMNZ抵抗性アメーバ性大腸炎の2例を報告した.両症例とも嚢子の残存がMNZ抵抗性の原因と考えられた.
本論文内容に関連する著者の利益相反:なし