2021 年 63 巻 9 号 p. 1573-1587
2021 年 63 巻 9 号 p. 1573-1587
消化性潰瘍の発症はHelicobacter pylori感染と非ステロイド性抗炎症薬(NSAIDs)を含む薬剤の使用が2大要因であるが,本邦ではH. pyloriの感染率の低下と酸分泌抑制薬の普及により,その罹患率は急激に減少しつつある.また,超高齢化を迎え,薬剤起因性の消化性潰瘍が占める率が高まり,日常臨床の現場ではその対策にも注意を払うべきである.2020年に「消化性潰瘍診療ガイドライン」が改訂され,新たな酸分泌抑制薬の使用方法,H. pylori除菌治療の選択法,NSAIDs内服者への対応,特発性潰瘍の対応などエビデンスの蓄積により新たな指針も示された.上部消化管内視鏡を使用した検診の需要も増し,H. pyloriの総除菌時代を迎える中で上部消化管内視鏡検査の役割はどのように果たすべきだろうか.本稿では,「消化性潰瘍診療ガイドライン」の改訂に合わせ,臨床の現場で遭遇する消化性潰瘍診療における問題点やガイドラインの改訂点,上部消化管内視鏡検査の重要性や役割について解説する.
高齢化社会,生活環境の変化,食生活の欧米化,ヘリコバクターピロリ菌(Helicobacter pylori)の感染率の低下などにより,日本人の酸分泌能が増加していることが報告され 1),いわゆる酸関連疾患の罹患率が増加傾向を示すことが予想されている.しかしながら,酸関連疾患の代表疾患である胃潰瘍と十二指腸潰瘍を含む消化性潰瘍の有病率は,消化性潰瘍の最大の原因であるH. pyloriの感染率の低下と強力な酸分泌抑制剤の普及により減少傾向を示している(Figure 1).2020年に発刊された「消化性潰瘍診療ガイドライン2020」では,非専門医に対する啓蒙と知っておくべき実際の対応策を明確に掲示するとともに,専門医にも日常臨床の現場で消化性潰瘍診療のバイブルとなるよう,最近のエビデンスを網羅する形で改訂された(Figure 2) 2).本ガイドラインでは新たな試みとして,臨床の現場で遭遇する主に治療や予防に関する疑問点をCQ(clinical question)と位置づけ,更に過去のエビデンスとして結論が出ているものをBQ(background question)とし,今後の更なるエビデンスの蓄積が必要な研究課題をFRQ(future research question)として区別することで,現時点における消化性潰瘍診療の課題を浮き彫りにした.昨今の国民総除菌時代の中で上部消化管内視鏡検査の重要性は増すばかりであり,近年,新たな内視鏡観察法として,narrow band imaging(NBI)やblue laser imaging(BLI),linked color imaging(LCI)などの画像強調観察(IEE)による胃癌や前癌病変の検出の有用性も示されている.本稿ではH. pyloriの総除菌時代における臨床の現場で遭遇する消化性潰瘍診療における問題点や消化性潰瘍診療ガイドラインの改訂点,上部消化管内視鏡検査の重要性や役割について解説する.

消化性潰瘍の罹患率の変遷;厚生労働省大臣官房統計情報部が報告する2017年の患者調査(傷病分類編)( https://www.mhlw.go.jp/toukei/saikin/hw/kanja/10syoubyo/dl/h29syobyo.pdf).

消化性潰瘍診療ガイドライン2020の消化性潰瘍の治療のフローチャート 2).
NSAIDS:非ステロイド性抗炎症薬,PPI:プロトンポンプ阻害薬,H2RA:ヒスタミン受容体拮抗薬,P-CAB:カリウムイオン競合型酸阻害薬.
厚生労働省大臣官房統計情報部が報告する2017年の患者調査(傷病分類編)を参照すると2017年の胃潰瘍の症例は20,100人,十二指腸潰瘍は3,300人,消化性潰瘍は23,700人であり,1984年と比較して17.8%(20,100/112,800人),7.3%(3,300/45,200人),14.4%(23,700/164,300人)と急激に減少している(Figure 1).また消化性潰瘍症例の年齢構成は1984年と比較して高齢化してきており,原因としてNSAIDsや低用量アスピリン(LDA)を内服する高齢者が多くなってきていることが大きいと考えられる.
新たな内視鏡機器の開発や改良により,内視鏡検査の画質は格段に進歩し,腫瘍や背景胃粘膜の質的診断や評価が比較的容易にできるようになってきている.これまでは,本邦ではH. pylori感染者が多いためにH. pylori陽性者を中心とした内視鏡診療であったが,保険適用拡大に伴うH. pylori除菌治療の普及や衛生環境の改善により本邦のH. pylori感染率は30-40%に低下し,内視鏡診療の対象者はH. pylori陽性者からH. pylori未感染者や除菌治療後の症例に移り変わりつつある 3),4).そのため,胃内環境に応じて適切な内視鏡診療を提供する必要があり,H. pyloriの感染状況の特徴を踏まえた内視鏡評価が重要となる.
現在,萎縮性胃炎の重症度や胃癌の高危険群を選別するために多数のスコアリングシステムが開発されているが,本邦では内視鏡検査を使用した京都胃炎分類によるリスク評価の有用性が報告されている 5),6).京都胃炎分類はH. pylori感染の特徴を示す所見により未感染・現感染・既感染を判断し,5つの評価項目(萎縮,腸上皮化生,粘膜ひだ腫大,鳥肌,びまん性発赤)を点数化し,胃癌リスクの層別化を行う(Table 1) 5)~7).H. pylori未感染者の特徴的な内視鏡所見は,胃粘膜の発赤性変化や萎縮性変化を認めず,粘膜上皮下に存在する集合細静脈が規則正しく配列する微小な発赤点であるRAC(regular arrangement of collecting venules)が胃角部から胃体下部の小彎に観察できる点である.ただし,胃粘膜萎縮が進行する前に除菌治療を行った場合には,びまん性発赤が改善した後に残存する胃粘膜にRACを認めることがあるため,未感染症例との鑑別に注意を要する.また一般的にH. pylori未感染者の胃粘膜の表面は平滑,かつ光沢を認め,胃内にみられる粘液は漿液性であることが多いことも特徴であり,Table 1で示すように胃底腺ポリープやヘマチン,稜線状発赤が認められることがある.

京都胃炎分類 7).
一方,H. pyloriの現感染者の胃粘膜の特徴は胃粘膜萎縮や腸上皮化生であり,現感染は炎症細胞浸潤の影響によるびまん性発赤,粘膜腫脹,粘膜ひだ腫大,白濁粘液があげられる.胃粘膜萎縮や腸上皮化生,黄色腫などはH. pylori感染の特徴ではあるものの,除菌後も残存するため現感染と既感染との鑑別はできないため注意を要する.また,胃癌発症のリスクの層別化を行う際の既感染症例における注意すべき所見に地図状発赤がある.地図状発赤は除菌治療により胃粘膜の発赤が消退するため,萎縮がない胃底腺領域は白色調となり,萎縮や腸上皮化生に発赤が残存するため色調逆転現象として観察される.ただし,地図状発赤は病理組織学的に腸上皮化生であることが報告されているが 8),除菌治療前に存在するすべての腸上皮化生が地図状発赤として観察されるわけではなく,除菌治療前に地図状発赤の出現を予測する内視鏡所見も同定されていない.また,最近報告されたメタアナリシスでは最も未感染者の診断をできる所見はRAC(感度:78.3%,特異度:78.3%)であり,現感染は粘膜浮腫(感度:63.7%,特異度:91.1%)であった 9).一方,地図状発赤は既感染例の絞り込みに特異度99.0%と高かったが,感度は13.0%と低いため 9),注意を要することを警告している.
京都胃炎分類の活用の意義は内視鏡診療でH. pylori感染状況を的確に把握し,胃癌発症のリスクの層別化を図ることを目標とした点であろう.われわれは1,200名の対象者を京都胃炎スコアで評価し,早期胃癌症例では萎縮スコアと腸上皮化生スコアが,非胃癌の慢性胃炎例よりも有意に高く,多変量解析では男性[オッズ比(OR):1.737,95% CI:1.102-2.739,p=0.017]と腸上皮化生(4.453,3.332-5.950,p<0.001)のみが早期胃癌の有意なリスク因子であることを報告した 6).今後は本スコアリングが未分化型胃癌のリスク評価に有効であるか否か,新たな項目の追加の必要性があるか否か,各項目の重みづけを変更する必要性があるか否かなどにつき検討する必要がある.内視鏡診療の現場では高度の萎縮性胃炎や腸上皮化生が分化型腺癌の危険因子であり,鳥肌や粘膜ひだ腫大が未分化型胃癌の危険因子であることを認識し,個々の症例で胃全体を適切に評価し,胃癌のリスクの層別化を的確に行う必要がある.
Ⅱ)欧米諸国の胃癌診療における内視鏡検査の現状と立ち位置胃炎・胃癌診療における診断治療法やサーベイランス法は世界各地で異なる.欧州では定期的な内視鏡検査とともにOLGA/OLGIM分類を使用して胃全体の胃粘膜萎縮や腸上皮化生の広がりを評価し,胃癌リスクの層別化をすることを基本としている 10).MAPS Ⅱは欧州の関連4学会が中心となって作成された胃癌診療ガイドラインの改訂版であり,胃粘膜萎縮と腸上皮化生を胃癌のリスク因子とし,H. pyloriの持続感染,胃癌の家族歴,自己免疫性胃炎の有無によりサーベイランス方法の推奨度が異なることが特徴である(Figure 3) 11).本ガイドラインは,欧州の内視鏡医は慢性胃炎や胃腫瘍の内視鏡診断に精通していないために内視鏡検査のみで診断を行うことは避けるべきであり,背景胃粘膜の病理組織学的な評価や腫瘍の質的診断を必須としている.本邦では病理組織学的な評価の有用性は認知されているものの,複数箇所の生検に伴う処置の煩雑さや生検後の出血が危惧され,一般臨床の現場で胃癌リスクの層別化を目的として経年的に胃粘膜萎縮や腸上皮化生の病理組織学的評価を行うことは一般的ではない.
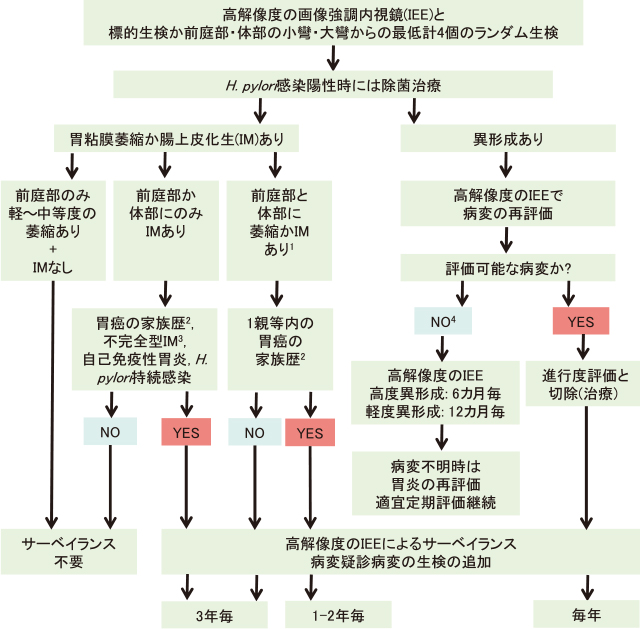
MAPS 2nd version:胃粘膜萎縮,腸上皮化生,異形成の患者における管理方法 11).
1.サーベイランスが必要な症例はOLGA/OLGIM分類のステージⅢ/Ⅳに相当する症例とされるべきである.腸上皮化生のない萎縮症例は,範囲に関わらず高危険群と捉えるべきではない.
2.第一親等の胃癌家族歴が胃癌の重要なリスク因子であり,厳重な定期評価が必要である.ただし,遺伝性/家族性胃癌には該当しない.
3.不完全型の腸上皮化生は胃癌高危険群の選定に有用だが,未だエビデンスは不足している.
4.異形成の診断後にIEEでも診断できない場合は,消化器専門の病理医により再診断を依頼するべきである.専門家に異形成が否定された場合は経過観察を行う必要はない.
本邦では一般的に白色光観察による評価を基本とし,診断能の向上のため拡大内視鏡検査やIEEを積極的に併用していくことが推奨されているが,欧米での考え方は白色光観察では胃の前癌状態の鑑別診断はできないことを前提とし(MAPS Ⅰ) 12),病理組織学的評価と高画質の色素内視鏡検査やIEEによって診断することの重要性を強調している.また,Figure 3の右側では病理組織で異形成を認めた症例の中で病変の認識ができる場合とできない場合で対応が異なるが,これは慢性胃炎の重症度評価のランダム生検を施行した際に偶然異形成の組織が混入する事態が多いことに起因していることが考えられる.本邦では標的生検で腫瘍の存在や組織型を評価することが多いため,このような事態となる機会は少ないものと思われる.
内視鏡サーベイランスの間隔はH. pylori診療を行う上で重要な課題である.胃癌の発症率は萎縮性胃炎症例で0.1-0.25%,腸上皮化生症例で0.25%であり,全体で胃腫瘍の発症は1.36人年に達すると報告されている 13),14).また,欧州からの報告で萎縮性胃炎症例では20年の経過観察で2.0%,腸上皮化生症例で2.5%の胃癌が発症すると報告され 15),本邦からの報告では高度萎縮性胃炎例で5年にて1.9-10%,腸上皮化生例で5.3-9.8%と報告されている 16).MAPS Ⅱでは萎縮や腸上皮化生の進展度に注目し,前庭部に限局する軽度萎縮例ではサーベイランスの有効性はないこと,病理組織学的に高度萎縮と腸上皮化生が確認されて初めてサーベイランスの意義があると示している.ただし,サーベイランスの間隔は,OLGA/OLGIM分類のステージ Ⅲ/Ⅳで3年毎の施行を推奨しているが,本邦は胃癌の発症率が高く,H. pyloriの感染歴がある症例は毎年内視鏡検査を行うことが必要であるため,サーベイランス間隔の推奨度は欧米諸国と異なる点に注意が必要である.
Ⅲ)H. pylori除菌後胃癌1997年に報告された症例対照研究では,高度萎縮例や広範囲に広がる腸上皮化生例では胃癌発症のリスクが高く,除菌治療による異時性癌の発症抑制効果は乏しいことが報告された 17).本邦で行われた前向き多施設ランダム化比較試験(RCT)では,3年間の経過観察で除菌治療により異時性胃癌発症のハザード比が0.339(95%CI:0.157-0.729)に抑制されることが示され 18),韓国の前向きプラセボ対象RCTでも,観察期間の中央値が5.9年で,異時性胃癌の発症率は除菌群で7.2%,プラセボ群で13.4%,ハザード比が0.50(95%CI:0.26-0.94)と,長期にわたる経過観察でも抑制効果があることが証明された 19).その後同様の研究がアジアを中心に行われ,それらをまとめたメタアナリシスでは,萎縮性胃炎例の胃癌発症は除菌例で162.3人年/100,000人年(72.5-588.2),未除菌例で272.7人年/100,000人年(180.4-322.4)であり,内視鏡治療後の異時性癌は除菌例で1,126.2人年/ 100,000人年(678.7-1,223.1),未除菌例で1,790.7人年/100,000人年(406.5-2,941.2)と,除菌治療により胃癌発症が有意に抑制されること,萎縮性胃炎例よりも異時性癌の方が胃癌発症の危険率が高いことが示された 20).
RCTを対象とした検討では胃癌発症に対するハザード比は萎縮性胃炎例で0.67(95%CI:0.47-0.96),異時性胃癌例で0.51(0.36-0.73)と除菌治療により40-60%の胃癌予防効果があることが示された(Figure 4) 20).以前は除菌治療対象者が萎縮性胃炎か,内視鏡治療後かにより胃癌抑制効果が異なると報告されていたが,このメタアナリシスでは初発癌でも異時性癌でも抑制効果は同等であった.また,欧米諸国の胃癌発症率は東アジア地域と比較して低く,除菌治療による胃発癌抑制効果を検討した報告は少ないが,近年大規模なコホート研究が行われ,東アジア地域と同様に除菌後に胃癌発症抑制効果があることが示された 21),22).

H. pylori除菌治療後の胃癌の発症リスク:メタアナリシス 20).
a:ランダム化比較試験(RCT)を使用した萎縮性胃炎例の初発胃癌に対する除菌治療の効果.
b:コホート研究を使用した萎縮性胃炎症例の初発胃癌に対する除菌治療の効果.
c:RCTを使用した内視鏡治療後の異時性胃癌の除菌治療の効果.
d:コホート研究を使用した内視鏡治療後の異時性胃癌の除菌治療の効果.
また,Takeらは,除菌後最長21.4年(平均7.4年)にわたる長期経過の除菌後胃癌の発症率を検討し,年間胃発癌率が0.35%であること,除菌後胃癌の危険性は胃粘膜萎縮の重症度で大きく異なること示した 23).注目すべきこととして,分化型腺癌の発症は除菌後10年以内に多いが,10年以降は未分化型癌が多く認められ,未分化型癌が発症した例では除菌前の胃粘膜萎縮の程度が軽度-中等症であったことである.今後H. pyloriの感染率が低下する中で胃癌の発症率も徐々に低下することが予想されるが,除菌後胃癌の比率は増加するため,現感染胃癌と除菌後胃癌の臨床的特徴の違いを捉えて的確な診療を行うことも重要である.
Ⅳ)H. pylori除菌後の胃食道逆流症/逆流性食道炎本邦の逆流性食道炎の罹患率は,この17年間で男性は6.6倍に,女性は2.7倍に増加したことが報告された 24).H. pylori感染と逆流性食道炎の発症は逆相関を示すため,この結果はH. pylori感染率が低下してきている現状を如実に表した結果と考えられる.実際にH. pylori陽性者では逆流性食道炎の有病率は少なく 25),26),メタアナリシスでは胃食道逆流症(GERD)症例のH. pylori感染率は38.2%(95% CI:20.0%-82.0%)であるのに対して,非GERD症例は49.5%(29.0%-75.6%)であり,GERDの有無でH. pylori感染率は有意に異なる 27).またサブ解析では,H. pylori感染のORは北米で0.70(95% CI:0.55-0.90),東アジアで0.24(0.19-0.32)と両地域ともにGERD症例で感染者は少なく,その影響は地域間で異なることが示された.東アジアと欧米諸国の違いは,H. pyloriの菌株が異なること,生活環境や遺伝子学的背景が異なること,胃粘膜萎縮や炎症を含めた背景胃粘膜の状態に違いがあることに起因していると考えられている 27).
除菌治療後には胃底腺領域の炎症の改善に伴って胃酸分泌能が回復し,逆流性食道炎の発症や既存の逆流性食道炎が増悪することが懸念されてきた 28).実際に除菌治療後に逆流性食道炎を発症する症例やGERD関連症状を訴える症例が存在し,特に食道裂孔ヘルニアの併発例や体部優位炎の症例で発症のリスクが高いことが報告されている.しかし,除菌治療後のGERD/逆流性食道炎の発症についてメタアナリシスが行われているが,GERD/逆流性食道炎と除菌治療との間で関連性は乏しいとしたものが多い 29),30).メタアナリシスは対象者の背景や評価するアウトカムを揃える必要があるが,除菌治療によるGERD/逆流性食道炎発症への影響を検討したメタアナリシスは,デザインの統一(RCT,コホート研究,症例対象研究),対象者の基礎疾患の統一(消化性潰瘍,GERD,逆流性食道炎,萎縮性胃炎),評価するアウトカムの統一(GERD,逆流性食道炎,逆流症状)がなされておらず,正しい評価が示されていない可能性がある.われわれは,その点を考慮してRCTと前向きコホート研究を調査対象論文とし,評価するアウトカムをGERDではなく,内視鏡検査で確認された逆流性食道炎としてメタアナリシスしたところ,胸焼け症状の出現は除菌前後で大きな変化を認めなかったものの(RR:0.98,95%CI:0.81-1.19),逆流性食道炎の発症は除菌治療により1.46倍(1.11-1.93)にリスクが増加することを報告した(Figure 5) 31).欧米諸国ではH. pylori感染時に過酸状態である前庭部の優位炎が多く,除菌治療後には相対的に酸分泌は正酸状態になり,GERDの発症は増加しないとする報告がみられるが,東アジア地域では体部優位胃炎が多いために,除菌後に酸分泌能が改善し,逆流性食道炎の発症や既存の逆流性食道炎が増悪する機会が多くなることが考えられる 28)~30).

H. pylori除菌治療における逆流性食道炎の発症のリスク:メタアナリシス 31).
酸関連疾患の治癒率は,治療中の胃内pH値と強く相関する 32)~34).目標とする胃内pH値は疾患ごとに異なるため,対象疾患ごとに治療目標を設定し,目標値を達成するような酸分泌抑制薬の投薬計画をたてることが酸関連疾患の治療には重要であり,消化性潰瘍の治療のためには胃内pHを3以上に,薬剤性の胃粘膜傷害の予防には胃内pHを5以上に保つべきである 35).
消化性潰瘍診療ガイドライン2020改訂第3版では消化性潰瘍に対する非除菌治療(初期治療)として4種類のプロトンポンプ阻害薬(PPI),またはカリウムイオン競合型アシッドブロッカー(P-CAB)の1つであるボノプラザン(VPZ)が第一選択薬として推奨されている 2).ただし,消化性潰瘍に対する初期治療は除菌治療が第一選択治療法であるため,この薬物治療は除菌治療に適応がない場合に限定されることに注意を要する.2015改訂第2版と比較してVPZについて言及した点が本改訂版の新たなポイントであり,実際にVPZは既存のPPIに比較して酸に安定すること,分泌細管内に高濃度で長期間集積すること,水溶性に優れていることから酸分泌抑制の作用発現がPPIと比較して速やか,かつ強力な酸分泌抑制効果を示す.そのため,消化性潰瘍診療の中心となることが期待される薬剤ではあるが 36),37),RCTでは消化性潰瘍の治癒率はランソプラゾールとの間に有意差は認めておらず 38),今後,新たなエビデンスの蓄積が期待される.
Ⅱ)H. pylori除菌療法H. pyloriに対する一次除菌治療はPPIもしくはVPZの酸分泌抑制薬と,アモキシシリン(AMPC)+クラリスロマイシン(CAM)の2種類の抗菌薬の投与で行うことが保険認可されている.ただし,除菌治療を巡る環境は2015改訂第2版の発刊時と比較してCAMに対する耐性菌率が35-40%前後に増加していること,除菌治療にVPZの使用が可能となったことの2点が変化している.欧米諸国の除菌治療はMaastricht V/Florence Consensus Report 39)やToronto Consensus 40)をもとに行われているが,それらのガイドラインでは除菌治療が行われる地域のCAM耐性菌率を考慮して除菌レジメンを選択する必要性を述べている 39).CAM耐性菌率が15%以下の低い地域ではPAC療法(PPI+AMPC+CAM)やビスマス製剤を含む4剤療法が推奨され,耐性率が15%以上の地域では,4剤併用療法やビスマス製剤を含む4剤療法が推奨されている(Figure 6).本邦のように耐性率が15%を超える地域では,本来はCAMを使用した除菌治療は避けるべきである.

H. pylori感染症に対する一次除菌治療のおけるMaastricht Ⅴ/Florence consensus reportの推奨 39).
AMPC:アモキシシリン,CAM:クラリスロマイシン,MNZ:メトロニダゾール,PPI:プロトンポンプ阻害薬.
本ガイドライン改訂版では保険認可の有無に関わらずRCTで評価されたレジメンの有効性を評価している.一次除菌治療における最初の疑問は,酸分泌抑制薬は何を選択するべきかという点であるが,除菌治療の成否には除菌治療中の酸分泌抑制度が重要であることから 41),VPZの高い有用性が示唆される.PPIとVPZの有効性を評価したメタアナリシスでは 42),VPZ使用時の除菌率は91.2%(ITT解析,95%CI:88.2%-93.7%)であり,PPI使用時の74.4%(70.0%-78.2%)と比較して有意に高い除菌率を示した(Figure 7-a).しかし,CAM感受性菌の場合には両レジメン間で92-95%と同程度であり,VPZの有用性はCAM耐性菌感染時に限定される.次に抗菌薬として一次除菌治療時にCAMとメトロニダゾール(MNZ)のどちらを使用するべきかの問題もある.CAMを使用した標準的PAC療法とMNZを使用した3剤療法(PPI+AMPC+MNZ;PAM療法)との有効性を比較したメタアナリシスでは,除菌率は両群間で同程度であったが(Figure 7-b),本邦からの報告を抽出した場合はPAM療法の有用性が示された(Figure 7-c) 43).そのため本邦ではCAM耐性菌率が高く,MNZ耐性菌率が低いため,保険適用外ではあるもののPAM療法を選択することが推奨される.ただし,その際にVPZを使用するか否かについてはエビデンスがなく,現時点でPAM療法との優劣をつけるのは難しい.

二次除菌治療時はPAM療法とVAM(VAM+AMPC+MNZ)療法が保険認可されている.しかしながら,メタアナリシスではPAM療法とVAM療法の除菌治療効果が同程度であり,酸分泌抑制剤の推奨については言及していない 42).
抗血栓薬服用者に対して内視鏡検査を行う時は抗血栓薬による消化管出血のリスクと休薬による血栓塞栓症リスクを考慮した対応が必要であるが,高齢化社会の到来により抗血栓薬服用者に対して内視鏡検査を行う機会が増加している.“抗血栓薬服用者に対する消化器内視鏡診療ガイドライン” 44)が発刊された後,抗血小板薬はチエノピリジン誘導体であるプラスグレルやチカグレロルが,抗凝固薬はリバーロキサバン,アピキサバン,エドキサバンの3種類の直接経口抗凝固薬(DOAC)が上市され,“直接経口抗凝固薬を含めた抗凝固薬に関する追補2017” 45)ではその対応策も改訂された.
ワルファリンはPT-INRによる薬効の評価を定期的に行い,血栓塞栓症予防および出血リスクの観点から至適内服用量を調整するが,内視鏡検査時に単に減量・休薬することは血栓塞栓症のリスクを増加させるため避ける必要がある.ワルファリン服用者に対する出血高危険度の消化器内視鏡処置は,従来より推奨されている未分画ヘパリンで置換するいわゆる“ヘパリン置換”以外に,PT-INRで3.0以下の治療域であればワルファリンを継続したまま,あるいは非弁膜症性心房細動の場合にはDOACに一時的に変更する対策で行うことも認められた.しかし,ワルファリンの薬理学的観点による制約や食生活の制約も多く,更にヘパリン置換で内視鏡処置を対応した場合には消化管出血のリスクも高いこともあり,今後はワルファリンよりもDOAC服用者が増加することが予想されている.
DOAC服用者に対する出血高危険度の内視鏡処置時は,処置当日朝から薬剤を中止し,出血の徴候がない場合には翌日朝から再開することを基本とし,血栓塞栓症の高危険例の場合には処置後よりヘパリン投与による対応も推奨されている.このように,追補版では症例のリスクに応じた対応策が示されたが,抗血栓薬非服用者の0.5%-3.4%の術後出血率と比較して,DOAC内服者の出血率は7.9%-22.2%と高く,DOAC服用者に対する対応には細心の注意を払う必要がある 46)~51).一般に抗血栓薬服用者の内視鏡後の消化管出血のリスク因子は患者側因子(年齢,既往歴,透析歴,遺伝学的背景等),処置関連因子(腫瘍の大きさ,占拠部位,処置内容,処置時間等),および薬剤側因子(抗血栓薬の種類,内服量等)により規定されている 52).しかし,DOAC自体の薬剤種の特性,薬物動態,薬物代謝の個人間差を含む薬理学的視点より内視鏡治療後の消化管出血のリスクに対して検討した報告は少ない.DOACの抗凝固作用は濃度依存性であり,トラフ濃度と血栓塞栓症の発症リスクは負の相関を,頭蓋内出血や消化管出血等の発症率とは正の相関を示すことが報告されている 53)~55).DOACの薬物代謝酵素(CYP3A4/5)やトランスポーター(P-glycoprotein,APT-binding cassette transporter G2[ABCG2])をコードする遺伝子には遺伝的多型性があり,DOACの血中濃度や抗凝固作用に影響を及ぼすことが示されている 56),57).そのため,現時点ではDOACの薬物血中濃度や遺伝子多型を日常診療で簡易に測定することはできないが,DOACの薬物血中濃度や抗Ⅹa活性,薬物代謝酵素の遺伝子多型がDOACの治療効果判定(抗凝固作用)や内視鏡治療後の消化管出血の予測マーカーとなる可能性が考えられる.
近年,経皮的冠動脈形成術(PCI)後のDAPT(dual anti-platelet therapy: 抗血小板薬2剤併用療法)や複数の抗血小板薬と抗凝固薬の併用により,ガイドラインの追補後も対応に苦慮する機会は多い.循環器領域ではDAPTスコア 58)やPRECISE-DAPTスコア 59)などのスコアリングシステムを使用して抗血小板薬服用者の出血リスクの層別化を行い,臨床現場で活用されている.また,DAPTを巡る問題点として,禁忌がない場合には恒久的なLDA内服が推奨されているが,最近ではLDAの消化管出血や頭蓋内出血のリスクの軽減効果と血栓イベントリスクの抑制を目的に,LDAではなくチエノピリジン系の薬剤の継続について検討されている.本ガイドライン追補版では両薬剤で休薬期間や処置時の対応方法が異なるために注意を要する.
2020年には日本の多施設共同研究で早期胃癌ESD後の出血の予測モデル(BEST-Jスコア)の有用性が報告された 60).10種類の要因(ワルファリン,DOAC,血液透析,チエノピリジン系抗血小板薬,LDA,シロスタゾール,腫瘍径30mm以上,腫瘍局在が肛門側1/3,複数の腫瘍,抗血栓薬の中止)に対してESD後出血に対するリスクに重みづけを行い,処置対象者の出血リスクを点数化したところ,0-1点の出血低リスク,2点の中リスク,3-4点の高リスク,5点以上の超高リスクの出血率は,それぞれ2.8%,6.1%,11.4%,29.7%となり,治療前の各種要因で術後の出血の危険性を予測できる可能性が示された 60).
消化性潰瘍診療の現状と消化性潰瘍関連疾患の変遷や注意点について消化性潰瘍診療ガイドライン改訂版の改訂点を交えながら概説した.消化性潰瘍は本邦の生活様式の変化,H. pylori感染率の低下,酸分泌抑制薬の普及により減少傾向があるものの,その病因や病態も変わり,日常一般臨床や内視鏡診療の現場で対応も変わりつつある.今後は更なるエビデンスを蓄積することで現行のガイドラインの検証を進めるとともに,多方面からの検討を行うことで安全な一般臨床や内視鏡診療を提供していくシステムを構築していく必要がある.
本論文内容に関連する著者の利益相反:河合 隆(武田薬品工業株式会社,大塚製薬株式会社,第一三共株式会社,アストラゼネカ株式会社,EAファーマ株式会社,オリンパス株式会社,富士フイルム株式会社)