2022 年 64 巻 1 号 p. 19-28
2022 年 64 巻 1 号 p. 19-28
内視鏡的全層切除術(Endoscopic Full-Thickness Resection;EFTR)は腹腔露出法(Exposed法)と腹腔非露出法(Non-exposed法)に分類される.Exposed法ではまず腫瘍周囲を全周性・全層性に切開し,その後消化管壁欠損部を内視鏡的に閉鎖する.閉鎖法としてはクリップ・留置スネア法や内視鏡縫合器を使用した縫合閉鎖法がある.Non-exposed法ではまず,腫瘍の底部を特殊なクリップを用い全層性に閉鎖し,その後クリップの上縁で腫瘍を切除する.Exposed法は腫瘍サイズによらず施行可能なことがメリットであるが,消化管壁欠損部の完全閉鎖が必須である.Non-exposed法は安全な方法であるが,クリップの大きさに限界があり,不完全切除のリスクがある.
近年になり,米国内に数々のベンチャー企業が立ち上げられ,ロボット技術を応用した腹腔鏡および軟性内視鏡手術システムを開発している.われわれの行った前向きランダム化比較試験では,ロボットを用いた大腸Endoscopic Submucosal Dissection(ESD)は,従来のESDと比較して手技時間が短く,一括切除率が高く,そして穿孔率が低いことが示された.米国で最近開発された最新のロボットシステムでは,内視鏡および手術用デバイスの操作すべてにロボット技術が応用されており,術者が両手を用い繊細かつ正確に手術を行うことが可能である.
内視鏡的粘膜切除術(EMR)や内視鏡的粘膜下層剝離術(ESD)のような内視鏡的切除法で切除不能な消化管の腫瘍性病変は,従来外科的切除の適応とされてきた.しかしながら近年,内視鏡的全層切除術(Endoscopic Full-Thickness Resection;EFTR)の出現により,これらの切除不能病変を内視鏡的に切除することが可能となった.
一方で米国では近年,様々な企業が手術用ロボットの開発に乗り出している.開発対象の多くは腹腔鏡下手術用のロボットであるが,管腔内手術用のロボット開発を手がける企業も出現してきている.
本稿では,米国における内視鏡的全層切除術および軟性ロボット内視鏡手術の現状について解説する.
アメリカ消化器内視鏡学会(American Society for Gastrointestinal Endoscopy;ASGE)の全層切除術ガイドライン 1)によれば,EFTRの適応は1.消化管上皮性の良性・悪性病変のうち,粘膜下層の強い線維化によりEMRまたはESDの施行が困難な病変,および2.粘膜下腫瘍のうち,第3層(固有筋層)由来のもの,もしくは固有筋層浸潤を認めるものとされる.また2017年に発表されたASGEのガイドライン 2)によれば,消化管壁第4層由来,2-4cmで増大傾向にある消化管粘膜下腫瘍に対し内視鏡的全層切除術を含めた局所切除が勧められている.粘膜下腫瘍に対しては超音波内視鏡下穿刺吸引および生検法(endoscopic ultrasound-guided fine-needle aspiration or biopsy;EUS-FNA or FNB)での組織診も可能であるが,その後長期的な内視鏡的経過観察が必要となる.医療費および患者への精神的負担を考えると,低侵襲な内視鏡的全層切除術で一括切除し病理検査を行うことが最も望ましい.
EFTRは手技的に大きく腹腔露出(Exposed)法および腹腔非露出(Non-exposed)法に分類される.実際には腹腔露出(Exposed)法には経口内視鏡的腫瘍核出術(per-oral endoscopic tumor resection;POET) 3)や粘膜下トンネル内視鏡的切除術(submucosal tunneling endoscopic resection;STER) 4)のようなトンネル法も含まれる 1)が,本稿では解説を割愛する.
1.内視鏡的全層切除術:Exposed法Exposed法ではまず腫瘍の全層切除を行い,その後消化管壁欠損部を内視鏡的に閉鎖する.この方法を安全に施行するためには全層切除施行後に消化管壁の欠損部を完全閉鎖することが鍵となる.しかしながら食道や十二指腸は狭い管腔であるため縫合のためのワーキングスペースが限られており,また大腸では消化管内容の腹腔内への漏出による腹膜炎への危惧があることから,Exposed法は一般的には胃病変に対して行われることが圧倒的に多い.この方法の利点としては,粘膜下層トンネルを利用しないため病変の大きさに関わらず腫瘍の完全切除が可能な点が挙げられる.一方で欠点としては,胃壁の全層欠損部が大きくなると送気による視野確保が困難になる点,緊張性気腹の状態となりVeress Needleなどによる腹腔穿刺および脱気が必要になる点,大きな動脈の分枝に遭遇した場合に予期せぬ大出血にあうリスクが挙げられる.欠損部の閉鎖にはより閉鎖性の高い連続縫合が望まれるが 5),手技的に困難な場合には結節縫合に変更することも可能である.病変径が3cmを超えるものでは欠損部の完全縫合閉鎖が困難で術後の縫合不全のリスクが高まると報告されている 6).
Exposed法は全例全身麻酔で行い,術前30分程度のタイミングで抗生剤の投与を行う.また,CO2送気は必須である.EFTRの技術的な側面はESDに準じる 7).まずESD同様,腫瘍の周囲にマーキングを行い,粘膜下局注ののちESDナイフを用い病変周囲に全周性の粘膜切開を置き粘膜下層および筋層を露出する.その後ニードル型のESDナイフで直接筋層に切り込みを入れ,腹腔内への穿孔を確認する.最終的に全周性に筋層漿膜を切開し病変切除を終了する.これが“露出(exposed)”法と呼ばれる所以である.ESDと比較して粘膜下の線維化による影響を受けないため,病変の切除自体は手技的には単純であるが,病変切除後の標本回収および消化管壁の閉鎖を確実に行うために,いくつかの問題点を理解することが肝要である.まず,特に広範囲な筋層切除が必要な病変,すなわち病変の大部分が固有筋層と接している病変や壁外発育型病変の場合,切除病変が腹腔内に迷入し回収が困難になることが危惧される.これを回避するために手技の最終局面で2チャンネル上部内視鏡に切り替え,把持鉗子で病変を保持しながら切除を終了する方法,またはOverStitch(Figure 1, Apollo Endosurgery, Austin, TX)を用い病変の一部に一針をかけトラクションをかけるプーリー法 8),9)が考え得る.

OverStitch(Apollo Endosurgery, Austin, TX).
また消化管壁欠損部の閉鎖法として,現在主に以下の3つの方法が用いられている.1つ目は止血クリップおよび留置スネアを用いる方法 10)である.この方法では2チャンネルスコープを用い,まず消化管壁欠損部の近傍で留置スネアを拡げる.その後止血クリップで留置スネアを全周性に欠損部縁に固定した後,留置スネアを締め上げ欠損部の閉鎖を行う.Ye LPらの報告 11)では,固有筋層由来の粘膜下腫瘍に対しExposed EFTRを施行した536例を検討した結果,完全切除率は97.1%であったものの88例(16.4%)に難治性の消化管穿孔が発生したと報告している.これはクリップと留置スネアを用いた消化管壁の閉鎖法の限界であると考えられる.次の方法は,Over-the-scope Clip(OTSC, Ovesco Endoscopy USA, Cary, NC)を用いた閉鎖法である.この方法を用いれば,消化管壁の全層性閉鎖が可能であるものの,クリップ径が最大で14mmであることから閉鎖可能な欠損部径に限界があり,比較的小さな欠損部の閉鎖に対して用いることが望ましい.
一方で,OverStitch のような内視鏡縫合器を用いれば,Figure 2のように外科的縫合に準じた様々な縫合パターン 12)で消化管壁欠損部の閉鎖が可能である.Figure 2-Dの巾着縫合は,外科的肥満手術後の消化管吻合部の縮小に用いられるため消化管壁欠損部の閉鎖に使用されることは稀であり,一般的にはFigure 2-A~Cの結節縫合,連続縫合,または8の字縫合が用いられる.縫合器による縫合閉鎖においては,外科的縫合と同様,粘膜面のみではなく筋層・漿膜面も確実に捉え全層性に縫合することが肝要である.2チャンネルスコープを使用するOverstitchでは,もう一方の鉗子孔から把持鉗子や螺旋状把持鉗子(Helix Device)を挿入し使用することが可能で,直視下に全層縫合の際の漿膜面と粘膜面を確認できることが大きな利点である.しかしながら病変が接線方向にある場合や内視鏡でのアプローチが困難な領域の場合,連続縫合を行うことが困難となる.そのような場合には適宜結節縫合に切り替え,確実に縫合閉鎖を行う.術中透視や術後透視は縫合不全を除外する目的で必須であるが,術中透視を行えば必要に応じ追加縫合を加えることが可能である.われわれは術後経過観察のために一泊入院で手技を施行しているが,翌日理学的所見に問題がなければ退院としている.

Non-exposed法の利点は,病変底部の消化管壁を病変切除前に全層性に閉鎖し,腹腔内容物や腫瘍細胞の腹腔外への漏出を最小限にできる点にある.適応病変としては主に壁内発育型粘膜下腫瘍や,線維化が非常に強くEMRやESDが困難な上皮性腫瘍性病変である.粘膜下腫瘍のうち広範囲で固有筋層に接する病変や壁外発育型病変は適応外である.閉鎖法として現在米国で用いられているデバイスとしては,Padlock Clip(US Endoscopy, Mentor, OH)および前述の OTSC が挙げられる.Padlock Clip(Figure 3-A)は,星形をしたNitinol製のクリップで,星のそれぞれの頂点から中央に向かい計6本の剣状の針が伸びるデザインを持つ.留置後に平坦な形状になるため,EFTRにおいてはその後のスネアリングが容易である.一方で,OTSC(Figure 3-B)は灣曲した形態であることから,留置後にスネアリングが困難になることがある.その場合にはハサミ型やフック型のESDナイフを用い病変の切除を行う.近年米国では,内視鏡的全層切除術用の専用デバイスであるFull Thickness Resection Device(Ovesco Endoscopy USA, Cary, NC)がアメリカ食品医薬品局(Food and Drug Administration;FDA)に承認された(Figure 4).このデバイスの利点は,13mm大のスネアがデバイス内に内蔵されており,病変底部の全層性閉鎖ののち,デバイスを交換することなくスネアリングに移行できることである.しかしながら,このデバイスはサイズが大きく,特にS状結腸の憩室症がある患者などにおいて右側結腸への挿入が不可能となる場合がある.181名の患者にFTRDを使用しNon-exposed法を施行した多施設前向き試験 13)では,手技成功率89.5%,完全切除率76.9%と良好であったものの,病変径20mm以上では20mm以下と比較し統計学的に有意に完全切除率が低いことが示された(81.2% vs 58.1%,p=0.0038).これは21mm大というクリップの大きさに完全切除率が影響を受けるという,Non-exposed法の限界を示しているものである.また,近年報告されたメタ解析 14)においては,Non-exposed法が行われた555症例に対して解析が行われた.手技成功率89.25%,完全切除率82.4%と前出の報告と同等で,術後偶発症も術後出血0.97%,post-polypectomy syndrome 2.2%,穿孔1.2%と良好であった.しかしながらこのデバイスの良い適応とされていた虫垂開口部近傍の病変に対する切除後に,19.7%の急性虫垂炎が発症したと報告されており,注意喚起が必要である.

内視鏡的全層切除術(Non-exposed法)で使用されるクリップ.
A:Padlock Clip(US Endoscopy, Mentor, OH).
B:Over-the-scope Clip(OTSC, Ovesco Endoscopy USA, Cary, NC).

Full Thickness Resection Device(Ovesco Endoscopy USA, Cary, NC).
軟性内視鏡による治療手技は,切開剝離・止血・縫合用の新しいデバイス開発により近年めざましい発展を遂げている.特にESDや経口内視鏡的筋層切開術(Peroral Endoscopic Myotomy;POEM),Overstitchを用いた内視鏡的肥満治療法である経口的吻合部縮小術(Transoral Outlet Reduction;TORe) 15)や内視鏡スリーブ胃形成術(Endoscopic Sleeve Gastroplasty;ESG) 16)などの出現により,従来外科的治療の適応であった疾患に対し,より低侵襲な方法で同等の治療効果が得られるようになった.しかしながらこれらの内視鏡手技は一般的に技術的難度が高い.
外科手術においてはまずTriangulation,すなわち複数の手術器具を離れた位置から異なる角度で挿入することでその操作を効率化し,器具同士の干渉を防止することが基本である.そして助手が対象臓器を把持・牽引することで実現されるTractionおよびCountertractionにより剝離面の視認性が向上し,そして組織に与えられた張力により切開剝離が効率化される.ESDやPOEMにおける切開・剝離・止血手技,そしてTOReやESGにおける縫合手技は外科手術と全く同様の手技である.しかしながらわれわれが使用している軟性内視鏡は従来,内視鏡観察・生検用に開発されたシングルチャンネルスコープであり,ほとんどの場合で一度に単一のデバイスしか使用できない.また軟性内視鏡の先端に与えられた動作としては,ダイヤルによる上下左右への回旋運動,トルクによる左右回転,そしてスコープの押し引きによる前後への移動のみである.われわれ内視鏡医は複雑な内視鏡手技を安全に,そして速やかに完遂するために,これらの内視鏡操作を駆使しスコープ先端を繊細にコントロールする技術を常に求められている.
今から10年ほど前に,EndoSAMURAI 17), Direct Drive Endoscopic System 18), Incisionless Operating Platform 19), Anubiscope 20)といった,両手操作が可能な軟性内視鏡プラットフォームが開発された.これらのプラットフォームのデザインは軟性内視鏡における上記の数々の問題を解決する画期的なものだったが,内部構造は従来の軟性内視鏡と同様,操作部と内視鏡先端をワイヤーで繋ぐ機械的なもので,狭い消化管腔内で繊細な作業を行うことは困難であった.
一方で米国では,1995年にFrederic Mollらが外科用ロボット開発のベンチャー企業としてIntuitive Surgical(Sunnyvale, CA)を設立し,最先端のロボット技術により遠隔操作が可能なda Vinci外科用ロボットシステム(Figure 5)を2000年に発売した.da Vinciシステムはその後4th generationまで進化し,急速に世界で普及した.しかしながらda Vinciの開発開始から20年経過した2016年頃からIntuitive Surgicalの数々の特許が期限切れを迎えた.それに伴い米国内では多くの企業が手術用ロボットの開発に乗り出し,現在Medtronic(Minneapolis, MN),Johnson & Johnson(New Brunswick, NJ),Asensus Surgical(Miami, FL)などが手術用ロボットの開発・販売を行っている.さらに米国の手術用ロボット関連企業は近年,軟性内視鏡領域にも参入してきている.Intuitive Surgicalは「Ion」と呼ばれる全く新しい軟性ロボット気管支鏡システム(Figure 6)を開発し,2019年に米国FDAに承認を受けた.また,Intuitive Surgical設立者のFrederic Mollが新たに立ち上げた企業であるAuris Health(Redwood City, CA)も,「Monarch Platform」と呼ばれる新しい軟性ロボット気管支鏡システム(Figure 7)を開発し,Intuitive Surgicalよりも先の2018年にFDA承認を受けている.これらの軟性ロボット気管支鏡システムの特徴は,従来の軟性気管支鏡とは異なりコントロール部とスコープが完全に分離しており,遠隔操作によりスコープ先端に繊細な動作を与えることが可能な点である.Johnson & Johnsonは2019年2月にAuris Healthを60億ドル(6,500億円)で買収し,現在は共同で軟性ロボット内視鏡手術システムを開発している.
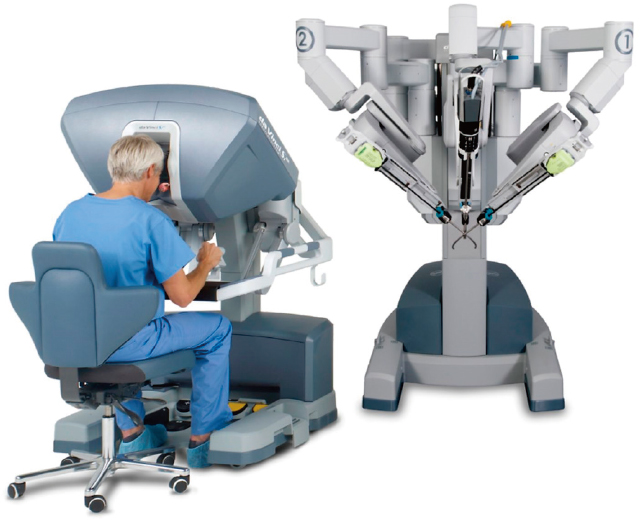
daVinci Surgical System(Intuitive Surgical, Sunnyvale, CA).

Ion(Intuitive Surgical, Sunnyvale, CA).

Monarch Platform(Auris Health, Redwood City, CA).
米国内では現在までに,主に2つの軟性ロボット内視鏡手術システムが開発されており,ここで紹介したい.
1.Medrobotics: Flex Systemまず1つ目は2017年にFDA承認を受けたMedrobotics社(Raynham, MA)の「Flex System」である.このシステムは,ロボット軟性内視鏡(Figure 8左)と術者用のロボット操作コンソール(Figure 8右)で構成される.ロボット内視鏡は25cm長で,18mm径のスコープの両サイドに4mm径のワーキングチャンネルを2つ有するデザイン(Figure 9)を持つ.この2つのワーキングチャンネルを介して,手術用デバイスを使用することが可能である.これらのデバイスには関節駆動部を有し上下左右への屈曲操作および回転操作が可能で,種類は多岐に渡り把持鉗子,フック型ナイフ,ハサミ型ナイフ,持針器などが使用可能である.モニターはハイビジョンで3D観察に対応しており,手術中の深部認識が容易となる.観察用のロボット内視鏡は術者用コンソールでの操作により,上下左右の回旋運動,前後運動,そして左右の回転運動が可能である.しかしながらワーキングチャンネルから挿入されるデバイスはロボット操作ではなく,腹腔鏡下手術と同様のマニュアル操作となる.われわれはこのシステムを用い,ロボットESDと従来法のESDを比較した前向きランダム化試験 21)を行った.大腸の切除臓器モデルを用い,ロボットESDと従来法のESDのいずれも未経験の若手内視鏡医5名が計2回ずつ手技を行った.ロボットESDでは一括切除率が100%であったが従来法のESDでは50%で有意に低く(P<0.0001),穿孔率は有意差がないもののロボットESDで低く(30% vs 60%,P=0.18),全手技時間(34.1分 vs 88.6分,P=0.001)および粘膜下層剝離時間(27.8分 vs 79.4分,P=0.002)もロボットESDで有意に短かった.ESDを安全に施行するためには非常に繊細で正確な内視鏡操作を求められ,技術的習熟を得るには数年間のトレーニング期間に多くの症例数をこなす必要がある.今回の研究ではESDの未経験者ではロボットESDの方がESDをより短時間で安全に完遂できることが示された.ロボットESDでは前述のTriangulationおよびトラクションにより外科手術と同様の条件下でのESDを施行することが可能で,今後ESDのトレーニング期間を短縮できる可能性が期待できる.

Flex System(Medrobotics, Raynham, MA).

Flex Systemロボット内視鏡の先端部.
Colubris MX(Houston, TX)は,テキサス大学の脳神経外科医であるDaniel Kimによって2017年に設立した医療用ロボット開発のベンチャー企業である.現在までに,管腔内手術用の軟性ロボット内視鏡手術システムである「Endoluminal Surgical(ELS)System」,シングルポート手術用ロボットシステムである「Single-Port Surgical(SPS)System」,そして胎児の先天性脊椎奇形の手術を子宮内で行うためのマイクロロボットシステムである「Microsurgical Robotic System」の3つを開発している.Figure 10-AはELS Systemの内視鏡ロボット本体で,Daughter Scopeおよび2本の手術用デバイスがMother Scopeに挿入される仕組みである.Figure 10-Bは内視鏡ロボットを遠隔操作する術者用コンソールで,da Vinciを始めとした手術用ロボットと同様,手術用デバイスの開閉や回転・回旋など,管腔内手術に求められる繊細なデバイス操作が可能である.画面上にはDaughter Scopeから映し出される映像の他,手術用デバイスの形状俯瞰が表示され,狭い管腔内でのデバイス同士の干渉を防ぐことが可能である.また足元のフットペダルを使用し,切開・凝固,コントロール先(Mother Scope,Daughter Scope,手術用デバイス)の切り替えなどを行う.前出のMedrobotics社のFlex Systemと根本的に異なる点は,このシステム内の内視鏡および手術用デバイスのすべてにロボット技術が採用されており,この術者用コンソールでの遠隔操作により集約的なコントロールが可能な点である.またFigure 11に示す様に,手術用デバイスとしては把持鉗子やハサミ型鉗子,フック型ナイフなど様々なデバイスが使用可能であるが,特筆すべき点はFigure 12に示す様に,これらのデバイスの先端は7-degrees-of-freedom(DOF)を実現するために多関節を有しており,軟性デバイスであるにも関わらず非常に自由度が高く滑らかな動きを実現できていることである.現在までに,南米のチリやブラジルを中心にこのシステムを使用したロボットESDや肥満治療の臨床試験が進行中であり,近々米国にも導入されFDAの承認に向け臨床試験を開始する予定である.

Endoluminal Surgical(ELS)System(ColubrisMX, Houston, TX).
A:ELS Systemの内視鏡ロボット本体.
太矢印:Mother Scope. 細矢印:Daughter Scope. 破線矢印:手術用デバイス.
B:術者用コンソール.

ColubrisMX ELS Systemで使用されるロボティックデバイス.
A:Pinching Forceps.
B:Monopolar Knife.
C:Needle Driver.
D:Monopolar Curved Scissors.
E:Rat Tooth Forceps.
F:Cadiere Forceps.

ELS Systemのロボティックデバイス.
A:ELS経直腸用デバイス(81cm).
B:ELS経口用デバイス(120cm).
C:6mm径のデバイス先端.多関節で7-DOFを実現している.
米国における内視鏡的全層切除術およびロボットESDの現状と今後の展望について概説した.新しいデバイスやロボット内視鏡システムの出現により,軟性内視鏡手術は今後さらにその対象疾患を外科領域に拡大していく可能性がある.特にロボット内視鏡システムは今後の内視鏡医療のあり方を大幅に変えていく可能性があり,今後の研究が期待される.
本論文内容に関連する著者の利益相反:なし