要旨
後天的な消化管狭窄の成因は,進行癌,炎症治癒後の瘢痕,内視鏡治療後の瘢痕,外科手術の吻合など,一様でない.ところが消化管狭窄が治療の対象となるとき,その理由は一様で,通過障害を起こしたときである.上部消化管の場合は食物を,下部消化管の場合は消化吸収された後の便を通すための治療が行われる.切除適応の進行癌であれば,狭窄の解除とともに根治を目指した外科手術が第一選択として行われることがあるが,多くのケースで狭窄解除を目的とした外科手術は最後の切り札である.とりわけ良性狭窄に対しては外科手術回避のために,機械的な拡張術が第一選択の方法としてかねてから行われてきた.本稿では,下部消化管の狭窄に対して,内科的に行われる,特に内視鏡を用いた拡張術について,ブジー,バルーン拡張術,Radial incision and cutting(RIC)の順に,現状を述べる.かつてと比べて,内視鏡下に狭窄部が拡張される様子を確認しながら施行することが圧倒的に多くなっているが,機械的拡張術の方法論じたいは長年画期的なブレイクスルーがなく代わり映えしない.現状の抱えている問題点や将来展望についてもあわせて述べる.
Abstract
The causes of acquired gastrointestinal stenosis vary, including advanced cancer, scars after healing of inflammation, scars after endoscopic treatment, and surgical anastomosis. However, the treatment of gastrointestinal stenosis is targeted only when it causes a passage obstruction. In the case of upper gastrointestinal tract stenosis, treatment is performed to allow foods to pass; in the case of lower gastrointestinal tract stenosis, treatment is performed to allow the passage of stool. In cases of advanced cancers that require resection, surgery aimed at relieving the stenosis and a radical cure may be the first choice. However, surgery aimed solely at relieving the stenosis is the last resort in many cases. Especially for benign stenosis, mechanical dilation has long been the first choice of treatment and the method to avoid surgery. In this paper, we describe the current status of endoscopic dilation for the lower gastrointestinal tract stenosis with bougie, balloon dilation, and radial incision and cutting (RIC). As compared to the past, one of the advances is that treatment is often performed using an endoscope to confirm how the stenosis is dilated. However, there has been no breakthrough in discussing the methodology of mechanical dilation. I would also like to describe the current problems and prospects.
Ⅰ はじめに
消化管狭窄は,食道から大腸まで,どの部位にも起こりうる
1)~3).最も大きな分類では,先天性狭窄
4),5)と後天性狭窄とに分けることができる.さらに後天性狭窄のなかには,悪性,すなわち進行癌による腫瘍性狭窄と
6),7),その他大多数が含まれる良性狭窄とがある.良性の消化管狭窄の原因としては,炎症治癒後の瘢痕に伴うもの,内視鏡治療後の瘢痕に伴うもの,外科手術の吻合などが考えられる.成因が何であれ,消化管狭窄が治療対象となるのは,それが原因で通過障害を起こしているときである.
炎症治癒後の瘢痕狭窄は,消化性潰瘍
8),薬剤性潰瘍
9),クローン病
10),11),潰瘍性大腸炎
10),12),虚血性腸炎
13),腸結核
14),非特異性多発性小腸潰瘍
15),16)などで生じることが知られている.管腔の径がより小さいほど,粘膜欠損の深さがより深いほど起きやすい.十二指腸潰瘍の繰り返しによる球部の狭小化
8)や,クローン病における小腸狭窄がその代表である.
消化管の内視鏡治療後の瘢痕狭窄は,人工潰瘍の環周率が全周に近づくほど生じやすいとされている
17).円柱上皮に比べて扁平上皮は伸展性が乏しいために,瘢痕狭窄が通過障害の発生につながりやすい.そのため内視鏡的粘膜下層剝離術(ESD)が普及してより大きな病変が内視鏡的に治療できるようになって以降,特に食道でしばしば問題になってきた
18),19).折角腫瘍が内視鏡的に根治切除できても,狭窄のために食事が摂れなくなったのではクオリティ・オブ・ライフ(QOL)を著しく損ねることになってしまい,目的を完遂したとは言えない.この場合の狭窄は,取った腫瘍が癌であっても良性狭窄に分類されるが,治療学的には腫瘍そのものと同様に重大な問題と言える.
最後に外科手術後の吻合部狭窄は,原病が狭窄形成に関与するクローン病を除くと
20),管腔が狭い食道と大腸に生じたとする報告が多い
21),22).切除や切開を加えた消化管同士を吻合すれば,それがどの部位であれ,炎症後や内視鏡治療後と同様,傷が治る過程で組織が癒着するのに伴って吻合直後よりは狭窄し,硬化ぎみに治癒していく
23).しかしながら,吻合部狭窄が治療の対象になるのはやはり通過障害を起こしたときであり,大多数の外科手術では臨床上問題にならない(以降「吻合部狭窄」は臨床上問題になるもののみを指すこととする).吻合部狭窄の発生は偶発的で,吻合部の血流障害が関与しているのではないかと考えられているが,原因は未だ明らかでない
24)~27).縫合不全があると治癒後に狭窄をきたしやすいことが知られており
28),29),術後早期の吻合部の炎症の程度が強ければ強いほど狭窄に関与しやすいものと思われる.かつては器械吻合の普及で吻合部狭窄が増えたと言われたことがあったが
30),最近では手縫いと同率または低率とされており,おそらく吻合の方法とは関係がない
31)~33).
本稿では,消化管狭窄のうち下部消化管に,特に後天的に生じた良性狭窄の治療法について既報をレビューし,その歴史と問題点を考察したい.消化管狭窄の治療の基本的なコンセプトは長年にわたり代わり映えがなく,大きなブレイクスルーを見ていない.そこで今後の将来展望についてもあわせて考察したい.
なお,ここでは神経障害などによる機能的な消化管狭窄,憩室炎や外科的吻合直後などで炎症極期に生じる粘膜浮腫による消化管狭窄は含まない.
Ⅱ 良性狭窄と悪性狭窄.治療に対する考え方の違い
後天的な消化管狭窄には,良性狭窄と悪性狭窄とがあることは前述のとおりだが,治療に関しては,特に外科手術の位置付けが大きく異なる.悪性狭窄と比較して良性狭窄では,通過障害解決のための外科手術に対するハードルがずいぶん高い.下部消化管でも,悪性狭窄に対しては,腫瘍の根治的
34),35)または姑息的な切除
34)に加え,バイパス手術
34),36),人工肛門造設など
34),37),外科手術のオプションが多数用意されており,実際に内視鏡的拡張術を経ることなく外科手術を第一選択として施行するケースも少なくない.悪性狭窄のみに適応がある金属ステントによる拡張術も外科的手術を意識した治療で,ステントの使用理由は安全な手術を行うため(bridge to surgery)であったり
38),手術ができないから仕方なく(palliative)であったりする
39).
それに比較して良性狭窄の治療では,外科的手術は他の治療法が手詰まりになったときの最終手段と位置付けられている.良性狭窄に対する拡張術は,手術を回避することを優先に治療方針を組み立てる.一度の拡張術で目的を達しない場合や,再狭窄した場合は,複数回繰り返すことで外科的手術を回避することも多い
40).また上記のとおり,一度留置すると基本的に抜去ができないステント治療はオプションに加わらない
41).
良性狭窄に対して拡張術を行うか否かは,冒頭に述べたように通過障害やそれに伴う症状があるか否かが最も重視されるが,目安として外径φ10 mm程度のスコープが通過するかどうかで判断されることが多い
42).同様に,拡張の目標もφ10mm以上のスコープが通過するあたりが目安になる.φ10mm以上のスコープが通過すれば,概ねの便通障害は解決すると考えられている
43).狭窄部に深い潰瘍が残るもの,瘻孔を伴うもの,膿瘍を合併しているものは,とりあえずその時点では拡張術を行わず,炎症の鎮静化を図ることを優先する
44),45).
Ⅲ ブジー法(Bougie)
体腔や臓器の間隙や瘻孔に差し込んで,その深さや走行,すなわち消息を探る棒をゾンデ(日本語で消息子)と呼ぶ.消息子のなかで,内腔の拡張を目的として,先端を楔形に成形したものをブジーと呼ぶ.多くは金属製で硬く,最大径の異なる数本が1セットになっており,細いものから太いものに順に挿入して目標値まで拡張する(Figure 1).ブジー法の歴史は古く,1800年代に尿道の狭窄に対する治療を目的に使用されたのが最初である
46).ブジー法が下部消化管に応用されるのは1970年代に入ってからで,原法は直腸肛門に限定して適用されている
47),48).深部腸管に適応しないのは,ブジー(消息子)が到達しないためである
49).肛門ブジーの適応疾患は主に慢性裂肛や痔瘻による狭窄,直腸や肛門管の術後吻合部狭窄である
50)~52).φ10mmから用意があり,狭窄の抵抗を消息子を握る手で感じながらゆっくりと挿入し,突破する.
原法は上記のごとくであるが,実臨床では,小指や示指を挿入する「用指ブジー(finger bougie)
53),54)」や,内視鏡を挿入する「内視鏡ブジー(scope bougie)
55),56)」という手技がよく活用されている.
用指ブジーの適応については原法と同様で,直腸肛門に限定される.外来で直腸診に引き続いて行うことができ簡便であることと,指で直接抵抗を感じながら施行できることがメリットと言える.術者が右利きなら,患者は左側臥位,術者が左利きなら,患者は右側臥位とする.術者は利き手に手袋か指囊を履き,医療用粘滑剤(リドカイン2%ゼリーが好ましい)を塗布して,まず示指で直腸診を行い狭窄の程度を確認する.狭窄の程度に応じて,示指をそのまま突破させるか,小指に入れ替えて突破させるかする.小指の平均径(第一/二関節部の最大径)は日本人の成人女性で約12/ 13mm,同成人男性で約13.5/15mm,示指はそれぞれ約14/16mm,15.5/18mmと言われている
57).必ずしも最大径まで挿入しなければならないことはなく,挿入の深度は指先の感覚によって加減する.
内視鏡ブジーは,ブジー法としては唯一深部大腸にも適用できる.内視鏡下に狭窄を確認し,そのまま力を入れてスコープを押し込み突破させる方法である
56).汎用消化管内視鏡は,先端部外径が挿入部最大径に比して細く作ってあるため,特別なデバイスを装着しなくとも,狭窄の抵抗を単純に突破させてスコープを十分に通過させるだけでブジー効果が期待できる.先述したように,消化管狭窄に対する治療適応の判断は10mm径前後のスコープが通過するか否かが目安で,拡張術の目標値はφ10mm以上のスコープが通過するあたりである
43),44),58),59).そのため,下部消化管の場合は,オリンパス社(東京・新宿)のスコープならばPCF-H290シリーズ(先端部外径φ11.7mm,軟性管外径φ11.5mm,挿入部最大径φ13.6-13.8 mm),富士フイルム社(東京・港)のスコープならばEC-760P-V/M(先端部径φ11.1mm,軟性部径φ11.5mm,挿入部最大径φ13.0mm)などが最終的に通過させるスコープのサイズとしては適当と思われる(Figure 2).いきなり目標値のスコープを突破させることが難しければ,原法と同様,上部消化管用ビデオスコープ(先端部外径がφ10 mm以下のものが多い)や,大腸用スコープでも先端部外径のより細いものから始めるとよい.内視鏡ブジーの工夫として,スコープ先端に先細りのフードを装着する方法がある
60),61).内視鏡ブジーの,他のブジー法にない利点は,狭窄部を内視鏡的に視認できることである.特にフードを装着した場合には,手元の感覚に加えて狭窄部が拡張していく様子がリアルタイムで確認できるため安全性の向上にも寄与する.先細りのフードがいくつか市販されているなかで,トップ社(東京・足立)のキャストフードⓇは,透明フード内のφ7 mm,φ8mm,φ9mmのところに全周に目盛が刻んであり,これを押し当てることによって狭窄径が何mmあるかを計測することができる
60),62).さらにキャストフードは添付文書上,拡張に用いることにも適応があり,拡張径を確認しながら内視鏡ブジーが施行できる仕様となっている(Figure 3).
Ⅳ バルーン拡張術(Endoscopic balloon dilation;EBD)
下部消化管の良性狭窄に対する治療として,現在最もよく行われている方法である
63)~68).消化管に対するバルーン拡張術は1980年代後半に登場し,上部/下部消化管とも外科手術後の吻合部狭窄に対する新たな治療法と位置付けられていた
68).1990年代には,良性の消化管狭窄全般に適応されるようになり一般化された.クローン病の回盲部狭窄にバルーン拡張術が適応されるようになったのもこのころである
69),70).かつては拡張時に内視鏡を用いず透視下に確認しながら行うover-the-wire(OTW)式拡張用バルーンもよく用いられていたが,through-the-scope(TTS)式の登場,普及におされてすっかり衰退してしまった
71).直近10年間で発売された消化管内視鏡のほとんどがφ3.2mm以上の鉗子口径を備えていることに加え,バルーン側も適合鉗子口径が小さくなり,その多くがφ2.8mmチャンネルに対応しているため,特殊な内視鏡を用いないとバルーンが入らないなどという事象がほぼ皆無となった.TTS式拡張用バルーンを用いれば,透視下だけでなく,内視鏡的にも狭窄部の様子をバルーン越しに確認しながら拡張を行うことができる(Figure 4)
43).さらには2003年に富士フイルム社(東京港区)がダブルバルーン内視鏡を発売して以降,深部小腸の良性狭窄に対してもバルーン拡張術が積極的に行われるようになった
72).特にクローン病においては,それまで深部小腸の内視鏡的拡張術の選択肢がなかったうえ,狭窄に対する外科手術を繰り返すことで短腸症候群になるというリスクを抱えているため,内視鏡的に治療を行い外科手術が回避できるというのは画期的なことであった
73).

バルーン拡張術は,狭窄が複数ある場合でも,肛門側から順番に拡張し,内視鏡を通過させることによって,個数に制限なく適応することができる
74).しかし一つの狭窄に対して腸管長軸方向に分割して拡張術を行うことは基本的にない.狭窄の口側端,肛門側端双方から,バルーンが十分出るようにセットして目標値まで膨張させるのが手技的なポイントの一つである.拡張用バルーンはどの製品も有効長が約5cm長あり,理論上は狭窄長がこの範囲内にあれば適応できるが,実際は膨張の過程でバルーンが狭窄部から逸脱したり,狭窄長が長いほど抵抗が強く無理をすれば腸管穿孔のリスクが上がったりするため,狭窄長2-3cm以内のものを適応としている施設が多いと思われる
43),65),67).狭窄長が短ければ短いほど効果が高く,最も有効なのは膜様狭窄である.
EBDの手順は30年以上にわたる長い歴史のなかでほぼ標準化されている.まず内視鏡検査で,狭窄の程度を肉眼所見とスコープが通過するか否かを中心に評価する.また狭窄内に活動性の深い潰瘍がないことも確認する.次に内視鏡下にガストログラフィンを注入し消化管造影を行って狭窄長の評価を行う.同時に管外へ造影剤のリーク,すなわち瘻孔がないことを確認する.狭窄をスコープが越えない場合は,造影チューブを通したり,鉗子孔から造影剤を圧入したりして,必ず狭窄の口側から造影を行う.造影検査を行うため,少なくとも初回のEBD時はX線透視室で施行する.上市されている拡張用バルーンは,φ6-8mm,φ8-10mm,φ10-12mm,φ12-15mm,φ15-18mm,φ18-20mmという具合に段階的に拡張できるようにラインアップされている.φ10mm径以上のスコープが通過することを拡張のゴールとしたとき,φ12mmの拡張では足りないことがあるが,φ15mmまで拡張すれば概ね全症例で目的を達する
43).大は小を兼ねず,拡張前に評価した狭窄の径に合わせて小さいものから順番に使用する.拡張用バルーンは加圧(atm)に比例してバルーン径が無段階に大きくなるが,その目安として加圧とバルーン径の関係を3点,製品に取り付けられたタグに明示してあることが多い.これを参考にしながら,最小径から段階的に大きい径に上げていく.透視下で施行する場合,加圧器(インデフレーター)に満たす液体は蒸留水にガストログラフィンを加えたものとし,拡張が有効であるか否かは,バルーンを前後に動かすことと,透視でノッチ(notch)を確認することにより行う(Figure 5).バルーンがほとんど抵抗なく前後に動く場合,拡張術は効いていない.ノッチが出ていなくても必ずしも拡張術が無効ということはないが,ノッチが出ていてそれが拡張術により消失した場合は間違いなく有効である.拡張術が効果的であれば,バルーンを萎ませた後に狭窄部は腸管長軸方向に適度な裂創を生じており少量の出血を伴う.基本的には拡張術1回ごとに内視鏡で狭窄部位を観察し,穿孔を含む予想外の深い裂創を生じていないことと,持続する多量の出血がないことを確認する.このときの所見により,次の拡張術を行うか否か,次の回でバルーンの加圧量を上げるか否かを判断する.1回の拡張時間,一つの狭窄に対して1日に行う拡張術の回数の上限,1日の治療でもとの径の何%まで拡張可能かの上限について,ガイドラインや添付文書内に明記されたものはない.これらのうち,1回の拡張時間は1-2分間としている施設が多いようである
62),69).無理をおして一度に目標値を達成する必要は全くなく,1週間以内に2セッション目を施行すればよい.なお本稿では,拡張術の内視鏡開始ボタン押下から終了ボタン押下までを「セッション」と定義する.EBDでは1セッションのなかで複数回の拡張術を行うことがある.

EBDは,限局した範囲の腸管内圧を人工的に異常に上昇させる行為である.人間は体内の腔の内圧が異常に上昇すると疼痛を生じるもので,拡張術の施行中は多くの患者が疼痛を訴える.この苦痛を低減させるため,EBDの際は鎮痛薬や鎮静薬が必須である
75),76).ただし,鎮痛鎮静薬によって全く痛みを訴えられない状態にしてしまうと,過拡張のサインを見逃してしまう恐れもあり,意識下鎮静(conscious sedation)にとどめ,ある程度痛みを自覚できるようにしておくべきという意見もある
77).この匙加減については二律背反で,患者ごと,拡張術ごとに調整する必要がある
78).
Ⅴ Radial incision and cutting (RIC)法
RIC法は,良性難治性食道狭窄に対する治療法として,2012年にMutoらにより初めて報告された
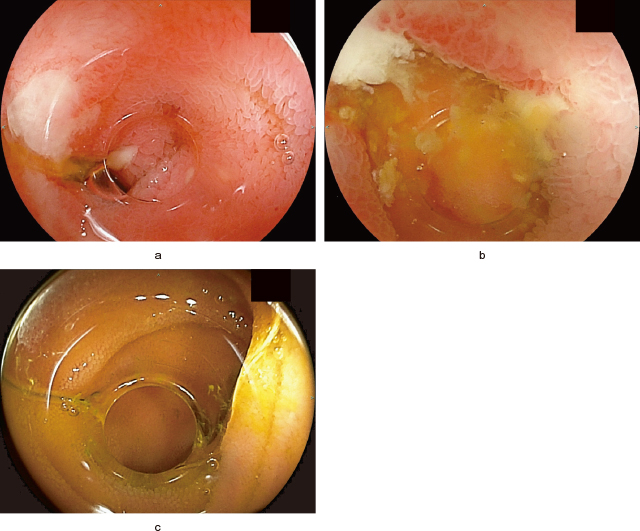
79).狭窄を形成している肉芽や瘢痕組織を全周に広く切除することで,大径の内腔確保を目指した内視鏡的拡張術の一つである.方法論的には,既に普及しているESD法の変法であり,ESDデバイスの一つであるInsulation Tip(IT) knifeまたはIT knife nano(いずれもオリンパス社,東京・新宿)を使用する.狭窄を形成している肉芽を放射状に切開して(A)フラップを形成し(B),このフラップを順に切除して(C),内腔を確保する(D)(Figure 6上段).
食道狭窄に対する治療では,施行回数,6カ月後の開存率,合併症発生率のいずれにおいてもEBDと比較してRIC法のほうが優れていたという報告がある
80),81).RIC法は食道において開発された治療法であり,また最初の報告からの歴史が浅いこともあって,他の臓器に応用されたという報告は少ない.理論的にはすべての消化管に応用が可能であるが,とりわけ直腸は腸管外に臀部の組織が裏打ちしているため穿孔のリスクが低く,さらに外科手術後の場合はステープラーや縫合糸が切除ラインの目印になるため安全に施行できる.
直腸の外科手術後に吻合部狭窄をきたすと,便の通過障害により著しいQOLの低下を招く.また,内科的または内視鏡的な狭窄治療でQOLが改善しなければ,次の選択肢は外科的手術であり人工肛門造設を余儀なくされる例も少なくない.ブジー法やバルーン拡張術で意図したような効果が得られなかったり,一時的に効果が得られても短期間で再狭窄を起こしたりしたケースで,これを解決しうる次のオプションとしてRICが考慮される
82)~89).
直腸吻合部狭窄の肉芽を切除するという発想は,ESDが普及する前の2000年前後にレーザー治療で行われていた歴史がある
90).従来の機械的拡張と比較して新発想の治療法で,それなりに治療成績もよかったようだが,消化管内視鏡領域におけるレーザー治療じたいが衰退したのに伴って行われなくなった.一方ESDはその普及とともに,数多くのデバイスが開発され,また高周波装置の性能も格段に向上した.ESDの技術は,他のさまざまな内視鏡治療にも応用されており,RICもその1例と言える.高周波装置の設定は各施設の大腸ESDの設定に準じるのでよく,基本的に切開波で切除を行う
86).放射状切開は,狭窄の口側および肛門側の粘膜の高さを目安にして十分に深く,また全周に対して少なくとも4カ所以上に入れる.放射状切開が浅いと,その後のフラップ・カットが,表層を薄くそぎ落とすだけになってしまい効果が悪い.前述のごとく,消化管吻合のステープラーが出てくるまでは全層切除になることはないので,切開や切除の深度についてはステープラーがよいランドマークになる(Figure 6下段).
外科手術後の吻合部狭窄には,吻合部と腸管壁の間に形成される膜様狭窄と,吻合部周囲組織の強固な線維化による瘢痕性狭窄がある
91).瘢痕性狭窄の一部は従来の機械的拡張では治療困難であったが,RICはそのようなケースでも解決策になる可能性がある.デバイスのブレード長は3.5-4.0mmであるが,狭窄長がその範囲である必要はなく,バルーン拡張術と違って,腸管長軸方向に分割して拡張術を行うことができる.現在のところ適応狭窄長に決められたものはないが,少なくともバルーン拡張術の対象になる2-3cm長の病変は治療可能である(Figure 7)(電子動画 1).
電子動画 1
下部消化管の良性狭窄に対してRIC法を応用したという報告はまだまだ少ない.報告されているものの多くは前治療があり,従来の機械的拡張術に抵抗を示すもの,機械的拡張術を多数回繰り返しているもの,ステープラーが露出しているためにバルーンを拡張すると破れてしまうものなどに適応されている.RIC法はそのような症例であっても少ないセッション数で効果を上げており,再狭窄が起きにくいか,起きるまでの時間を延ばすことができているように思われる(Table 1)
82)~89).高周波装置とESD用ナイフを使用して,放射状切開だけを加えるEndoscopic electorocautery incision(EECI)または瘢痕切除をほとんど行わないEndoscopic incision and selective cutting(EISC)という手技も今もって行われている
92)~96).彼らがフラップ・カットを行わないのは,RIC法は全周性のESDを行っているようなものでむしろ狭窄の温床になる可能性があるというのが言い分である
97).RICやEECIの後に続けてバルーン拡張術を何セッションか加えるとより効果が高いとする報告もある
98).Table 1にはRICが初めて報告された2014年以降で,高周波装置を使用した切開を伴う下部消化管拡張術の成績を提示する.今年になってMoroiらの多施設研究
89)が発表されるまでは,炎症治癒後の狭窄に適応した報告はなく,すべて術後吻合部狭窄に対する手技で,直腸が圧倒的に多かった.いずれも少数例のケースレポートやケースシリーズのみであるが,報告されている範囲では治療法間で成績に差はないように見える.ただし最近になるにつれてEECIやEISCの報告は減っている.
Ⅵ 治療成績とわが国における保険診療上の扱い
(1)合併症
内視鏡的拡張術の代表的な合併症は,腸管穿孔と出血である.Morarらはクローン病による狭窄に対するEBDについてメタ解析を行い,564患者,1,228セッションのうち,合併症率(穿孔+出血)は6.4%(95% CI:5.0-8.2;I2 4.0%)と算出した.さらに穿孔だけに限ると,654患者,1,281セッション中,3%(95% CI;2.2-4.0%;I2 0%)であるとしている.バルーンの拡張径や,目標圧到達後に減圧するまでの時間(拡張時間)と,合併症率との間には明らかな相関は認められなかった
99).その一方で,狭窄長が5cmを超えると穿孔のリスクが上がるとする報告もある
100).本稿のテーマである下部消化管の狭窄には該当しないが,Josinoらは食道の良性狭窄に対する拡張術について,ブジー法とEBDを比較した系統的レビュー論文のなかで,出血についても穿孔についても,両治療法の間で差はないと結論した
101).同様にXinopoulosらは直腸の術後吻合部狭窄に対する拡張術について,2002年から2004年の間に行った15例のブジー法と,2005年から2008年の間に行った24例のEBDとを遡及的に比較検討し,両群とも大きな合併症はなく,治療成績も差がなかったと報告している
102).合併症が生じたのちにどのような転帰をたどったかについて詳しくまとめた文献はないが,Bettenworthらはクローン病の小腸大腸狭窄に対するEBDを受けた1,463人の患者のなかで,2.8%がEBD手技の合併症により入院を要したとまとめている
65).検索しえた範囲では,これまでのところ内視鏡的拡張術の合併症により救命ができなかったという事案は報告されていない.ただし消化管の内視鏡的拡張術の合併症として生じる穿孔は,頻度は必ずしも高くないが,ひとたび起きると大穿孔になり外科的手術を要すほど重篤になるものと思われる.特に機械的拡張術の場合は,もとの狭窄径から一度に何倍にも拡げることを目標にせず,狭窄径に合わせて径の小さいデバイスから始め,その都度内視鏡で狭窄部の裂創の程度や出血の量を確認しながら,順々に無理のない範囲でサイズアップしていくことが,現時点で考えうる最大の合併症予防策と考えられる.
(2)再狭窄
下部消化管の良性狭窄に対する拡張術の目的は,便の通過障害を改善し,それに伴う症状を軽快させることである.前述のように,その目安は外径φ10mm以上のスコープが通過できることである.ところが長きにわたり行われてきた機械的拡張術では,治療により一度目標値の開存が得られたのちに再狭窄を起こしやすいことが問題になってきた.Araujoらは結腸直腸術後吻合部狭窄に対するEBDにおいて,92%の症例で目的を達したものの,18%の症例で再狭窄を起こし,2-4セッションの追加拡張を要したと報告している
103).Belvedereらの調査では,結腸直腸狭窄に対するEBDで87%の患者が短期間(3週間)は症状の改善を自覚していたのに,4カ月後までにこの割合が66%まで減少していた.つまりこの差にあたる患者においては,一旦改善した狭窄が再燃した疑いがあると考えられた
104).Pietropaoloらの検討では,1セッションのみで狭窄にまつわる臨床的な問題が解決する割合は,EBDで約77%,ブジー法で約52%と算出している
105).Tanらはその著書のなかで,機械的拡張では瘢痕はただ裂けるだけで,その裂創が治癒する過程において新たな狭窄を生じることが通過障害再燃の理由ではないかと述べている
95).再狭窄は膜様狭窄よりも瘢痕性狭窄のほうが生じやすいと考えられている.しかしその対策法については特にエビデンスと呼べるものがなく,例えばバルーン拡張術の拡張時間を長くすればするほど再狭窄までの時間稼ぎができるのか否かとか,機械的拡張術の繰り返し症例では何回目で無効の判断をすればよいのかといったことに一定の見解はない.
拡張術後の再狭窄を起こしにくくする手段として,ステロイドの使用が最近再び注目を浴びてきている.きっかけは2010年前後に,環周率の高い食道ESDの直後にトリアムシノロンアセトニドの局所注入を行うと,術後狭窄が予防できるとする報告が本邦から相次いで発表されたことにある
106).実は狭窄予防のためのステロイド局注は拡張術後が原法であって
107),108),ESD後はこれを応用したものである.ステロイドのなかでもトリアムシノロンアセトニドがよく使用されているのは,もともとケナコルトⓇ-A水懸注薬の適応症に「食道拡張術後」が入っていたことがヒントになっている
109).食道拡張術にステロイドを併用するのは,古くは1970年代に
107),本邦でも1990年代から有効性の報告がある
108).下部消化管でも同様の効果を期待して,適応外使用ながら拡張術後のステロイド局注が試みられている.角田らはEBD後短期間に再狭窄をきたし再拡張を繰り返した,閉塞性大腸炎による良性大腸狭窄に対し,トリアムシノロン局注を併用したところ長期開存が得られたと報告した
109).また五十畑らは同様にEBD後の再狭窄を繰り返した狭窄型虚血性大腸炎に対しメチルプレドニゾロン局注を併用したところ狭窄の改善を得られたと述べた
110).同様にEastらは,週末回腸を含むクローン病の狭窄においてもEBD後のステロイド局注に効果があるという研究結果を報告している
111).
(3)医科診療報酬点数表上の扱いと問題点
本稿で紹介した内視鏡的な狭窄拡張術はK735-2小腸・結腸狭窄部拡張術(内視鏡によるもの)が保険診療上適用され,令和4年度の改訂時点で11,090点の診療報酬がついている
112).保険診療上,拡張の方法については特に規定されていないため,本稿で紹介したどの方法であっても,内視鏡下に施行したものであればK735-2で算定できる.クローン病の小腸狭窄に対する拡張術を想定して,バルーン内視鏡やスパイラル内視鏡を使用した場合は3,500点の高額加算がついている.しかし大腸ESDにおけるバルーン内視鏡加算と違って,他に条件が付されていないことには問題があり,下部消化管用汎用スコープで到達可能なものについてはみだりに加算しないよう自制されたい.手技料は短期間または同一入院期間中(1シリーズ)において2回(=手技的にはセッションと同義)まで算定可能と明記されており,バルーン拡張術の項で述べたとおり,無理をおして一日のうちに目標値を達成する必要は全くなく,1週間を目安に2セッション目を施行すればよい.令和2年度の改訂までは1回(=1シリーズあたり1セッション)に限り算定とされていたことを考えると,より治療の実情に合わせた評価がなされるようになったと言える.ところが連続する2セッションの拡張術で目標を達成しなかった場合に,3セッション目までにどの程度期間をあければこれを再治療(2シリーズ目)の1回目として算定してよいのかということには決まりがなく,各実施施設や各地域の審査委員会の判断に委ねられている.入院で治療を行う場合は,7日以内の同一傷病名による再入院はDPC算定上の問題が生じるため,このあたりをリセットポイントにしている国内施設が多いのではないかと思われる.上記のように消化管狭窄は治療後の再狭窄のために複数セッションの拡張術を要すことが少なくなく,どこまでが連続治療で,どこからが再治療かということには定義づけが必要ではないかと考えている.また,拡張用のアタッチメントを装着せずに結果的に内視鏡ブジーになってしまった症例を,デバイスを用いる他の拡張術と同列に扱ってよいのかとか,従来の機械的拡張術とは手技的な発想が異なるRICを保険適応の治療として他の拡張術と同列に扱ってよいのかとかいうことについても,厳密には多少の疑問を残しているのが現状である.
Ⅶ 将来展望
日本消化器内視鏡学会が監修・責任編集している消化器内視鏡ハンドブックの最新版である改訂第2版(2017年刊行)のなかで,大腸狭窄治療について記載があり,その冒頭は「大腸狭窄をきたす良性疾患では,原則的にバルーン拡張術を行い」という一節で始まる
113).これは2012年発行のハンドブック第1版,ハンドブックの前身で2006年刊行の消化器内視鏡ガイドライン第3版でも同様で,少なくともここ15年以上にわたって下部消化管の良性狭窄に対する拡張術の標準治療はずっとEBDである
114),115).EBDは合併症率が低いことに加え,手技が簡便で,汎用性もあり,目的達成の側面からしても大多数の症例はEBDで事足りるというのが,これに取って代わる治療法が育たない要因だろう.良性消化管狭窄に対する内視鏡的拡張術は,ブジーの時代を含め,数分内の短時間に物理的に無理やり拡げて,一度でだめなら少し間をあけて同じことを繰り返すというやり方が長きにわたり主流であり続けている.
その意味でRIC法は管腔を狭窄させている組織を削って取るという,機械的な拡張術とは発想の異なる新たな治療法と言える.機械的拡張術に抵抗性の症例に有効であったり,再狭窄までの時間を延長することができたりという点で,従来法を凌駕している側面もあるが,EBDが抱えている再狭窄や治療繰り返しの問題を完全に解決するには至っておらず,未だこの分野のゲームチェンジャーたりえていない.
2016年,Abbott Vascular社(米国イリノイ州)が製造した,冠動脈拡張用の生体吸収性ステントが世界で初めてアメリカ食品医薬品局の承認を受けた
116).本ステントは外科手術で使用する吸収糸と同じ,自然分解性ポリマー(ポリジオキサノン)を材料としている
117).冠動脈を月単位でゆっくり時間をかけて拡張し,2年後には跡形もなく消え去るということで,革新的で商業的にもたいへん期待されていた.ところがステント血栓症の発生リスクが高いことが報告されて,日本での保険収載からわずか数カ月後に製品じたいの販売が中止となり,循環器の分野では開発までもすっかり下火になってしまった歴史がある.翻って消化管においては,加水分解されたステントが詰まって臨床的に問題になる可能性は低く,海外では既に臨床応用されて現在に至る
118).本邦でも特に食道において,外科手術やESD後の難治性狭窄の治療もしくは予防目的での臨床導入を目指して,複数の施設で有効性の検討や新規開発が進められている
119).下部消化管でも特に拡張術後の再狭窄予防に応用できると考えられ,これまでステント治療が適応になかった良性狭窄にとってはエポックメイキングな方法と期待される(Figure 8).
Ⅷ おわりに
下部消化管の良性狭窄に対する内視鏡治療の現状について解説し,問題点と将来展望について述べた.良性狭窄の治療法が,さまざまな問題を抱えながら開発が進まないことのもう一つの理由は,症例の絶対数が少ないことにある.個々の施設で集積できる症例数には限界があり,特に難治性狭窄の治療においては,院内での外科との連携や,病病連携,病診連携が必須である.将来的にも,消化管の拡張術は外科ではなく内視鏡治療が主役であろうと思われる.より有効で侵襲性の少ない,患者に優しい治療法の開発が望まれる.
本論文内容に関連する著者の利益相反:なし
補足資料
電子動画 1 RIC法の実際.
Figure 7と同一症例の動画.治療時間は約60分.その後2年以上にわたり再狭窄を起こすことなく良好に経過している.
文 献
- 1. Pregun I, Hritz I, Tulassay Z et al. Peptic esophageal stricture:medical treatment. Dig Dis 2009; 27:31-7.
- 2. 太田 弓子.【外科医が知っておくべき-最新Endoscopic Intervention】.消化管 幽門狭窄に対する内視鏡的金属ステント留置術.臨床外科 2018;73:176-9.
- 3. Chan J, Hilden K, Fang J et al. Duodenal and colonic stent placement with 0.025” and 0.035” guidewires is equally safe and effective. Dig Dis Sci 2012; 57:726-31.
- 4. 入江 理絵, 土岐 彰, 千葉 正博ほか.先天性食道狭窄症の治療方針―自験10例からの考察―.日小外会誌 2019;55:933-8.
- 5. 青沼 宏, 岡村 慎也, 大久保 剛ほか.成人の先天性直腸膜様狭窄の1例.日本大腸肛門病会誌 1992;45:466-70.
- 6. Troncone E, Fugazza A, Cappello A et al. Malignant gastric outlet obstruction:Which is the best therapeutic option? World J Gastroenterol 2020; 26:1847-60.
- 7. Boeding JRE, Ramphal W, Crolla RMPH. Ileus caused by obstructing colorectal cancer-impact on long-term survival. Int J Colorectal Dis 2018; 33:1393-400.
- 8. 福島 尚子, 矢野 文章, 秋元 俊亮.25歳難治性十二指腸潰瘍狭窄の1例.日臨外会誌 2020;81:1786-91.
- 9. Abraham NS, Graham DY. NSAIDs and gastrointestinal complications:new clinical challenges. Expert Opin Pharmacother 2005; 6:2681-9.
- 10. 大塚 和朗, 竹中 健人, 渡辺 守.炎症性腸疾患の診断と活動性評価における内視鏡・画像診断の進歩.日消誌 2018;115:254-61.
- 11. Takeuchi K, Harada K, Hiraoka S et al. Usefulness of Intestinal Ultrasound to Detect Small Intestinal Stenosis in Patients with Crohnʼs Disease J Ultrasound Med 2022 Jun 11. doi:10.1002/jum.16038. Online ahead of print.
- 12. Park SC, Jeen YT. The Clinical Significance and Risk Factors of Colorectal Stricture in Ulcerative Colitis. Gut Liver 2020; 14:535-6.
- 13. Mehmood F, Khalid A. Mahmood S. Colonic Stricture Secondary to Recurrent Ischemic Colitis. Cureus 2021; 13:e15478.
- 14. 鈴木 将大, 三井 啓吾, 貝瀬 満ほか.内視鏡の読み方 終末回腸に多発する潰瘍・狭窄により再発性腸閉塞をきたした回腸結核の1例.臨床消化器内科 2017;33:124-8.
- 15. 堀江 知史, 細江 直樹, 石川 景子ほか.内視鏡的拡張術が有効であった非特異性多発性小腸潰瘍症の1例.Progress of Digestive Endoscopy 2017;91:160-1,12.
- 16. 永山 学, 矢野 智則, 坂本 博次ほか.【小腸の炎症性病変を見直す】Cryptogenic multifocal ulcerous stenosing enteritis(CMUSE)の病態.Intestine 2017;21:526-30.
- 17. 石原 立, 有馬 美和子, 飯塚 敏郎.食道癌に対するESD/EMRガイドライン.日本消化器内視鏡学会雑誌 2020;62:221-71.
- 18. Hikichi T, Nakamura J, Takasumi M et al. Prevention of Stricture after Endoscopic Submucosal Dissection for Superficial Esophageal Cancer:A Review of the Literature. J Clin Med 2020; 10:20.
- 19. 竹内 学, 橋本 哲, 小林 正明ほか.食道ESD後の狭窄対策.日本消化器内視鏡学会雑誌 2011;53:3064-72.
- 20. Lian L, Stocchi L, Remzi FH et al. Comparison of Endoscopic Dilation vs Surgery for Anastomotic Stricture in Patients With Crohnʼs Disease Following Ileocolonic Resection. Clin Gastroenterol Hepatol 2017; 15:1226-31.
- 21. Rice TW. Anastomotic stricture complicating esophagectomy. Thorac Surg Clin 2006; 16:63-73.
- 22. 里見 大介, 榊原 舞.ステロイド投与が有効であった大腸術後吻合部狭窄の4例.日本大腸肛門病学会雑誌 2018;71:41-7.
- 23. Luchtefeld MA, Milsom JW, Senagore A et al. Colorectal anastomotic stenosis. Results of a survey of the ASCRS membership. Dis Colon Rectum 1989; 32:733-6.
- 24. Guyton KL, Hyman NH, Alverdy JC. Prevention of Perioperative Anastomotic Healing Complications: Anastomotic Stricture and Anastomotic Leak. Adv Surg 2016; 50:129-41.
- 25. Wang S, Li X, Zhang C et al. Balloon dilatation complications during esophagogastric anastomotic stricture treatment under fluoroscopy:Risk factors, prevention, and management. Thorac Cancer 2022; 13:1570-6.
- 26. 小柳 和夫, 小澤 壯治, 數野 暁人.食道癌術後縫合不全・吻合部狭窄の発症要因,予防対策と対応.外科 2019;81:710-5.
- 27. 濱田 円.直腸癌術後縫合不全・吻合部狭窄の発症要因,予防対策と対応.外科 2019;81:737-40.
- 28. Hallbook O, Sjodahl R. Anastomotic leakage and functional outcome after anterior resection of the rectum. Br J Surg 1996; 83:60-2.
- 29. Lim M, Akhtar S, Sasapu K et al. Clinical and subclinical leaks after low colorectal anastomosis:a clinical and radiologic study. Dis Colon Rectum 2006; 49:1611-9.
- 30. 大平 雅一, 曽和 融生, 浅井 毅.食道吻合部狭窄に対する内視鏡的治療.日消外会誌 1990;23:2507-11.
- 31. Wang WP, Gao Q, Wang KN et al. A prospective randomized controlled trial of semi-mechanical versus hand-sewn or circular stapled esophagogastrostomy for prevention of anastomotic stricture. World J Surg 2013; 37:1043-50.
- 32. Tagkalos E, van der Sluis PC, Uzun E et al. The Circular Stapled Esophagogastric Anastomosis in Esophagectomy:No Differences in Anastomotic Insufficiency and Stricture Rates Between the 25mm and 28mm Circular Stapler. J Gastrointest Surg 2021; 25:2242-9.
- 33. 篠原 徹雄, 前川 隆文, 三上 公治ほか.直腸前方切除後の吻合部狭窄の検討.日本大腸肛門病会誌 2009;62:27-31.
- 34. 大腸癌研究会.大腸癌治療ガイドライン医師用2022年版.金原出版,東京,2022.
- 35. 田上 創一, 町田 水穂, 佐近 雅宏ほか.腹腔鏡下手術が有用であったイレウスで発症した原発性小腸癌の1例.日臨外会誌 2014;75:1301-7.
- 36. 井田 在香.小腸-横行結腸バイパス術を施行した消化管閉塞を伴う進行再発大腸癌の3例.癌と化学療法 2016;43:1632-4.
- 37. Güenaga KF, Lustosa SA, Saad SS et al. Ileostomy or colostomy for temporary decompression of colorectal anastomosis. Systematic review and meta-analysis. Acta Cir Bras 2008 ; 23:294-303.
- 38. Lim T, Tham HY, Yaow CYL. Early surgery after bridge-to-surgery stenting for malignant bowel obstruction is associated with better oncological outcomes. Surg Endosc 2021; 35:7120-30.
- 39. van Hooft JE, Veld JV, Arnold D et al. Self-expandable metal stents for obstructing colonic and extracolonic cancer:European Society of Gastrointestinal Endoscopy(ESGE) Guideline-Update 2020. Endoscopy 2020; 52:389-407.
- 40. Chan RH, Lin SC, Chen PC et al. Management of colorectal anastomotic stricture with multidiameter balloon dilation:long-term resultsTech Coloproctol 2020; 24:1271-6.
- 41. 斉田 芳久.大腸閉塞に対する大腸ステント治療のコツと実際.日本消化器内視鏡学会雑誌 2016;58:2201-10.
- 42. Truong S, Willis S, Schumpelick V et al. Endoscopic therapy of benign anastomotic strictures of the colorectum by electroincision and balloon dilatation. Endoscopy 1997; 29:845-8.
- 43. 遠藤 克哉, 志賀 永嗣, 黒羽 正剛ほか.腸管狭窄に対するバルーン拡張のコツ.日本消化器内視鏡学会雑誌 2013;55:3617-23.
- 44. Kirat HT, Remzi FH, Shen B et al. Pelvic abscess associated with anastomotic leak in patients with ileal pouch-anal anastomosis(IPAA):transanastomotic or CT-guided drainage? Int J Colorectal Dis 2011; 26:1469-74.
- 45. Mangiavillano B, Auriemma F, Bianchetti M et al. Complete colonic closure with an over-the-scope clip placed for a colorectal anastomotic fistula:a big mistake. Endoscopy 2020; 52:521-2.
- 46. Shaw W. History of a Case of Introsusception;and an Account of Two Cases of Stricture in the Urethra, Removed by Tobacco Bougies;in a Letter to Dr. Redman Coxe, of Philadelphia. Med Phys J 1807; 18:350-2.
- 47. Borgeskov S, Struve-Christensen E. Bougie therapy of esophageal strictures with flexible esophagoscope by Eder-Puestowʼs method. Ugeskr Laeger 1975; 137:2692-4.
- 48. Silvis SE, Nebel O, Rogers G et al. Endoscopic complications. Results of the 1974 American Society for Gastrointestinal Endoscopy Survey. JAMA 1976; 235:928-30.
- 49. Gamliel Z, Wesson D. Prograde dilatation with Tucker bougies:a technique for managing postoperative rectal strictures. J Pediatr Surg 1991; 26:1285-8.
- 50. Garcea G, Sutton CD, Lloyd TD et al. Management of benign rectal strictures:a review of present therapeutic procedures. Dis Colon Rectum 2003; 46:1451-60.
- 51. Kashkooli SB, Samanta S, Rouhani M et al. Bougie dilators:simple, safe and cost-effective treatment for Crohnʼs-related fibrotic anal strictures. Can J Surg 2015; 58:347-8.
- 52. Bravi I, Ravizza D, Fiori G et al. Endoscopic electrocautery dilation of benign anastomotic colonic strictures:a single-center experience. Surg Endosc 2016; 30:229-32.
- 53. 落合 匠, 杉谷 通治, 岡田 豪.経肛門的腸管減圧術が低位前方切除術後吻合部狭窄改善にも有用であった1例.日本大腸肛門病会誌 1997;50:59-64.
- 54. Lee SY, Kim CH, Kim YJ et al. Anastomotic stricture after ultralow anterior resection or intersphincteric resection for very low-lying rectal cancer. Surg Endosc 2018; 32:660-6.
- 55. Morimoto K, Watanabe K, Noguchi A et al. Clinical impact of ultrathin colonoscopy for Crohnʼs disease patients with strictures. J Gastroenterol Hepatol 2015; 30(Suppl 1):66-70.
- 56. 菊池 大輔, 鈴木 悠悟, 田中 匡実.消化管狭窄に対するバルーン内視鏡と細径内視鏡を用いた新しいアプローチ;Balloon endoscopy and ultra-thin endoscopy method(BUT method).日本消化器内視鏡学会雑誌 2019;61:2510-7.
- 57. AIRC-人工知能研究センター.AIST日本人の手の寸法データ. https://www.airc.aist.go.jp/dhrt/hand/data/list.html(2022年5月20日閲覧).
- 58. Josino IR, Madruga-Neto AC, Ribeiro IB et al. Endoscopic Dilation with Bougies versus Balloon Dilation in Esophageal Benign Strictures:Systematic Review and Meta-Analysis. Gastroenterol Res Pract. 2018 Jul 15; 2018:5874870.
- 59. Virmeet V Singh VV, Draganov P. Efficacy and safety of endoscopic balloon dilation of symptomatic upper and lower gastrointestinal Crohnʼs disease strictures. J Clin Gastroenterol 2005; 39:284-90.
- 60. 矢野 智則, 坂本 博次, 小林 泰俊ほか.クローン病小腸狭窄に対する内視鏡的バルーン拡張術(動画付き).日本消化器内視鏡学会雑誌 2018;60:1107-15.
- 61. Shiwaku H, Yamashita K, Ohmiya T et al. New endoscopic finding of esophageal achalasia with ST Hood short type:Corona appearance. PLoS One 2018; 13:e0199955.
- 62. Nomura T, Sugimoto S, Oyamada J et al. GI endoscopic submucosal dissection using a calibrated, small-caliber-tip, transparent hood for lesions with fibrosis. VideoGIE 2021; 6:301-4.
- 63. 山本 博徳, 矢野 智則, 荒木 昭博ほか.クローン病小腸狭窄に対する内視鏡的バルーン拡張術ガイドライン(小腸内視鏡診療ガイドライン追補).日本消化器内視鏡学会雑誌 2021;63:2253-75.
- 64. Biraima M, Adamina M, Jost R et al. Long-term results of endoscopic balloon dilation for treatment of colorectal anastomotic stenosis. Surg Endosc 2016; 30:4432-7.
- 65. Bettenworth D, Gustavsson A, Atreja A et al. A Pooled Analysis of Efficacy, Safety, and Long-term Outcome of Endoscopic Balloon Dilation Therapy for Patients with Stricturing Crohnʼs Disease. Inflamm Bowel Dis 2017; 23:133-42.
- 66. Rueda Guzmán A, Wehkamp J, Kirschniak A et al. Endoscopic balloon dilatation of Crohnʼs-associated intestinal strictures:High patient satisfaction and long-term efficacy. United European Gastroenterol J 2016; 4:794-9.
- 67. Ragga J, Garimellaa V, Castb J et al. Balloon Dilatation of Benign Rectal Anastomotic Strictures - A Review. Dig Surg 2012; 29:287-91.
- 68. Whitworth PW, Richardson RL, Larson GM. Balloon Dilatation of Anastomotic Strictures. Arch Surg 1988; 123:759-62.
- 69. Breysem Y, Janssens JF, Coremans G et al. Endoscopic balloon dilation of colonic and ileo-colonic Crohnʼs strictures:long-term results. Gastrointest Endosc 1992; 38:142-7.
- 70. Couckuyt H, Gevers AM, Coremans G et al. Efficacy and safety of hydrostatic balloon dilatation of ileocolonic Crohnʼs strictures:a prospective longterm analysis. Gut 1995; 36:577-80.
- 71. 小林 清典, 小川 大志, 勝又 伴栄.大腸狭窄に対する内視鏡的バルーン拡張術.日本消化器内視鏡学会雑誌 2021;48:1252-8.
- 72. Okazaki N, Harada K, Hiraoka S et al. Findings of Retrograde Contrast Study Through Double-balloon Enteroscopy Predict the Risk of Bowel Resections in Patients with Crohnʼs Disease with Small Bowel Stenosis. Inflamm Bowel Dis 2017; 23:2097-103.
- 73. Lan N, Shen B. Endoscopic Stricturotomy Versus Balloon Dilation in the Treatment of Anastomotic Strictures in Crohnʼs Disease. Inflamm Bowel Dis 2018; 24:897-907.
- 74. Rieder F, Zimmermann EM, Remzi FH et al. Crohnʼs disease complicated by strictures:a systematic review. Gut 2013; 62:1072-84.
- 75. Hirai F, Beppu T, Takatsu N et al. Long-term outcome of endoscopic balloon dilation for small bowel strictures in patients with Crohnʼs disease. Dig Endosc 2014; 26:545-51.
- 76. Lerner MZ, Bourdillon AT, Dai F et al. Safety considerations for esophageal dilation by anesthetic type:A systematic review. Am J Otolaryngol 2021; 42:103128.
- 77. 三浦 昭順, 宮本 昌武, 加藤 剛ほか.食道癌術後狭窄に対する内視鏡治療のコツ.日本消化器内視鏡学会雑誌 2009;51:1342-8.
- 78. 後藤田 卓志, 赤松 拓司, 阿部 清一郎ほか.内視鏡診療における鎮静に関するガイドライン(第2版).日本消化器内視鏡学会雑誌 2020;62:1635-81.
- 79. Muto M, Ezoe Y, Yano T et al. Usefulness of endoscopic radial incision and cutting method for refractory esophagogastric anastomotic stricture(with video).Gastrointest Endosc 2012; 75:965-72.
- 80. Yano T, Yoda Y, Satake H et al. Radial incision and cutting method for refractory stricture after nonsurgical treatment of esophageal cancer. Endoscopy 2013; 45:316-9.
- 81. Pih GY, Kim DH, Na HK et al. Comparison of the Efficacy and Safety of Endoscopic Incisional Therapy and Balloon Dilatation for Esophageal Anastomotic Stricture. J Gastrointest Surg 2021; 25:1690-5.
- 82. Osera S, Ikematsu H, Odagaki T et al. Efficacy and safety of endoscopic radial incision and cutting for benign severe anastomotic stricture after surgery for lower rectal cancer(with video).Gastrointest Endosc 2015; 81:770-3.
- 83. Kawaguti FS, Martins BC, Nahas CS et al. Endoscopic radial incision and cutting procedure for a colorectal anastomotic stricture. Gastrointest Endosc 2015; 82:408-9.
- 84. Harada K, Kawano S, Hiraoka S et al. Endoscopic radial incision and cutting method for refractory stricture of a rectal anastomosis after surgery. Endoscopy 2015; 47(Suppl 1):E552-3.
- 85. Asayama N, Nagata S, Shigita K et al. Effectiveness and safety of endoscopic radial incision and cutting for severe benign anastomotic stenosis after surgery for colorectal carcinoma:a three-case series. Endosc Int Open 2018; 6:E335-9.
- 86. 永田 信二, 朝山 直樹, 鴫田 賢次郎ほか.大腸癌術後吻合部狭窄に対するradial incision and cutting(RIC)法.日本消化器内視鏡学会雑誌 2019;61:186-91.
- 87. Nepal P, Mori S, Kita Y et al. Radial incision and cutting method using a transanal approach for treatment of anastomotic strictures following rectal cancer surgery:a case report. World J Surg Oncol 2019; 17:48.
- 88. Lee TG, Yoon SM, Lee SJ. Endoscopic radial incision and cutting technique for treatment-naive stricture of colorectal anastomosis:Two case reports. World J Gastrointest Surg 2020; 12:460-7.
- 89. Moroi R, Shiga H, Nochioka K et al. Endoscopic radial incision and cutting for benign stenosis of the lower gastrointestinal tract:An investigation of novel endoscopic treatment in multicenter trial. J Gastroenterol Hepatol 2022; 37:1554-60. doi:10.1111/jgh.15882.
- 90. 佐藤 純人, 石田 康男, 畑山 年之ほか.直腸癌術後の難治性吻合部狭窄に対して内視鏡下半導体レーザー治療が著効した1例.日本消化器内視鏡学会雑誌 2011;53:2012-7.
- 91. 小田 一郎, 阿部 清一郎, 野中 哲ほか.食道癌治療後良性狭窄に対する内視鏡治療のコツ.日本消化器内視鏡学会雑誌 2016;58:1250-8.
- 92. Kwon JH, Han KH, Kim MH et al. Two cases of electrocautery incision therapy using an insulated-tip knife for treatment of symptomatic benign short-segment colonic stenosis following colonic resection. Korean J Gastroenterol 2014; 64:164-7.
- 93. Wallstabe I, Teich N. Successful endoscopic incision of pouchanal stricture in a patient with ulcerative colitis. Tech Coloproctol 2015; 19:429-30.
- 94. Bravi I, Ravizza D, Fiori G et al. Endoscopic electrocautery dilation of benign anastomotic colonic strictures:a single-center experience. Surg Endosc 2016; 30:229-32.
- 95. Tan Y, Wang X, Lv L et al. Comparison of endoscopic incision and endoscopic balloon dilation for the treatment of refractory colorectal anastomotic strictures. Int J Colorectal Dis 2016; 31:1401-3.
- 96. Lee TG, Yoon SM, Lee SJ. Endoscopic radial incision and cutting technique for treatment-naive stricture of colorectal anastomosis:Two case reports. World J Gastrointest Surg 2020; 12:460-7.
- 97. Jain D, Sandhu N, Singhal S. Endoscopic electrocautery incision therapy for benign lower gastrointestinal tract anastomotic strictures. Ann Gastroenterol 2017; 30:473-85.
- 98. 江副 康正, 青山 育雄, 武藤 学.難治性食道良性狭窄に対する radial incision and cutting(RIC)法.日本消化器内視鏡学会雑誌 2013;55:3160-6.
- 99. Morar PS, Faiz O, Warusavitarne J et al. Systematic review with meta-analysis:endoscopic balloon dilatation for Crohnʼs disease strictures. Aliment Pharmacol Ther 2015; 42:1137-48.
- 100. Bessissow T, Reinglas J, Aruljothy A et al. Endoscopic management of Crohnʼs strictures. World J Gastroenterol 2018; 24:1859-67.
- 101. Josino IR, Madruga-Neto AC, Ribeiro IB et al. Endoscopic Dilation with Bougies versus Balloon Dilation in Esophageal Benign Strictures:Systematic Review and Meta-Analysis. Gastroenterol Res Pract 2018; 2018:5874870.
- 102. Xinopoulos D, Kypreos D, Bassioukas SP et al. Comparative study of balloon and metal olive dilators for endoscopic management of benign anastomotic rectal strictures:clinical and cost-effectiveness outcomes. Surg Endosc 2011; 25:756-63.
- 103. Araujo SE, Furtado Costa A. Efficacy and safety of endoscopic balloon dilation of benign anastomotic strictures after oncologic anterior rectal resection. Report on 24 cases. Surg Laparosc Endosc Percutaneous Tech 2008; 18:565-8.
- 104. Belvedere B, Frattaroli S, Crabone A et al. Anastomotic strictures in colorectal surgery:treatment with endoscopic balloon dilation. G Chir 2012; 33:243-5.
- 105. Pietropaolo V, Masoni L, Ferrara M et al. Endoscopic dilation of colonic postoperative. Surg Endosc 1990; 4:26-30.
- 106. Hanaoka N, Ishihara R, Takeuchi Y et al. Intralesional steroid injection to prevent stricture after endoscopic submucosal dissection for esophageal cancer:a controlled prospective study. Endoscopy 2012; 44:1007-11.
- 107. Mendelsohn HJ, Maloney WH. The treatment of benign strictures of the esophagus with cortisone injection. Ann Otol Rhinol Laryngol 1970; 79:900-4.
- 108. 大川 敬一, 恩田 昌彦, 宮下 正夫ほか.食道癌術後の難治性吻合部狭窄に対するステロイド局注と内視鏡拡張術併用療法の1例.日本消化器内視鏡学会雑誌 1995;37:2740-5.
- 109. 角田 潤哉, 西 知彦, 稲熊 岳ほか.ステロイド局注が有効であった閉塞性大腸炎による大腸狭窄の1例.大腸肛門病会誌 2020;96:166-7.
- 110. 五十畑 則之, 根本 大樹, 遠藤 俊吾.内視鏡的バルーン拡張術およびステロイド局注が有効であった狭窄型虚血性大腸炎の1例.大腸肛門病会誌 2015;68:86-91.
- 111. East JE, Brooker JC, Rutter MD et al. A pilot study of intrastricture steroid versus placebo injection after balloon dilatation of Crohnʼs strictures. Clin Gastroenterol Hepatol 2007; 5:1065-9.
- 112. 社会保険研究所.医科診療報酬点数表 令和4年4月版.
- 113. 日本消化器内視鏡学会.消化器内視鏡ハンドブック 改訂第2版.日本メディカルセンター,東京,2017.
- 114. 日本消化器内視鏡学会.消化器内視鏡ハンドブック.日本メディカルセンター,東京,2012.
- 115. 日本消化器内視鏡学会.消化器内視鏡ガイドライン第3版.医学書院,東京,2006.
- 116. Rizik DG, Padaliya BB. Early US. Experience Following FDA Approval of the ABBOTT Vascular Bioresorbable Vascular Scaffold:Optimal Deployment Technique Using High Resolution Coronary Artery Imaging. J Interv Cardiol 2016; 29:546-8.
- 117. 浅原 智彦.先端外科手術用の高分子材料―生体吸収性縫合糸―.高分子 2007;56:754-7.
- 118. Walter D, van den Berg MW, Hirdes MM et al. Dilation or biodegradable stent placement for recurrent benign esophageal strictures:a randomized controlled trial. Endoscopy 2018; 50:1146-55.
- 119. Yano T, Yoda Y, Nomura S et al. Prospective trial of biodegradable stents for refractory benign esophageal strictures after curative treatment of esophageal cancer. Gastrointest Endosc 2017; 86:492-9.