要旨
H. pyloriの除菌療法の個別化療法には,抗菌薬の感受性試験に応じた抗菌薬の選択のみならず,薬物過敏症の状況に応じた薬物の選択,個々の症例の併用薬を考慮したレジメンの工夫等がある.一次除菌療法では,クラリスロマイシン(CAM)の感受性試験結果に応じてメトロニダゾール(MNZ)を活用することでの除菌率の向上が報告されている.三次除菌療法ではシタフロキサシン(STFX)を用いた除菌療法がよく行われている.ペニシリンアレルギーの症例ではCAMとMNZ,STFXとMNZの組み合わせが多い.但し,CAMやMNZは併用薬との薬物間相互作用が多く,注意が必要な薬物である.しかしながら,保険診療上はH. pyloriの除菌レジメン二次除菌まで固定されており,個別の対応をしにくいのが現状である.個々の症例に応じたレジメンが構築できるよう,制度の改善が望まれる.
Abstract
Personalized therapy for Helicobacter pylori eradication comprises optimal antimicrobial agents selected not only according to susceptibility testing but also individual patient characteristics, such as drug hypersensitivity and interactions with co-administered drugs. The eradication rate of the first-line treatment has been reportedly improved by personalized therapy using antibacterial agents selected based on bacterial susceptibility testing. In third-line therapy, a sitafloxacin-containing regimen is often used. For patients allergic to penicillin, a combination of metronidazole and clarithromycin or sitafloxacin is often prescribed. However, clarithromycin and metronidazole require caution in terms of their interaction with other concomitant drugs. Moreover, first- and second-line regimens for H. pylori eradication are inflexible in Japan’s health insurance guidelines. They should be modified to accommodate individual cases.
Ⅰ はじめに
H. pyloriの除菌療法は,2010年の11月にプロトンポンプ阻害薬(Proton Pump Inhibitor:PPI)とアモキシシリン(AMO)とクラリスロマイシン(CAM)の三剤療法から始まった.当初は90%程度の除菌率を示したが
1),CAM耐性菌の割合の増加に伴い除菌率は低下していった.しかし,2013年に,CAMをメトロニダゾール(MNZ)に置き換える二次除菌療法が認可されると,それにて90%程度の除菌率が達成できるため,本邦の一次除菌,二次除菌の二段階の除菌を経れば最終的には95%以上の症例で除菌成功に至ることとなった.一方,諸外国では一次除菌療法からの除菌率の向上をめざし,三剤療法から種々の四剤療法に移行してきている.実際,これらの治療法では90%台の除菌率が報告されている
2),3).そしてこれらの治療法での除菌率は感受性試験に応じた除菌療法に劣らないことも示されている
4).ただ,これらの治療方法は本邦で認可されていないビスマス製剤を用いたり,AMO,CAM,とMNZや類薬のチニダゾール(TNZ)を,順番で内服したり(Sequential therapy,hybrid therapy),同時に内服するものであるが(Concomitant therapy),内服期間も長く,用量も本邦保険収載のレジメンからは大きくかけ離れており,本邦で実施されることはほとんどなかった.それよりも,CAM耐性菌での,三剤PPI/AMO/MNZ療法による除菌率が高いことから,一次除菌からCAMをMNZに置き換えたり,感受性試験に応じてCAMとMNZを選択するいわゆる個別化療法が研究的に行われてきた.しかし,2015年にカリウムイオン競合型アシッドブロッカー(P-CAB)であるボノプラザン(VPZ)が除菌に用いられると,一次除菌率は再び90%台を達成できるようになり
5),現在の一次除菌療法はとりあえず三剤VPZ/AMO/CAM療法に落ち着いてきた感がある.しかし,この三剤療法での治験の成績においてもCAM耐性菌での除菌率が有意に低いことが示されており
5),一次除菌から感受性試験に応じた除菌療法を望む意見は多い.また,CAMには薬物代謝酵素のCYP3A4やトランスポータのMDR1を阻害するなど併用薬に対する影響があったり
6),QT延長も報告されている
7).また,一次除菌,二次除菌のいずれのレジメンにもAMOが含まれているが,ペニシリンアレルギーの症例には使用できない.CAMアレルギー,MNZアレルギーの症例も存在する.従って,すべての症例に一律で同一のレジメンで治療することには限界がある.本稿では,H. pylori除菌に関する個別化療法に関して,治療効果のみならず,安全性の面からも考察することとする.
Ⅱ 胃酸分泌抑制薬(PPI)の個別化療法
PPIはCYP2C19で代謝されるために,CYP2C19の遺伝子多型で血中濃度,胃酸分泌抑制効果が異なるため,CYP2C19のジェノタイプでPPIの用量を変更することで除菌率を高める方法が先進医療で行われていた
8).CYP2C19のExtensive metabolizer(EM)ではPPIの常用量では除菌率が低下するが,PPIの3-4倍量を用いることで90%以上の除菌率が達成できた.この過程で明らかになったことはH. pylori除菌療法における胃酸分泌抑制の重要性であり,標準療法でのPPIの用量はCYP2C19のPoor metabolizer(PM)に適した用量であり,EMには不十分であったということである.そのため,全例にPPIの4倍量を投与するという方法も考案され,三次除菌のレジメンであるが高い除菌率が報告された
9).その後VPZが上市され,除菌に必要な胃酸分泌抑制効果がCYP2C19遺伝子多型に依存せず安定的に得られるため
10),現在では本邦でのH. pylori除菌療法での胃酸分泌抑制薬はVPZが主流となっている.
Ⅲ 抗菌薬耐性に応じた個別化療法
1.CAM耐性検査の問題点
H. pylori感染の治療は緊急を要することはなく,感受性試験を行い,その結果に応じた抗菌薬の選択ができれば,除菌率は向上すると考えられる.メタアナリシスの結果でも,CAM耐性率が20%を超える場合には,感受性試験に応じた除菌率が有効であることが示されている
11),12).そして,クラリシッドの添付文書
13)には「用法・用量に関連する使用上の注意」のところに「本剤の使用にあたっては,耐性菌の発現等を防ぐため,原則として感受性を確認し,疾病の治療上必要な最小限の期間の投与にとどめること」とあり,添付文書上でも感受性試験が推奨されているため感受性試験をすべきであろう.しかし,本邦では感受性試験の結果に関わらず一次除菌療法で使用可能な抗生物質は決められており,感受性試験をしても選択の余地がなく,また,MNZも一次除菌での使用は原則保険適応外であり,感受性試験でCAMに耐性と判明してもMNZを一次除菌で用いることは現行の保険診療の範囲内では容易ではない.こうしたこともあり,H. pyloriの抗菌薬感受性試験は保険収載されていない.しかし,日本ヘリコバクター学会のガイドライン
14)や日本消化器病学会のステートメント
15)では,CAM耐性状況を検査して適切な抗菌薬を選択することが推奨されている.
2.CAM耐性に応じた個別化療法
1)CAMから他剤へ変更する方法
Kawaiら
16)は,三剤ランソプラゾール(LPZ)/AMO/CAM療法において,便中のH. pyloriよりCAM耐性を判断し,CAM感受性であればそのままCAMを使用し,CAM耐性であれば,CAMに代えてMNZを用いるというプロトコールで前向きの比較試験を行った.標準療法群での除菌率は71.4%であったのに対し,個別化療法群では94.3%であり,有意に除菌率が向上することが報告された.海外でもCAM耐性の場合に感受性試験に応じた抗菌薬の変更で除菌率が向上することが報告されている
17).
著者ら
8)も,通常の三剤LPZ/AMO/CAM療法においてCAM感受性であれば,CAMを用い,耐性であれば,PPIとAMO 500mgの4回投与による除菌(高用量PPI/AMO療法)を行ったところ,標準療法群での除菌率が70%であるのに対し,個別化療法群では96.0%の除菌率を達成したとしている.なお,この研究ではPPIの用量をCYP2C19遺伝子多型に応じた用量を用いている.
胃酸分泌抑制薬にVPZを使用した場合であっても,三剤VPZ/AMO/CAMの除菌率はCAM感受性では96.3%であるが,CAM耐性の場合は82.9%と低下してしまうが,個別化療法群で98.0%と高い除菌率が得られることが報告されている
18).安藤ら
19)の報告でも同様の傾向を示しており,全体として除菌率は個別化療法の方が標準療法を上回っている(Table 1).従って,CAM耐性の場合にCAMをMNZに置き換える治療は胃酸分泌抑制薬にVPZを使用しても有用な治療戦略である.
2)CAMをレジメンから除く方法
CAM耐性時にCAMをMNZに変更する戦略に加えて,新たな治療戦略の可能性が報告された.三剤VPZ/AMO/CAM療法と二剤VPZ/AMO療法を比較した前向き研究において,CAM感受性の場合では,三剤VPZ/AMO/CAM療法の除菌率がよかったものの,CAM耐性では,二剤VPZ/AMO療法の除菌率が三剤VPZ/AMO/CAM療法を上回ったのである
20).抗生物質の特性上,CAMとAMOとの間には薬力学的な拮抗作用があることが他菌種では報告されている
21).H. pylori除菌療法において,CAM感受性の場合ではCAMが奏効するためこの拮抗作用は問題ないが,CAMが弱耐性の場合には,中途半端にCAMが影響するため薬力学的拮抗作用によりAMOの効果が減じてしまうため,CAMは除菌においてマイナスに働く可能性が示唆されている
22).さらに,二剤VPZ/AMO療法では,AMOを3分割投与とすることで90%以上の除菌率を達成できることも報告されており
23),CAM耐性では,CAMをレジメンから除いてAMOの投与方法を工夫するだけで除菌率の向上が期待できる.前向きにこの戦略を証明した試験はまだ報告されていないが,こうした事実からもCAM耐性の有無を検査してから除菌レジメンを決定すべきである.
3)CAM耐性の検査方法
H. pyloriの抗菌薬感受性試験は培養法による方法が一般的であり,CAMのみならず,AMO,MNZ,ミノサイクリン(MINO),シタフロキサシン(STFX)に対する感受性試験が行われる.このうち,一次除菌療法で重要なものは,CAM耐性であり,一次除菌ではCAM耐性のみで個別化療法は可能である.
このCAM耐性は23S rRNAの2142と2143位のAからGへの⼀塩基多型(SNP)によることが分かっており,その変異の有無を検査することでCAM耐性は判別可能である.そして,迅速にこのSNPを検査する方法が開発されており,内視鏡検査を施行した当日にSNPに応じた除菌薬の処方が可能となる
24),25).実際,迅速検査による個別化療法の実例が報告されている
26).
3.三次除菌療法での個別化療法
二次除菌まで除菌に不成功である場合に三次除菌療法が行われる.三次除菌療法に関しては,学会のガイドラインではPPI(VPZ)/AMO/STFX,PPI(VPZ)/MNZ/STFX,高用量PPI/AMO療法が推奨されている
14).そのうち,STFXを用いた三次除菌は報告例も多く(Table 2),除菌率は70-90%程度であるが
27)~32),メタアナリスの結果ではVPZ/AMO/STFXを用いた除菌が最もよいとされている
33).
このSTFXを用いた除菌療法の除菌率は耐性変異であるgyrAの変異の有無の影響を受けることが報告されている
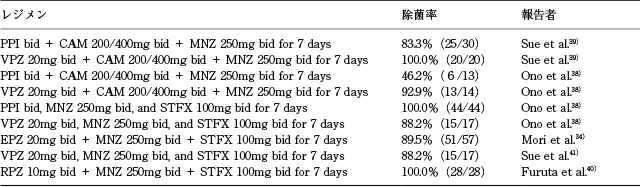
34).従って,STFX耐性の有無によってSTFXの使用を検討する必要性があるが,STFX耐性の場合の除菌レジメンの候補に関しては,一定の見解はなく,感受性試験の結果に応じて各施設で他の三次除菌の候補レジメンから選択している状況である.三次除菌療法における耐性状況別の除菌レジメンと成績についてTable 3に示す
35).これらを参考に除菌レジメンを考案することが可能かもしれない.なお,STFX耐性の頻度は7%程度と低く
31),感受性試験結果に応じた除菌率の優越性を示すには多数の症例の組み入れが必要であるが,VPZレジメンで二次除菌まで不成功の頻度は低く,実施は容易ではないと考えられる.
Ⅳ 薬物アレルギーに応じた個別化療法
除菌治療の構成薬にアレルギーがある場合には,その薬物を除菌レジメンに加えることができない.除菌療法でよく問題になるのは,ペニシリンアレルギー症例での除菌である.ペニシリンアレルギーの頻度は3-7%と比較的高く
36),37),その場合には,AMOを除いたレジメンでの除菌となる.
Table 4に本邦からのペニシリンアレルギー症例での除菌の報告例を示す.CAMとMNZを併用したレジメンは保険収載薬の組み合わせで可能であるが,本邦ではCAM耐性率が高く,PPIとの併用では除菌率が低くなるため
38),VPZの使用が推奨される
38),39).MNZとSTFXの組み合わせでは,PPIでもVPZでも良好な除菌率が報告されている
34),39)~41).他に,MINOとMNZの組み合わせも候補となる
14),42).
一次除菌療法で薬疹が出現した場合には,AMOのみならず,CAMやPPI/VPZにアレルギーの可能性もある.従って,DLST検査は参考となるが感度は十分ではないため,一次除菌での使用薬物はすべて除くなど,慎重にレジメンを検討する必要がある.
Ⅴ 併用薬を考慮した個別化療法
除菌療法を受ける症例は,H. pylori感染以外の基礎疾患を有している場合があり,併用薬との薬物間相互作用が懸念される場合もあり,除菌療法を行う場合には,個々に配慮が必要である.
PPI,VPZ,CAM,MNZのいずれも肝臓の薬物代謝酵素であるCYPの分子種への影響が報告されている
43)~47).特にCAMやMNZに関しては多くの併用薬への注意喚起がされている
13),48).CAMにはQT延長のリスクが報告されている
49).VPZとAMOによる除菌療法は,CAMはMNZを含まない点で,比較的相互作用の少ない除菌レジメンであり有用な可能性がある
23).
Ⅵ まとめ
本邦のH. pylori感染頻度は低下したが,依然として多数のH. pylori感染者が存在している.従って,H. pyloriの除菌療法は今後も多くの症例で実施されると考えられる.しかし,症例毎に耐性菌の状況,薬物過敏の有無,併用薬の状況等様々である.本稿では触れなかったが腎機能や肝機能の低下例も存在する.従って,国民総除菌の時代においては,個々の症例の状況を十分に配慮して除菌レジメンを構築すべきであり,一律のレジメンでの除菌療法は見直す時期にきていると考えられる.
本論文内容に関連する著者の利益相反:古田隆久(アストラゼネカ,武田薬品工業,第一三共)
文 献
- 1. Asaka M, Sugiyama T, Kato M et al. A multicenter, double-blind study on triple therapy with lansoprazole, amoxicillin and clarithromycin for eradication of Helicobacter pylori in Japanese peptic ulcer patients. Helicobacter 2001; 6:254-61.
- 2. Molina-Infante J, Romano M, Fernandez-Bermejo M et al. Optimized nonbismuth quadruple therapies cure most patients with Helicobacter pylori infection in populations with high rates of antibiotic resistance. Gastroenterology 2013; 145:121-8, e1.
- 3. Hsu PI, Wu DC, Wu JY et al. Modified sequential Helicobacter pylori therapy:proton pump inhibitor and amoxicillin for 14 days with clarithromycin and metronidazole added as a quadruple(hybrid) therapy for the final 7 days. Helicobacter 2011; 16:139-45.
- 4. Gisbert JP. Empirical or susceptibility-guided treatment for Helicobacter pylori infection? A comprehensive review. Therap Adv Gastroenterol 2020; 13:1756284820968736.
- 5. Murakami K, Sakurai Y, Shiino M et al. Vonoprazan, a novel potassium-competitive acid blocker, as a component of first-line and second-line triple therapy for Helicobacter pylori eradication:a phase Ⅲ, randomised, double-blind study. Gut 2016; 65:1439-46.
- 6. Rodvold KA. Clinical pharmacokinetics of clarithromycin. Clin Pharmacokinet 1999; 37:385-98.
- 7. Curtis LH, Ostbye T, Sendersky V et al. Prescription of QT-prolonging drugs in a cohort of about 5 million outpatients. Am J Med 2003; 114:135-41.
- 8. Furuta T, Shirai N, Kodaira M et al. Pharmacogenomics-based tailored versus standard therapeutic regimen for eradication of H. pylori
. Clin Pharmacol Ther 2007; 81:521-8.
- 9. Sugimoto M, Furuta T, Shirai N et al. Comparison of an increased dosage regimen of rabeprazole versus a concomitant dosage regimen of famotidine with rabeprazole for nocturnal gastric acid inhibition in relation to cytochrome P450 2C19 genotypes. Clin Pharmacol Ther 2005; 77:302-11.
- 10. Kagami T, Sahara S, Ichikawa H et al. Potent acid inhibition by vonoprazan in comparison with esomeprazole, with reference to CYP2C19 genotype. Aliment Pharmacol Ther 2016; 43:1048-59.
- 11. Gingold-Belfer R, Niv Y, Schmilovitz-Weiss H et al. Susceptibility-guided versus empirical treatment for Helicobacter pylori infection:A systematic review and meta-analysis. J Gastroenterol Hepatol 2021; 36:2649-58.
- 12. Lopez-Gongora S, Puig I, Calvet X et al. Systematic review and meta-analysis:susceptibility-guided versus empirical antibiotic treatment for Helicobacter pylori infection. J Antimicrob Chemother 2015; 70:2447-55.
- 13. 大正製薬株式会社.クラリシッド錠200mg 添付文書(第35版).2020.
- 14. 日本ヘリコバクター学会ガイドライン作成委員会.
H. pylori感染の診断と治療のガイドライン 2016改訂版.先端医学社,東京,2016.
- 15. 日本消化器病学会H.pylori診断治療委員会.「ヘリコバクター・ピロリ感染胃炎」に対する除菌治療に関するQ&A一覧. https://www.jsge.or.jp/member/shikkan_qa/helicobacter_pylori_qa2014.(閲覧日:2016年8月1日)
- 16. Kawai T, Yamagishi T, Yagi K et al. Tailored eradication therapy based on fecal Helicobacter pylori clarithromycin sensitivities. J Gastroenterol Hepatol 2008; 23(Suppl 2):S171-4.
- 17. Park CS, Lee SM, Park CH et al. Pretreatment antimicrobial susceptibility-guided vs. clarithromycin-based triple therapy for Helicobacter pylori eradication in a region with high rates of multiple drug resistance. Am J Gastroenterol 2014; 109:1595-602.
- 18. 佐々木 誠人, 前川 高天, 西林 宏之ほか.クラリスロマイシン耐性がヘリコバクター・ピロリ除菌治療に及ぼす影響―多施設共同レトロスペクティブ研究―.日本ヘリコバクター学会雑誌 2018;19:127-32.
- 19. 安藤 貴志, 堀江 隆介, 村上 貴彬ほか.PCAB時代における,ピロリ菌の薬剤感受性を考慮した一次除菌療法の有効性.日本ヘリコバクター学会雑誌 2020;21:74-7.
- 20. Suzuki S, Gotoda T, Kusano C et al. Seven-day vonoprazan and low-dose amoxicillin dual therapy as first-line Helicobacter pylori treatment:a multicentre randomised trial in Japan. Gut 2020; 69:1019-26.
- 21. Drago L, Nicola L, Rodighiero V et al. Comparative evaluation of synergy of combinations of beta-lactams with fluoroquinolones or a macrolide in Streptococcus pneumoniae. J Antimicrob Chemother 2011; 66:845-9.
- 22. Furuta T, Yamade M, Kagami T et al. Influence of clarithromycin on the bactericidal effect of amoxicillin in patients infected with clarithromycin-resistant strains of H. pylori
. Gut 2020; 69:2056.
- 23. Furuta T, Yamade M, Kagami T et al. Dual Therapy with Vonoprazan and Amoxicillin Is as Effective as Triple Therapy with Vonoprazan, Amoxicillin and Clarithromycin for Eradication of Helicobacter pylori
. Digestion 2019; 101:1-9.
- 24. Furuta T, Soya Y, Sugimoto M et al. Rapid Automated Genotyping of CYP2C19 and Helicobacter pylori 23S rRNA Gene in Gastric Juice. Journal of GHR 2013; 2:508-12.
- 25. ミズホメディー.全自動遺伝子解析装置 Smart GeneⓇ
. https://www.mediceo.co.jp/poc_web/products/equipment/em_47186677.html.
- 26. 山出 美穂子, 樋口 友洋, 鈴木 崇弘ほか.Vonoprazanを用いた除菌治療における,内視鏡下吸引胃液によるClarithromycin耐性遺伝子変異検査の意義.日本ヘリコバクター学会雑誌 2019;20:69-70.
- 27. Sue S, Shibata W, Sasaki T et al. Randomized trial of vonoprazan-based versus proton-pump inhibitor-based third-line triple therapy with sitafloxacin for Helicobacter pylori
. J Gastroenterol Hepatol 2019; 34:686-92.
- 28. Saito Y, Konno K, Sato M et al. Vonoprazan-Based Third-Line Therapy Has a Higher Eradication Rate against Sitafloxacin-Resistant Helicobacter pylori
. Cancers(Basel) 2019; 11:116.
- 29. Hirata Y, Serizawa T, Shichijo S et al. Efficacy of triple therapy with esomeprazole, amoxicillin, and sitafloxacin as a third-line Helicobacter pylori eradication regimen. Int J Infect Dis 2016; 51:66-9.
- 30. Furuta T, Sugimoto M, Kodaira C et al. Sitafloxacin-based third-line rescue regimens for Helicobacter pylori infection in Japan. J Gastroenterol Hepatol 2014; 29:487-93.
- 31. Murakami K, Furuta T, Ando T et al. Multi-center randomized controlled study to establish the standard third-line regimen for Helicobacter pylori eradication in Japan. J Gastroenterol 2013; 48:1128-35.
- 32. Hirata Y, Ohmae T, Yanai A et al. Sitafloxacin resistance in Helicobacter pylori isolates and sitafloxacin-based triple therapy as a third-line regimen in Japan. Int J Antimicrob Agents 2012; 39:352-5.
- 33. Nishizawa T, Munkjargal M, Ebinuma H et al. Sitafloxacin for Third-Line Helicobacter pylori Eradication:A Systematic Review. J Clin Med 2021; 10:2722.
- 34. Mori H, Suzuki H, Matsuzaki J et al. Efficacy of 10-day Sitafloxacin-Containing Third-Line Rescue Therapies for Helicobacter pylori Strains Containing the gyrA Mutation. Helicobacter 2016; 21:286-94.
- 35. 古田 隆久.耐性菌に対するHelicobacter pylori除菌療法.Helicobcater Research 2021;25:162-71.
- 36. Muranaka M, Kabe J, Umezono K et al. [Incidence of Drug Hypersensitivity]. Arerugi 1964; 13:431-4.
- 37. Muranaka M, Okumura H, Takeda K et al. Population studies on drug hypersensitivities. Acta Allergol 1973; 28:50-61.
- 38. Ono S, Kato M, Nakagawa S et al. Vonoprazan improves the efficacy of Helicobacter pylori eradication therapy with a regimen consisting of clarithromycin and metronidazole in patients allergic to penicillin. Helicobacter 2017 Jun; 22(3). doi:10.1111/hel. 12374. Epub 2017 Jan 18.
- 39. Sue S, Suzuki N, Shibata W et al. First-Line Helicobacter pylori Eradication with Vonoprazan, Clarithromycin, and Metronidazole in Patients Allergic to Penicillin. Gastroenterol Res Pract 2017; 2017:2019802.
- 40. Furuta T, Sugimoto M, Yamade M et al. Eradication of H. pylori Infection in Patients Allergic to Penicillin Using Triple Therapy with a PPI, Metronidazole and Sitafloxacin. Intern Med 2014; 53:571-5.
- 41. Sue S, Sasaki T, Kaneko H et al.
Helicobacter pylori rescue treatment with vonoprazan, metronidazole, and sitafloxacin in the presence of penicillin allergy. JGH Open 2021; 5:307-11.
- 42. Murakami K, Sato R, Okimoto T et al. Effectiveness of minocycline-based triple therapy for eradication of Helicobacter pylori infection. J Gastroenterol Hepatol 2006; 21:262-7.
- 43. Kagami T, Yamade M, Suzuki T et al. Comparative study of effects of vonoprazan and esomeprazole on anti-platelet function of clopidogrel or prasugrel in relation to CYP2C19 genotype. Clin Pharmacol Ther 2018; 103:906-13.
- 44. Wang Y, Wang C, Wang S et al. Cytochrome P450-Based Drug-Drug Interactions of Vonoprazan In Vitro and In Vivo. Front Pharmacol 2020; 11:53.
- 45. Funakoshi R, Tomoda Y, Kudo T et al. Effects of proton pump inhibitors, esomeprazole and vonoprazan, on the disposition of proguanil, a CYP2C19 substrate, in healthy volunteers. Br J Clin Pharmacol 2019; 85:1454-63.
- 46. Roedler R, Neuhauser MM, Penzak SR. Does metronidazole interact with CYP3A substrates by inhibiting their metabolism through this metabolic pathway? Or should other mechanisms be considered? Ann Pharmacother 2007; 41:653-8.
- 47. von Rosensteil NA, Adam D. Macrolide antibacterials. Drug interactions of clinical significance. Drug Saf 1995; 13:105-22.
- 48. 塩野義製薬.フラジール内服錠 添付文書(第17版).2019.
- 49. Iannini PB. Cardiotoxicity of macrolides, ketolides and fluoroquinolones that prolong the QTc interval. Expert Opin Drug Saf 2002; 1:121-8.