2023 年 65 巻 7 号 p. 1255-1265
2023 年 65 巻 7 号 p. 1255-1265
十二指腸腫瘍に対する内視鏡切除の重要性が認識されつつあるが,EMRは出血や穿孔などの偶発症が一定の頻度で起こる.近年,局注を行わずに病変を浸水させ,スネアリングで切除するUnderwater EMRの有用性の報告が増えてきている.一括切除率の上昇や施行時間の短縮が報告されているが,部位によっては水が溜まりにくかったり,残渣などにより浸水下での視認性の低下などが問題となることがある.そこで水の代わりに,内視鏡止血時の視野確保Gelを用いて病変を浸漬させるGel immersion EMR(Under-Gel EMR)の報告が散見されるようになってきた.本稿ではその方法や展望について述べる.
The importance of endoscopic resection for duodenal tumors is increasingly being recognized; however, the high frequency of complications, such as bleeding and perforation, during EMR has become a problem.
In recent years, an increasing number of studies have demonstrated the clinical usefulness of underwater EMR, in which the intestinal lumen is filled with water, and lesions are resected by snaring without injection. This technique has been shown to have a higher en bloc resection rate and a shorter procedure time than conventional EMR. However, some areas are difficult to fill with water, and bile and mucus slime in water can reduce visibility. Therefore, the use of gel immersion EMR (also called undergel EMR), in which lesions are immersed in a gel for endoscopic hemostasis instead of in water, has occasionally been reported. This paper describes the methods and prospects of gel immersion EMR.
以前より食用ゼリーを用いた内視鏡治療(gel immersion endoscopy)の有用性についてはいくつかの報告があった.2016年のYanoらによるGel状の経口補水液(OS-1ゼリー:大塚製薬工場,徳島県)を用いた消化管出血に対する止血法 1),また2018年のAkasakaらのOS-1ゼリーを用いた内視鏡的粘膜下層剝離術(ESD)の報告である 2).Yanoらは消化管出血の17症例にOS-1ゼリーを用い,良好な視野が得られて内視鏡止血に有用であることを報告した.OS-1ゼリーを用いたのは局所麻酔用のゼリーが内視鏡先端に付着した際に良好な視野が得られたことがきっかけとのことであった.Akasakaらは以前より浸水下でのESDを行いその有用性を報告していたが,粘膜下層の剝離の際の出血により視野不良となることが問題であった.そこでOS-1ゼリーを用いると良好な視野のまま食道および大腸のESDを行うことができることを報告している.
筆者は以前,大腸ポリープに対する浸水下でのEMR(Underwater endoscopic mucosal resection: UEMR)の有用性を報告した多施設共同研究に関わった経緯から 3),日常臨床で浸水下での内視鏡を多用していた.しかししばしば濁りによる視野不良や溜まりにくい部位があることも経験していた.その折にYanoらやAkasakaらの話を聞いて,Underwaterの代わりにGelを用いたGel immersion EMR(Under-Gel EMR)の可能性を報告したのがきっかけである 4).
2021年には大塚製薬工場より内視鏡の視野確保のためのGel(ビスコクリア)が発売された.ビスコクリアは無色透明なゲル状の製品で,主な組成であるキサンタンガムおよびローカストビーンガムによってその粘性が保たれている.キサンタンガムは,デンプンを原料として微生物の発酵によって産生される多糖類で,水と混合すると高い粘度をもち安定しているため,ソースなどの様々な食品に使用されている.ローカストビーンガムは豆科の植物からとれる増粘多糖類で,ゲル化剤としてプリンやゼリーなど様々な食品や医薬品などに用いられている.これらは単体で使用した場合は分子鎖間の結合が生じないためゲル化しないが,併用するとゲル化作用が生じる.ゲル化作用が生じると粘度が高くなりまた非常に安定するため,血液や残渣と混じり合わず透明な空間を作り出すことができる.それによって内視鏡の視野を保つことが可能となり,内視鏡治療の際に非常に有用である.また,電解質を含まないことによりGel浸漬下でも通電性は良好である.本稿では表在性非乳頭部十二指腸上皮性腫瘍(Superficial Non-ampullary Duodenal Epithelial Tumors:SNADETs)に対して浸水下(Underwater)からGel浸漬下(Under-gel)の内視鏡切除に至った経緯とその方法および治療成績について述べる.
近年の内視鏡診断技術の向上により,SNADETsの発見が増えてきている 5).なかでも十二指腸腺腫は癌に進展する可能性があるため 6),ガイドラインにおいても積極的ではないものの内視鏡治療の対象とされている 7).EMRは,20mmまでのSNADETsに対する最も一般的な内視鏡治療法となっている 8).しかし,有害事象の発生率は術中穿孔が0~3%,遅発穿孔が0~3.6%,後出血が0~13%と報告されている 9)~12).特に遅発穿孔を来すと長期間の絶食や緊急外科手術を要するなど重篤な経過をたどり 9),EMRは決して安全な治療法とはいえない.さらに遺残再発率が低くないことも問題となっている 13)~15).
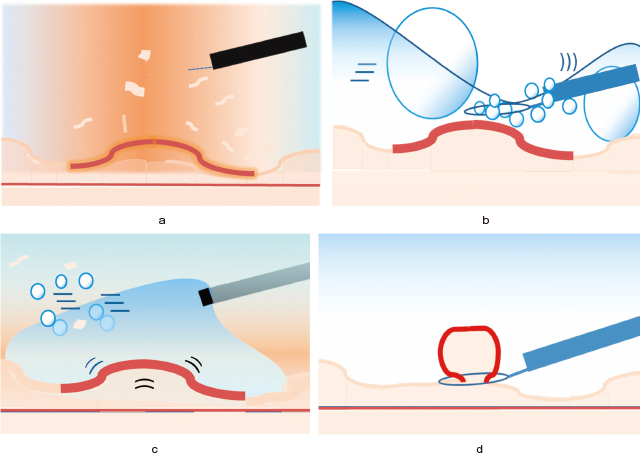
近年,Binmoellerらが報告した浸水下でのUEMRが 16),SNADETに対する安全で有効な治療法として注目を集めている 17)~19).UEMRは局注を行わず,消化管管腔内を脱気して注水し病変を浸水させて切除する方法である.従来のEMRは局注にある程度の技術を要し,不適切な局注や血腫が生じるとスネアリングが困難になる.また局注による膨隆によって病変の表面積が増すことにより一括切除もまた難しくなる.一方でUEMRでは局注は不要であり,消化管管腔内を脱気して注水を行い,病変を完全に浸水させるのみであるため特別な技術は必要ない.浸水下では平坦な病変でもポリープ様に隆起しまた表面積も小さくなるため,容易にスネアリングを行うことができる.超音波内視鏡(EUS)で観察すると粘膜のたわみにより粘膜下層は厚くなり筋層は病変から遠ざかってリング状になるため,筋層をつかんで穿孔する可能性も低い(Figure 1-a).Binmoellerの言葉を借りると病変がfloatingしポリープ様の形態を呈するとのことである 16).また腸管管腔内の内圧も通常送気下と比べて低くなるため,切除に時間を要したり,複数病変を切除する場合でも患者の苦痛を軽減できる可能性がある 20).しかし,水は流動性があるため,水を溜めることが困難な部位や蠕動により溜まりにくい場合がある.さらに,水は腸液や残渣など他の物質と混ざりやすいため,濁ってしまい視認性が悪くなることもしばしば経験する.このような場合,水の濁りをとるために大量の水を必要とするため,さらなる腸蠕動の誘発や時間を要することもある.

a:EUSを用いて観察すると,浸水下では粘膜はたわんで厚くなりFloatingしてポリープ様の形態を呈している.また筋層はリング状で表層から遠ざかっている.しかし残渣や気泡による水の濁りをしばしば認める.
b:Gel浸漬下でも同様の効果が得られ,粘膜はポリープ様の形態を呈する.さらに残渣や気泡は容易に除去されるため水の濁りは認められない.
2021年に新しい内視鏡的処置・治療用ゲル製品(ビスコクリア:大塚製薬工場,徳島県)が発売された.ビスコクリアはその粘性によって血液や残渣などの拡散や流動を抑えるため内視鏡の全面に透明な視野を確保できる.消化管に注入して消化管出血時の精査にGel immersion Endoscopyの有用性が報告されるようになった 21),22).Gelは水と異なって血液や腸液,残渣と混ざらないため消化管管腔内を良好に観察することができる.そこでわれわれはGelを用いたGel immersion Endoscopyにヒントを得て水の代わりにGelに病変を浸漬させ,切除するGIEMRの安全性と有効性を報告した 4).浸水下と同様に粘膜のたわみにより病変がポリープ様の形態を呈し筋層は病変から遠ざかってリング状になるため,安全,簡便に切除できる(Figure 1-b).さらに,その粘性により注入部位に留まる傾向があるため,少ない注入量で病変を浸漬させることが可能である.これらの利点により治療時間の短縮が期待できる.その後にわれわれはSNADETに対するUEMRとGIEMRの有効性と安全性を比較検討し,治療成績はUEMRと遜色なく治療時間がUEMRよりも有意に早いことを示した 23).
当院ではガイドライン 7)の内視鏡治療の適応に準じて,主に20mm以下の腺腫が疑われる病変に対して内視鏡切除を行っている.2020年10月まではUEMRを主に行っていたがビスコクリアが発売されたそれ以降はGIEMRを主に行っている.
使用する上部内視鏡は以前はGIF-Q260Jを使用していたが近年はGIF-H290T(オリンパスメディカルシステムズ,東京)を主に用い,フード(D-201-11804,オリンパスメディカルシステムズ)を装着している.どちらの内視鏡も3.2mmの鉗子チャンネルを備えており,2.8mmの鉗子チャンネルの内視鏡と比べるとGelの注入がしやすい.内視鏡の鉗子挿入口に装着する鉗子栓はBioShield irrigator(U.S.E.. Endoscopy,Mentor,Ohio,USA)を用いる.これはイリゲーションラインが鉗子栓についており,処置具の挿入と水やGelの注入が同時に可能である(Figure 2).内視鏡の副送水チャンネル(いわゆるウォータージェット)から内視鏡用送水ポンプ(OFP-2,オリンパスメディカルシステムズ)を用いたGelの注入も可能であるが,Hirakiらの検討によるとポンプを用いた注入はGelに高度な圧力がかかり,粘度の低下がみられる 24).それを避けるため,われわれは鉗子口からの注入を行っている.しかし鉗子口からのシリンジを用いた手押しでの注入は助手が必要であるため,人員が不足している場合は送水ポンプを用いたGelの注入もやむを得ないと考える.その際もHirakiらの検討によれば副送水路につなぐのではなく,BioShield irrigatorのイリゲーションラインに送水ポンプを接続した方がGelの粘度を保つことができる 24).

BioShield irrigatorを装着するとスネアを挿入しながら,シリンジよりGelの注入が可能となる.順序としては①スネアを挿入し,②BioShield irrigatorのロックを解除して③Gelを注入する.注入後は吸引によってGelが吸引されてしまうためロックを閉めておく.
GIEMRの手順は以下の通りである(Figure 3).

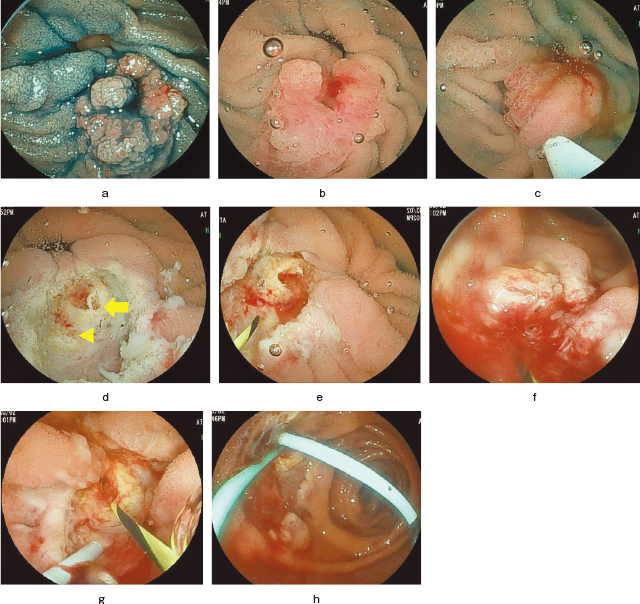
GIEMRの実際.
a:下行部に10mm大の0-Ⅱa病変を認める.
b:浸水を行うと胆汁や残渣の影響で視野不良である.
c:NBIでも同様に視野不良で境界が不明瞭である.
d:Gelを注入すると速やかに視野が改善され,境界も明瞭に認識できるようになった.
e:粘膜のたわみも浸水下と同様にあるため容易にスネアリングできる.
f :合併症なく一括切除できた.
(1)病変に到達後,十二指腸管腔内を十分に脱気する.処置中に口側から空気が流入してくることもあるので胃内も十分に脱気しておく.
(2)Gel(ビスコクリア;大塚製薬工場,徳島県)を充填した20~30mlのシリンジをBioShield irrigatorに装着しておく(Figure 2).
(3)なるべくゆっくりGelを注入する.注入圧を上げすぎると,粘度が低下したり鉗子チャンネルから逆流してしまったりするので注意が必要である.病変が完全に浸漬するまでGelを注入する.われわれの検討では十二指腸の場合では100mlほどのGelで十分であった.
(4)スネアを用いて病変部と周辺粘膜を絞扼する.当院ではバイポーラスネア(DRAGONARE 26mm;ゼオンメディカル株式会社,東京)を使用している.バイポーラスネアは,高周波電流がスネアとシース先端部のみに流れるため,粘膜の熱損傷を軽減できる可能性があり,SNADETに対する安全性と有効性が近年報告されている 25),26).
(5)絞扼後に高周波手術装置(VIO300D;Erbe Elektromedizin,Tübingen,Germany)を用いて基本的には凝固波でゆっくり切除する(設定auto-cut mode,effect 3,30W;forced coagulation mode,effect 1,15W.).
(6)切除後は病変が肛門側に流出しないように速やかに回収する.Gel浸漬下では標本がその場に留まるため,浸水下に比べて回収が容易であり肛門側に流れていく心配も少ない.潰瘍底を観察し遺残や露出血管がないことを確認してクリップにて粘膜欠損部を完全に縫縮し終了する.
以下に参考までに当院でのUEMRの手順も記しておく.(1)GIEMR時と同様に胃内および十二指腸内腔を完全に脱気し,(2)内視鏡のウォータージェットチャンネルからポンプ(OFP-2;オリンパスメディカルシステムズ)により病変部が完全に浸水するまで生理食塩水を内腔に注入する.(3)Bipolar Snare(DRAGONARE26mm;ゼオンメディカル株式会社),またはモノポーラ スネア(SnareMaster 15mm;Olympus Medical System,Tokyo,Japan)にて病変を絞扼後に(4)高周波電気発生装置(VIO300D;Erbe Elektromedizin)を用いて切除する.切除後はクリップを用いて潰瘍底の完全縫縮を行っている.
以下に当院におけるSNADETsに対するGIEMRおよびUEMRの治療成績を示す.対象は術前の内視鏡生検で腺腫または内視鏡診断で腺腫と診断された患者であった.14病変14人がUEMRで治療され,17病変15人がGIEMRで治療された.患者背景はTable 1の通りであった.

患者背景.
評価項目は,処置時間,一括切除割合,R0切除割合,偶発症の発生割合とした.処置時間は,UEMRは生理食塩水を,GIEMRはGelを十二指腸内腔に注入してから病変が完全に切除されるまでの時間と定義した.手技関連アウトカムをFigure 4に示す.手技時間の中央値はGIEMR群がUEMR群より有意に短く(10分 vs. 5分,P=0.016),効果量は大であった(Cohenʼs d=0.99)(Figure 4).一括切除率(93% vs 100%,P=1.0,Cramerʼs V=0.18),R0切除率(57% vs 80%,P=0.39,Cramerʼs V=0.24)はUEMR群とGIEMR群の間に有意差はなかった.非治癒切除はUEMR群では水平断端陽性3例,水平断端不明3例であり,GIEMR群では水平断端不明が4例であった.病変部を完全に浸すのに必要な水またはGelの量はGIEMR群で有意に少なかった(170ml vs. 100ml,P=0.0012,Cohenʼs d=1.49)(Table 2).

施行時間.

その他の治療関連の結果.
偶発症については穿孔および遅発性出血は両群とも認めなかった.術中出血はGIEMR群に1例,UEMR群に1例あったがいずれもクリップにて止血しえた.その他の重篤な合併症は両群とも認めなかった(Table 3).

偶発症関連の結果.
今回のわれわれの検討ではSNADETsに対するUEMRとGIEMRの有効性と安全性を比較した.GIEMRはUEMRに比べ,有害事象の発生率を増加させることなく,内視鏡切除の施行時間が有意に短縮されることが示された.さらに,GIEMR群は腫瘍径の中央値が有意に大きかったにもかかわらず,有意差はないものの一括切除率およびR0切除率が高いことが示された.他の消化管病変をGelに浸漬させESDやEMRに応用した報告が,われわれの報告以外にもいくつかなされている 2),4),27)~29).今回のわれわれの検討では経験の浅い内視鏡医も6症例施行しており(Table 2),1症例で分割切除となったものの他の治療成績は熟練医と遜色なかった.これらの結果はGIEMRが日常臨床でも安全で有用である可能性を示していると考えられる.
内視鏡治療時にGelによって浸漬する方法(Gel immersion endoscopy)は,消化管出血の新しい治療法として矢野らによって初めて報告された 1).従来は消化管出血の内視鏡止血時に水によって血液や残渣を洗い流し出血源を探していたが,水は血液や腸液,食物残渣とすぐに混ざり合ってしまうため,良好な視野を確保することが難しく止血困難となる場合がしばしばあった.Gelによる浸漬は内視鏡の鉗子挿入口から水の代わりにGelを注入することで,内視鏡の前方に透明な空間を作り,良好な視野を確保することができる.これにより,出血源の特定が容易になり,様々な部位の内視鏡的止血に有用であることが報告されている 22).
近年,病変を水に浸水させて内視鏡切除を行うUEMRが注目されており,従来のEMRよりも効果的で安全な内視鏡手術であることが報告されている 30)~32).UEMRでは,従来のEMRと比較して,脱気と浸水による粘膜のたわみにより病変部が隆起し,また腸管の屈曲も直線的になるためスネアリングが容易となり,一括切除率やR0切除率が高くなると考えられている 3),17).また,局注を行わないため,内視鏡切除後の潰瘍縁の粘膜は収縮しており,切除後のクリップ閉鎖も容易である.これらに加え浸水による冷却効果で粘膜の熱損傷が軽減されることも,Post-polypectomy coagulation syndromeなどの有害事象の予防につながると考えられている 33).しかし,十二指腸管腔内を浸水させると胆汁などの腸液と混ざることや(Figure 5-a),気泡が流れ込んで視認性が悪くなることがある(Figure 5-b).今回,GIEMRはGelを使用することでスネアリングがしやすい良好な視野が容易に得られるため(Figure 5-c,d),UEMRに比べて処置時間を短縮することができたと考えられる.UEMRでも残渣などで視認性が悪い場合や気泡や水の流出により病変部を水に浸すことが困難な場合でも,空気を抜いて大量の水を注入することを数回繰り返して,UEMRを行うことが可能な場合がある.しかし,この作業を繰り返すと時間がかかり,蠕動運動が起きて切除が困難になる可能性がある.背景や定義が異なるため直接比較はできないが,これまでの報告では,UEMRにおけるSNADETの処置時間は5~11分である 17),18),30).本検討におけるGIEMRの処置時間の中央値は6分であり,既報より短い傾向にあった.これはGelの粘弾性により気泡が容易に除去され,またGelが容易に病変周辺に留まるため少量の注入で十分であるからである.今回の検討では病変部を浸漬するのに必要なGelの量の中央値がわずか100mlでUEMR群の注水量の170mlより有意に少なく,また既報のUEMRの検討で報告されていた330mlより少なかったことからもこのことは裏付けられている 18).
a:浸水下では胆汁や残渣により視野不良となることがある.
b:同様に気泡の流入により病変の浸水が困難な場合もある.
c:Gelを注入すると残渣や気泡が除去され,クリアな視界が得られる.また少量のGelで病変の浸漬も可能である.
d:浸水下同様に病変のfloatingも得られ,容易に一括切除が可能となる.
GIEMRでは,SNADETの内視鏡治療において,en bloc切除率94%,R0切除率76%と合併症なく良好な内視鏡治療成績が得られた.一般的に病変の長径が10mmを超えると一括切除率が低下することが知られている 34),35).しかし,今回の検討ではGIEMR群では,ほとんどの症例で病変径が10mmを超えたものの,ほぼ全例で一括切除が得られた.先行研究では,UEMRにおけるSNADETの一括切除率は75.4~100%,R0切除率は50.8~88.2%と報告されている 17)~19),30)~32).われわれの検討では症例数が少ないものの,GIEMRの一括切除率,R0切除率ともに,これまでのUEMRの研究に比べて高い値を示した.
最後にGel immersion papillectomyについても少し述べる.乳頭部腫瘍に対する内視鏡的乳頭切除術(endoscopic papillectomy:EP)も近年普及してきている.以前より浸水下でのEP(Underwater papillectomy)の有用性についての報告はあったが 36),37),UEMRと同様に浸水時に水と胆汁,残渣などが混濁しまた空気の流入により,視野が不良となることをしばしば経験する.これらを克服するためにGelを用いたEP(Gel immersion endoscopic papillectomy:GI-EP)の有用性に関してToyonagaらの報告がある 38).当院ではダブルバルーン内視鏡を用いた術後再建腸管に対する内視鏡的逆行性膵胆管造影法(ERCP)を積極的に行っており,術後再建腸管での乳頭部腫瘍に対するEPもしばしば経験する.術後再建腸管に対するEPはUnderwaterでの有用性の報告はあるが 39),処置を行う際に術式によっては通常のEPと同様に水の溜まりが悪くなったり空気の流入があり乳頭部の腫瘍を完全に浸水させるのが困難な場合もある.われわれは術後再建腸管に対してのGelを用いたGI-EPも行っている 40).その利点としては上述の良好な視野が得られるなどのメリットに加えて,先端バルーンを用いるためGelの溜まりがよくなり,少量のGelで病変の浸漬が可能となる.また浸水下では切除後の検体が肛門側に流出すると側視鏡であるため回収に困難を伴うが,ダブルバルーン内視鏡を用いたGl-EPの場合はGelの滞留性および先端バルーンにより検体がその場に留まるため回収が容易になる.さらに切除後の胆管開口部および膵管開口部が視認しやすくなるためEP後の胆管膵管ステントを留置も容易となることなどが挙げられる(Figure 6).
a:GI-EPの実際.Roux-en-Y再建後のためショートタイプのダブルバルーン(EI580BT,フジフイルム株式会社,東京)を使用している.乳頭部に15mm大の腫瘍性病変を認める.
b:イリゲーター(BioShield irrigator,U.S.E.. Endoscopy)を用いてGelを注入した.ダブルバルーン内視鏡の先端バルーンを膨らませて口側への流出を防ぐことで,腸管内のGelの貯留はより良好となった.
c:Gel浸漬下では浸水下と同様に周囲粘膜はたわんで腫瘍は隆起性病変のようにFloatingし,スネアリングにて容易に一括切除が可能であった.
d:Gel浸漬下では胆管開口部(矢印),膵管開口部(矢頭)の視認も容易である.
e:ステント留置のため膵管にガイドワイヤーを挿入した.Oozingが出現したがGel浸漬下では視認性は保たれている.
f :Gelを吸引除去すると潰瘍底に血液が広がり,視野不良となった.
g:再度Gelを注入すると血液が除去されて良好な視野が得られ,容易に胆管にガイドワイヤーを挿入できた.
h:胆管ステント,膵管ステントを留置して偶発症なく終了した.
GIEMRはSNADETsに対して安全かつ有用であり,UEMRと比較しても手技時間を短縮できることを示した.また術後再建腸管を含めた乳頭部腫瘍に対するEPにおいてもGelによる浸漬が有用である可能性もある.しかし小数例での検討であるため,さらなる症例の集積が必要である.
本論文内容に関連する著者の利益相反:なし