2016 年 33 巻 2 号 p. 121-127
2016 年 33 巻 2 号 p. 121-127
症例は56歳男性。検診で高カルシウム血症と腎機能障害を指摘された。Intact-PTHが高値であり原発性副甲状腺機能亢進症が疑われた。頸部超音波検査で,甲状腺左葉に囊胞変性を伴った結節性甲状腺腫と,甲状腺右葉下極の甲状腺外背側に副甲状腺腫を疑わせる充実性結節を認めた。99mTc-MIBIシンチグラム検査では両病変に集積を認めた。甲状腺左葉切除と右下副甲状腺腫摘出が施行された。左葉の結節は免疫染色を含めてカルチノイド腫瘍を疑わせる病理像を呈していたが,頭頸部内分泌腫瘍免疫染色アルゴリズムに沿って鑑別することで,甲状腺内副甲状腺腺腫と診断された。右葉下極の結節も副甲状腺腺腫であり,重複副甲状腺腺腫であった。原発性副甲状腺機能亢進症と診断された症例では,異所性副甲状腺腫を含む重複副甲状腺腫を念頭に置いた精査が必要と考えられた。術後3年,重度の骨飢餓症候群を認めたが,活性型ビタミンD製剤投与にて血清カルシウム値コントロール良好で推移しており,明らかな再発所見は認めていない。
原発性副甲状腺機能亢進症(pHPT)の治療の基本は,責任病変の副甲状腺摘出術であり,術前の局在診断が最も重要であるが,副甲状腺は発生過程で異所性に存在することも少なくない。近年,超音波検査やCT検査,99mTc-MIBI(methoxyisobutylisonitrile:sestamibi)シンチグラムなど画像診断の進歩に伴い,ほとんどの症例で局在診断が可能になってきている。しかし,腫瘍径が小さい症例や縦隔内など異所性に存在する症例では,局在診断が困難な場合もある。また,pHPTでは種々の結節性甲状腺病変を合併しやすいことも知られており,甲状腺内副甲状腺との鑑別も必要となる[1~3]。副甲状腺腺腫の確定診断は病理組織学的診断によって行われるが,通常の副甲状腺腺腫の細胞は円形の核と淡明な細胞質を有しており,副甲状腺由来の病変であることはHE染色,PTH免疫染色で診断可能である。しかし,腺腫,過形成,癌の鑑別診断は病理学的に非常に難しいとされている。今回,術前診断および最終病理にてカルチノイド腫瘍も含め,様々な鑑別を要した甲状腺内副甲状腺腺腫を経験したので,若干の文献的考察を加えて報告する。
患 者:56歳,男性。
主 訴:なし。
既往歴:特記事項なし。骨折,胃潰瘍,尿路結石の既往なし。
家族歴:特記事項なし。
現病歴:職場検診で左頸部腫瘤指摘され,近医を受診。頸部超音波検査で甲状腺左葉に3cm大の腫瘤を指摘されたが,穿刺吸引細胞診(FNAC)でclassⅠのため経過観察となった。2年後の検診採血で腎機能障害と血清カルシウム値16.0mg/dl(基準値:8.7~10.3mg/dl)と高カルシウム血症を指摘され,近医を受診した。Intact-PTHは959pg/ml(基準値:10~65pg/ml)と高値であり,頸部超音波検査で甲状腺右葉下極周囲に腫瘤を認めたため,右下副甲状腺腫によるpHPTが疑われた。甲状腺左葉の結節の大きさは不変であったが再度FNAC施行し,classⅠの診断であった。左葉内結節は穿刺時に腫瘍内出血きたし,サイズ増大認めた。右下副甲状腺腫によるpHPTと甲状腺左葉結節性甲状腺腫の診断で当科に紹介となった。
入院時現症:身長165cm,体重65kg。栄養状態は良好。意識清明で口渇などの高カルシウム血症を示唆する自覚症状は認めなかった。血圧124/82mmHg,脈拍80/分整,体温36.3℃。浮腫および眼球突出なし。消化器症状なし。頸部では甲状腺左葉に3cm大の境界明瞭,可動性良好,弾性硬な腫瘤を触知した。胸部,腹部には異常所見を認めなかった。
血液生化学所見(表1):血清カルシウム値15.9mg/dl,intact-PTH 967pg/mlと著明な上昇を認めたため,ゾレドロン酸水和物4mgを投与した。投与後6日目には血清カルシウム12.8mg/dlまで低下したが,血清Cre値は1.21mg/dl,ALP 718IU/l,分画でALP3(骨型)が82.3μg/Lと上昇していた。甲状腺機能,サイログロブリン値はすべて基準値内で,抗サイログロブリン抗体・抗TPO抗体も陰性であった。その他,特記すべき異常所見は認めなかった。

入院時血液検査結果
胸部X線検査所見:甲状腺左葉の腫瘤による気管の軽度右方偏移を認めたが,不整や狭窄は認めなかった。また,肺野に異常は認めなかった。
頸部超音波検査所見:甲状腺左葉に27×25mmで囊胞成分を伴った内部不均一な腫瘤(図1a)を認め,甲状腺右葉下極背側には17×18×23mmの境界明瞭で内部均一な低エコー腫瘤を認めた(図1b)。
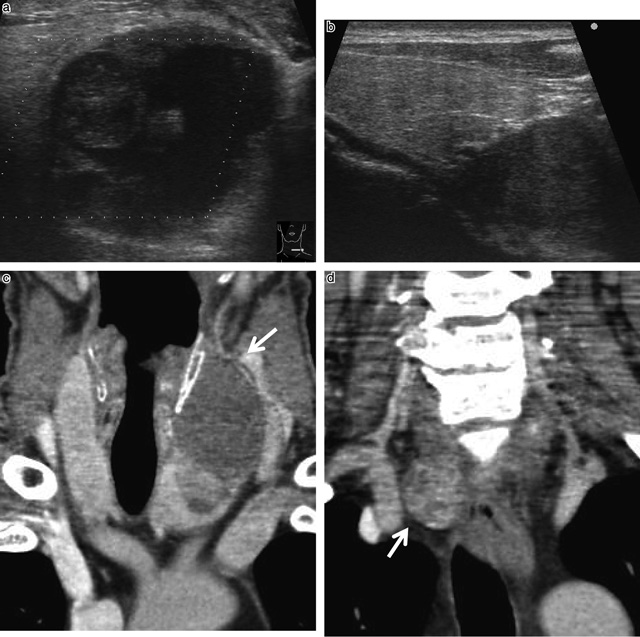
a:頸部超音波検査:甲状腺左葉に35.6×28.5mmの液体貯留と内部に一部充実部分伴う結節を認めた。
b:頸部超音波検査:甲状腺右葉下極に境界明瞭な17×18×23mmの低エコー結節を認めた。
c:頸部CT:甲状腺左葉に34×34×55mmの囊胞性分伴う一部充実性の腫瘤を認めた。
d:頸部CT:甲状腺右葉下極背側に20×19×25mmの境界明瞭で造影効果伴う腫瘤を認めた。
頸部CT検査所見:甲状腺左葉に上方部分は造影効果を認めない34×34×55mmの境界明瞭な腫瘤(図1c)を認めた。また,甲状腺右葉下極背側に20×19×25mmの造影効果を伴う境界明瞭な腫瘤(図1d)を認めた。
99mTc-MIBIシンチグラム所見:甲状腺左葉下極と甲状腺右葉下極周囲とに集積を認めた(図2)。

99mTc-MIBIシンチ:甲状腺右葉下極と左葉下極付近に集積認める。
上記所見より,甲状腺左葉結節性甲状腺腫および右下副甲状腺腫による原発性副甲状腺機能亢進症と診断し,甲状腺左葉切除および右下副甲状腺腫摘出術を施行した。
手術所見:甲状腺左葉内に約25mmの弾性軟な腫瘤と甲状腺右葉下極背側周囲に約20mmの弾性軟な類円形腫瘤を触知した。両病変とも周囲への浸潤所見は認めなかった。明らかなリンパ節腫大も認めず,リンパ節郭清は施行しなかった。
切除標本肉眼所見:甲状腺左葉内結節は比較的境界明瞭で黄白色充実性であり内部に出血を伴っており,厚い被膜に覆われていた(図3)。右下副甲状腺は境界明瞭な白色結節を有しており,その内部には小囊胞を認めた(図4)。

甲状腺左葉結節性病変割面:横断面で切り出されている。比較的境界明瞭で被膜を有する黄白色充実性であり内部に出血を伴っていた。

右下副甲状腺腫割面:境界明瞭な白色結節を有しており,その内部には小囊胞を認めた。
病理組織検査所見:HE染色で甲状腺左葉の結節は厚い被膜を有し,円形で,均一な核を持つ細胞が大きな胞巣を形成しており,胞巣間には線維性隔壁を認め,壊死や核分裂像はみられないが,一部は硝子化していた(図5)。以上の所見からは,鑑別疾患として甲状腺内副甲状腺腫,甲状腺髄様癌,カルチノイドなどが挙げられた。また,Grimelius染色で細胞質に陽性の顆粒を認めた。免疫染色では,腫瘍細胞はchromograninA,keratinに陽性であった(図6)。calcitonin,TTF-1,NSE,neurofilament,CD56,S-100,EMAはいずれも陰性で,MIB-1陽性細胞は1%以下であった。さらにPTH(parathyroid hormone)が陽性(図7)であり,最終的に甲状腺内副甲状腺腺腫の診断となった。

甲状腺左葉内結節HE染色(×200):円形で均一な核を持つ細胞が大きな胞巣形成し,胞巣間には繊維性隔壁が認められる。腫瘍細胞の核は豊富な細胞質の中央にあり,核分裂像はほとんど認めない。

甲状腺左葉内結節特殊染色:Grimelius染色で細胞質に陽性の顆粒を認めた。免疫染色では,腫瘍細胞はchromograninA,keratinに陽性であった。calcitonin,TTF-1,NSE,neurofilament,CD56,S-100,EMAはいずれも陰性で,MIB-1陽性細胞は1%以下であった。

PTH(parathyroid hormone)特殊染色(×400):陽性
甲状腺右葉下極背側周囲の結節は,被膜に囲まれており,多角形の胞体の中央に円形核を持つ腫瘍細胞が敷石状に配列して充実性胞巣を形成しており,胞巣周辺には核が一列に並ぶ柵状配列もみられた(HE染色)。被膜外浸潤や血管浸潤像は認めず副甲状腺腺腫と診断された(図8)。

右下副甲状腺腺腫(×40)。被膜浸潤や脈管侵襲を認めず腺腫と判断した。
術後経過:術後6日目で血清カルシウム11.2mg/dlまで低下し,自宅退院となった。術後1カ月で血清カルシウム8.8mg/dl,Cr 1.78mg/dlと改善が認められた。重度の骨飢餓症候群を認めたが,アルファカルシドール内服下で現在の血清カルシウムは正常範囲であり,明らかな再発所見は認めていない。
pHPTの責任病腺の局在診断には種々の画像診断が用いられるが,異所性副甲状腺腫の検出率は頸部超音波検査で21.4~59.0%[4,5]99mTc-MIBIシンチグラムで50.0~89.0%[4,5],頸胸部CTで33.3%,頸部MRIで40.0%,Tl-Tcシンチグラムは14.3%,内頸静脈サンプリングでは66.7%と報告されている[4]。99mTc-MIBIシンチグラムと頸部超音波検査の組み合わせで,sensitivityは90%という報告もある[5]。
pHPTを伴う副甲状腺腺腫症例では,約78~85%が単腺の副甲状腺腫大を呈し,5.4%~12.0%に多腺の副甲状腺腫大を認める[6~9]。pHPTにおける異所性副甲状腺腫の頻度は6.1~16.0%[4,5,8]であり,術前局在診断が困難な症例も存在する。Lowら[10]は副甲状腺手術866例中(腎性副甲状腺機能亢進症も含む)120例(13.9%)に異所性副甲状腺腫を認め,25例が縦隔内,43例が胸腺内,34例が甲状腺内,18例が気管食道背側に認めたと報告している。他に頻度は少ないが,頸動脈鞘[11]や副咽頭間隙[12],中咽頭[12],迷走神経内[12]などの報告もある。甲状腺内副甲状腺の頻度は,pHPTの1.3~4.2%,甲状腺結節性病変の0.4%との報告がある[1,13~17]。pHPTのDouble parathyroid adenomaの頻度は,2.6~12.0%[7~9,18]であり,甲状腺内副甲状腺の頻度は少ないが,本症例のように甲状腺内副甲状腺腫を伴ったDouble parathyroid adenomaの場合,高カルシウム血症が,正常位置にある副甲状腺腫のみが原因であると判断する可能性があるため,術前診断において甲状腺内副甲状腺腫と結節性甲状腺腫との鑑別が重要である。
pHPTでは種々の結節性甲状腺病変合併しやすいことが知られており,pHPTには結節性甲状腺腫が22~70%と比較的高頻度に合併している[1~3,13]。甲状腺内結節病変を伴ったpHPT症例での腺腫検出率は,頸部超音波で53%,99mTc-MIBIシンチで73%,組み合わせて85%との報告がある[19]。
本症例では99mTc-MIBIシンチグラムで甲状腺右葉下極と甲状腺左葉下極に集積遅延を認めており,遡って考えると両病変とも副甲状腺腫を示唆していた。左葉下極にのみ集積を認めたのは,結節の中部から上方は囊胞成分で占められていたためと考えられた。また,結節性甲状腺腫にも集積を認めることがあり[20],頸部超音波所見と合わせて,臨床的に結節性甲状腺腫と判断した。
穿刺細胞診については,副甲状腺腫瘍を疑った場合は穿刺細胞診によって播種をきたす可能性があるため禁忌であるとする意見もあるが,FNAB-PTHが有用であるという報告も認められ,一定の見解は得られていない[15,21]。しかし,Tseleniらは細胞診での甲状腺病変と副甲状腺病変との鑑別は困難であると報告しており[22],鑑別は困難であったと考えられる。
Double parathyroid adenomaはsingle parathyroid adenomaや多腺過形成よりも血中PTH値が高値であるという報告がある[6]。本症例でも術前の血清カルシウム値が16.0mg/dl,Intact-PTH 959pg/mlと著明に高値であったことから,副甲状腺癌だけでなくDouble parathyroid adenomaも鑑別に挙げるべきであった。血清カルシウム値やIntact-PTHが非常に高い症例では,家族歴がなくても多腺副甲状腺腫の可能性も念頭に入れて治療にあたる必要があると考えられる。
治療方針は病的腺腫が単腺腫大の場合には腺腫摘出,過形成の場合は亜全摘,または全摘と一部筋肉内に自家移植するのが標準である。多腺副甲状腺腫が疑われれば,MEN1型,2A型などの遺伝性疾患や二次性副甲状腺機能亢進症も鑑別しながら治療方針を決定していく。本症例では,家族歴がないこと,術前に右下副甲状腺腫の単腺腫大と甲状腺左葉の結節性甲状腺腫と診断したことより術前の遺伝子検査は行わなかったが,術後も患者本人が希望しなかったため施行できていない。pPHTの一期的手術成功率は95%といわれているが,病変が異所性副甲状腺腫により局在が同定できない場合は不成功になることもある[14]。確実に責任病巣が摘出されたかを評価する手段として術中PTH測定の有用性の報告もあり[23,24],測定可能な施設では確実な手術を行うための一助になると考えられる。
副甲状腺腫細胞は通常Hematoxylin Eosin染色(HE染色)にて診断される。本症例の病理組織学的検査では,甲状腺右葉下極背側の腫瘤はparathyroid adenomaと診断された。甲状腺左葉の腫瘤は,HE染色でカルチノイド様の増殖形態を呈しており,免疫染色にてchromograninA・keratin陽性,carcitonin陰性であったため,当初neuroendcrine tumor(NET),中でも甲状腺原発carcinoid tumorが疑われた。甲状腺carcinoidはこれまでに一例しか報告がみられていない非常に稀な疾患である[25]。確定診断のために追加免疫染色を行ったところPTHが陽性であり,最終的に甲状腺内副甲状腺腺腫の診断となった。切除標本では被膜が非常に厚く,副甲状腺癌の可能性も考えられたが,核分裂像や被膜外浸潤,静脈浸潤を認めないことから腺腫と判断した(図8)。頭頸部内分泌腫瘍に対する免疫染色アルゴリズム[26](図9)によれば,Cytokeratin陽性であれば,TTF-1・Thyroglobulin・chromogranin・carcitonin・PTHを調べ,鑑別していく。本症例では,増殖パターンや免疫染色の結果などからNETの可能性も考えたが,頭頸部内分泌腫瘍に対する免疫染色アルゴリズムに沿って検査することにより,甲状腺内副甲状腺腺腫と診断することが可能であった。

Algorithm of head and neck endocrine tumors
甲状腺内副甲状腺腺腫を伴うDouble parathyroid adenomaの一例を経験した。頭頸部内分泌腫瘍に対する免疫染色アルゴリズムに沿って鑑別することにより甲状腺内副甲状腺腺腫と診断することが可能であった。血清カルシウムやIntactPTHが異常高値を呈する症例では,Double parathyroid adenomaも念頭に入れる必要があると考えられた。