2018 年 67 巻 3 号 p. 366-372
2018 年 67 巻 3 号 p. 366-372
髄液一般検査においては,Samson染色を用いて細胞数算定および単核球と多形核球の分類を行うこととされている。多形核球を多数認める場合,好中球増加を伴う細菌性髄膜炎をきたしていることが多いが,稀に好酸球増多を認めることがある。髄液中に好酸球増多を認める病態を好酸球性髄膜炎(eosinophilic meningitis)と呼び,主な原因として寄生虫感染に対する免疫応答が挙げられる。しかし,非感染性の原因によっても好酸球性髄膜炎を呈することが報告されている。髄膜炎の原因鑑別は適切な治療にとって重要となる。髄液検査における多形核球の形態分類にはMay-Giemsa標本による鏡検を要するが,Samson染色でも形態から鑑別が可能な場合がある。Samson染色は手技が簡便であり,多形核球分類のスクリーニングに有用と考えられる。今回当院において髄液中に好酸球を多数認めた4症例はいずれもSamson染色で好酸球の鑑別が可能であったことから,Samson染色による多形核球の形態分類の重要性が示唆された。
Samson染色を用いた髄液一般検査では,細胞数算定とともに,出現細胞を単核球と多形核球に分類することとされている。多形核球には好中球,好酸球,好塩基球が含まれるが,最も頻繁に認めるのは好中球であり,したがって多形核球優位の細胞数増加は細菌性髄膜炎を示唆する所見である。しかし,稀に髄液中に好酸球を認めることがあり,さらにこの髄液中に好酸球が増加する病態を好酸球性髄膜炎(eosinophilic meningitis)と称する。好酸球性髄膜炎はMay-Giemsa標本における白血球分画において好酸球を8%以上認める病態と定義され,主な原因としては寄生虫の感染によるものが多い。しかし,非感染性の原因によっても髄液中に好酸球増多を認めることが報告されている。
今回,当院では髄液中に好酸球を多数認めた症例を4例経験し,髄液一般検査における多形核球の形態分類の重要性が示唆されたので報告する。
髄液一般検査は髄液検査法20021)により実施した。これに記載されているSamson染色による好酸球の鑑別点に基づき,各症例における好酸球の形態的特徴を検討した。また,好酸球の算定はMay-Giemsa染色を用いて行った。なお,本検討は東京大学大学院医学系研究科・医学部倫理委員会の承認を得て実施した。
現病歴:水頭症の診断で帝王切開にて出生した。生後6か月に脳室-腹腔(ventriculoperitoneal; VP)シャント術を施行したが,その後大泉門膨隆やシャントバルブ周囲の髄液瘤を認め,精査目的のため入院となり髄液検査が行われた。
検査所見:髄液細胞数307個/μL,単核球18%,多形核球82%であった。May-Giemsa標本を鏡検したところ,好酸球87.5%であった(Figure 1)。Figure 1AのSamson染色では,好中球と異なり細胞質にむらのある橙色調の顆粒を認めた。
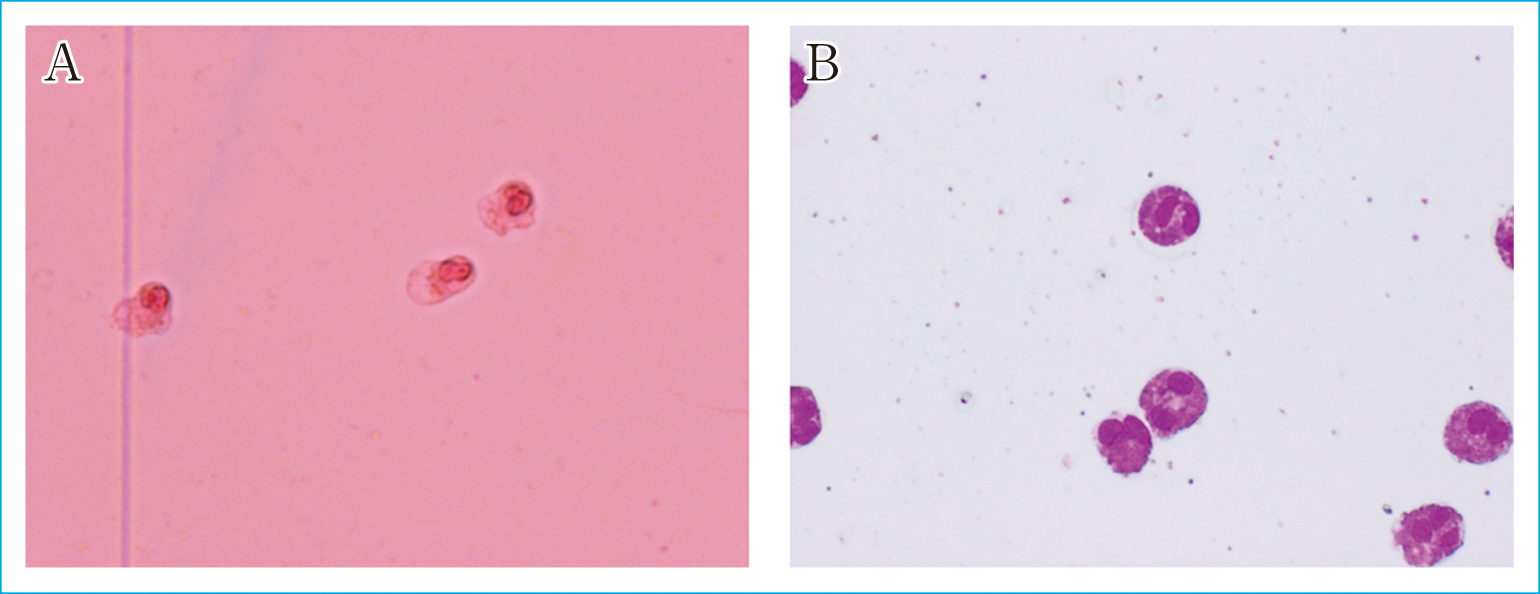
[Case 1] Cytology of the cerebrospinal fluid with Samson staining (A), and May-Giemsa staining (B). Scale: ×400
臨床経過:シャントグラフィの結果から腹腔側のシャント不全が考えられたため,腹腔鏡下癒着剥離および腹側シャントチューブ再挿入術を施行した。術中所見にて術創直下の腹壁に大網が癒着しており,この中にシャントチューブが入り込んでいたことが判明した。チューブをダグラス窩に留置することで改善し,その結果頭囲の縮小およびCTで脳室の縮小が認められた。
2. 0歳2か月男児現病歴:胎児機能不全疑いのため緊急帝王切開術にて出生した。その後,脳室内出血に伴う交通性水頭症の診断でオンマイヤーリザーバー留置術を施行した。生後2か月で頭部CTにて右硬膜下水腫を認め,その後拡大した。これにはリザーバーをつたい髄液が硬膜下腔に貯留し拡大している可能性が考えられたため,オンマイヤー抜去および硬膜下ドレナージ術を施行し,その際髄液検体が提出された。
検査所見:髄液細胞数19個/μL,単核球68%,多形核球32%で好酸球を38%認めた(Figure 2)。Figure 2AはSamson染色したサンプルを尿沈渣検査と同様の方法で鏡検したものであり,細胞は円形,メガネ状の2核を示し,細胞質はむらのある橙色調を呈した。
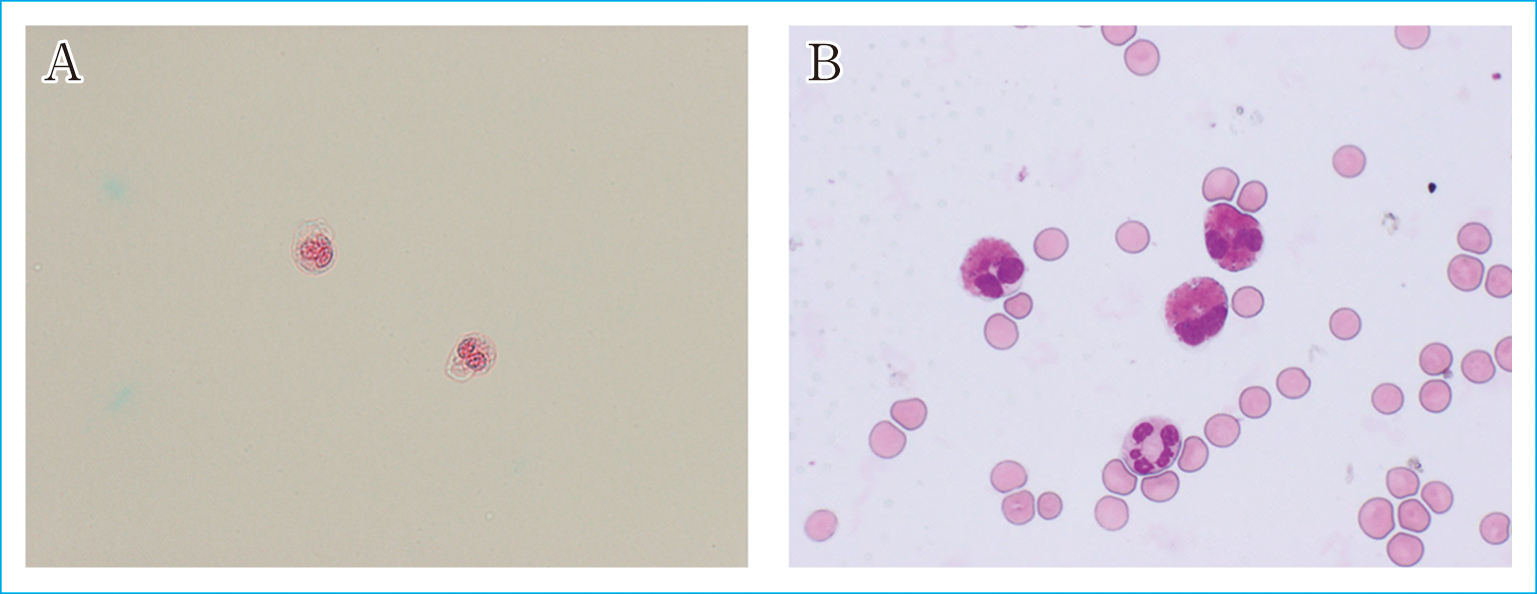
[Case 2] Cytology of the cerebrospinal fluid with Samson staining (A)20), and May-Giemsa staining (B). Scale: ×400
臨床経過:硬膜下ドレナージ術により脳室拡大の改善を認め,ドレナージを抜去した。
3. 62歳男性現病歴:13年前に発症した関節リウマチの患者で歯突起骨折を指摘され,後頭骨頸椎固定術(O-C4固定)を施行した。5か月後,スクリュー逸脱が疑われ後頭骨頸椎再固定術を実施した。術後にせん妄が遷延し,術後8日目に38度の発熱をきたしたが,創部感染徴候は認めなかった。ステロイド不足を考慮しプレドニゾロン5 mgの投与を開始するも,術後11日目に意識障害を認めたため髄液検査を実施した。
検査所見:髄液細胞数791個/μL,単核球57%,多形核球43%で好酸球を49%認めた(Figure 3)。Figure 3AのSamson染色では,好酸球は円形で,メガネ状の2核,および細胞質に橙色調の顆粒を認めた(矢印)。
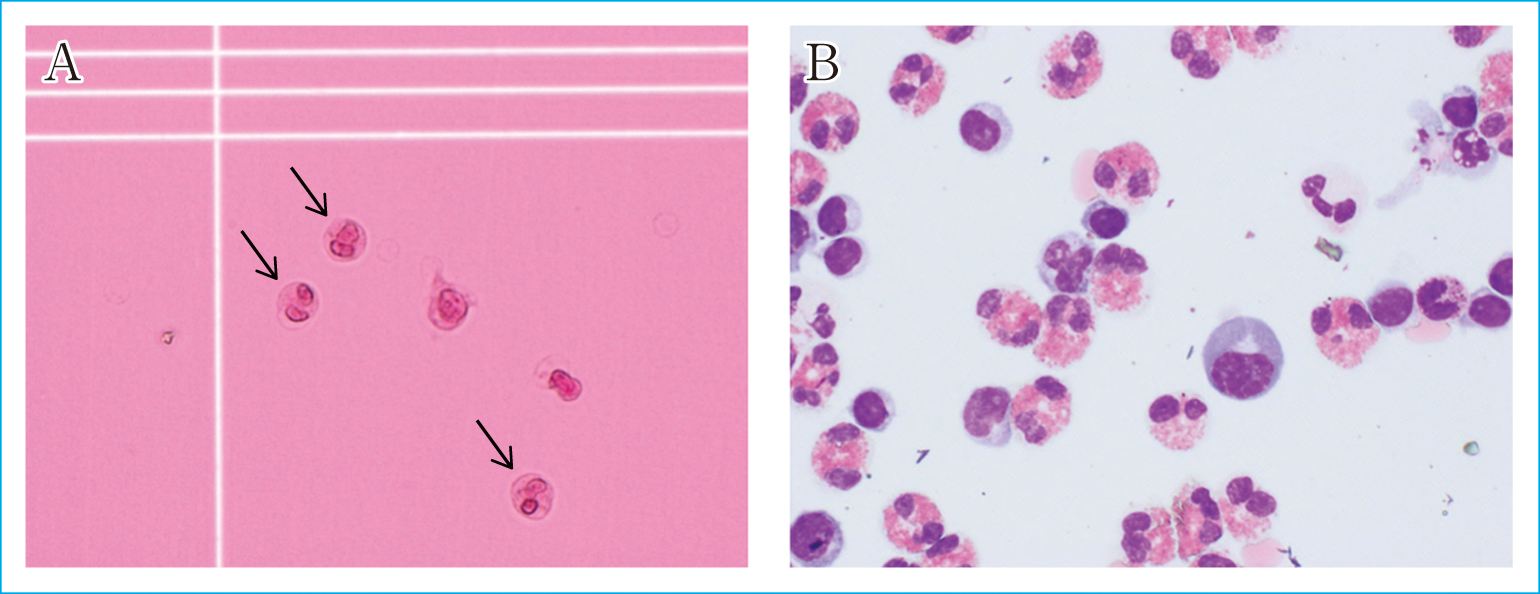
[Case 3] Cytology of the cerebrospinal fluid with Samson staining (A), and May-Giemsa staining (B). Arrows in (A) show eosinophils. Scale: ×400
臨床経過:細菌培養の結果は陰性であったが,感染症を完全に否定できないためセフェピム2 g × 3回,バンコマイシン1 g × 2回をそれぞれ投与し,相対的ステロイド不足を考えプレドニゾロンを10 mgに増量した。その後は良好な経過をたどり,術後20日目に抗生剤を中止し27日目にメトトレキサートの内服を再開した。
4. 65歳男性現病歴:6年前に左項部痛が出現し近医を受診,左C1/2に砂時計腫を指摘されたが本人の希望で外来にて経過観察となっていた。その後手術を希望したため腫瘍切除術を施行し,術中迅速組織診断にて硬膜外病変が神経鞘腫,硬膜内病変が髄膜腫と診断された。そのため硬膜切除を追加し,ゴアテックスを用いて硬膜を再建した。術後に頭痛が持続し,術後8日目で39度の発熱と酸素飽和度の低下を認めた。遷延する頭痛に対しプレガバリンの投与を開始したが,その後薬剤の副作用疑いで安息香酸ナトリウムカフェイン,ゾルピデム,セレコキシブを中止した。しかし,発熱が継続していたため髄膜炎を疑い,術後10日目に腰椎穿刺を実施した。
検査所見:髄液細胞数264個/μL,単核球87%,多形核球13%で好酸球を15%認めた(Figure 4)。Figure 4AのSamson染色では,好酸球は円形,メガネ状の2核を呈し,細胞質に橙色調の顆粒を認めた(矢印)。
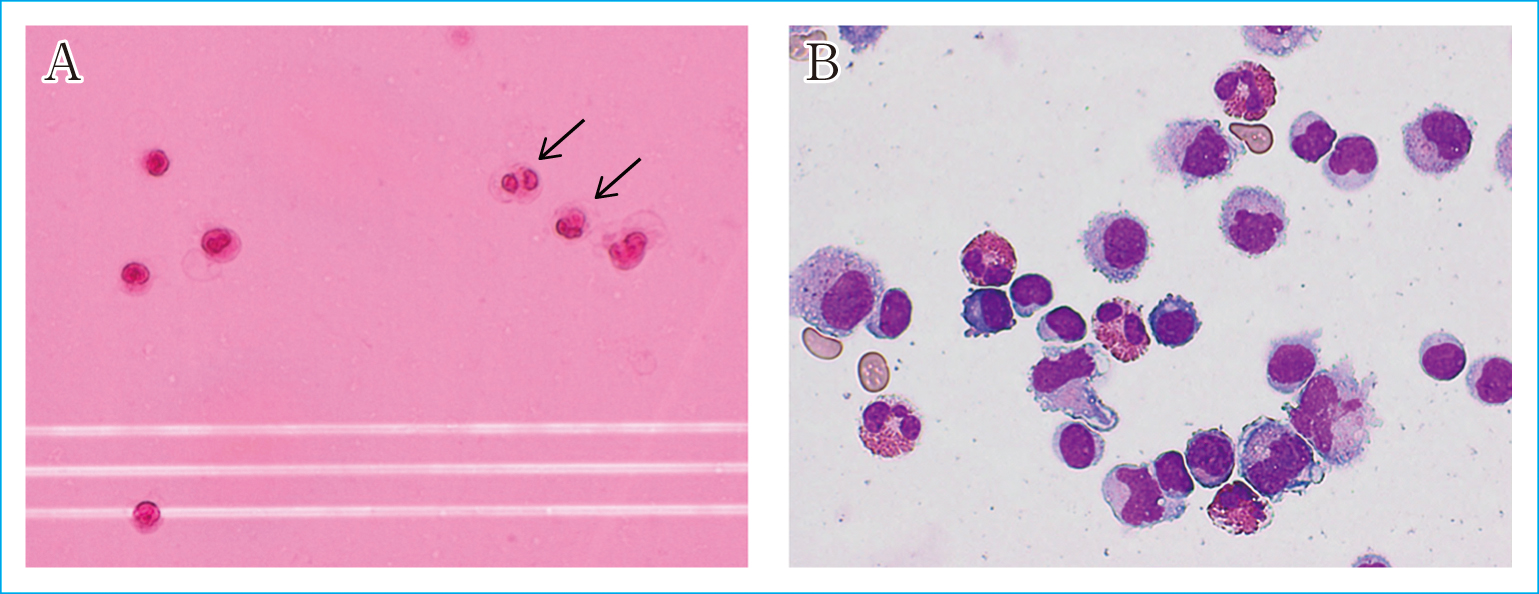
[Case 4] Cytology of the cerebrospinal fluid with Samson staining (A), and May-Giemsa staining (B). Arrows in (A) show eosinophils. Scale: ×400
臨床経過:細菌感染の所見はなかったが,バンコマイシンおよびセフェピムを開始,またプレガバリンは中止した。術後13日目にステロイド不足を疑いプレドニゾロン20 mg/dayの投与を開始したが,感染症は否定されたため抗菌薬は中止した。硬膜再建術に用いたゴアテックスに対するアレルギー反応を考慮し,パッチテストを実施したが陰性であった。その後,徐々に熱型・食思は改善し術後34日目にはプレドニゾロンを7.5 mg/dayへ減量した。
中枢神経系における炎症反応で髄液中に好酸球増加を伴うことは稀であり,1%以下であるとの報告2)もある。好酸球性髄膜炎は大きく感染性と非感染性の2つに分けることができる。感染性の例はそのほとんどが寄生虫の侵入に対する免疫応答だと考えられており,世界的には広東住血線虫による髄膜炎の発症頻度が高いとされ3),特に東南アジアや日本においても多く報告されている4)~6)。他にも有棘顎口虫やイヌ回虫などの感染により,好酸球性髄膜炎を呈した症例報告が複数ある7),8)。また,後述するように脳室内シャント術に伴う感染も好酸球性髄膜炎を引き起こす。感染は脳室内シャント患者の約13%にみられるとの報告があるが9),好酸球性髄膜炎で最も頻回に認められる起因菌はStaphylococcus epidermidis,Staphylococcus aureus,Propioniumbacterium acnesなどであるという10)。
一方,非感染性では脳室ドレナージや脳室内シャント,悪性腫瘍の中枢神経浸潤に対する二次的反応11),特発性好酸球増多症候群12)などが挙げられる。そのうち,脳室内シャントは主に水頭症などに対して行われるが,施行患者の34%に好酸球性髄膜炎が認められたとの報告13)がある。ただしその症状は一過性であり,シャント感染の治療やシャントの置換によって改善するとされている。脳室内シャントに関連した好酸球性髄膜炎の病因として,細菌感染の他では異物,血液の髄液への溢出,循環障害などが挙げられる。異物には縫合糸や手袋のパウダー,バンコマイシンやゲンタマイシンなどの抗生物質,ラテックスやシリコンといったシャントチューブの素材などが含まれる。このバンコマイシンやゲンタマイシンについては症例報告14)があるものの,その影響や詳細なメカニズムについては明らかにされていない。
今回,当院で経験した好酸球性髄膜炎を4例報告した。Table 1に髄液検査を施行した経緯および好酸球性髄膜炎をきたした推定原因について示す。症例1は水頭症によりVPシャントを施行した症例で,感染性が否定されたためシャントチューブに対するアレルギー反応が原因と思われた。事実,シャントグラフィの結果から腹腔側のシャント不全と考え,シャントの置換により症状は改善した。症例2は硬膜下ドレナージのカテーテルに対するアレルギー反応が原因と考えられた。ドレナージにより脳室拡大は改善し,リザーバーの抜去により髄液細胞数および好酸球の割合も減少した。症例3で好酸球を多数認めた原因として臨床上最も疑われたのは,薬剤もしくは手術のストレスによる相対的なステロイド不足であった。細菌感染も考えられたが培養の結果は陰性であり,感染症を原因とした好酸球性髄膜炎の可能性は否定的であった。一方,非ステロイド性抗炎症薬(non-steroidal anti-inflammatory drugs; NSAIDs)による好酸球性髄膜炎の報告15)はあり,本症例でも術後継続する頭痛に対しロキソプロフェンを頓服しており,NSAIDsが原因である可能性は否定できない。また,関節リウマチの既往がありステロイドを服用していたが,この周術期による相対的な不足で好酸球増多をきたした可能性を考慮し,プレドニゾロンを増量した。好酸球性髄膜炎の原因特定には至らなかったが,結果として被疑薬であるNSAIDsの中止およびステロイドの増量により全身状態は改善し,経過良好で退院となった。症例4については,砂時計腫の切除術後に発熱が続いており,その原因として臨床では手術部位感染(surgical site infection; SSI),薬剤熱,薬剤性髄膜炎,ゴアテックスアレルギーなどが疑われた。SSIの可能性を考え抗菌薬が投与されたが,培養の結果は陰性で感染症は否定的であった。その後,造影MRI・髄液検査・パッチテストを含めた精査が行われたがいずれも確定診断には至らなかった。好酸球が増加した原因として,薬剤もしくは硬膜再建に使用された人工硬膜の素材であるゴアテックスに対するアレルギーが考えられた。しかし,本症例においても症例3と同様,ステロイドの投与により全身状態の改善を認め,経過良好で退院となった。これまでにも,ステロイドが著効した好酸球性髄膜炎の症例報告16)があり,症例3・4は免疫学的な機序の関与が示唆されたものであった。
| Case | 1 | 2 | 3 | 4 |
|---|---|---|---|---|
| Age | 4 months | 2 months | 62 | 65 |
| Sex | Male | Male | Male | Male |
| Cells /μL | 307 | 19 | 791 | 264 |
| Mononuclear % | 18 | 68 | 57 | 87 |
| Polymorphonuclear % | 82 | 32 | 43 | 13 |
| Eo % CSF | 87.5 | 38.0 | 49.0 | 15.0 |
| Eo % blood | 1.0 | 5.0 | 8.1 | 5.7 |
| Bacteria | negative | negative | negative | negative |
| Symptoms | liquorrhea | ventricular enlargement | disorders of consciousness | fever |
| Observations | shunt failure | allergy to drain catheter | allergy to drugs, loss of steroids | allergy to drugs, or goatex |
髄液検査法20021)の改訂版として2015年に発刊された髄液検査技術教本17)によれば,髄液一般検査では細胞数算定とともに白血球は単核球と多形核球に分類することとされている。単核球にはリンパ球・単球・組織球などが含まれる。髄膜の炎症やくも膜下出血など髄膜への刺激に対する反応(無菌性髄膜反応)では,単球・組織球系の細胞の増加を認めることから,計算盤上でこれらの細胞を分類する意義は大きい18)。一方,多形核球には好中球,好酸球,好塩基球があり,このうち好塩基球を鑑別することは困難であるが,好中球と好酸球を分類することはある程度可能である。実際,本報の4症例はいずれもSamson染色で好酸球の鑑別が可能であった。好酸球は好中球と比較して円形のものが多く,細胞質に好酸性顆粒を持つためやや輝くような淡い橙色調を示すのが特徴である19)。鏡検時,コンデンサーを下げると光り輝くことから鑑別の一助となる。またメガネ状の2核を認めることも特徴のひとつとされる。本報では上記の3点を基準にSamson染色による好酸球の形態的特徴を検討し,いずれも鑑別が可能であると考えられた(Table 2)。また,Figure 2AはSamson染色したサンプルを尿沈渣検査と同様の方法で遠心し,その残渣をスライドガラスに滴下しカバーガラスをかけて鏡検した像であり,この方法20)を用いることで2核がより明瞭に確認でき,細胞質の好酸性顆粒もより捉えやすくなると考えられた。
| Case 1 | Case 2 | Case 3 | Case 4 | |
|---|---|---|---|---|
| Circular cell | − | + | + | + |
| Bilobed nuclei* | − | + | + | + |
| Orange granular cytoplasm | + | + | + | + |
* 2 lobes like a pair of glass
ただし,計算盤上では細胞に対して様々な方向から観察しているため,単核様に見えることもあることに留意しておかなければならない。したがって,計算盤上で好酸球を判定することは避けるべきであり,詳細な分類にはMay-Giemsa染色による細胞の観察が必要である。しかし,全髄液検体に対しMay-Giemsa標本を作製するのは日常業務上効率的とはいえない。それに比べSamson染色は簡便かつ迅速なため,これを用いて好酸球を疑う細胞をいち早く見つけ出すことが重要であり,必要に応じてMay-Giemsa標本を作製し詳細に観察するといった検査手順が,より効率的かつ有用であると考えられる。
好酸球性髄膜炎は国内でも報告が少なく稀な疾患である。一般的に,現在の報告様式では単核球と多形核球の分類のみであり,多形核球優位であった場合にはまず細菌性髄膜炎が疑われ,抗生物質が投与されることが多い。Samson染色を用いた簡便かつ迅速な髄液一般検査で好酸球を疑う細胞をいち早く検出し,May-Giemsa染色と併せて報告することによって,治療に関わる情報を早期に臨床へ伝えることができ,髄液一般検査の有用性がさらに高まると考えられる。
髄液中に好酸球を多数認めた症例を4例経験した。Samson染色による好酸球の鑑別は,技術的にもある程度可能であり,臨床的にも細菌感染症と区別するうえで重要である。日常検査において髄液中に好酸球を認めることは稀であるが,好酸球出現の可能性を常に念頭に置きながら検査をすることが肝要である。
本論文に関連し,開示すべきCOI 状態にある企業等はありません。