2023 年 72 巻 3 号 p. 452-457
2023 年 72 巻 3 号 p. 452-457
50歳代女性。乳がん,骨転移のため化学療法中であった。来院1か月前から腹痛を認め,血液検査とCT検査の結果,閉塞性黄疸と診断され入院となった。内視鏡的逆行性胆道膵管造影(ERCP)にて胆管ステントを留置後に発熱を認め,血液培養が採取された。培養18時間後に血液培養からグラム陰性桿菌が検出され,VITEK2によりPseudomonas aeruginosa/Pseudomonas putidaと判定された。追加試験としてアシルアミダーゼ試験と42℃での発育の有無を確認したが,P. aeruginosa,P. putidaのどちらにも合致しないため,同定不能とした。薬剤感受性試験ではImipenem(IPM),Meropenem(MEPM)に感性であったものの,Doripenem(DRPM)に耐性を示していたためmodified carbapenem inactivation method(mCIM)を実施した結果,カルバペネマーゼ産生菌と判定された。これらの結果からPseudomonas otitidisを疑い,他施設にて質量分析装置MALDI Biotyperでの同定検査を実施したところ,P. otitidisと同定された。P. otitidisは染色体性メタロβ-ラクタマーゼを保有しているが,16S rRNA遺伝子解析や質量分析装置を用いなければ同定できない。これらを有していない施設では,薬剤感受性のパターンや類似菌のキーとなる性状を把握することで本菌の推定が可能になり,適切な抗菌薬治療や過剰な感染対策を防ぐことへ繋がると考える。
A woman in her 50s was undergoing chemotherapy for breast cancer and bone metastasis. She had been admitted to our hospital with a diagnosis of obstructive jaundice since she had abdominal pain for one month. Blood culture was performed for a detailed examination of fever after biliary stent placement by endoscopic retrograde cholangiopancreatography (ERCP). Gram-negative bacilli were observed in blood cultures after 18 h of culture. It was determined to be Pseudomonas aeruginosa or Pseudomonas putida by VITEK2. As an additional test, the acyl amidase test was conducted and growth at 42°C was confirmed, but the results did not match those of either P. aeruginosa or P. putida, and thus the cells were not identifiable. In the drug susceptibility test, the strain was susceptible to both imipenem and meropenem, but resistant to doripenem. The strain was also found to be a carbapenemase-producing strain, as shown by the results of the modified carbapenem inactivation method. On the basis of these results, Pseudomonas otitidis was suspected. It was finally identified as P. otitidis, which is characterized by the presence of chromosomal metallo-β-lactamase determined using MALDI Biotyper. P. otitidis can only be identified using 16S rRNA gene sequence analysis and MALDI Biotyper. If we understand the pattern of drug susceptibility test results and the key biochemical characteristics of similar bacteria, we should be able to presume P. otitidis. We believe that this will lead to appropriate antimicrobial treatment and correct nosocomial infection control.
Pseudomonas otitidisは耳の感染症の原因菌として2006年に報告されたPseudomonas属の一種である1)。Pseudomonas属では初めてPOM-1型の染色体性メタロβ-ラクタマーゼを産生する菌種として報告された2)。P. otitidisは2022年現在,16S rRNA解析,また,質量分析装置ではMALDI Biotyper(ブルカージャパン)に限り同定可能となっており,生化学的性状での同定では他のPseudomonas属に誤同定される可能性が高い。感染例としては耳の感染症の他に,壊死性筋膜炎や腹膜炎,肺炎などが報告されている3)~5)。今回我々は,P. otitidisによる菌血症を伴った胆管炎症例において,薬剤感受性試験と生化学的性状から本菌を推定できた症例を経験したので報告する。
患者:50歳代,女性。
現病歴:右乳がん,骨転移のため外科外来に通院しており,化学療法による治療中であった。1か月前から腹痛を訴えており,来院時の血液検査にて肝・胆道系酵素の上昇と,CT検査で肝内胆管拡張を認めたことから閉塞性黄疸と診断され,原因精査のために翌日より入院となった。
入院時検査所見:Table 1に示す。
| First day of admission | Day 2 after admission (When the blood culture was positive) |
|
|---|---|---|
| WBC | 5.4 × 103/μL | 11.4 × 103/μL |
| RBC | 350 × 104/μL | 302 × 104/μL |
| Hb | 10.3 g/dL | 9.1 g/dL |
| Ht | 30.30% | 26.80% |
| Plt | 34.5 × 104/μL | 27.6 × 104/μL |
| Neutro | 73.90% | 95.20% |
| Lymphocyte | 11.50% | 2.10% |
| Monocyte | 6.70% | 2.30% |
| Eosinophil | 7.20% | 0.20% |
| Basophil | 0.70% | 0.20% |
| AMY | 39 IU/L | 392 IU/L |
| T-Bil | 4.1 mg/dL | 8.6 mg/dL |
| D-Bil | 3.0 mg/dL | 6.5 mg/dL |
| I-Bil | 1.1 mg/dL | 2.1 mg/dL |
| AST | 161 IU/L | 154 IU/L |
| ALT | 125 IU/L | 108 IU/L |
| ALP | 2,168 IU/L | 1,819 IU/L |
| LDH | 314 IU/L | 282 IU/L |
| γ-GT | 648 IU/L | 660 IU/L |
| CRP | 1.07 mg/dL | 8.12 mg/dL |
身体所見:体温36.6℃,血圧101/68 mmHg,脈拍74 bpm,呼吸数17回/分,SpO2 98%(室内気)。
臨床経過:入院1日目,内視鏡的逆行性胆道膵管造影(ERCP)が実施され,中部胆管の狭窄,それより肝側の胆管拡張を認めた。下部胆管に明らかな結石や狭窄は確認されなかったが,Mirizzi症候群が疑われ,胆管ステントを留置し,Cefmetazole(CMZ)が投与された。入院2日目の午前に,39.0℃の発熱を認めたため,胆管炎またはドレナージ不良を疑い,血液培養2セットを採取後に2度目のERCPが行われた。その結果,乳頭部は浮腫をきたしており,胆汁の排泄はみられなかったため,内視鏡的乳頭括約筋切開術を実施した。再度,胆管ステントを留置したところ,緑色混濁した胆汁が排泄されたため培養検査が提出された。ERCP後,呼びかけで覚醒するものの血圧が80/50 mmHgと低く,ノルアドレナリンの投与が開始された。CMZ投与後の発熱であったため抗菌薬は耐性菌を疑い,MEPMへ変更された。入院3日目,血液培養が陽性となったが,グラム陰性桿菌であったこと,体温も解熱していたことから抗菌薬はMEPMが継続投与された。入院5日目にカルバペネマーゼ産生のPseudomonas属と判明したため,抗菌薬をCiprofloxacinとAztreonamへ変更し,接触感染予防対策と個室隔離を開始した。7日間の抗菌薬継続投与でバイタルは安定し,入院12日目に退院となった(Figure 1)。
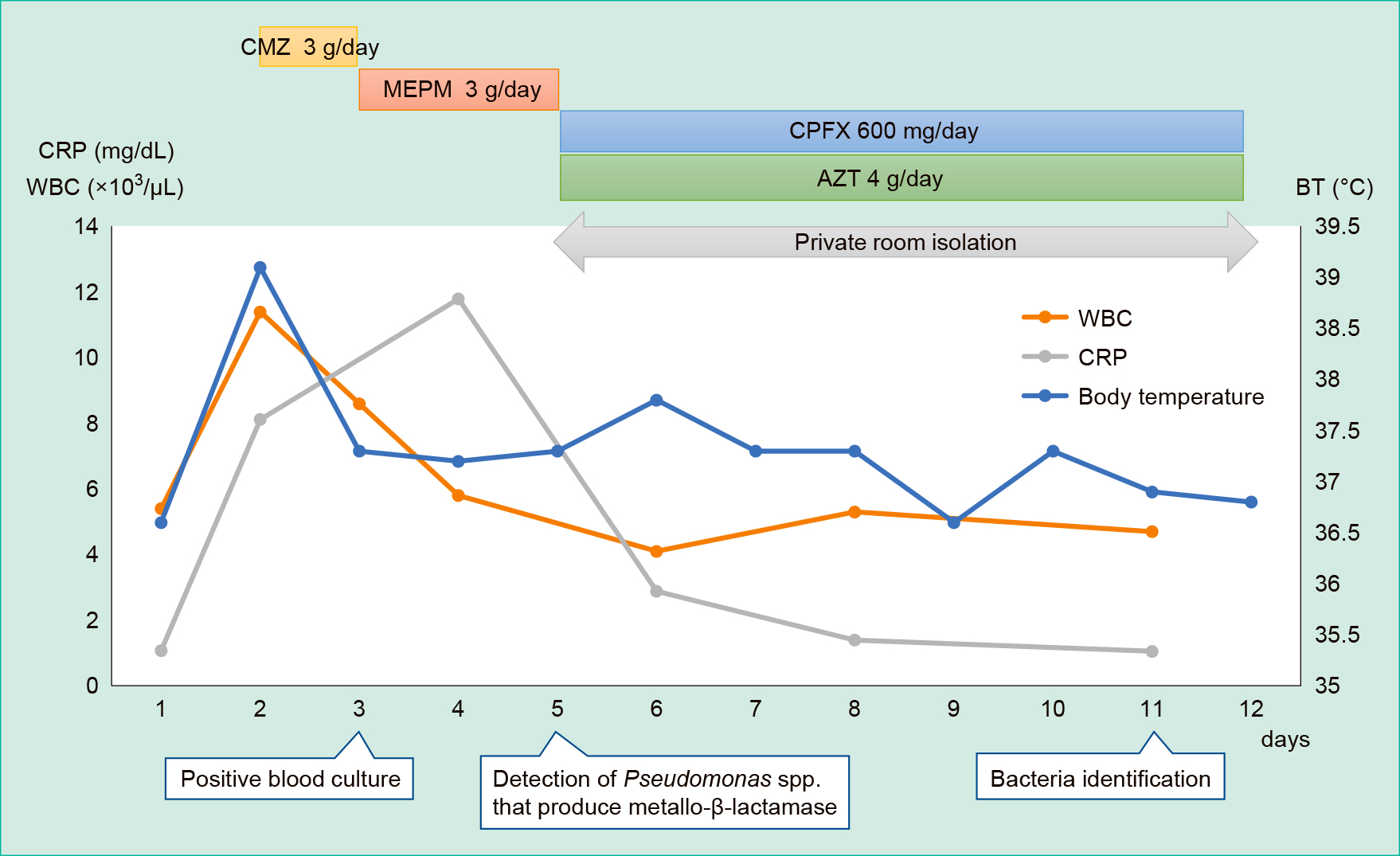
CMZ: Cefmetazole, MEPM: Meropenem, CPFX: Ciprofloxacin, AZT: Aztreonam
血液培養検査は,BDバクテック™ FXシステム(日本BD)にてBDバクテック™ 23F好気用レズンボトルPおよびBDバクテック™ 22F嫌気用レズンボトルPを用いて2セット培養を行った。培養18時間後に,2セット中,好気ボトルのみ2本が陽性となった。グラム染色(フェイバーG,日水製薬)を行ったところ,細いグラム陰性桿菌を認めたため,ニッスイ分画プレート 羊血液寒天/ドリガルスキー改良(日水製薬),チョコレート寒天培地(日本BD),TSI寒天培地(栄研化学)にて35℃,好気培養を行った。
2. 同定検査培養6時間後の菌を用いて,VITEK2(ビオメリュージャパン)GNカードにて同定検査を実施したところ,Pseudomonas aeruginosa/Pseudomonas putidaと判定された。培養翌日にはPseudomonas属を疑うラフな非溶血性のコロニーを認めた(Figure 2)。追加試験を実施したが,アシルアミダーゼ非産生,42℃での発育陽性となり,P. aeruginosa,P. putidaのどちらにも合致しないため,同定不能とした。(Table 2)。後日,他施設にてMALDI Biotyperによる精査を実施してもらったところP. otitidis(Score Value 2.02)と同定された。また,2度目のERCP時に採取された胆汁からも同菌が単一で検出された。

| Isolated strain | P. aeruginosa | P. putida | P. otitidis | |
|---|---|---|---|---|
| Acylamidase production | − | + | − | − |
| Growth at 42°C | + | + | − | NT |
| Acid production from | ||||
| Glucose | + | + | + | NT |
| Galactose | NT | + | + | − |
| Fructose | NT | + | + | − |
| Xylose | NT | − | + | − |
VITEK2による同定検査と同時にドライプレート栄研(栄研化学)を使用して薬剤感受性試験を実施した。35℃,好気環境下にて16時間培養後,CLSI M100-S30 P. aeruginosaの基準に準じて判定を行った(Table 3)。DRPMが耐性であったためmCIMを実施した結果,阻止円を認めず,カルバペネマーゼ産生菌と判定された。追加試験として,Yamadaら6)により報告されているSodium Mercaptoacetic Acid(SMA)ディスクを用いたinhibitor-combination mCIMによるメタロβ-ラクタマーゼの確認とXpert® Carba-R(ベックマン・コールター)でカルバペネマーゼ産生遺伝子の確認を実施した。Inhibitor-combination mCIMではMEPMとSMAディスクを同時にインキュベートすることで,MEPM単剤と比較して阻止円の拡大を認めたため,メタロβ-ラクタマーゼ産生菌であると推定された。しかしXpert® Carba-Rを用いた検査の結果,5つの遺伝子(KPC, NDM, VIM, OXA-48, IMP-1)は全て陰性であった。
| Antimicrobial agents | MIC (μg/mL) | MIC categories |
|---|---|---|
| Piperacillin (PIPC) | 4 | S |
| Tazobactam/piperacillin (TAZ/PIPC) | ≤ 4/16 | S |
| Ceftazidime (CAZ) | 2 | S |
| Cefepime (CFPM) | ≤ 1 | S |
| Aztreonam (AZT) | 8 | S |
| Imipenem (IPM) | 2 | S |
| Meropenem (MEPM) | 2 | S |
| Doripenem (DRPM) | ≥ 8 | R |
| Tobramycin (TOB) | ≤ 0.5 | S |
| Amikacin (AMK) | ≤ 1 | S |
| Levofloxacin (LVFX) | ≤ 1 | S |
| Ciprofloxacin (CPFX) | ≤ 0.12 | S |
P. otitidisは他のPseudomonas属と異なり染色体性メタロβ-ラクタマーゼであるPOM-1を保有しており,正確な菌名同定が,適切な抗菌薬選択や過剰な感染対策を防ぐことへ繋がると考える。現状として16S rRNA遺伝子解析やMALDI Biotyperを用いた同定方法しか確立されておらず,これらの方法で同定できる施設はまだ多くはないと考える。また,コロニーの性状もP. aeruginosaと類似しているため,多くは誤同定されている可能性がある。P. otitidisは特徴的な薬剤感受性パターンが報告されており,そのパターンを考慮することで本菌が推定できると考える。既知の報告では,多くのP. otitidisはカルバペネム系薬に中等度耐性から耐性であることに加え,セファロスポリン系薬に感性と判定されている2),3),5),7)。これらの文献では,カルバペネム系薬はIPMとMEPMが多く測定され,MEPMのみ,もしくは両薬剤に耐性と判定されている株が多数を占めるが,本症例ではセファロスポリン系薬に感性,かつIPMとMEPMが感性であり,カルバペネム2薬剤のみの測定ではカルバペネマーゼ産生を疑えなかった。しかし当院ではDRPMも測定しており,DRPMに耐性を示したことがカルバペネマーゼ産生確認試験を実施するきっかけとなった。西山らの報告でも6例全てにおいてDRPMは高いMIC値を示していた(Table 4)5),7)。カルバペネム系薬の中でもDRPMの測定が,P. otitidisの推定の鍵になると考える。
| MIC (μg/mL) | |||||||
|---|---|---|---|---|---|---|---|
| Isolated strain |
Nishiyama (n = 6)5) | ||||||
| Imipenem | 2 | 2 | 2 | 8 | 2 | 2 | 2 |
| Meropenem | 2 | ≥ 16 | 4 | ≥ 16 | 8 | ≥ 16 | 8 |
| Doripenem | ≥ 8 | ≥ 8 | ≥ 8 | ≥ 8 | ≥ 8 | ≥ 8 | ≥ 8 |
本症例の同定検査ではVITEK2でP. aeruginosaとP. putidaの2菌種が候補に挙がったものの,追加試験として実施したアシルアミダーゼ試験,42℃での発育試験の結果がいずれにも一致しなかったことから,別の菌種であることが推定された。P. aeruginosaとP. putida,P. otitidisの糖分解性状を比較したところ,P. otitidisは前者2菌種と異なり,ガラクトース,フルクトース,キシロースの全てにおいて糖分解による酸産生は認めない(Table 2)1),8)。しかし,当院で同定検査に使用しているVITEK2とアピ20NE(ビオメリュージャパン)ではこれらの項目が搭載されていないため,今回実施した2つの追加試験が菌の鑑別に有用であったと考える。
今回の症例を踏まえ,過去に当院で血液培養から分離され,P. aeruginosaと同定されたセファロスポリン系薬に感性,かつメタロβ-ラクタマーゼ産生菌1株をMALDI Biotyperにて再検査したところ,P. otitidisと同定された。検出時,VITEK2にてP. aeruginosa(同定確率93%)と判定されたため,追加試験を実施せずに菌名報告を行っていた。今回の症例のように,アシルアミダーゼ試験や42℃での発育の有無を確認していれば,P. otitidisを推定することが可能であったかもしれない。過去の症例では,プラスミド性カルバペネマーゼ産生P. aeruginosaとして報告を行ったため,当院の感染予防策マニュアルに則り,入院中19日間の個室隔離を実施していた。現在はセファロスポリン系薬に感性であるカルバペネマーゼ産生のPseudomonas属が検出された場合には,誤同定を避けるため,VITEK2に加えアシルアミダーゼ試験と42℃での発育の確認も行うこととしている。
P. otitidisの同定には16S rRNA遺伝子解析やMALDI Biotyperによる解析が必要となってくる。当院のように自施設において実施できない場合でも,本菌の薬剤感受性パターンや類似菌のキーとなる性状を把握することで,用手法を駆使してP. otitidisを推定することができ,適正な抗菌薬療法と過剰な感染対策を防ぐことが可能であると考える。
本論文に関連し,開示すべきCOI 状態にある企業等はありません。