Abstract
症例は61歳の女性で,肝腫瘍に対し各種画像検査を行ったが確定診断に至らず,肝生検を施行し転移性肝癌と診断した.各種検査で原発巣の同定が困難だったため,悪性と診断した肝腫瘍の切除を行う方針とした.術中,肝腫瘍の他に胃壁内腫瘤と胃小彎リンパ節の腫大を認め,迅速組織診で悪性の結果であったため,胃癌肝転移と診断し,肝切除に加え,胃全摘,リンパ節郭清を行った.永久標本の病理組織学的検査所見では,肝臓,胃,リンパ節とも全て類上皮血管内皮腫と診断された.肝腫瘍は典型的な類上皮血管内皮腫の組織像を呈したのに対し,胃では腫瘍細胞は主に血管内に疎らに存在するのみであったため,肝原発類上皮血管内皮腫の胃壁内およびリンパ節転移と診断した.
はじめに
類上皮血管内皮腫(epithelioid hemangioendothelioma;以下,EHと略記)は,緩除に進行するまれな非上皮性悪性腫瘍である.原発臓器としては肝臓1),肺2)が多いが,軟部組織3)などその他さまざまな臓器での発生が報告されている.初診時に単一臓器もしくは複数の臓器に多発する腫瘍として発見されることもあり4),臨床上,転移性悪性腫瘍との鑑別が問題になることが多い.また,その組織像も低分化腺癌,特に印環細胞癌と紛らわしい像を含むことから5),腫瘍の一部からの生検では正しい診断に至ることが難しいことがある.
今回,我々は術前診断に苦慮した肝臓のEHの1例を経験した.術中所見で胃壁内および胃小彎リンパ節にも腫瘤を認め切除したところ,これらもEHと診断された.病理組織学的検査所見から肝臓に原発したEHが,胃壁内および胃小彎リンパ節に転移したと推察された.
症例
症例:61歳,女性
主訴:特になし.
既往歴:特記事項なし.
家族歴:特記事項なし.
現病歴:人間ドックの腹部超音波検査で肝腫瘤を指摘され,前医を受診した.腹部CTで肝S3,S5に低吸収腫瘤を認め,経過観察していたところ,9か月後のCTでS3腫瘤の増大を認めたため,当院紹介受診となった.
血液検査所見:血算,生化学検査では,γGTPの軽度上昇を認める以外に異常を認めず,CEA,CA19-9,AFP,CA125などの腫瘍マーカーにも異常は認めなかった.HBs抗原,HCV抗体はともに陰性だった.
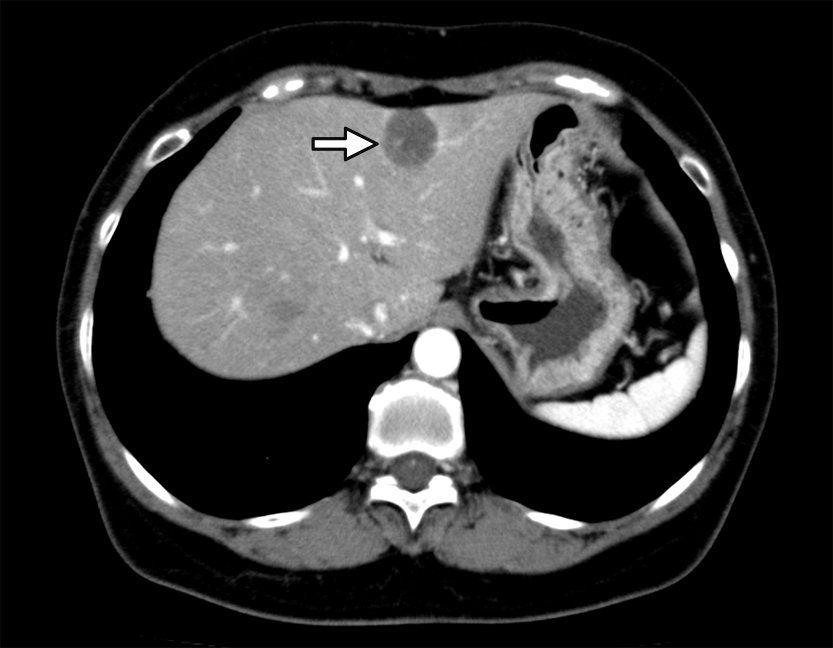
腹部造影CT所見:肝S3に23 mm,S5 に18 mmの,内部に線状の造影効果を有する類円形の低吸収腫瘤を認めた(Fig. 1).
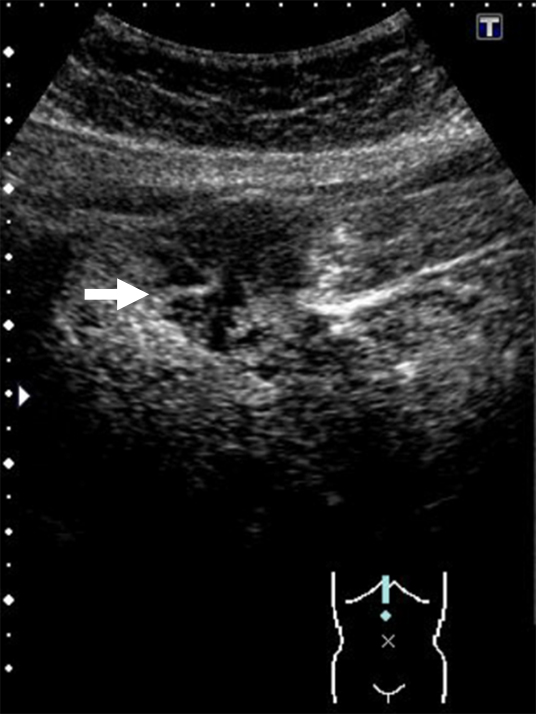
腹部造影エコー所見:S3の腫瘤は,境界明瞭な低エコー腫瘤として描出され,辺縁低エコー帯は認めなかった.ソナゾイド投与後の動脈相では腫瘤には染影を認めなかったが,腫瘤内部に既存の血管と思われる染影を認めた(Fig. 2).Kupffer相では腫瘤は周囲肝実質より著明な低エコーを示した.S5の腫瘤は造影前エコーでは認識できなかったが,Kupffer相では低エコー腫瘤として描出された.
FDG-PET-CT所見:S3の腫瘤にmaximum standardized uptake value:4.4のFDG集積を認めたが,S5の腫瘤にはFDG集積を認めなかった.
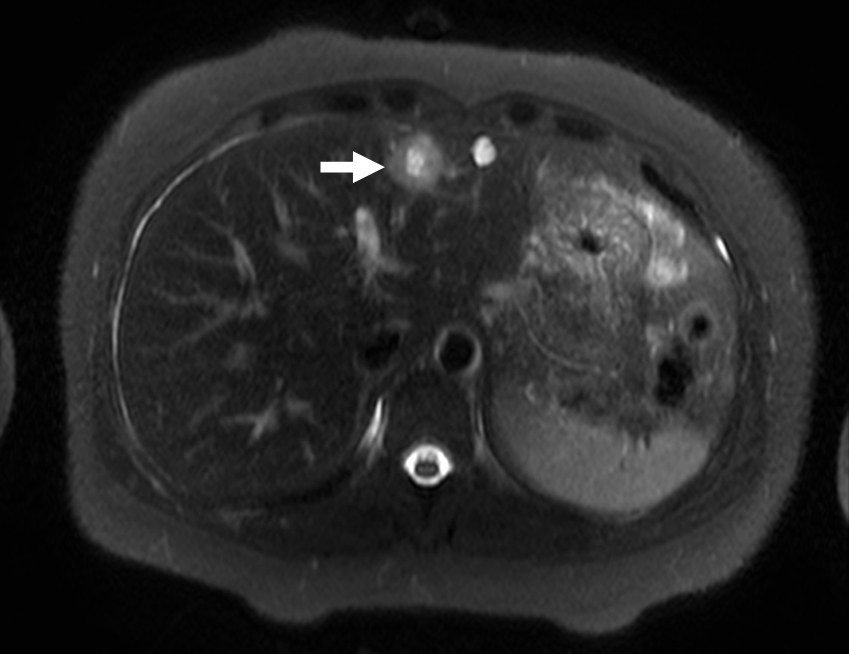
造影MRI所見:S3の腫瘤は,T1-weighted imageで低信号,T2-weighted imageで辺縁がやや高信号で中心部に強い高信号を認めた(Fig. 3).EOB・プリモビストによる造影動脈相では,内部に線状の濃染部を認めた.肝細胞相では腫瘤は低信号を示し,diffusion weighted imageでは高信号を示した.S5の腫瘤も同様の所見であった.
消化管内視鏡検査所見:上部消化管内視鏡では,胃体中部小彎に4 mmの粘膜下腫瘍と思われる所見を認めた.下部消化管内視鏡では,小ポリープを認めるのみだった.
CT,腹部超音波,MRI所見から当初は転移性肝癌を疑い,上部および下部消化管内視鏡検査を行ったが,原発巣と考えられる病変は認めなかった.造影エコー,PET-CTなどからも確定診断には至らず,肝生検を行う方針となった.
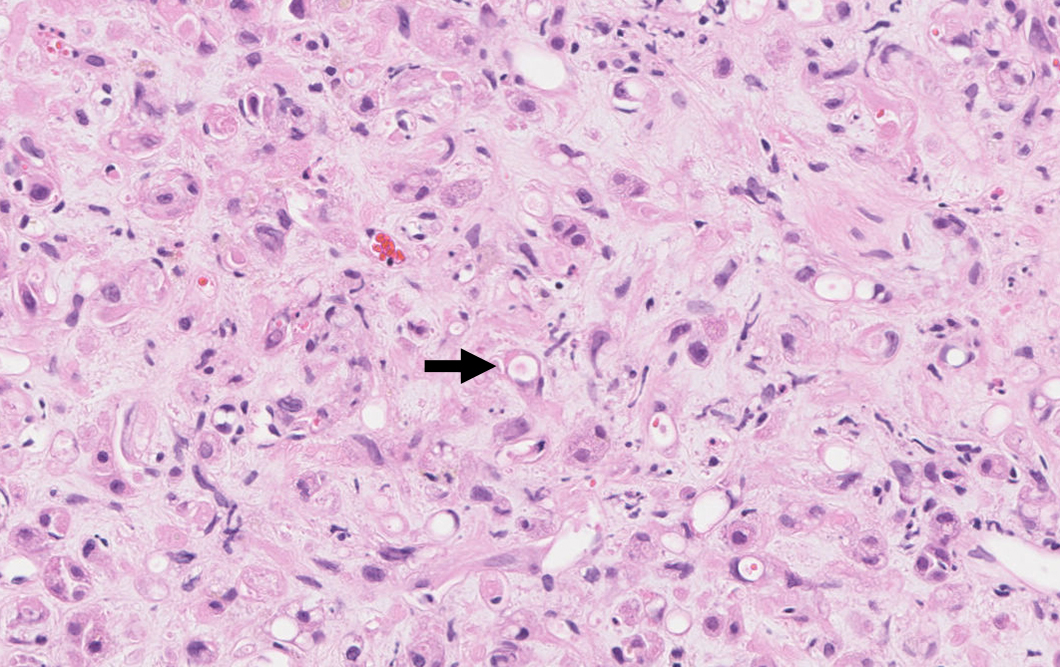
肝生検所見:分化度の低い腫瘍細胞がびまん性に増殖し,腫瘍細胞の一部は印環細胞様の形態を呈し,脈管浸潤を疑わせる所見が散見された(Fig. 4).免疫染色検査ではcytokeratin 7(+),cytokeratin 20(–),cytokeratin 19(–),hepatocyte(–),thyroid transcription factor-1(–)であり,低分化腺癌の転移と考えた.
原発不明癌として抗癌剤治療の施行も検討したが,薬剤選択が難しく,複数科で検討した結果,肝病変と開腹所見から追加情報を得る目的で,悪性と診断した肝病変の切除を行う方針となった.
手術所見:肝S3,S5に硬い腫瘤を触知し,既知の病変と考えられた.また,胃体中部小彎前壁に2 cm大の粘膜下腫瘍様の病変を触知し,その近傍に腫大したリンパ節を認めた.この胃病変とリンパ節を迅速組織診に提出したところ悪性所見を認めたため,術中診断として胃癌およびその肝転移と考え,胃切除,D2郭清,肝部分切除を行う方針とした.胃切除は,はじめに幽門側切除を行ったが,胃の口側断端に異型細胞を認めたため,最終的に胃全摘(胆囊摘出術併施)となった.手術時間は9時間58分,出血量は606 mlであった.
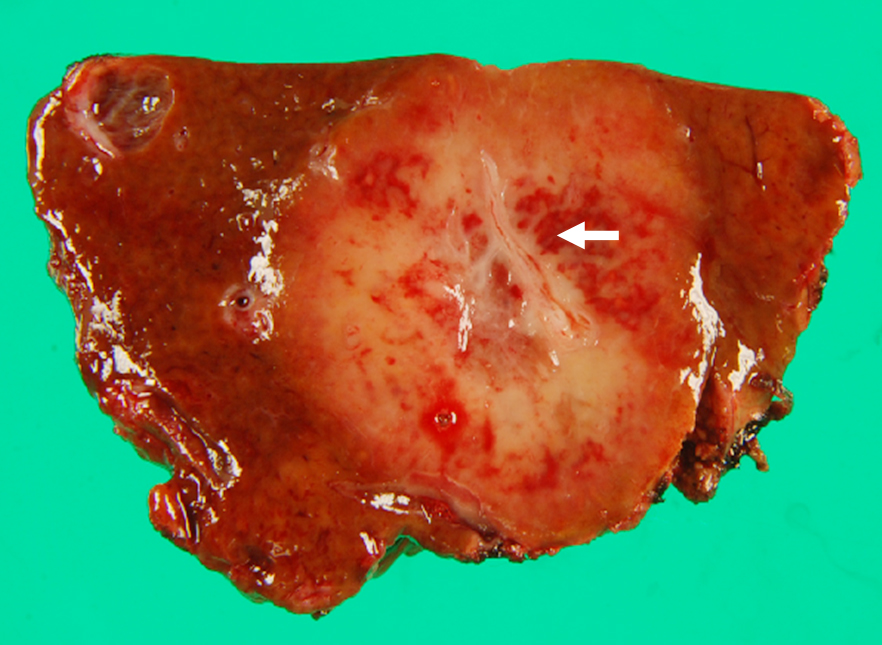
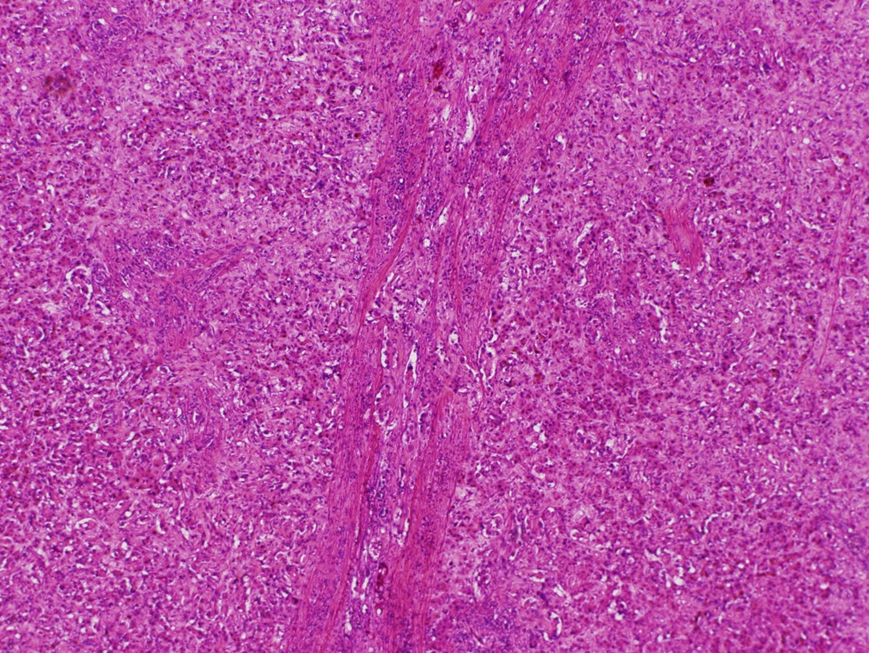
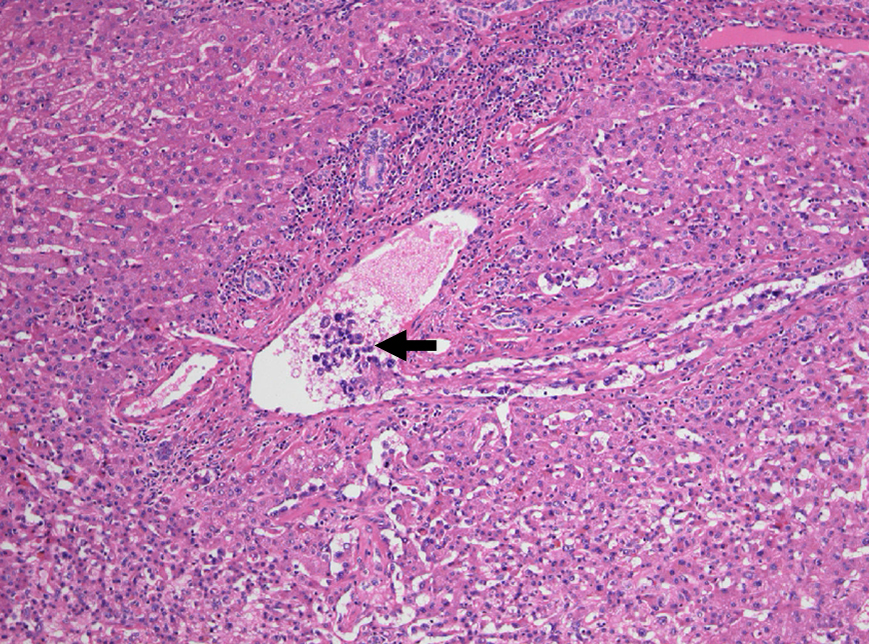
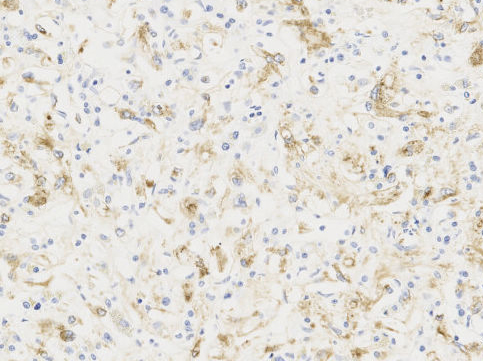
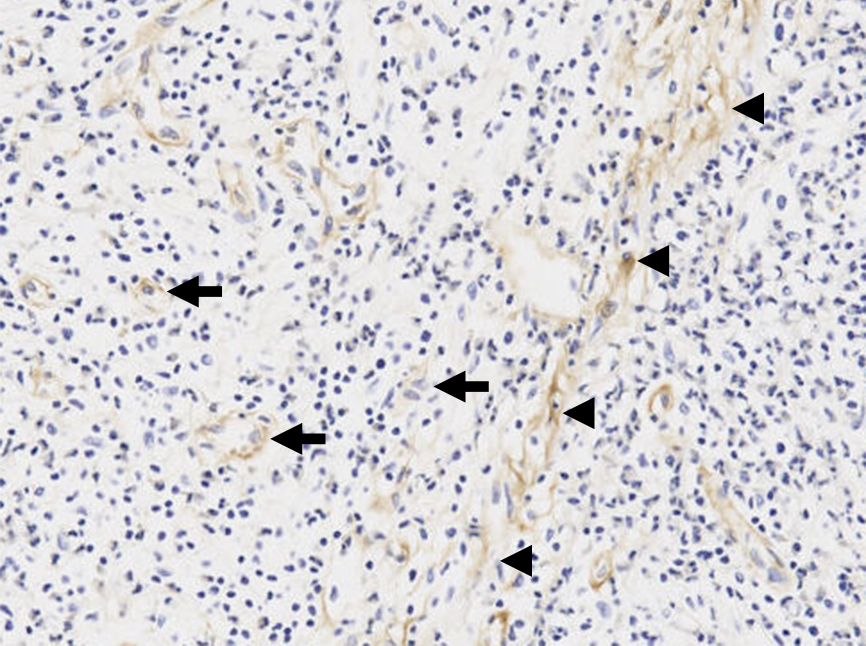
病理組織学的検査所見:肝S3,S5に,それぞれ22×21 mm,22×9 mmの白色調で光沢を持ち,やや境界不明瞭で浸潤性に増殖する腫瘍を認めた.腫瘍内部には既存の血管と思われる像を認め(Fig. 5),その血管内に腫瘍細胞の浸潤を認めた(Fig. 6).腫瘍細胞は類円形核を持ち,胞体が豊富で類上皮様の形態を示し,一部に乳頭状増殖や門脈内への浸潤(Fig. 7),静脈閉塞像を認めた.免疫染色検査では第VIII因子関連抗原(+)(Fig. 8),CD31(+),CD34(+),AE1/AE3(–),cytokeratin 7(+)であり,HE像と合わせEHと診断した.胃体中部小彎前壁の粘膜下腫瘍部では,炎症細胞浸潤とともに第VIII因子関連抗原(+)の腫瘍細胞を孤在細胞~小集簇として疎らに認め,腫瘍細胞は主に静脈内に存在していた(Fig. 9, 10).腫大リンパ節にも同様の細胞を認めた.肝腫瘍は腫瘍組織量・間質の変化ともに豊富でEHの典型的な組織像を示していたのに対し,胃では腫瘍細胞は主として静脈内に疎らに存在するのみで,硝子様基質形成などEHで見られる組織変化も認めなかった.以上から,肝臓に原発したEHが,胃壁内および胃小彎のリンパ節に転移したと考えた.
術後経過:経過良好で術後12日目に退院し,術後1年9か月後の現在,無再発生存中である.
考察
EHは,1982年にWeissら3)により癌の転移と間違われることのある血管内皮細胞に由来するまれな悪性腫瘍として,独立した疾患として初めて提唱された.これまで報告されているものの多くは肝臓1),肺2)に発生したものであるが,軟部組織3)など体内のさまざまな臓器での報告がある.緩除に進行する低悪性度の腫瘍であるが,転移を来すなど致死的な経過をたどることからWHO分類第4版6)では,悪性腫瘍として位置づけられている.
肝臓原発のEH(以下,H-EHと略記)は,1984年に本邦からFukayamaら1)が,国外からはIshakら7)が報告している.Mehrabiら8)が402例の報告をreviewとしてまとめるなど報告例は多いが,まれな腫瘍であり実際に臨床で接することは少ない.それ故に,本症例もいくつかの臨床的・病理学的課題を包含している.
第一の課題は,術前診断の困難性である.H-EHの典型的画像所見は,肝辺縁に存在し,造影CTではわずかな造影効果を有する低吸収腫瘤であるとされる8).腹部超音波では低エコーを示し,MRIではT1強調像で低信号,T2強調像で高信号を示すのが典型的とされ8),腫瘍の中心部と辺縁での信号強度が異なり‘的(まと)’のように見えるtarget signが特徴的であるとの報告もある9).また,PETでは周囲肝よりもわずかに高いFDGの集積を示すとされる10).
本症例ではCT,MRI,エコーの各種造影検査で腫瘍内部に線状の造影効果を認めた.病理組織学的検査所見では腫瘍内部を貫くように存在する既存の血管と思われる構造を認めており,これが造影されたものと考えられる.これまでの報告でこの所見に言及したものはなかったが,比較的悪性度の低い腫瘍としてのH-EHの特徴を反映している可能性がある.
H-EHの画像所見は転移性肝癌のそれとよく似たものが多く,両者の鑑別に難渋することが多い.本症例でも画像検査による診断が困難であったため,腫瘍生検を行った.腫瘍を構成する細胞には,血管形成を示唆するような細胞質内空胞を持つ細胞があり,H-EHに特徴的とされているが,この細胞が印環細胞癌に似て紛らわしい.空胞内部に赤血球を認めることが鑑別所見になるとされるが5),全ての細胞内に認められるわけではない.Makhloufら11)は,H-EHのうち初回の病理組織学的検査所見で正診に至ったものは25%に過ぎなかったと報告しており,病理組織学的にもEHを診断することの困難性が伺える.EHの診断には免疫染色検査が有効であり,血管内皮マーカーの第VIII因子関連抗原(von Willebrand因子),CD31,CD34が陽性となる5).サイトケラチンなどの上皮系マーカーは通常陰性であるが,15%程度に陽性を示すとされ5),本症例でもCK7が陽性となったことで術前診断を更に困難にさせた.生検では腫瘍全体の組織像を捉えることが難しい場合もあり,その評価には注意が必要である.臨床経過や画像検査所見なども合わせ,なによりEHを想起できるかが鑑別診断を行ううえで重要であると考える.
本例の第二の課題は手術適応に対する考え方である.本症例の手術治療が完遂するまでに二回の方針決定の機会があった.一つ目は原発巣不明の転移性肝癌と診断して手術に踏み切った時点である.原発不明癌としてそのまま抗癌剤治療を行うという選択肢もあったが,複数科で検討した結果,肝部分切除で病変切除が可能で手術リスクは高くないことや,開腹所見および切除標本組織から原発巣推定ができる可能性を考え,肝切除を行う方針とした.二つ目は開腹所見で胃癌,リンパ節転移,肝転移と診断した時点である.現在,胃癌肝転移に切除を勧めるガイドラインはないが,症例を選んで肝切除を行うことで予後改善につながる可能性もあり12),当施設では3個以内の胃癌肝転移に対しては積極的に肝切除を行っているため,本症例も胃切除,肝切除の方針とした.
本例の第三の課題は,原発臓器に対する考え方である.本例のように同種の腫瘍が複数の臓器に認められるときは,原発巣と転移巣の関係である場合と,それぞれが別々に発生した腫瘍(多中心性発生)13)である場合とが考えられる.また,EHの転移様式には,血行性,リンパ行性ともにあり得る11).本症例では,肝腫瘍は腫瘍組織量・間質の変化ともに豊富でEHの典型的な組織像を示していたのに対し,胃では腫瘍細胞は孤在細胞~小集簇として疎らに存在するのみで,主として静脈内腫瘍栓として存在し,硝子様基質形成などEHで見られる組織像も見られなかった.胃原発EHのこれまでの報告例をみると,壁外発育型腫瘤もしくは粘膜下腫瘍様の形態を取り,その組織像は本症例の肝臓に見られたような典型的なEHの像であり14)~17),本症例の胃病変とは明らかに異なる.これらから考えると,本症例は肝臓に原発し,胃へ血行性に転移したと考えるのが妥当であると考えられた.この転移経路は門脈血流とは逆方向であるが,肝細胞癌では経門脈的な胃転移の報告が散見されており18)19),本症例でも同様の転移経路による可能性がある.リンパ節転移に関しては,肝臓からリンパ節へ直接転移した場合と,肝臓から胃に転移した後にリンパ節へ転移した場合が考えられるが,本症例では肝臓,胃ともにはっきりとしたリンパ管侵襲は認められず,その転移経路の推定は困難である.また,リンパ節に生じたEHは原発20),転移21)22)ともに報告がある.リンパ節に原発したものの初期像を観察している可能性は否定しきれないが,頻度は転移によるものが多く,胃病変を転移と考えた場合の病変の広がりから考えて,転移のほうが考えやすい.
医学中央雑誌で「類上皮血管内皮腫,胃」をキーワードに1983年1月から2013年12月までの期間で,またPubMedで「epithelioid hemangioendothelioma, gastric」,「epithelioid hemangioendothelioma, stomach」をキーワードに1950年から2013年12月までの期間で検索を行ったところ,肝原発の類上皮血管内皮腫が胃に転移した報告はMakhloufら11)の報告例中に1例認めるのみで,非常にまれな症例であると考えられた.
EHは一般的に比較的緩徐な経過を呈する腫瘍であるが,急速進行した症例21)や,術後98か月してから再発した症例も報告されており22),本症例も注意深く経過を観察していきたい.
利益相反:なし
文献
- 1) Fukayama M, Nihei Z, Takizawa T, Kawaguchi K, Harada H, Koike M. Malignat epithelioid hemangioendothelioma of the liver, spreading through the hepatic veins. Virchows Arch A Pathol Anat Histopathol. 1984;404(3):275–287.
- 2) Kitaichi M, Nagai S, Nishimura K, Itoh H, Asamoto H, Izumi T. Pulmonary epithelioid haemangioendothelioma in 21 patients, including three with partial spontaneous regression. Eur Respir J. 1998 Jul;12(1):89–96.
- 3) Weiss SW, Enzinger FM. Epithelioid hemangioendothelioma: a vascular tumor often mistaken for a carcinoma. Cancer. 1982 Sep;50(5):970–981.
- 4) Bollinger BK, Laskin WB, Knight CB. Epithelioid hemangioendothelioma with multiple site involvement. Literature review and observations. Cancer. 1994 Feb;73(3):610–615.
- 5) 芳賀 博典.血管・間葉系腫瘍およびその他 類上皮血管内皮腫.中沼安二,坂元亨宇編.腫瘍病理鑑別診断アトラス 肝癌.東京:文光堂;2010. p. 153–156.
- 6) Miettinen M, Fletcher CDM, Kindblom LG, Zimmermann A, Tsui WMS. Mesenchymal tumours of the liver. In: Bosman FT, Carneiro F, Hruban RH, Theise ND, editors. WHO classification of tumours of the digestive system. Lyon: IARC; 2010. p. 241–250.
- 7) Ishak KG, Sesterhenn IA, Goodman ZD, Rabin L, Stromeyer FW. Epithelioid hemangioendothelioma of the liver: A clinicopathologic and follow-up study of 32 cases. Hum Pathol. 1984 Sep;15(9):839–852.
- 8) Mehrabi A, Kashfi A, Fonouni H, Schemmer P, Schmied BM, Hallscheidt P. Primary malignant hepatic epithelioid hemangioendothelioma: a comprehensive review of the literature with emphasis on the surgical therapy. Cancer. 2006 Nov;107(9):2108–2121.
- 9) Chen Y, Yu RS, Qiu LL, Jiang DY, Tan YB, Fu YB. Contrast-enhanced multiple-phase imaging features in hepatic epithelioid hemangioendothelioma. World J Gastroenterol. 2011 Aug;17(30):3544–3553.
- 10) Dong A, Dong H, Wang Y, Gong J, Lu J, Zuo C. MRI and FDG PET/CT findings of hepatic epithelioid hemangioendothelioma. Clin Nucl Med. 2013 Feb;38(2):e66–73.
- 11) Makhlouf HR, Ishak KG, Goodman ZD. Epithelioid, hemangioendothelioma of the liver: a clinicopathologic study of 137 cases. Cancer. 1999 Feb;85(3):562–582.
- 12) 松村 優, 竹村 信行, 斎浦 明夫, 佐野 武, 山口 俊晴.【胃癌肝転移に対する治療戦略】 胃癌肝転移に対する肝切除の適応と予後.臨床外科.2013;68(13):1426–1432.
- 13) Nerlich A, Berndt R, Schleicher E. Differential basement membrane composition in multiple epithelioid haemangioendotheliomas of liver and lung. Histopathology. 1991;18(4):303–307.
- 14) Lee KC, Ng WF, Chan JK. Epithelioid hemangioendothelioma presenting as a gastric polyp. Histopathology. 1988 Mar;12(3):335–337.
- 15) Versaci A, Macri A, Scuderi G, Leonello G, Fedele F, Certo A, et al. Epithelioid hemangioendothelioma of the stomach: clinical-pathological features, nosologic setting, and surgical therapy. Report of a case. Surg Today. 2002;32(3):274–277.
- 16) Sanjay P, Raman S, Shannon J, Williams GT, Woodward A. Gastric epithelioid haemangioendothelioma: a rare cause of upper gastrointestinal bleeding. Postgrad Med J. 2005 Aug;81(958):e7.
- 17) Tavares AB, Almeida AG, Viveiros FA, Cidade CN, Barbosa JM. Gastric epithelioid haemangioendothelioma. BMJ Case Rep. 2011;2011:bcr0120113791.
- 18) 柴田 哲男, 中野 哲, 北村 公男, 綿引 元, 武田 功, 小沢 洋.胃に血行性転移を来たした肝細胞癌の一剖検例.日本消化器病学会雑誌.1998;78(10):110–114.
- 19) 矢後 修, 渕上 哲, 魚住 隆雄, 梶原 建熈, 野木村 昭平, 伊藤 忠弘.結腸間膜および胃に血行性転移をきたした肝細胞癌の二期的切除例.日本消化器外科学会雑誌.1984;17(7);1456–1459.
- 20) 増田 信二.リンパ節類上皮血管内皮腫の1例.病院病理.2000;17(1):40.
- 21) Komatsu Y, Koizumi T, Yasuo M, Urushihata K, Yamamoto H, Hanaoka M, et al. Malignant hepatic epithelioid hemangioendothelioma with rapid progression and fatal outcome. Intern Med. 2010;49(12):1149–1153.
- 22) Lerut JP, Orlando G, Adam R, Schiavo M, Klempnauer J, Mirza D, et al. The place of liver transplantation in the treatment of hepatic epitheloid hemangioendothelioma: report of the European liver transplant registry. Ann Surg. 2007;246(6):949–957.