2015 年 48 巻 2 号 p. 126-131
2015 年 48 巻 2 号 p. 126-131
症例は63歳の男性で,急性心筋梗塞(3枝病変)で冠動脈バイパス術(coronary artery bypass grafting;以下,CABGと略記)の既往がある.術後経過観察中に上腹部不快感と灰白色便および閉塞性黄疸を認め,精査にて中部胆管癌と診断された.経皮経肝胆道ドレナージを行い,減黄したのち膵頭十二指腸切除術を施行した.バイパス血管が右胃大網動脈(right gastroepiploic artery;以下,RGEAと略記)だったため,術前に経皮的冠動脈形成術(percutaneous coronary intervention;以下,PCIと略記)を行った.手術では同動脈を温存しIV型再建とした.病理組織学的検査所見は中~低分化型管状腺癌でpT2N0M0,stage IIIBであった.術後経過は良好で術後第7病日より経口摂取を開始し,著明な合併症もなく第32病日に退院となった.RGEAを用いたCABG後の上腹部手術は胃癌での報告例が散見されるが胆道悪性腫瘍ではまれである.安全性も高く,根治性を損なわない手術を遂行するために,術前に心機能を厳密に評価し,本症例のように手術に先立ってPCIを行うことが重要であると思われる.
近年冠動脈バイパス術(coronary artery bypass grafting;以下,CABGと略記)において動脈グラフトが頻用されているが,その長期開存性から右胃大網動脈(right gastroepiploic artery;以下,RGEAと略記)も多く使用されている1).その際に問題となるのがCABG後に上腹部疾患に罹患し手術を要するものである.今回,我々はCABG後の胆管癌に対し,RGEAを温存しつつ膵頭十二指腸切除術が可能であった症例を経験したので報告する.
症例:63歳,男性
主訴:上腹部不快感,灰白色便
既往歴:30歳より糖尿病でインスリン治療中であった.62歳時に心筋梗塞でCABGを施行した.グラフトは左内胸動脈,RGEA,大伏在静脈を使用した.なおRGEAは左回旋枝(left circumflex coronary artery;以下,LCXと略記)の後側壁枝に吻合した.
家族歴:特記すべきことなし.
現病歴:上記既往で当院内科通院中であった.20XX年3月頃より上記主訴を自覚するようになった.血液検査で肝胆道系酵素の上昇と黄疸を指摘され精査加療目的に入院となった.
入院時現症:身長153 cm,体重46 kg.眼球結膜は黄染し眼瞼結膜は蒼白であった.胸腹部に皮膚黄染を認めたものの,聴打診上明らかな異常を認めなかった.また,表在リンパ節も触知しなかった.
血液生化学所見:ヘモグロビンが11.1 g/dlと軽度低下していた.生化学では肝胆道系酵素の上昇を認めた.また,CA19-9が279.5 U/mlと異常高値を示していた.
腹部造影CT所見:総胆管および肝内胆管の拡張を認めた.中部~下部胆管にやや造影効果に乏しい充実性部分を認め,同部を閉塞機転と判断した.肝門部や傍大動脈リンパ節に有意な腫大はなく腹水も見られなかった(Fig. 1).
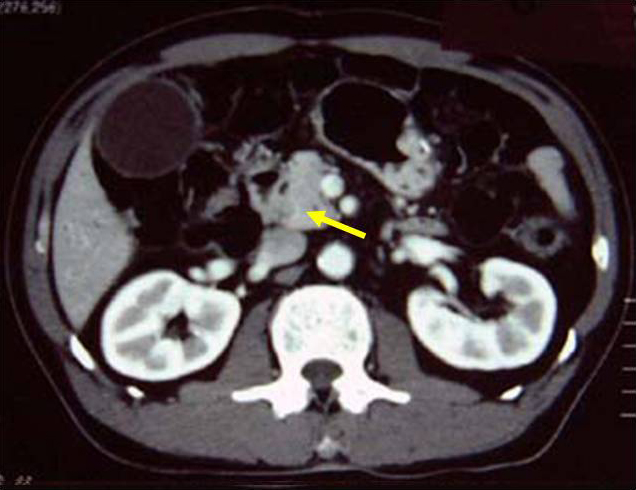
Abdominal CT: Abdominal CT shows dilatation from the CBD to the IHBD, and reveals a solid tumor of the middle CBD (arrow). CBD: common bile duct, IHBD: intrahepatic bile duct
経皮経肝胆道造影検査所見:総胆管および肝内胆管の著明な拡張を認めた.中部~下部胆管は不整に途絶していた(Fig. 2).

PTC: PTC shows remarkable dilatation of the upper CBD and occlusion with irregular taper of the middle lower CBD (arrows).
経肝的胆道内視鏡検査所見:中部胆管レベルに不整な顆粒状の発赤を認め,同部からの生検で高分化腺癌を認めた.
血管造影検査所見:冠動脈造影で右冠動脈起始部(#1)に90%の狭窄を認めた.腹腔動脈造影で総肝動脈は腹腔動脈より分岐し,総肝動脈から胃十二指腸動脈(以下,GDAと略記)の分岐が見られた.RGEAはGDAから分岐しておりそこからLCXへの血流を確認した.明らかな腫瘍濃染やencasementは認めなかった.手術予定のため経皮的冠動脈形成術(percutaneous coronary intervention;以下,PCIと略記)を施行し,50%の開存を得た(Fig. 3a~c).また,PCI以前の左室駆出率が50%とバイパス術後としては比較的良好であり,循環器内科の評価もふまえ50%の開存で耐術可能と判断した.
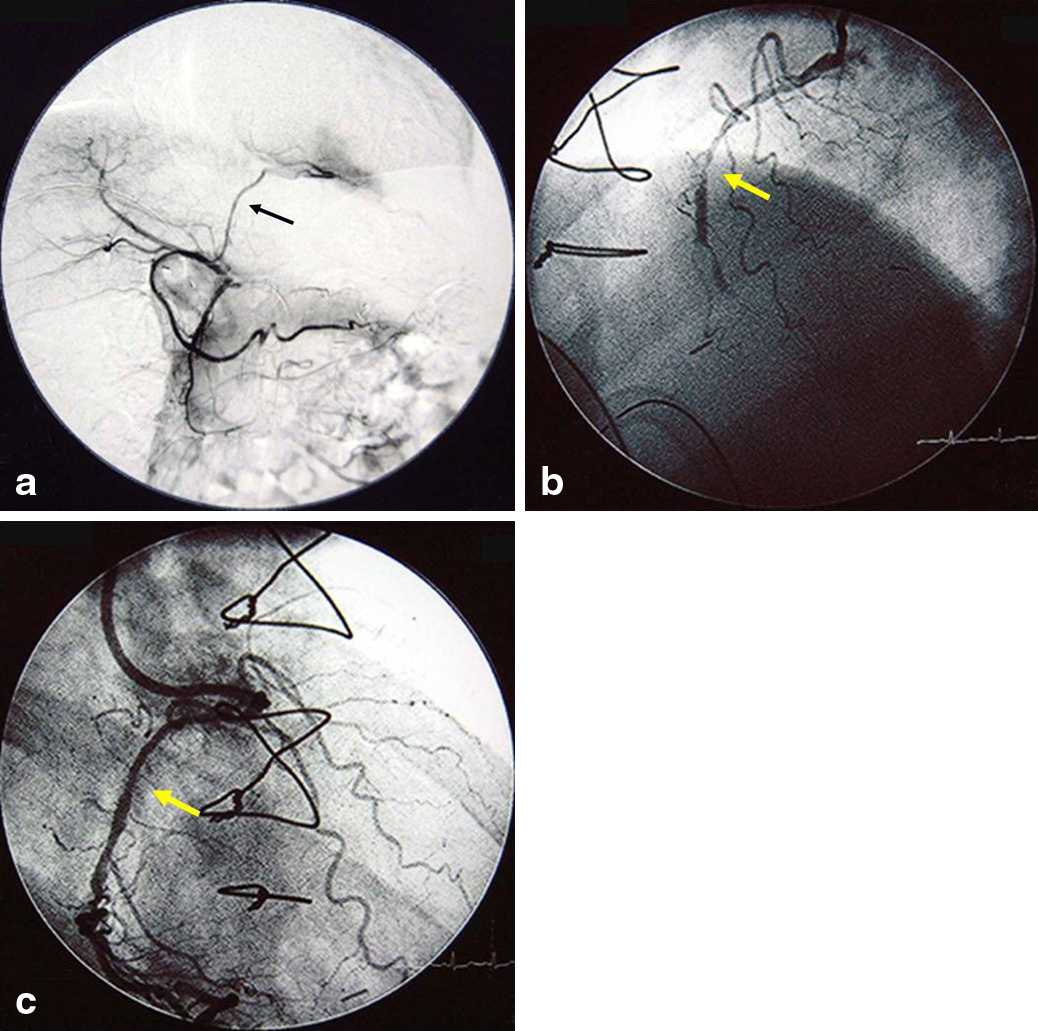
a: Celiac angiography: There was no variation up to the divergence of the artery. The common hepatic artery diverged from theceliac artery, and RGEA diverged from the gastroduodenal artery. Celiac angiography showed the blood flow from RGEA to LCX (arrow). No obvious tumor stain or encasement was seen. RGEA: right gastroepiploic artery, LCX: left circumflex coronary artery. b: CAG, prePCI: CAG shows 90% stenosis at #1 segment of the right coronary artery (arrow). CAG: coronary angiography, PCI: percutaneous coronary intervention. c: CAG, post PCI: PCI was performed successfully and the coronary artery shows 50% patency (arrow).
以上より,胆管癌の診断のもと,経皮経肝胆道ドレナージで減黄した後に膵頭十二指腸切除を行う方針とした.術前のPCIで冠血流は確保されていると判断していたが,術中モニタリングをしつつ可能であればRGEAを温存することとした.
手術所見:右季肋下切開に上腹部正中切開を追加する形で開腹した.癒着はほとんど見られず,RGEAはskeltonizeされた状態で胃幽門腹側から肝鎌状靭帯左縁を通り胸腔内へ続いていた(Fig. 4a).手術に先立って冠血流低下が起きないかRGEAをブルドッグ鉗子で遮断し,15分間の血流遮断で心電図モニター上虚血性変化は見られなかったので,切離による心機能への深刻な影響は少ないと判断したが,不測の事態を考慮し,RGEAを温存しつつ,可及的に根治性を求められると考える術式を行った.グラフトはCABGの際にskeltonizeされており所属リンパ節No. 6の有意な腫大は見られなかった.まずコッヘルの受動を行い膵頭部の剥離脱転を行ったのちに小網を切開し,膵上縁の郭清を行った.左胃動脈周囲#7から8および12リンパ節への郭清をしつつ膵上縁で門脈に流入する左胃静脈を結紮切離した.その後膵下縁にて上腸間膜静脈を同定し,#14リンパ節の郭清をしつつ同静脈の腹側から膵背側の剥離をすすめ膵臓のトンネリングを行った.膵頭十二指腸切除可能と判断したのち,胃十二指腸動脈からRGEAグラフトへの分岐をあらわにするために幽門輪の肛門側で胃と十二指腸を観音開きをするように離断した.十分に視野を確保して総肝動脈から連続する上十二指腸動脈を膵臓より剥離し,同動脈よりRGEAをもとめつつ,途中で分岐した後および前上膵十二指腸動脈をおのおの結紮切離した.グラフト温存を確実にしたのちは型のごとく膵頭十二指腸切除を行い,胃の切離は幽門側2分の1とした.再建は口側より端側膵胃吻合,残胃空腸端端吻合,胆管空腸吻合とするIV型再建を行った(Fig. 4b).手術時間は5時間50分,出血量は430 gであった.

a: Surgical findings: The RGEA graft was detected easily at the left side of the falciform ligament and hanged up caringly with vessel string. The RGEA graft was preserved with no injury and the GDA was cut off at the peripheral side separating from the graft. GDA: gastroduodenal artery. b: Surgical findings: PD was performed successfully with type IV reconstruction, pancreatogastrostomy.
切除標本および病理組織学的検査所見:肉眼所見では中下部胆管に壁肥厚と狭窄を認めた.組織学的には中分化から低分化の腺管形成に乏しい大小不同の腫瘍細胞が見られ一部神経周囲への浸潤が見られた.病理組織学的検査所見はBd,nodular-infiltrating type,circ,18×10 mm,tub2>por,pT2(SS),int,INFb,ly+,v+,ne+,pN0,pDM0,pHM0,pEM0,pPV0,pA0,R0でありT2N0M0,Stage IIIBであった(Fig. 5).
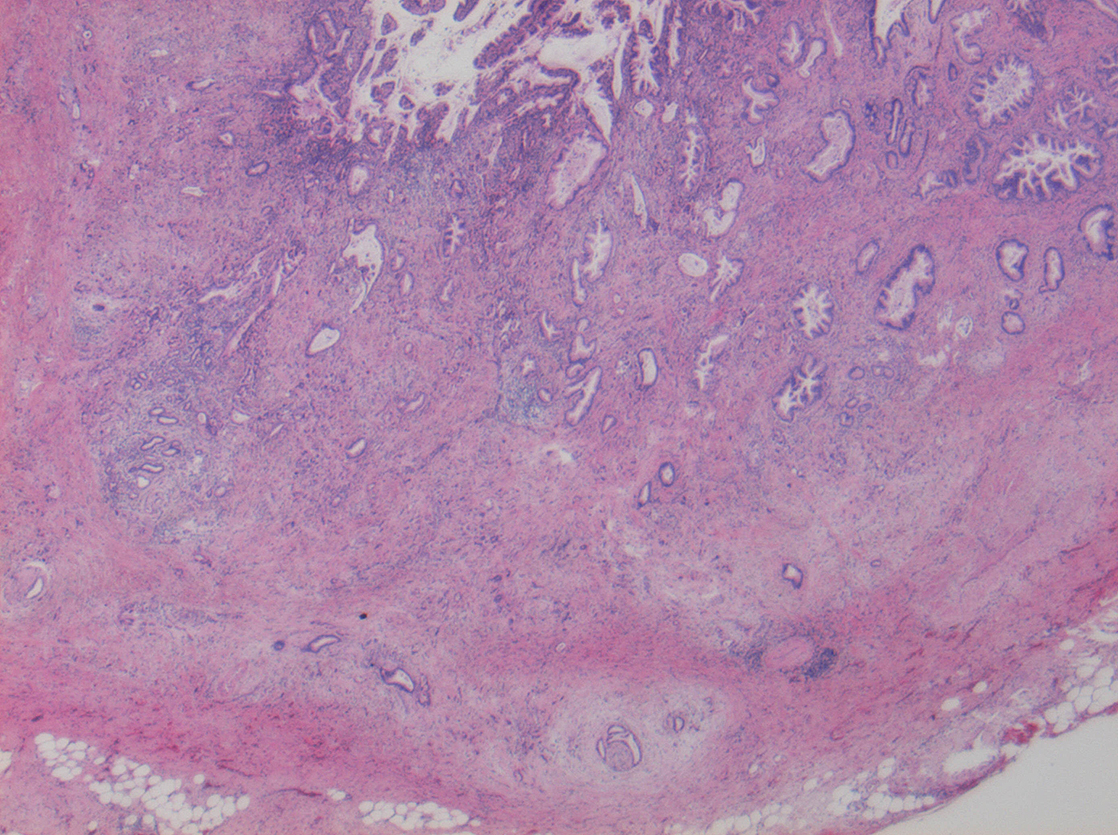
Microscopic findings: Microscopic findings show tumor cells invading into interstitial tissue with moderate or poor differentiation.
術後経過:術後7病日より経口摂取を開始した.術後に軽度の膵液漏を認めたが保存的に改善し32病日で退院となった.退院後は外来で経過観察していたが,13か月目に肺転移を認め治療の甲斐なく17か月目に永眠した.
CABGにおいて近年,その良好な長期開存性からRGEAは左右内胸動脈に次いで積極的に用いられるようになってきた1).それに伴いCABG術後の上腹部疾患への罹患,特に胃癌や食道癌といった手術を必要とする疾患に対する治療が問題となるが,集約すればグラフト使用による解剖の変異と周術期の冠血流保護であると考える.自験例と同様の膵頭十二指腸切除の報告例について,1983年から2014年3月までの医学中央雑誌で「冠動脈バイパス術後」,「右胃大網動脈」,「膵頭十二指腸切除」をキーワードとして検索(会議録を除く)すると自験例を除いて4例と非常に少ない2)~5).
一般的にCABGで使用されるRGEAグラフトは,in situ graftとして用いられることが多く,胃腹側を通り肝左葉腹側を経由して横隔膜を貫き胸腔内に至る2)6).症例によっては強固に癒着している可能性もあり,位置関係を十分に把握しておくことで開腹の際のグラフト損傷を回避することができるためバイパス術の際の詳細な情報の把握は不可欠である.また,動脈グラフトは剥離の際にも機械的刺激や低温などにより容易にスパスムを起こすため,癒着剥離や後述するグラフト周囲のリンパ節郭清を要する際には慎重で愛護的な操作が要求される7).RGEA流域のNo. 4および6リンパ節は胃癌のみならず膵,胆道系悪性腫瘍の所属リンパ節で,リンパ流は通常RGEA末梢から胃十二指腸動脈へ向かうが,CABGでskeltonizeされたRGEAはそのリンパ流もグラフト作成時に遮断されているため同部位へのリンパ節転移は少ないと考えられている8)~11).自験例では術前のPCIで十分に冠血流確保は行われておりまた術中のグラフト遮断でも冠血流低下を認めなかったのでRGEA処理も可能ではあったが,グラフトがすでにskeltonizeされ腫大したリンパ節も認めなかったため,グラフトを処理せずに郭清を行いえた.一方で進行胃癌において転移を認めたという報告もあり,根治性を追求する上でRGEAの根部処理についてはその必要性を認めつつも冠血流の低下を招く危険を否定できず議論の余地の残るところである12).城田ら8)のように症例により根治性を高めるためにRGEAを根部処理し,必要ならば再バイパス手術を行うという報告もある.しかしながら安全性の担保が不十分といわざるをえず,諸家の報告のとおり術前のPCIや再CABGなどにより,十分に偶発症に備え冠血流を確保することで膵頭十二指腸切除をはじめとする高難度手術にも対応できると考える7)13).
利益相反:なし