2015 年 48 巻 2 号 p. 111-117
2015 年 48 巻 2 号 p. 111-117
右房内進展を伴う肝細胞癌の切除は人工心肺下での開心術を要し,肝切除のみに比べ侵襲が高い.我々は右房内へ進展した肝細胞癌に対し肝切除先行total hepatic vascular exclusion(全肝血行遮断;以下,THVEと略記)を達成,開心術をせず原発巣と右房内腫瘍栓を摘出しえた症例を経験した.本術式は心房内進展を伴う進行肝細胞癌に対し,開心術併用と比較し低侵襲術式になると思われた.症例は69歳男性で,検診で異常を指摘された.CT で肝右葉に右房内に進展する腫瘍を認め当院紹介となり,肝細胞癌の診断で手術を行った.術式は肝脱転,肝静脈根部剥離,右グリソン処理の後肝切離を行い,肝右葉が右肝静脈のみで繋がる状態とした.肝右葉の牽引により腫瘍栓が右房外に出ることをエコーで確認し,THVEの後に右肝静脈根部を切開,腫瘍栓と肝右葉を一括で摘出した.術後74日目に退院した.術後2年間,無再発生存中である.
肝細胞癌は進行すると脈管内に浸潤する傾向があり,肝静脈から下大静脈を経て右房内に腫瘍栓を形成することも少なくない.その多くは肺など他臓器へ転移を来し予後不良であり1),また肺動脈塞栓により突然死することもある2).治療は手術による原発巣切除・右房腫瘍栓摘出であるが,total hepatic vascular exclusion(全肝血行遮断;以下,THVEと略記)や人工心肺下開心術を要することもある高侵襲手技である.我々は肝切除先行THVEにより開心術を要することなく切除可能であった症例を経験したため,今回報告する.
患者:69歳,男性
主訴:自覚症状なし.
現病歴:高血圧,糖尿病で近医通院中であった.2011年10月,胸部レントゲンで異常を指摘され精査目的にCTを撮影された.肺野に異常はなかったが,肝右葉に腫瘤性病変を認め当院紹介となった.
既往歴:高血圧,糖尿病
家族歴:父親が胃癌で死去
初診時身体所見:身長162.0 cm,体重59.0 kg,血圧118/72 mmHg,脈拍88回/分整,体温36.4°C.眼球結膜に黄疸,貧血なし.腹部平坦軟で圧痛なし,肝脾腫なし,腫瘤触知せず.頸部から腹部,鼠径部まで体表リンパ節腫脹なし.
血液検査所見:血液検査は正常であった.生化学検査は,総ビリルビン0.7 mg/dlと正常だが,AST 107 IU/l,ALP 500 IU/l,LDH 710 IU/l,γ-GTP 410 IU/lと肝機能に若干の上昇を認めた.腫瘍マーカーではAFP 17,408 ng/ml,PIVKA-II 140,690 mAU/mlと著明な上昇を認めた.肝炎ウイルスは陰性であり,凝固異常も見られなかった.Child-Pugh分類A(5点),肝障害度A,ICG15分値は6.0%であった.
胸部単純X線撮影所見:右横隔膜の拳上を認めた(Fig. 1).
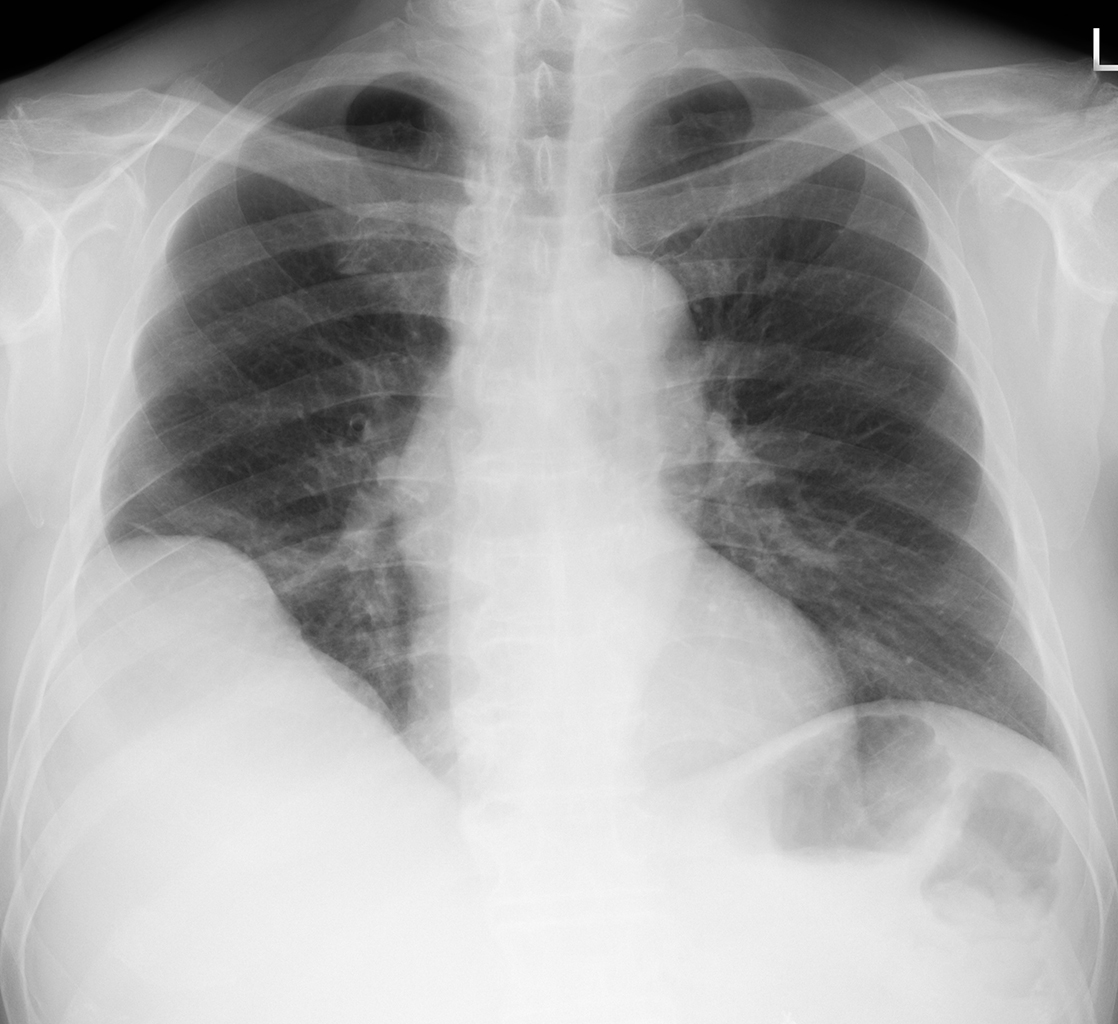
Chest X-ray showing elevation of the right diaphragm.
経胸壁心臓超音波検査所見:壁運動異常や収縮拡張能の異常,弁膜症所見は見られなかった.右房内に腫瘍栓と思われる索状構造を認めた.
胸腹部造影CT所見:肝右葉後区域を中心に腫瘍を認め,これに連続した下大静脈腫瘍栓が見られた(Fig. 2矢印).腫瘍栓は右心房内に約2~3 cm進展していた(Fig. 2矢頭).腹水,腹膜播種や他臓器転移は認めなかった.

Abdominal CT showing the tumor in the right lobe of the liver and tumor emboli in the inferior vena cava (a, b, arrow). Tumor emboli progress to the right atrium (c, arrowhead). No evidence of peritoneal or other organ metastases is seen.
以上より,術前診断T3N0M0 Stage IIIの肝細胞癌と診断した.腫瘍は右房内腫瘍栓を形成していたが他臓器転移などなく,一括切除可能と判断した.肝右葉切除およびTHVE下での右房内腫瘍栓摘出術を予定したが,術中に人工心肺下循環下開心術を要する可能性もあり,心臓外科医と合同で手術を行った.
手術所見:開腹し腹水,腹膜播種,他臓器転移はいずれも認めなかった.肝両葉を左右から脱転後,下大静脈前面の短肝静脈を全て処理して肝背側の下大静脈を露出し,下大静脈と横隔膜の間を剥離し下横隔膜静脈も処理して,右肝静脈根部,中+左肝静脈根部および肝静脈根部直下の下大静脈をテーピングした.次いで右グリソンを一括処理しPringle法で肝実質を切離して,肝右葉が右肝静脈のみで繋がる状態にした.さらに,肝静脈流入部より下流の肝背側下大静脈を全周性に剥離・血管処理(de-vascularization)することで,THVE中に肝静脈を切開する際の下大静脈からの出血を防止した.血圧維持のため右大腿静脈と左鎖骨静脈間に補助循環バイパスを置き,胸骨下縁の横隔膜付着部を横に切開・開放し心囊も切開して胸部下大静脈右房流入部をテーピングした.ここで右肝静脈を術者左手に触診しつつ肝右葉を尾側に牽引すると,右房内腫瘍栓が下大静脈内に引き込まれることが術中超音波で確認できたため,THVEが心房外の胸部下大静脈クランプで達成可能と判断した.左グリソン鞘,肝静脈流入部より下流の肝背側下大静脈,中+左肝静脈,下大静脈右房流入部をクランプしてTHVEとし,右肝静脈根部を約2 cm切開して腫瘍栓を引き出し肝右葉とともに摘出した(Fig. 3).下大静脈切開部は縫合閉鎖した.THVE時間は30分であった.THVE終了時の出血量は1,200 g,手術時間は6時間22分であった.

Operative procedure for liver resection-preceding total hepatic vascular exclusion.
摘出標本肉眼所見:肝右葉に多結節融合型を呈する境界明瞭な腫瘍を認めた.明らかな被膜はないが,腫瘍内部には隔壁が見られた.腫瘍は肝静脈へ浸潤し右房内腫瘍栓まで連続していた(Fig. 4).
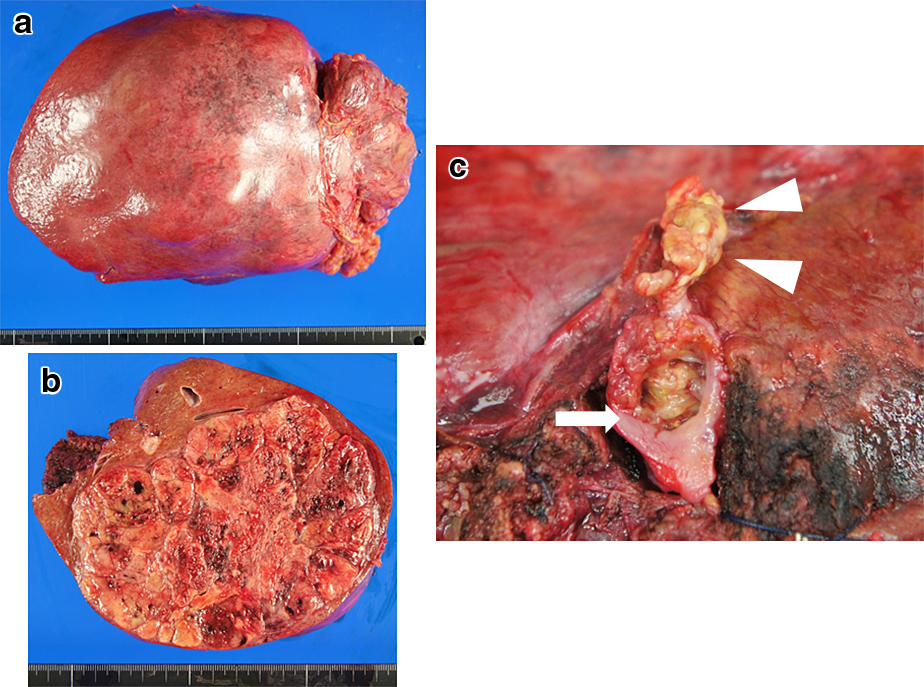
Resected specimen. A large, confluent, multinodular-type tumor is apparent in the right lobe of the liver (a, b). The tumor has infiltrated the right liver vein (c, arrow) and continued to the right atrium (c, arrowheads).
病理組織学的検査所見:組織検査では核異型の乏しい腫瘍細胞が不規則な索状構造を呈しており,高分化型肝細胞癌と診断した(Fig. 5).最終診断はH3,St-PAM,17 cm,Eg,Fc(–),Sf(+),S1,N0,Vp0,Vv3,Va0,B0,P0,SM(+:腫瘍栓部),T3N0M0,Stage IIIであった.
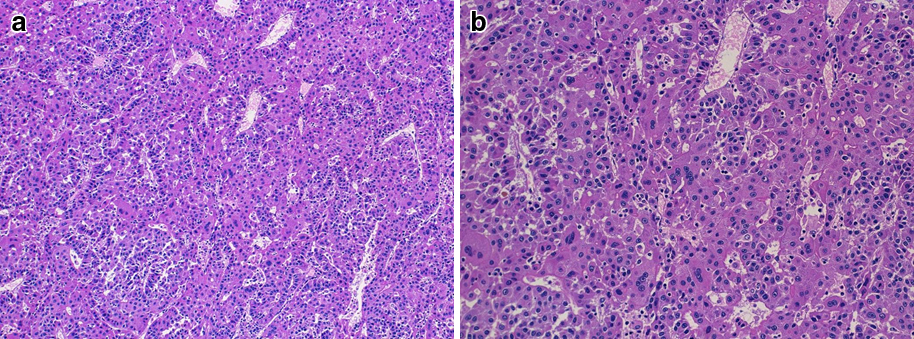
Microscopic examination of the tumor, showing an irregular trabecular structure consisting of tumor cells (a, HE staining ×40). Tumor cells show mild cytopenia, so well-differentiated hepatocellular carcinoma was diagnosed (b, HE staining ×100).
術後,一過性に高ビリルビン血症を来したが改善し,術後74日目に退院した.現在術後約2年目で無再発生存中である.
現在,肝細胞癌の治療はガイドラインが確立し,非手術療法でも良好な結果が得られている.だが肝細胞癌は進行すると門脈や下大静脈に浸潤する傾向があり,特に下大静脈から右房へ進展し右房内腫瘍栓を形成すると予後は悪くなり1),また腫瘍による肺動脈塞栓から突然死を起こす危険性もある2).このような症例では根治的肝切除および腫瘍栓摘出術が望ましいが,肝硬変による肝機能障害で切除適応外である,肺など他臓器転移を既に発症しているなど手術適応となる症例は少ない.このような症例に対してフルオロウラシル,シスプラチンやその他の化学療法,肝動注療法により2年以上の生存を得られた報告や3)4),化学療法に腫瘍栓摘出術を併せて行った報告が散見される4)~6).しかし,腫瘍栓摘出術のみでは突然死のリスクを一時的に軽減するものの,原発巣が進行するため生命予後自体は改善せず,化学療法奏効例においてもviableな病変が残存していた場合は再発を来すことから4)5),現状ではこれらの治療は肝切除および腫瘍栓摘出術に代わる根治療法にはなりえない.
右房内腫瘍栓を伴う肝細胞癌に対する肝切除および腫瘍栓摘出術は,本邦ではOnitsuka ら7)が初めて報告し,その後尾関ら8)9)やFujisakiら10),Nimuraら11),杉本ら12)などが続いている.医学中央雑誌で1983年から2013年3月までの期間で同様の症例を検索すると,「肝細胞癌」と「右房内腫瘍栓」をキーワードとした検索(会議録除く)で7例,また「肝細胞癌」と「心房内腫瘍栓」のキーワードで6例の症例報告を認めるのみであった.その中でも根治切除が可能であったものは6例,人工心肺を用いずに手術したのは尾関ら8)9),佐野ら13),京兼ら14)の報告のみとさらに少なかった.
人工心肺下開心術に関して,尾関ら8)9)は抗凝固薬使用による肝切離面からの出血量増加や腫瘍細胞の血行性散布を主な問題として挙げている.それに加え脳梗塞などの術後合併症発生リスクも高く,人工心肺および開心術の施行は慎重に判断する必要がある.
我々の手術も人工心肺を準備して行ったが,胸部下大静脈クランプによるTHVEのみで腫瘍栓の摘出が可能であった.術式上の工夫として肝両葉脱転,グリソン処理,そして肝切離を先行し摘出肝が肝静脈のみで繋がっている状態とすることで,肝臓を確実に尾側へ牽引し腫瘍栓を下大静脈側へ引き出せるようにした.我々の経験上,下大静脈内へ浸潤した肝細胞癌であっても十分な牽引によって腫瘍栓を引き出せることが多いが,牽引に際しては血管を損傷しないよう留意が必要である.さらに,腹腔内下大静脈クランプ部を肝静脈流入部付近として,肝静脈流入部からクランプ部までの下大静脈周囲のde-vascularizationを行った.これにより,THVE中に肝静脈を切開し腫瘍栓を引き抜く操作での出血を抑えることが可能となった.このように本法は開心術の前にまず試みる価値があるが,病変が三尖弁に達している症例では,肝授動操作の際に腫瘍栓による三尖弁閉鎖の危険があるため施行できない13).また,腫瘍栓の形状がくびれている場合,肝切除を先行することで腫瘍栓が逸脱し肺動脈塞栓を起こす可能性があり12)15)本術式はやはり適応外である.そのような症例では,腹腔内操作の前に人工心肺下の腫瘍栓摘出が必要である.
また,胸部下大静脈へのアプローチ法も複数の方法が報告されており,最も多いのは胸骨正中切開し心囊切開する方法であった16)~18).胸骨正中切開は視野が良好であり,開心術を要する症例に適していると思われるが,欠点として術後疼痛が強いことが挙げられる.その他,右開胸開腹から横隔膜切開を加える報告19),そして我々と同様に胸骨付着部で横隔膜を切開・開放し心囊切開をする報告20)が見られた.それぞれの手技の優劣に言及したものはなかったが,術前から人工心肺下開心術が予想される症例では胸骨正中切開を,本例のように右房内進展が比較的軽度で,THVEのみで手術を完遂できそうな症例では腹腔側からの横隔膜切開と心囊切開が良いのではないかと思われた.
Nimuraら11),佐野ら13)の報告はほぼ同様の手技だが,体外循環を置いていない点と,THVE時の下大静脈クランプを肝下部で行っている点が我々とは異なり,また数例で術中に血圧低下を認め補液と数回のテストクランプを要していた.我々は今回右大腿静脈-左鎖骨下静脈にバイパスを補助として置き,THVE中の血圧低下を予防した.補助循環中はヘパリンを使用したが,肝切離面からの出血量増加はなく,安全のための補助循環は問題ないと思われた.
右房進展を伴う肝細胞癌の予後は不良であるが,治癒切除により長期生存が期待できる.その際,本術式は開心術を併用した手術よりも侵襲が低く,検討する価値があると思われた.
利益相反:なし