2019 年 52 巻 9 号 p. 485-493
2019 年 52 巻 9 号 p. 485-493
目的:術前CT解析における予定残膵/脾臓CT値比(以下,予定残膵P/S比と略記)が膵体尾部切除術(distal pancreatectomy;以下,DPと略記)後の膵液漏(pancreatic fistula;以下,PFと略記)発生を予測しうるかどうかを検討する.方法:2007~2017年に当科でDPを施行した52症例について,術前因子を年齢,性別,術前アルブミン値,prognostic nutritional index(PNI),糖尿病の有無,body mass index(BMI)に加えて,術前CT画像で測定した,内臓脂肪面積,皮下脂肪面積,腹部縦径,切離線における膵臓の厚さ,予定残膵におけるCT値(以下,予定残膵CT値と略記),予定残膵P/S比とし,術中因子を出血量,手術時間,術中輸血の有無,膵断端の処理法と定義し,術後のPFの発生(Clavien-Dindo分類II度以上)にかかわる因子について後方視的に検討した.結果:術後PFの発生は52例中14例(26.9%)に認め,術後在院日数中央値は19日(9~71日)であった.単変量解析では,PFの発生は,年齢が低い(P=0.006),残膵CT値が高値(P=0.0313),予定残膵P/S比が高値(P=0.0187)において有意に多かった.病理学的な検討でも,切除断端における膵臓の脂肪化と,残膵CT値および予定残膵P/S比には有意な関連がみられた.結語:予定残膵P/S比の測定は,DP後のPF発生を予測しうる可能性がある.
Purpose: To investigate whether the ratio of the CT value in future pancreas remnant to spleen (remnant P/S ratio) can predict the occurrence of postoperative pancreatic fistula (POPF) after distal pancreatectomy (DP). Materials and Methods: Our study is a retrospective study. We selected 52 patients who underwent DP between 2007 and 2017 in our hospital. We examined the relationship between preoperative factors (age, gender, preoperative albumin score, prognostic nutritional index (PNI), visceral fat area, subcutaneous fat area, thickness of pancreas, CT value of future pancreas remnant, and P/S ratio), intraoperative factors (blood loss, operative time, blood transfusion, the way of pancreatic stump closure) and occurrence of POPF by using statistical method. We defined POPF if severity was Grade 2 or higher according to the Clavien-Dindo classification. CT value in both future pancreas remnant and spleen parenchyma was measured using unenhanced CT. We selected 5 points (not overlapping nearby vessels and other organs) and measured CT value, and calculated the median score for each organ. Result: POPF after DP occurred in 14 cases (26.9%) and median postoperative hospital stay was 19 days. In univariate analysis, younger age (P=0.006), high CT value of future pancreas remnant (P=0.0313), and high P/S ratio (P=0.0187) showed a significant relationship with the occurrence of POPF. In histopathological examination, the grade of degenerative fatty change in pancreatic cut margin and CT value of future pancreas remnant and P/S ratio revealed a significant relationship. Conclusion: Measurement of CT value ratio of future pancreas remnant and P/S ratio may predict the occurrence of POPF after DP.
膵体尾部切除術(distal pancreatectomy;以下,DPと略記)は,同じ膵切除術式である膵頭十二指腸切除術(pancreaticoduodenectomy;以下,PDと略記)に比べると再建を必要としないため,手術時間や出血量も比較的少ない.しかしながら,膵液漏(pancreatic fistula;以下,PFと略記)の発生は30%前後といわれており1)2),重症化すれば術後出血の原因となり致命的になりうる合併症である.
膵切除におけるPFの発生は膵液産生能が高い膵臓,つまり膵外分泌能が高い膵臓ほどリスクが高いであろうことは予想できるが,定量的に表すことは困難である.膵外分泌能を評価する方法としてpancreatic function diagnostant(以下,PFDと略記)試験,呼気試験,糞便中脂肪測定などがあるが,現時点で保険適応があるのはPFD試験のみである3).しかし,同試験は内服薬の休薬や長時間の蓄尿など患者に強いる負担があり,簡易な評価法とは必ずしもいえない.
近年はCT画像解析の進歩が著しく,術前のCT画像を解析することにより患者の肥満度のみならず,切除臓器である膵臓の厚さやCT値を測定できるようになった.Kawaiら4)は膵切離線における膵臓の厚さが12 mm以上の場合には,膵断端をstaplerで処理した場合のPFのリスクが高くなる,という報告をしており,CTで測定できる因子によりPFの発生を予測しうる可能性があると推測される.
自施設においてDPを行った52症例について,術前の患者背景および術中因子に,CT画像で測定可能な因子を加え,PF発生にかかわるリスク因子を明らかにすることを目的とした.
2007~2017年の11年間で当科において膵疾患に対して開腹DPを行った52症例を対象とした.対象症例からは胆囊および左副腎以外の臓器の合併切除もしくは血管合併切除を要した拡大切除症例は除外した.また,膵切離線が門脈前面である症例を対象とし,切離線がPV右縁を超え,膵断端の処理が困難となるような症例や,PV左縁よりも尾側で膵切離を行った症例は,PV直上に比べて膵臓の厚さが増すことに加え,手術手順や剥離範囲が異なることが多いため,対象より除外した.
2. 評価方法本検討では術後在院日数に影響を与える可能性がある,Clavien-Dindo分類II度以上のPFを本検討における「PFあり」と定義した.
術前因子は,年齢,性別,術前Alb値,術前糖尿病の有無,prognostic nutritional index(以下,PNIと略記),body mass index(以下,BMIと略記)に,術前CT画像で測定した内臓脂肪面積(visceral fat area;以下,VFAと略記),皮下脂肪面積(subcutaneous fat area;以下,SFAと略記),腹部縦径に,切離線における膵臓の厚さ,予定残膵におけるCT値(以下,予定残膵CT値と略記),予定残膵/脾臓CT値比(以下,予定残膵P/S比と略記)を加えた.
PNIは小野寺の予後栄養指数:PNI=(10×Alb)+(0.005×総リンパ球数)を用いて算出した.VFA,SFA,腹部縦径はCT画像における臍のスライスの高さにおいて,VFAとSFAはSynapse VINCENT®における脂肪解析を用いて測定し,BMIとともに患者の肥満度を表す指標とし,腹部縦径はCTのaxial画像で臍直下の腹壁下から脊椎前面までの直線距離を測定し,術野の深さを表す指標とした.膵臓の厚さは術前のCTにおけるaxial画像で手術記録に記載されている膵切離線において膵臓の長軸に対して垂直方向に測定した値を用いた.予定残膵CT値およびP/S比は,単純CTで予定残膵である膵頭部および脾臓においてそれぞれ脈管の重ならない部位かつ臓器の範囲内で測定した約100 mm2のregion of interest(ROI)を用いて5か所のCT値(平均値)を測定し,その中央値を採用し二つの値の比を算出した(Fig. 1A, B).
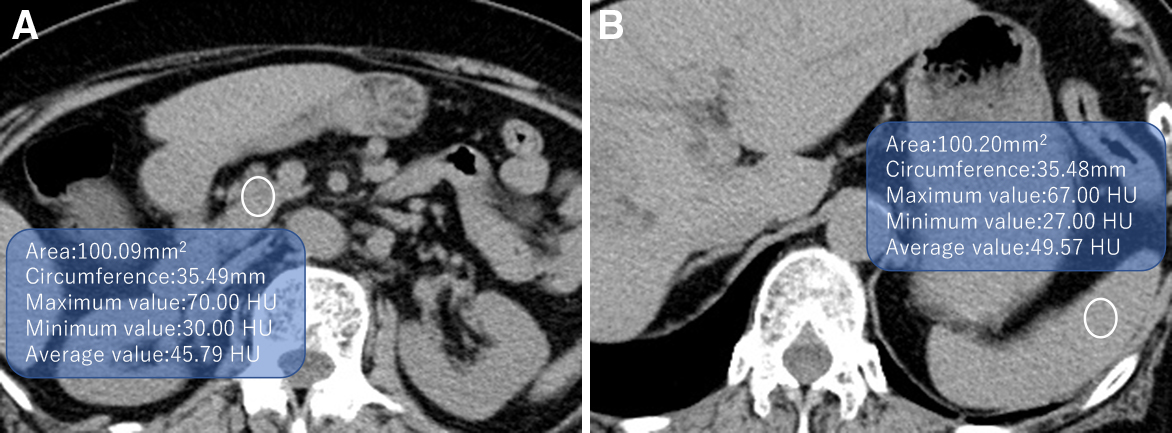
Measurement of CT value of remnant pancreas and spleen in plain CT (A: pancreas, B: spleen).
術中因子は術中の出血量(ml),手術時間(min),術中輸血の有無,膵断端の処理法とした.膵断端の処理法は,staplerと,hand sewnの2群に分類し,hand sewnについては膵切離線において主膵管の結紮に加え,膵実質の縫合閉鎖を行ったもの,と定義した.
また,残膵の性状をより強く反映していると思われる,術中に提出した膵断端の迅速組織診断標本,もしくは切除標本における膵断端を組織学的に評価した.本検討では脂肪化と線維化の程度をそれぞれ3群に分類し(Table 1, Fig. 2),実際の残膵CT値とP/S比との関連を調べた.
| Fatty degeneration | Fibrosis | |
|---|---|---|
| Grade 1 | There is little or no fatty change. | There is little or no fibrosis and each lobules are closely contact. |
| Grade 2 | Fatty change is mild. | Fibrosis is mild. |
| Grade 3 | Fatty change is high. The distance between each lobules is large. |
Strong fibrosis is seen. The distance between each lobules is large, or the structure of lobules was destroyed. |

Histological findings on classification for fatty degeneration and fibrosis grade at the pancreatic stump.
また,Eckerら5)は,2,026例のDP症例を解析し,膵内分泌腫瘍(pancreatic neuroendocrine tumor;以下,PNETと略記)およびnon-malignantをhigh risk,膵癌,膵囊胞性腫瘍,転移性膵腫瘍をlow riskに分類し,病理所見をPFの有意なリスク因子として報告しており,本検討でもリスク因子に加えることとした.
3. 統計学的手法単変量解析:術前および術中因子における名義変数とPF発生については,カイ2乗検定を用い,さらにセルの期待値が5以下となりうる症例については,Fisherの直接確率算出法を用いた.また,連続変数とPF発生についてはt検定(両側検定)を用い,病理学的な所見とCT値についての3群間の比較は,ノンパラメトリック法であるKruskal-Wallisの順位和検定を用いた.いずれもP値が0.05未満を有意差あり,と定義した.
患者背景をTable 2に示す.52例における術前診断の内訳は,膵癌が34例(65%),膵IPMNが7例(13%),膵MCNが4例(7%),PNETが3例(5%),その他の膵腫瘍が4例(7%)であった.出血量中央値は275 ml(31~1,877 ml),手術時間中央値は282分(155~720分)であった.II度以上のPFを14例(26%)に認めたが,再手術を要するIIIb以上のPFは認めず,手術関連死亡もなかった.術後在院日数中央値は19日(9~71日)であった.
| Variables | Value |
|---|---|
| Age, mean (±SD) | 68.5 (±11.9) |
| Gender (Female/Male) | 26/26 |
| Diabetes | 16 (30%) |
| Serum albumin, g/dl, median | 4.2 (3.1–5.0) |
| PNI, median | 49.6 (36–64.5) |
| BMI, median | 22.8 (16.4–33.0) |
| VFA, mm2, median | 76.1 (5.0–365.7) |
| SFA, mm2, median | 110.4 (4.4–266.8) |
| Vertical diameter, mm, median | 67.8 (29.7–151.9) |
| Thickness of pancreas, mm, median | 10.8 (4.8–20.1) |
| CT value of remnant pancreas | 39.2 (−39.34–53.58) |
| Remnant P/S ratio, median | 0.84 (−1.11–1.43) |
| Blood loss, ml, median | 275 (31–1,891) |
| Operative time, min, median | 282 (155–720) |
| Blood transfusion | 3 (5.7%) |
| Pancreatic stump closure (hand sewn/stapler) | 34 (65.3%)/18 (34.6%) |
| Pancreatic fistula (≥Grade II) | 14 (26.9%) |
| Postoperative hospital stay, median, days | 19 (9–71) |
PNI: prognostic nutritional index, BMI: body mass index, VFA: vesceral fat area, SFA: subcutaneus fat area
単変量解析の結果をTable 3に示す.年齢が低い(若い)症例(P=0.0060),残膵CT値が高い症例(P=0.0313),予定残膵P/S比が高い症例(P=0.0187)において,有意にPFが多いという結果であった.肥満度を表すBMI,VFAやSFA,術野の深さに関連すると思われる腹部の縦径,切離線における膵臓の厚みや術中の出血量や手術時間,膵断端の処理法は,今回の検討においてPFの発生を予測する因子としては抽出されなかった.
| Variables | PF(+) (n=14) | PF(−) (n=38) | P-value |
|---|---|---|---|
| Age, mean (±SD) | 61.2 (±12.2) | 73.5 (±10.8) | 0.0060 |
| Gender | 0.5312 | ||
| Female (% of PF) | 6 (23.0%) | 20 (76.9%) | |
| Male (% of PF) | 8 (30.7%) | 18 (69.2%) | |
| Diabetes Mellitus | 3 (21.4%) | 13 (34.2%) | 0.7253 |
| Serum albumin, g/dl, median (range) | 4.2 (3.3–5.0) | 4.2 (3.1–4.7) | 0.1995 |
| PNI, median (range) | 49.6 (38–64.5) | 49.7 (36–56.5) | 0.1347 |
| BMI, median (range) | 23.0 (18.7–28.5) | 22.7 (16.4–33.0) | 0.7216 |
| VFA, mm2, median (range) | 75.8 (5.0–224.2) | 76.1 (9.2–365.79) | 0.8130 |
| SFA, mm2, median (range) | 113.9 (4.4–242.7) | 109.0 (27.0–266.8) | 0.7883 |
| Vertical diameter, mm, median (range) | 64.9 (50.3–115) | 69.8 (29.7–151.9) | 0.7926 |
| Thickness of pancreas, mm, median (range) | 11.6 (6.2–14.4) | 10.7 (4.8–20.1) | 0.8114 |
| CT value of remnant pancreas, median (range) | 44.0 (32.6–51.4) | 36.8 (−39.3–53.5) | 0.0313 |
| Remnant P/S ratio, median (range) | 1.00 (0.69–1.20) | 0.78 (−1.11–1.43) | 0.0187 |
| Blood loss, ml, median (range) | 194 (59–1,475) | 282 (31–1,891) | 0.6484 |
| Operative time, min, median (range) | 246 (165–470) | 296 (155–720) | 0.1768 |
| Blood transfusion | 0 (0%) | 3 (9%) | 0.5547 |
| Pancreatic stump closure | 0.1628 | ||
| hand sewn (% of PF) | 7 (20.5%) | 27 (79.4%) | |
| stapler (% of PF) | 7 (38.8%) | 11 (61.1%) | |
| Pathology | 0.6662 | ||
| High risk (neuroendocrine, non-malignant) | 3 (37.5%) | 5 (62.5%) | |
| Low risk (PDAC, cystic neoplasm, pancreatitis, metastatic tumor) | 11 (25.0%) | 33 (75.0%) |
PF(+): pancreatic fistula grade II or higher according to Clavien-Dindo classification, PNI: prognostic nutritional index, BMI: body mass index, VFA: visceral fat area, SFA: subcutaneous fat area
また,術後の病理結果においてもEckerら5)の分類によるhigh risk,low risk群の間にはPFの発生に有意差はみられなかった.
病理学的な検討における脂肪化および線維化のGradeの分布をTable 4に示す.線維化についてはGrade 3の高度の線維化がみられた2例は,いずれも病理診断が慢性膵炎であり,他の症例は大部分がGrade 1もしくは2であった.

Relationship between CT value of remnant pancreas, remnant P/S ratio and histological change (fatty change, fibrosis) in the pancreatic cut margin
脂肪化について各々のGradeと残膵CT値および予定残膵P/S比との関連について3群間で比較したところ,組織学的な膵臓の脂肪化Gradeは,CT画像における残膵CT値の低下(P<0.0001)および予定残膵P/S比の低下(P=0.0006)と有意な関連がみられた.線維化の程度による残膵CT値および予定残膵P/S比の変化はみられなかった.
Table 3で行った単変量解析において有意差が示された,年齢,残膵CT値,予定残膵P/S比について,ROC曲線を用いてcut off値およびAUC値を求め,それぞれの項目について算出した感度,特異度,陽性的中率,陰性適中率をTable 5に示す.いずれもAUC値は0.7以上であり,特異度,陽性適中率はやや低いものの,感度,陰性適中率は高値であった.
| Cut off value |
AUC value |
Sensitivity | Specificity | Positive predictable value |
Negative predictable value |
|
|---|---|---|---|---|---|---|
| Age | 62 | 0.756 | 57.1% | 86.8% | 61.5% | 84.6% |
| CT value of remnant pancreas | 39.2 | 0.719 | 85.7% | 63.1% | 46.1% | 92.3% |
| Remnant P/S ratio | 0.846 | 0.793 | 78.5% | 63.1% | 44.0% | 88.8% |
AUC: area under the curve
DPはPDに比較すると切除範囲が狭く,剥離を必要とする主要な血管も少ないことに加え,再建を必要としないため,手術時間や出血量のみならず,PFの発生においても術者や施設間による差が少ないことが予想される.
膵切除において肉眼的な膵臓の性状を表す言葉として,いわゆるsoft pancreasとhard pancreasという表現が用いられることが多い.これは腫瘍による主膵管の閉塞によって随伴性膵炎が引き起こされ,残膵側における分枝膵管の閉塞と主膵管の拡張が伴うことに関連した言葉であるが,hard pancreasがsoft pancreasに比べると吻合が容易であり,特にPDにおいてはPFの発生に関連した因子として既知の事実である.一方DPにおいては,たとえ腫瘍により閉塞性膵炎を伴っていても当該部位は切除側に含まれることが多く,膵切離線を含めた残膵側は主膵管拡張のないsoft pancreasであることがほとんどであり,切離線における膵臓の肉眼的な性状に大きな差異はなさそうである.
DPにおけるPFの発生は施設間の違いはあるものの,30%前後と報告1)2)されており,時に重症化すれば術後出血の原因となり致命的になりうるため,膵断端の処理法についてはさまざまな工夫が試みられている6).しかし,現段階では器械吻合と手縫い吻合の比較試験であるDISPACT試験7)や,Kawaiら8)によるstaplerとpancreaticojejunostomy(PJ)の比較試験においてPFの発生には有意差が認められず,PFを未然に防ぐための膵断端の処理法はいまだ議論の対象となっている.Staplerを用いた膵切離については膵臓の厚さとPFとの関連が報告されているが5),用手的な処理とPFのリスクに関連した報告はなく,staplerもしくは用手的な処理が,どのような症例に適しているか,という報告もない.我々は膵切離線における臓器条件としていわゆるsoft pancreasが多く,前述の報告のように膵断端処理による差が認められていないにもかかわらず,PFが発生する症例とそうでない症例があることから,肉眼的には認識できない臓器因子が強く関連している可能性があると仮定し,残膵の萎縮が少なく,膵外分泌能が保たれている症例ほど膵液の産生能が高く,PFのリスクになりうるのではないかと仮定した.
過去の報告では膵切除後のCT画像解析から,主膵管径や膵臓の厚みから膵外分泌能の変化を予測することが試みられており9),さらに近年ではCT画像の解像度が増したことで,膵実質におけるCT値が膵臓の脂肪置換を反映する,という報告もなされている10).Kimら11)の報告によると膵実質のCT値の低下は,膵臓の脂肪変性による脂肪成分の増加とそれに伴う腺房組織の減少を反映していると考えられ,またYuasaら12)の報告により膵切除後の膵断端の組織学的所見における腺房組織の面積と術後膵外分泌能との強い相関関係が報告されている.
佐藤13)は膵外分泌能の評価法であるPFD試験を行い,さらに同症例の単純CTにおけるP/S比を測定し比較することで,P/S比は術後の膵外分泌能を反映する客観的な指標になりうることを報告している.
NAFLD/NASH診療ガイドライン2014において14),腹部CTでは肝臓の線維化を評価することは困難であるが,脂肪化については脾臓とのCT値の比(肝脾CT値比:liver to spleen ratio:L/S比)の測定により脂肪沈着量の推定が可能であると記載されている.これらの結果から,予定残膵CT値の測定のみでなく,脂肪化や線維化の少ない実質臓器である脾臓のCT値との比である予定残膵P/S比が,予定残膵の脂肪化をより反映する指標になりうると考えて,今回の検討を行った.
我々の検討では,単変量解析において年齢が若い症例,予定残膵CT値が高い症例,予定残膵P/S比が高い症例が,単変量解析において術後PFのリスク因子として抽出された.組織学的には,52例中高度の線維化を来していた症例は2例とわずかであり,CT画像における残膵CT値の分布は,主に膵臓の脂肪化の程度を反映しているものと推測される.
腹部単純CTにおけるCT値は,脾臓が約50 Hounsfield unit(以下,HUと略記),膵臓が約45 HUである.本検討における組織学的な分類において萎縮の少ない膵臓と判定された脂肪化Grade 1の残膵CT値の平均が44.7 HUであることは,残膵CT値と組織学的な所見に整合性があると考えられる.
これらを合わせて考えると,CT値が正常に近い,組織学的にも脂肪化が少なく腺房細胞がより保たれている膵臓,つまり膵外分泌能がより高い症例が,PFのhigh risk症例になりうると考えられる.同様にリスク因子として抽出された年齢については,より若い症例ほど膵臓の脂肪化が少なく,膵外分泌能が維持されているからであると推測される.これらの結果は,膵切除術であるDPにおいては,臓器機能が良好であるほど,術後の合併症のリスクが高くなるのではないか,という当初の仮定を支持するものと考えている.さらに,予定残膵P/S比を用いたDP術後のPF発生に関連した報告は,医学中央雑誌において1970年1月~2017年12月まで,「膵体尾部切除術」,「術後膵液漏」,「P/S比」をキーワードとして,PubMedにおいて「distal pancreatectomy」,「postoperative pancreatic fistula」,「pancreas to spleen ratio:P/S ratio」をキーワードとして1950年~2017年12月までの期間で検索したかぎりでは会議録も含め,予定残膵および切除側の膵断端の病理学的所見にも言及した報告は我々の報告が初めてであった.
今回検討に用いた予定残膵CT値と予定残膵P/S比は単純CTを用いて簡便に測定しうることから,残膵の外分泌能を予測しうる簡便な指標になると考えられる.
Fukudaら15)は122例のDP症例を解析し,膵臓の厚さが10~20 mmの症例においては,単純CTにおける膵臓CT値がより低い症例が,よりsoftなpancreasであり,PFのリスク因子になりうる,という結果を報告しており,我々の報告と逆の結果となっている.しかし,本検討は,対象症例全例における切除膵断端の病理所見と,残膵側のCT値を対応させたうえでPFのリスクとの関連を示しており,意義があるものと考える.
今回の検討の欠点として,一つは症例数が少ないことが挙げられる.多変量解析を行うには症例数が少なく,今回示したPFのリスク因子は独立した危険因子として示すことはできなかった.
もう一つは,CT値の測定における誤差の問題である.膵臓の脂肪化が限局している例では測定値にばらつきが生じる可能性があるし,脂肪変性部位が線維化を起こしている場合には,脂肪化をCT値からうまく検出できない場合があると思われる.また,脂肪化および線維化のGradeは本検討においてのみ用いた分類であり汎用性については疑問が残る.これらについては今後の検討課題であろう.
現在DP後のPF発生のリスク因子に関する報告は多数あるものの5)15)16),いまだPFを予測しうる因子は報告によりさまざまであり,手術手技の定型化や術後管理が発達した今日でも,依然その発生率は大きく変わらない.本検討において,我々はPFの危険因子として,予定残膵の外分泌能が保たれていることが一つの因子になりうると考える.肉眼的にはsoft pancreasであっても,組織学的に腺房の萎縮が少ない正常膵もあれば,脂肪化によって腺房細胞が減少している場合もあり,これらの症例に全て同じ膵断端処理法を用いてPFを予防しようとすることは限界があるのかもしれない.ただし,術後PFの発生は既報にもあるようにさまざまな因子が関連している可能性があるため,今後さらなる症例の蓄積と解析が必要と思われる.
利益相反:なし