2020 年 53 巻 6 号 p. 524-532
2020 年 53 巻 6 号 p. 524-532
食道癌手術において,具体的にどの操作で反回神経損傷を起こしているかは明らかにされていない.今回,縦隔鏡下食道亜全摘術における反回神経損傷の早期同定と,直接的原因の特定を目的とした,術中持続神経刺激モニタリング(continuous intraoperative nerve monitoring;以下,CIONMと略記)の使用経験を報告する.迷走神経本幹に持続電極を装着し,声帯収縮能をlatency,amplitudeの2項目で評価することで反回神経の機能をモニタリングした.左反回神経周囲の剥離操作時,左反回神経に緊張がかかり,一時的にamplitudeの低下を認めたが,操作を中止すると速やかに改善した.左右迷走神経ともにamplitudeの値の変化は基準値の50%以内の低下で操作を終了でき,術後は両側とも反回神経麻痺を認めなかった.CIONMは危険な操作をリアルタイムに感知,認識することで,不可逆的な反回神経損傷への移行を未然に防ぐことが可能となり,有用な方法であると考える.
The specific cause of operative manipulation has not yet been identified. Here, we report a successful case for the detection of impending recurrent laryngeal nerve (RLN) injury during mediastinoscopic subtotal esophagectomy using the continuous intraoperative nerve monitoring system (CIONM). After attaching a monopolar automatic periodic stimulation electrode on the vagal nerve, the latency and the amplitude of the vocal cord contractility were monitored as the RLN function. During the nodal dissection around the left RLN, a 50% or greater decrease in the amplitude relative to the baseline values was temporarily recorded by retracting the left RLN from the dorsal to the ventral direction. However, it improved promptly after relieving the retraction of the RLN. Throughout the operation, the amplitude values of both RLNs were kept at 50% or greater relative to the baseline value, and as a result, RLN palsy did not occur after surgery. CIONM may be useful in preventing irreversible RLN injury by monitoring the real-time function of the RLN and alerting the dangerous maneuver leading to decreased levels of vocal cord contractility.
食道癌に対する食道切除術は,2011年の本邦のNational Clinical Databaseによると,周術期合併症41.9%,手術関連死亡率3.4%1)と,消化器外科手術の中でも最も侵襲の高い手術の一つである.一方で,術後反回神経麻痺は主要な術後合併症の一つであるが,正確な評価方法が定まっていないためにその報告は0~70%と大きなばらつきがある2)~6).ひとたび反回神経麻痺をおこすと,嗄声を来すのみならず誤嚥や肺炎にもつながり2),入院期間の延長やQOLの低下を来すため,術中の神経損傷をいかに予防するかが重要な課題である.
近年,神経刺激装置を使用した術中刺激モニタリング(intraoperative neural monitoring;以下,IONMと略記)により,術中神経損傷のリスク減少に期待がもたれている7).本邦においては,Medtronic社製のNerve Integrity Monitoring System(以下,NIMと略記)が筋電計(位置決定用神経探知刺激装置)として薬事承認がなされ,2012年4月より耳下腺良性・悪性腫瘍摘出術における顔面神経などの術中神経モニタリングを,2014年4月からは甲状腺悪性腫瘍摘出術における反回神経などの術中神経モニタリングを,それぞれNIMを用いて行うことで手術医療機器加算(K930脊髄誘発電位測定等加算)の保険請求が可能となった.また,2016年にはautomatic periodic stimulation(以下,APSと略記)TM電極が薬事承認され,持続神経刺激モニタリング(continuous intraoperative nerve monitoring;以下,CIONMと略記)を行うことが可能となった.これにより従来のIONMよりもより神経麻痺を減少させる可能性に期待がもたれている8)9)が,食道悪性腫瘍手術に対しては2017年8月現在で手術医療機器加算の保険収載はされていない.
今回,縦隔鏡下食道亜全摘術において,反回神経損傷の早期同定,ならびに,直接的原因の特定を目的とし,CIONMを使用したためその経験を報告する.
患者:76歳,男性
既往:心房細動,高血圧症,肺気腫
術前診断:食道癌Mt cT1bN0M0 cStage I
術前呼吸機能検査所見:肺活量2,500 ml,一秒量1,470 ml(一秒率56.5%)
早期癌であること,閉塞性肺障害であることを考慮し,肺の圧排が不要で肺への負担が最小化となるように,非胸腔食道亜全摘術を選択し,CIONMを併用した.なお,CIONMに関しては,院内倫理委員会の承認(承認番号:HM17-256)を得て行った.
1. CIONMの使用方法・設定気管内チューブはNIM TriVantage® EMG TUBE(Medtronic社)を使用した(Fig. 1).持続刺激として1 Hzの電気刺激を100 μs毎に送り,チューブのカフ上につけられたセンサーで声帯の収縮能を,反応潜時(latency)と声帯反応の振幅(amplitude)の2項目で評価した(Fig. 2).Latencyが操作前値を基準とした際の10%延長し,且つamplitudeが50%以上低下したときに警告音がなる設定とした.麻酔導入時に筋弛緩薬を使用した後は筋弛緩薬を使用せず,鎮静・鎮痛を十分効かせた状態で頸部・縦隔操作を行った.腹部操作に移行してからは従来通り筋弛緩薬の投与を開始した.
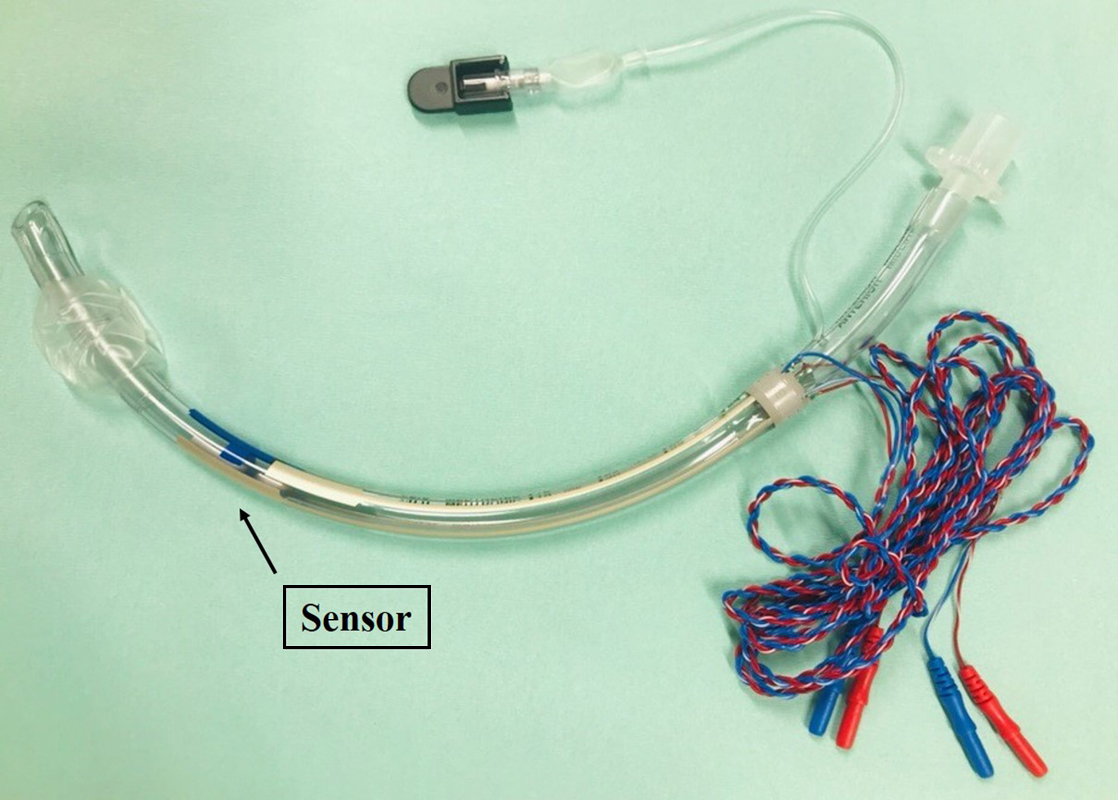
NIM TriVantage® EMG TUBE.
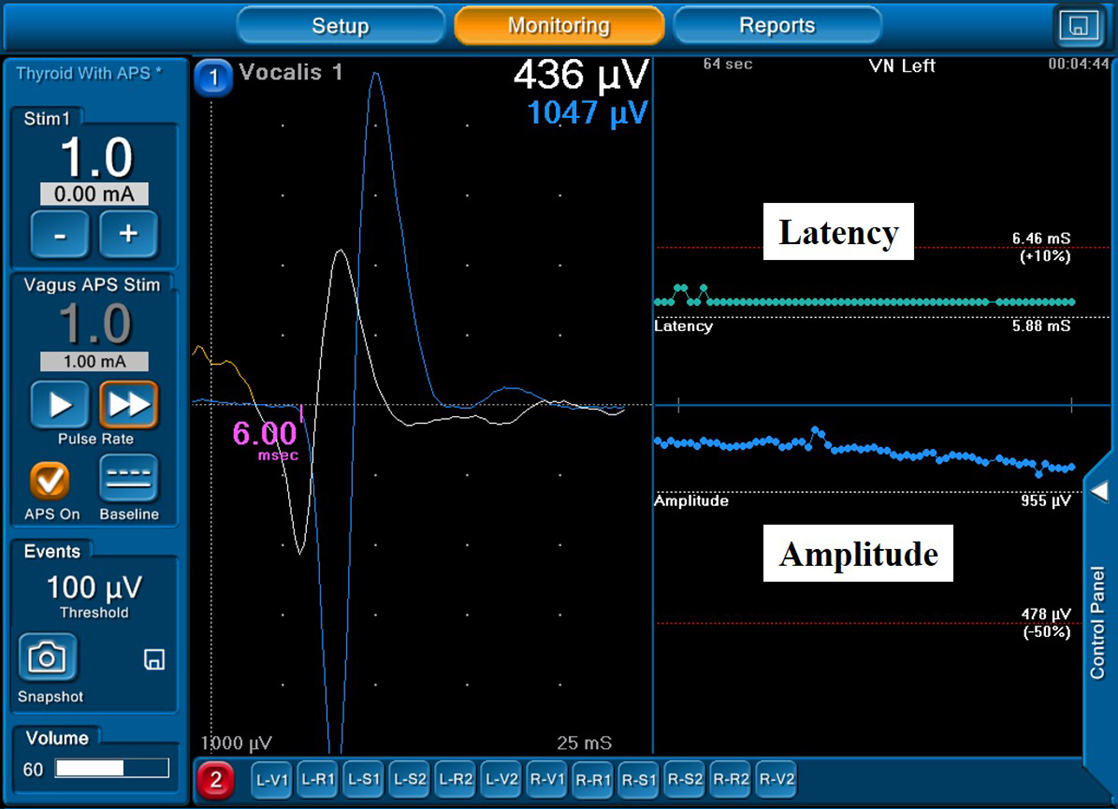
The representative image of NIM. The latency is shown in the right upper field of the monitor, and the amplitude is shown in the right lower field of the monitor.
縦隔鏡操作ならびに縦隔郭清は,Fujiwaraら10)の方法に準じて行った.左頸部を約6 cm弧状切開し広頸筋を切離した.皮弁形成はせず,前頸筋群は適宜sealing deviceにて胸骨付着部で切離した.胸鎖乳突筋内側縁より剥離を進め左頸動脈鞘に到達し,左迷走神経本幹を同定した.左迷走神経周囲の組織をなるべく剥離した状態で,APS電極を装着した(Fig. 3).
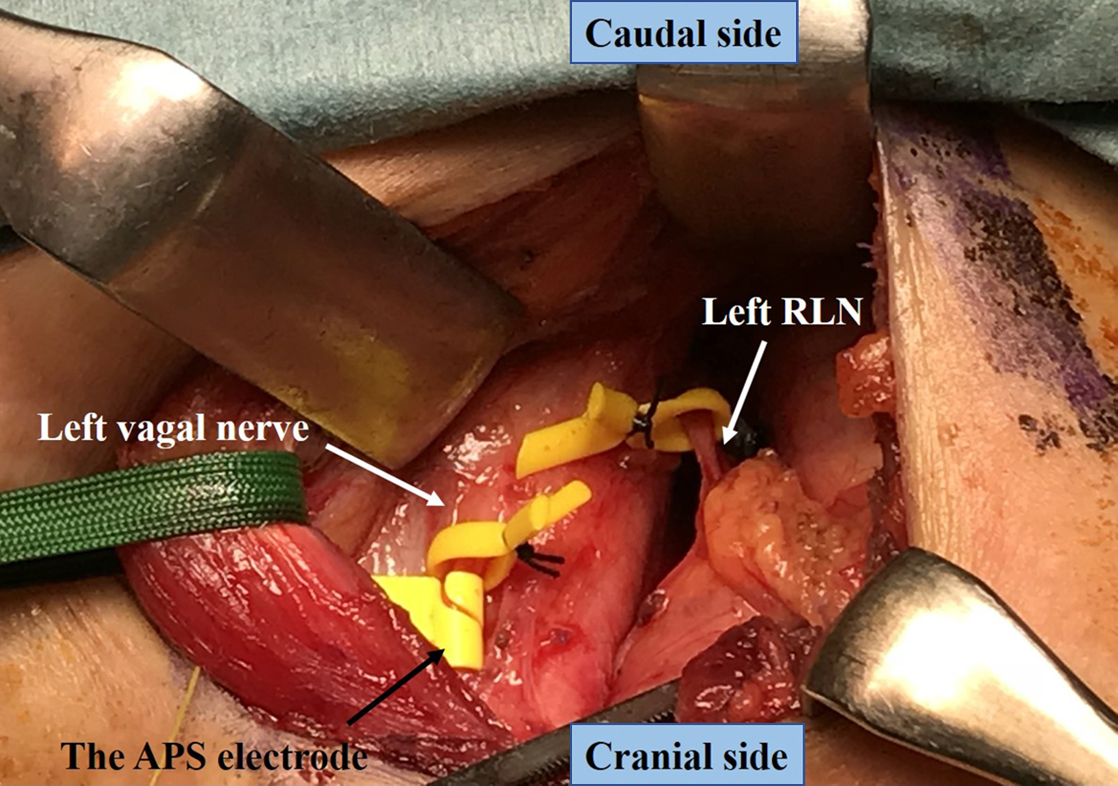
The operative findings of attachment of the APS electrode on the left vagal nerve inside carotid sheath. RLN; recurrent laryngeal nerve.
#101Lを含む脂肪織と左反回神経を一塊にしてテーピングし,食道も全周性に確保した後テーピングした.左反回神経を同定した後に#101Lを含む脂肪織を郭清し,頸部創にE・Zアクセス®(八光メディカル社)を挿入し,8 mmHgで気縦隔を開始した.E・Zアクセス®を装着した際,amplitudeの基線の低下を認めた.食道周囲の剥離は,背側は椎前筋膜前面で,左側は左鎖骨下動脈もしくは大動脈弓,下行大動脈に沿って,右側は気管左側縁に沿って進め,食道腹側で左反回神経沿いに#106recLリンパ節を含む脂肪織を食道側につけるように郭清操作を進めた.反回神経を含む組織を鉗子で腹側に圧排すること(Fig. 4)や左反回神経根部周囲で大動脈弓を圧排することでそれぞれ左反回神経に緊張がかかるとamplitudeの低下とlatencyの遷延を認めた(Fig. 5).操作を中断すると数分後にはこれらは改善した.106recL郭清時に反回神経周囲の組織を剥離する際(Fig. 6)や食道枝切離の際には変化は認めず,中縦隔の郭清時も変化は認めなかった(Fig. 7).
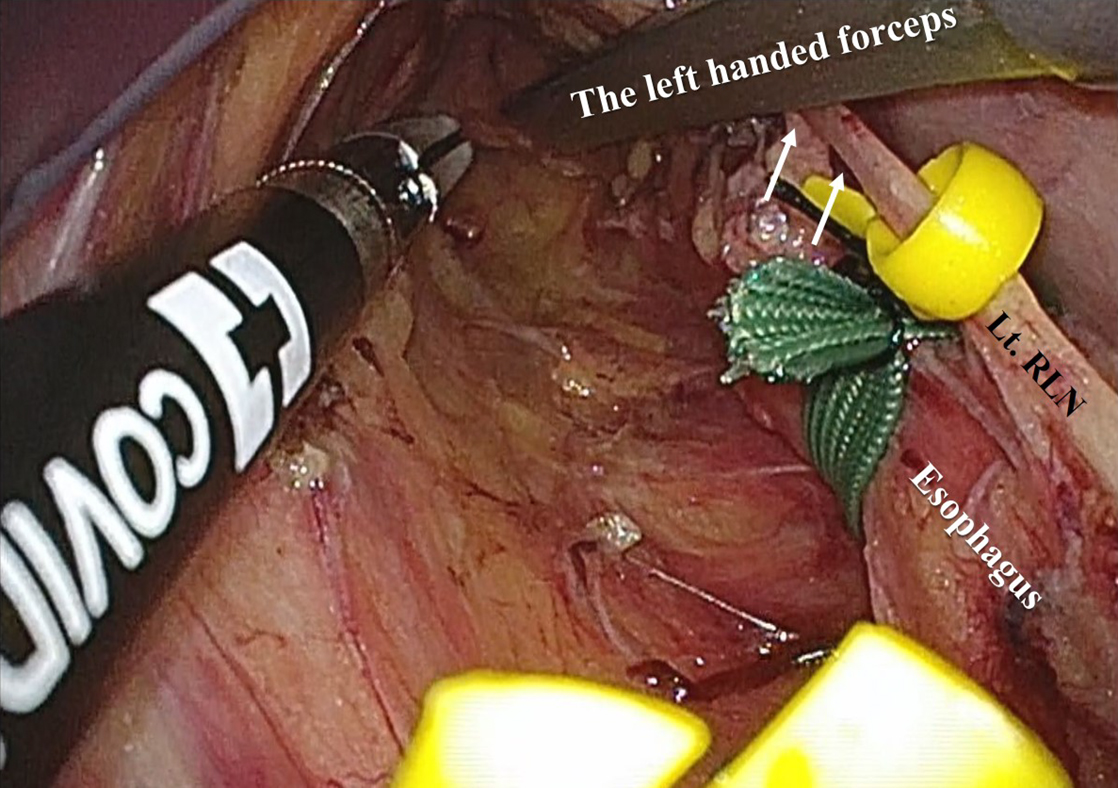
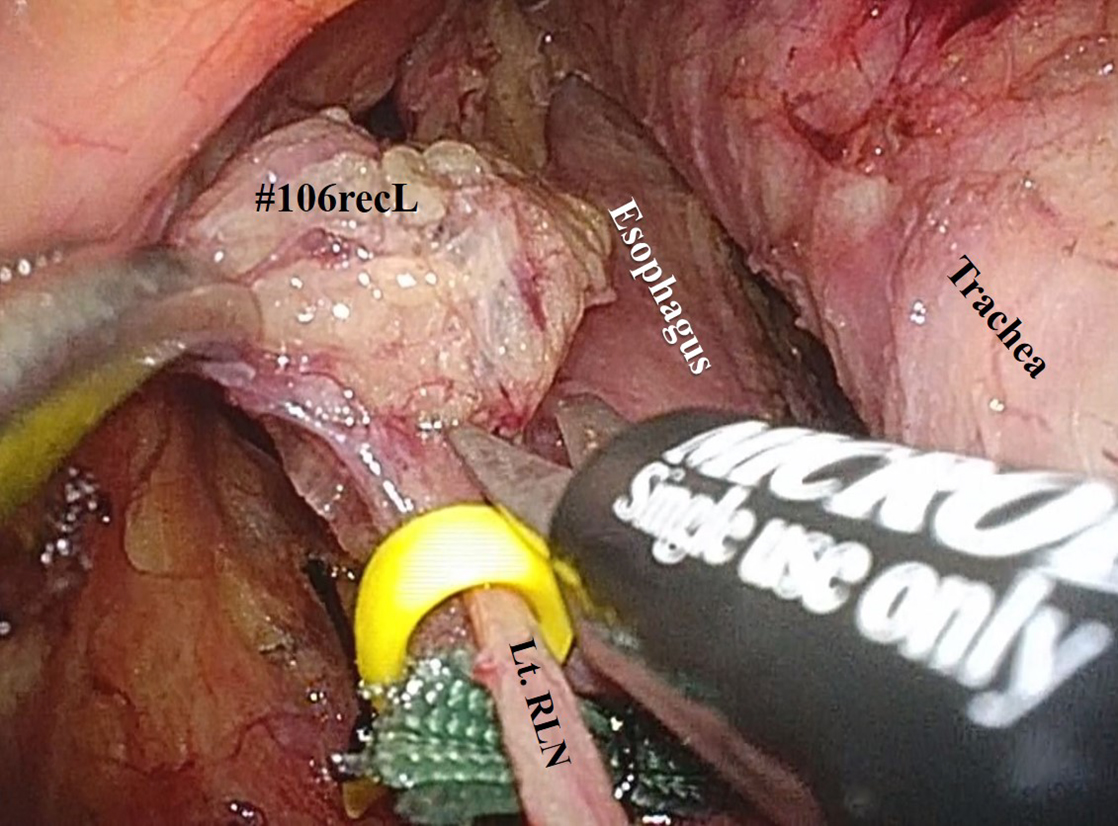
Dissection of the esophagus. The landmarks for dissection line in the dorsal, left, and right aspects were the prevertebral fascia, the outermost layer of the left subclavicular artery, and the left side of the tracheal wall, respectively. The left recurrent laryngeal nerve (Lt. RLN) was retracted or stretched by left handed-forceps (white arrows).
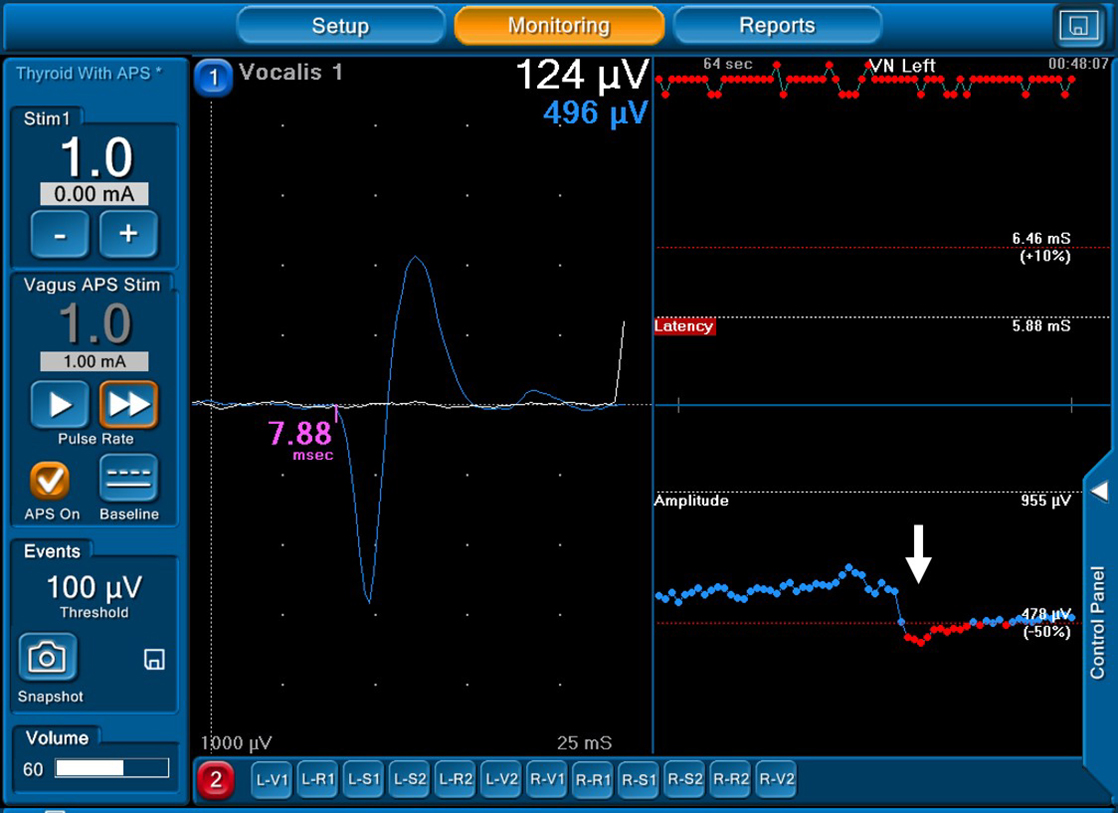
Signs of prolonged nerve latency and declined nerve amplitude were found in the nerve integrity monitoring system, when the left recurrent laryngeal nerve was retracted or stretched (white arrow).
Dissection of the adipose tissue containing #106recL lymph nodes from the left recurrent laryngeal nerve (RLN).
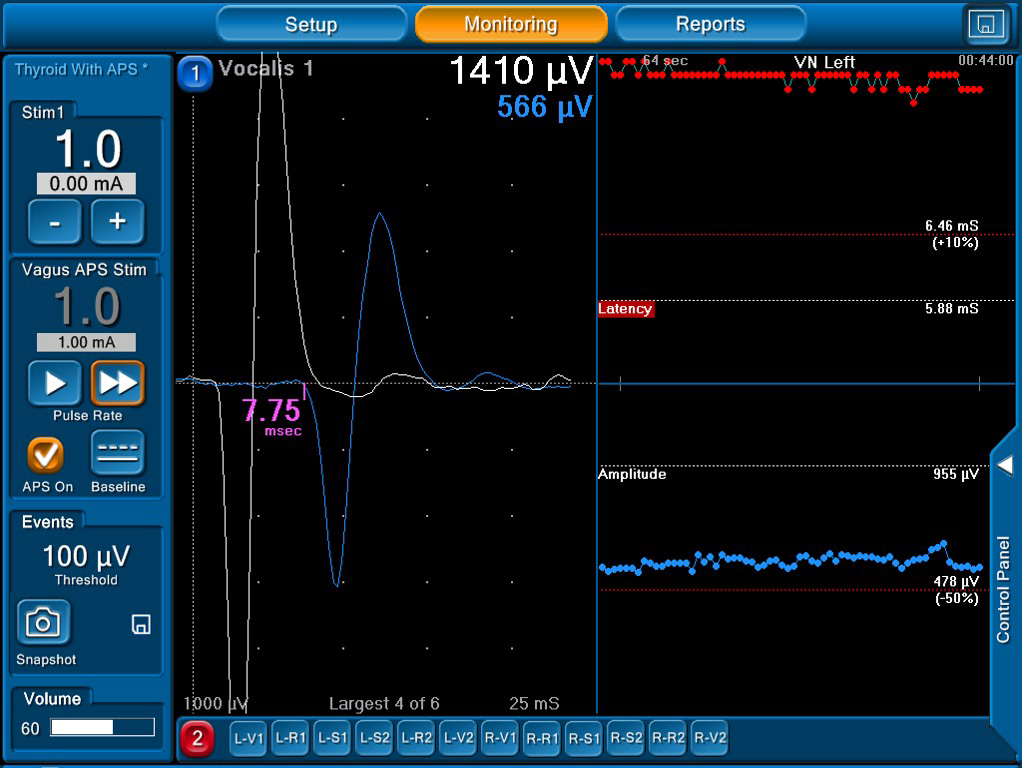
The nerve amplitude in the nerve integrity monitoring system was not changed by separating the adipose tissue from the left recurrent laryngeal nerve, or detaching the esophageal branch of the nerve during dissection of 106recL lymph nodes.
左側を#109まで郭清した後,縦隔鏡操作を終了し,右側の郭清に移った.右頸部を約5 cm皮膚切開し,右迷走神経本幹を同定した後,APS電極を装着した.電極刺激により周期的に収縮する右反回神経を容易に同定することができ,これを損傷しないように温存しながら直視下に#101Rを含む脂肪織を郭清した.右反回神経を中枢側方向においながら,右鎖骨下動脈の反回部までを確認し同部周囲の脂肪織を切除し,#106recR郭清とした.反回神経周囲の組織を把持して緊張をかけて剥離する操作で若干のamplitudeの低下を認めたが,50%以上低下することなく右側の郭清を終了した.
左右とも,latencyは10%以上遷延した状態が持続していたが,amplitudeは50%以上を維持していた(Fig. 8).頸部と上・中縦隔操作終了後,腹腔鏡下胃管作成ならびに経裂孔的下縦隔郭清を行い,剣状突起下の小開腹創より食道を摘出し,胸骨後経路で亜全胃管にて頸部手縫い吻合で再建を行った.経裂孔的下縦隔郭清時に左右の縦隔胸膜は合併切除しており,右胸腔にドレーンを1本留置した.胃瘻を造設して手術終了とした.手術時間は685 分で,そのうち頸部操作は278 分(左頸部直視下操作54 分,頸部縦隔鏡操作186 分,右頸部直視下操作38 分)であった.出血は26 gで,術中輸血は行わなかった.術中偶発症も特に認めなかった.
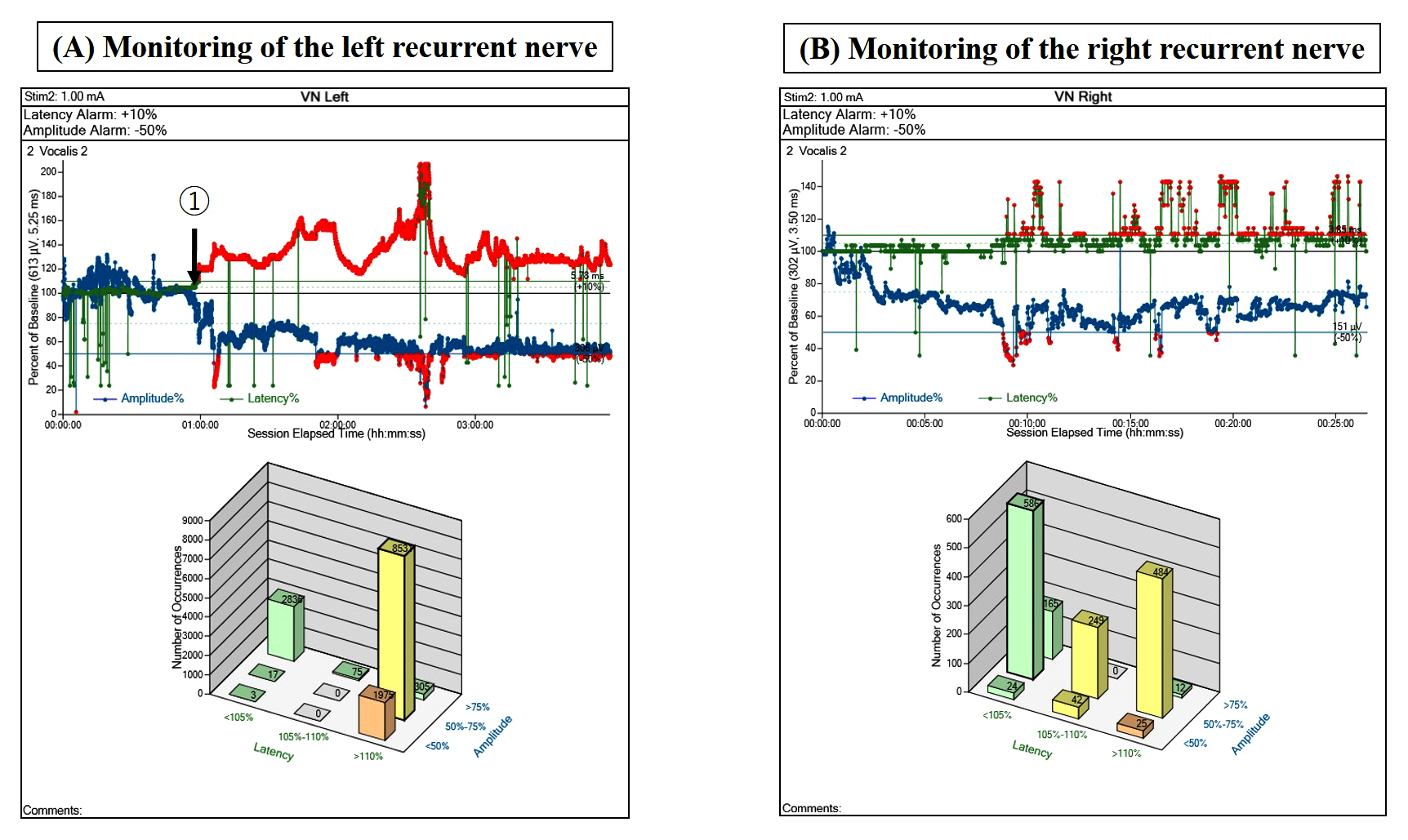
(A) Record of continuous intraoperative nerve monitoring in the left recurrent laryngeal nerve; the baseline of the amplitude was declined when the EZ access was inserted to the incisional wound (①). After that, the amplitude showed a stable line, except for the temporary declining by intraoperative maneuver. (B) Record of the continuous intraoperative nerve monitoring in the right recurrent laryngeal nerve; the latency and amplitude were almost kept at the baseline throughout the procedure.
手術翌日に抜管し,自科での喉頭観察では声帯運動に異常を認めず,嗄声も認めなかった.術後7日目の耳鼻咽喉科の喉頭鏡観察による評価でも反回神経麻痺はないと診断された.しかし,縫合不全を起こしたため,保存的に加療し術後75日目に自宅退院となった.
術後病理所見では,摘出リンパ節55個のうち4個のリンパ節(#101R(2/9),#106recL(2/3))に転移を認め,pT1bN2M0 pStage IIと最終診断された.術後10か月現在,外来通院中である.
食道癌において反回神経周囲リンパ節は転移頻度が高く11)~13),1群ないしは2群領域リンパ節に定められている重要な部位である14).その一方で反回神経は非常に繊細な神経であり,手術操作によって容易に損傷されうる.神経への直接的な操作,熱損傷,過度の牽引,虚血などがリスクといわれている15).しかし,具体的にはどのような操作が術後反回神経麻痺の直接的な原因であるかは,明らかにされていない.今回,反回神経損傷の早期同定,ならびに損傷リスクの高い手術操作の特定を目的としてAPS電極を用いたCIONMを併用した非胸腔食道亜全摘術を施行した.本術式の適応や手術手技・郭清度合などの有用性においては議論の余地があり,当科においても明確に確立してはいない.そのため,適応には慎重を要するが,自験例のように術前に早期食道癌と診断され,かつ呼吸機能に懸念のある場合には低侵襲化手術の選択肢の一つとして期待できると考える.
CIONMを利用した術中反回神経モニタリングの経験により,反回神経を左右へ牽引するなどの直接的な緊張をかける操作だけでなく,食道の背側から腹側への圧排や気管を右側へ圧排する操作などの左反回神経への間接的な緊張をかける操作によってもamplitudeが低下することが示唆された.その一方で,神経周囲の組織剥離や食道枝の切離,反回神経の比較的近傍でのエネルギーデバイスの使用など,これまで反回神経損傷のリスクが高いと考えていた操作ではamplitudeに変化は認めなかった.また,左反回神経の郭清終了後以降の反回神経に緊張がかかりにくい状態では,中縦隔操作においても問題なかった.よって,反回神経に対し直接的のみならず間接的に緊張をかける操作こそが神経損傷の大きな要因である可能性が示唆された.また,最初にE・Zアクセス®を装着することによりamplitudeは若干低下しており,頸部創を広げて甲状腺や気管などに緊張がかかっても反応低下を来しうる可能性にも留意する必要があると考えられた.
CIONMの場合には,amplitudeの50%以上低下,ならびにlatencyの10%以上遷延が20分以上持続し反応低下が不可逆的な状態になると術後神経麻痺となる可能性が高くなるといわれている8).本症例では一過性の低下は認めたものの,低下したamplitudeはその原因となった手術手技を一旦中断することで,数分で元の値にまで回復した.これは,一時的な可逆的変化の段階で留めることができた結果と考えられる.一方でIONMは間欠的なモニターであるため,モニター時点ではすでに反回神経が不可逆的変化を来してしまっていることもある.その場合には,原因となりうる操作を特定することが困難である.ここにCIONMとIONMの大きな違いがあり,危険な操作のリアルタイムな感知あるいは認識が可能となることで不可逆的な反回神経損傷への移行を未然に防ぐ可能性が高まる点で,CIONMが有用と考えられる.
これまでに食道癌においてIONMが行われた報告は散見される15)が,CIONMの報告は1編のみである16).その理由として,以下の2点が考えられる.一つは手術医療機器加算の保険適応が承認されていないためであるが,もう一つの理由として,体位の問題がある.腹臥位や左側臥位の場合には,左迷走神経本幹にAPS電極を安定してつけておくことが困難と思われる.その点で,Fujiwaraら10)が考案した縦隔鏡下食道亜全摘術は仰臥位のままで手術手技が完遂する利点があり,これはCIONMを行ううえでも大きな利点である.右反回神経に関しては,直視下のみの操作であるためその必要性は高くない可能性もある.しかし,中には反回神経が細い症例もあること,また知らずに反回神経を牽引し損傷を来すリスクもあること,持続刺激により断続的に右反回神経が収縮を来すことで脂肪組織の中に埋もれた反回神経をより安全に同定できうる点などを考慮すると,右側であっても有用性があると考える.
その一方で,本症例では課題もみられた.神経へのダメージがリアルタイムでわかるため,アラームがなってしまう手術操作が必要とわかっていてもその後に行いづらくなることや,神経機能の回復を待つために操作の中断を余儀なくされるなど,手術時間の遅延を来してしまう欠点がある.しかし,手術時間延長による患者負担よりも,術後の反回神経麻痺による患者QOLの低下が回避できることを考慮すると,多少の手術時間延長は現段階では許容されると考える.それよりも今後の症例の蓄積に伴って,危険行為の特定により反回神経損傷リスクを極力回避しながら効率よく手術遂行ができる手順を確立していくことが求められる.もう1点は,術野外の操作に関しても注意が必要な点である.特に深部操作になるほど,カメラの視野内の操作が原因とはかぎらず,視野外で気付かないで鉗子のシャフト部分が反回神経を圧排,牽引している可能性がある.1例毎に慎重に確認,検討を行い,経験を積み重ねていく必要がある.
本術式ならびにCIONMは,麻酔科との連携が重要である.頸部縦隔鏡操作時には筋弛緩薬を使用しないため,反回神経の機能が維持される反面,十分な麻酔深度が得られずに手術操作へ支障を来す可能性が懸念される.当科では麻酔科と密に連携し,深い鎮静と鎮痛による全身麻酔をすることにより,筋弛緩薬を使用せずとも咳嗽反射や疼痛刺激に対する反応などは十分に抑制され,手術操作に支障を来すことなく郭清操作を行うことができた.また,術中操作により気管チューブ先端が移動することがあり,単にセンサー部分のずれによる反応低下の可能性があることも念頭に入れるべきである.そのため,センサーが常に良好な位置にあるかどうかにも気を配る必要がある.そういった点で本手法はまだ発展途上であるため,今後も改良する余地は大いに残されている.まだ1例のみの臨床経験であるため,今後の症例の蓄積に期待したい.
利益相反:なし