Abstract
症例は78歳の女性で,嘔吐を主訴に受診し,進行胃癌と診断し,胃全摘術を施行する方針とした.バイアスピリン,ワルファリン,クロピドグレルを内服しており,休薬の上でヘパリン持続投与を開始した.術前に超音波ガイド法を用いて右鎖骨下静脈を穿刺し中心静脈カテーテル(central venous catheter;以下,CVCと略記)を挿入した.3日後に急激に出血性ショックを来した.造影CTで右胸壁に巨大血腫を認め,圧迫止血を試みたが出血の持続が懸念された.血管造影を行い,胸肩峰動脈の鎖骨枝の損傷による出血性ショックと診断し,CVCを抜去し,経動脈塞栓術を行った.これにより全身状態は安定化し,塞栓術から8日後に胃全摘術を施行した.鎖骨下静脈穿刺によるCVC挿入において動脈損傷は約8%に生じるとされる.血管造影は動脈損傷の確定診断と治療に際して非常に有用である.抗凝固療法など易出血性の素因がある症例においては遅発性に出血が顕在化する場合もあり,特に注意が必要である.
Translated Abstract
We report a case of delayed hemorrhagic shock due to thoracoacromial artery injury after insertion of a central venous catheter (CVC) into the right subclavian vein for perioperative nutritional management. A 78-year-old woman was admitted to our hospital because of vomiting. She was diagnosed with advanced gastric cancer and total gastrectomy was planned. For preoperative nutrition management, the right subclavian vein was punctured using real time ultrasonic guidance, and a CVC was inserted. Three days later, the patient developed acute hemorrhagic shock. Contrast-enhanced CT showed a massive hematoma in the right anterior chest wall. Angiography just after CVC removal showed injury of the clavicular branch of the thoracoacromial artery. Selective arterial embolization of this branch was performed. This stabilized the general condition, and total gastrectomy was successfully performed 8 days after embolization. Arterial injuries occur in about 8% of CVC insertions by subclavian venipuncture. Angiography is useful both in diagnosis and treatment of arterial injury. Our case shows that bleeding may manifest late in cases with anticoagulation therapy.
はじめに
栄養管理,周術期の循環管理,化学療法,透析などを目的とした中心静脈カテーテル(central venous catheter;以下,CVCと略記)挿入は,消化器外科領域のみならず臨床上必須の手段である1).しかし,出血(動脈穿刺),血胸,気胸,カテーテル感染,迷入,pinched off syndromeなど種々の合併症が報告されている2).特に出血については,高齢者や心血管併存症に対する抗凝固療法の症例も増えつつある現状もあり,最も注意すべき合併症の一つである.今回,遅発性に胸肩峰動脈損傷による出血性ショックを来した例を経験したので報告する.
症例
症例:78歳,女性
現病歴:繰り返す嘔吐を主訴に前医を受診した.上部消化管内視鏡検査で,胃体上部小彎から前庭部後壁にかけて4型腫瘍を認めた.同部位の生検結果はGroup 5(tub2~por)であり,手術加療目的に当科を紹介受診した.
既往歴:不安定狭心症,心原性脳梗塞,高血圧症,脂質異常症,左内頸動脈-後交通動脈分岐部動脈瘤,慢性腎不全
内服薬:ワルファリン1.25 mg,クロピドグレル75 mg,バイアスピリン10 mg,カルベジロール2.5 mg,フロセミド20 mg,ニコランジル15 mg,クエン酸第一鉄ナトリウム50 mg,ランソプラゾール15 mg,酸化マグネシウム990 mg
上部消化管内視鏡検査所見:胃体上部小彎から前庭部後壁にかけて小彎側を中心とした4分の3周性,易出血性の4型病変を認めた.
腹部CT所見:胃体部から前庭部に壁肥厚を認め,原発巣と考えられた.胃角部には脂肪織濃度上昇を認め,漿膜浸潤が疑われた.大彎側,小彎側ともに胃周囲に腫大リンパ節を散見し,所属リンパ節転移が疑われた.遠隔転移を疑う所見を認めなかった.
血液検査所見:赤血球数:425×104/μl,Hb:12.0 g/dl,Ht:37.4%で高度の貧血はなく,血小板数:26.1×104/μlと正常であった.PT:49.0秒,PT-INR:3.40,APTT:47.8秒と凝固能はワルファリン内服中に矛盾しない所見であった.アルブミン:2.8 g/dlと低下を認めた.
頻回の嘔吐を契機に発覚した胃癌(UML,Less,Type 4,tub2~por,cT4aN1M0 Stage IIIA)に対して,胃全摘術を行う方針とした.クロピドグレル,バイアスピリン,ワルファリンを内服していたため,院内の規定に則って手術予定日の14日前にクロピドグレルを中止し,7日前にバイアスピリンとワルファリンを中止してヘパリンの持続投与を開始した.ヘパリンの単位数はAPTTが正常の1.5倍~2.5倍を目標に適宜調節した.ヘパリン流量,PT-INRとAPTTの推移を示す(Table 1).
Table 1
Changes of PT-INR and APTT
|
Admission |
|
|
|
CVC insertion |
|
|
Embolization |
|
|
Total gastectomy |
| Day |
|
–7 |
–6 |
–4 |
–2 |
0 |
1 |
3 |
4 |
5 |
6 |
7 |
10 |
13 |
| Dose of heparin |
10,000 U |
 |
|
|
10,000 U |
 |
| PT-INR |
|
|
1.88 |
1.51 |
1.17 |
1.18 |
|
1.04 |
0.97 |
|
|
1.07 |
|
|
| APTT |
|
|
74.3 |
68.8 |
63.5 |
47.5 |
|
60.1 |
37.6 |
41.7 |
41.6 |
79 |
|
|
| Hb |
|
|
|
|
11.7 |
|
12 |
6.8 |
9 |
8.2 |
7.8 |
9.6 |
9.6 |
9.5 |
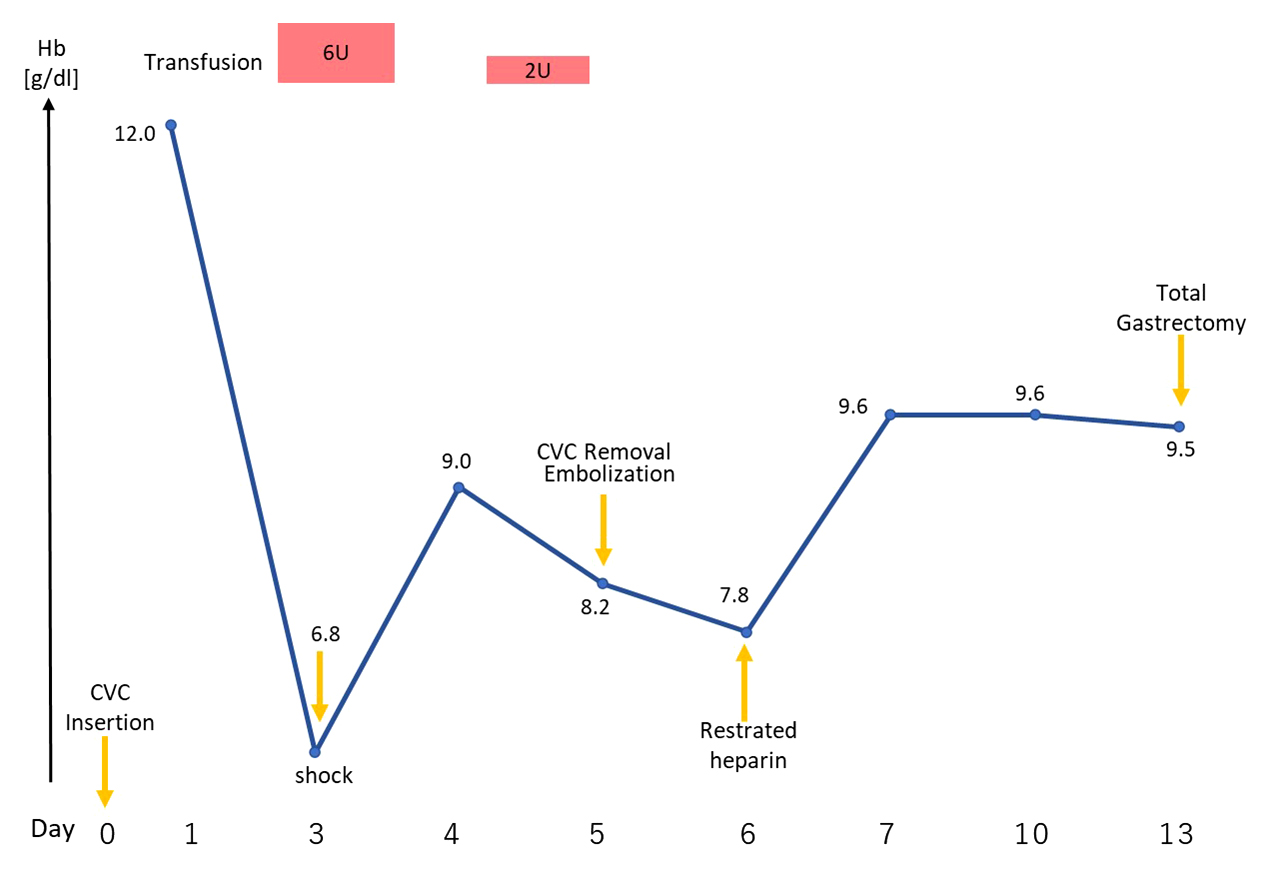
術前栄養管理として外来初診時から経口栄養剤を処方し,服用可能であった.入院後も経口造影にて液体は十二指腸へ通過することを確認できたため,当初は流動食+経口栄養剤での管理継続の方針としていたが,嘔吐の増悪が見られたため,経口摂取での管理では不十分と判断しCVCを挿入する方針とした.当初,上肢からの末梢挿入式CVC挿入を検討したが,複数の医師により挿入を試みるも困難であった.胃全摘術予定3日前(以下,day 0と略記)に右鎖骨下静脈にCVCを留置した.穿刺は全てリアルタイム超音波ガイド法で行い,試験穿刺で2回,本穿刺で1回穿刺の計3回穿刺しそれぞれ逆血を確認した.いずれの穿刺でも動脈誤穿刺はなかった.明らかな合併症なく終了し,術後の胸部エックス線では先端位置に問題はなく,気胸や血胸を認めなかった(Fig. 1).また,皮下にも血腫を認めなかった.穿刺翌日の血中Hb値は12 g/dlで貧血進行を認めなかった.留置したCVCを用いて胃全摘術予定当日までの3日間,中心静脈栄養を行った.
胃全摘術当日(day 3)の午前0時より持続ヘパリン化を中止した.午前7時30分歩行時にふらつきを自覚し,橈骨動脈を触知したところ微弱であった.仰臥位安静にて橈骨動脈は触知可能となり意識状態の変容もなかった.しかし,低血圧が遷延し,59/47 mmHg,心拍数115回/分であった.CVC内腔に明らかな閉塞はなく,細胞外液1,000 mlと5%アルブミン製剤250 mlを投与したが,なおも低血圧は遷延した.緊急血液検査を行いHb 6.8 g/dlと高度な貧血の進行を認めた(Fig. 2).経鼻胃管からは血性の排液は認めなかった.出血源は不明であるも出血性ショックが第一に疑われ,手術を延期し,ICUに入室した.
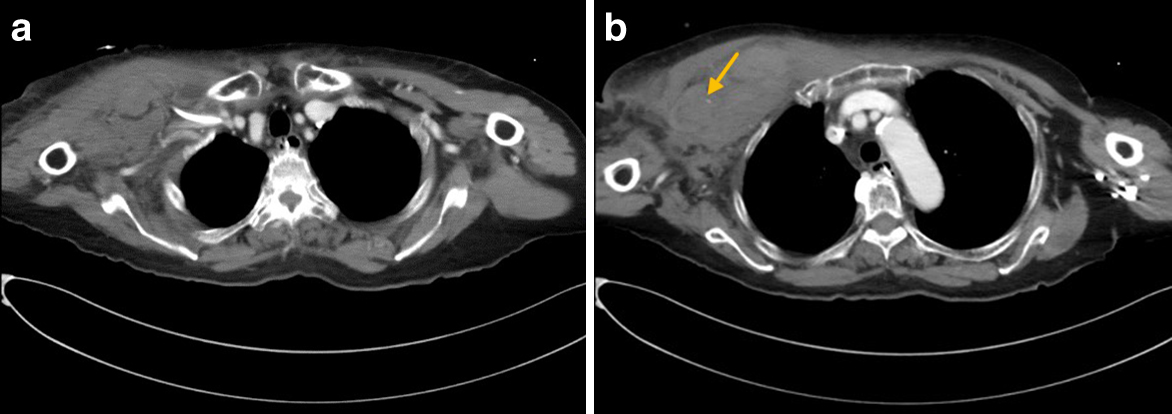
ICU入室時に右前胸部を中心に,背部右側や腋窩,右上腕にかけて硬結を伴う腫脹を認めた.5%アルブミン製剤750 mlと濃厚赤血球液6単位を投与し,収縮期血圧は100 mmHg程度まで上昇,Hb値も9.8 g/dlに上昇した.出血源同定のためダイナミックCTを施行したところ,右鎖骨下静脈の穿刺部から右胸壁に沿って大胸筋下に最大横径135 mmの広範な血腫と推察される低吸収域を認めた(Fig. 3a).血腫の頭側に胸肩峰動脈周囲に血管外漏出像を認め,動脈性出血が疑われた(Fig. 3b).CVCは留置のまま,刺入部を枕子と弾性包帯を使用して圧迫固定した.
CVC挿入day 5には,体表所見上は上腕中央,右側腹部まで皮下出血斑が拡大したが血腫の分散として判断できる程度であった.しかし,Hb値は8.2 mg/dlとさらに低下し,出血の持続を疑った.血管外科のバックアップのもと,CVC抜去および血管造影にて出血部位を確認する方針とした.
右上腕動脈を穿刺し,右鎖骨下動脈を造影したが,明らかな血管外漏出像を認めなかった(Fig. 4a).当初,CTで関与が疑われた右胸肩峰動脈に関しても明らかな異常は認めなかった.右鎖骨下静脈に留置されたCVCを抜去し,再度右胸肩峰動脈に対して選択的に造影検査を行ったところ,胸肩峰動脈の鎖骨枝とCVCが重なっていた位置で血管壁の不整を認めた(Fig. 4b).この部位が出血源であると診断し,胸肩峰動脈の鎖骨枝に対して選択的に金属コイルとゼラチンスポンジ細片を用い経動脈的塞栓術を施行した.
その後は貧血の進行なく経過し,day 6にヘパリン投与を再開,day 7にICUを退室した.予定していた胃癌に対する胃全摘術をday 13に施行できた.胃全摘術後も塞栓術部の再出血は認めていない.
考察
CVCは今日の医療において,周術期管理,化学療法,静脈栄養,透析など多岐に渡って臨床上重要な手段である1).穿刺の対象となる静脈は主に内頸静脈,鎖骨下静脈,大腿静脈,表在静脈(尺側皮静脈,肘正中静脈,橈側皮静脈)であり,それぞれに利点・欠点がある1).鎖骨下静脈穿刺は患者の快適性や安定性から長期管理に適合し,感染率の低さ,血栓形成の少なさにおいて内頸・大腿静脈穿刺に勝ると報告されている2).特にカテーテル感染に関しては,内頸・大腿静脈と比較してそのリスクは1/2~1/3程度に低下する.しかし,カテーテルの迷入が多く,pinched off syndromeや気胸・血胸のリスクも高い3).内頸静脈は気胸の危険性は少ないが,動脈穿刺やカテーテル感染の頻度は鎖骨下静脈より高い3).大腿静脈は穿刺手技はさほど難関ではないが,血栓を形成しやすくカテーテル感染が最も起きやすい3).これらの利点・欠点を踏まえたうえで穿刺血管を決定する.本症例は当初表在静脈を使用しての末梢挿入型CVCを選択したが留置困難であった.感染率の低さ,血栓形成の少なさを重視し,長期管理に適した経路として鎖骨下静脈穿刺を選択した.
中心静脈の穿刺法には,超音波を使用しない古典的なランドマーク法と超音波を使用した超音波ガイド法がある.超音波ガイド法はランドマーク法と比較して動脈穿刺,血腫,気胸のいずれの合併症の頻度も低いと報告され,本邦でのガイドラインでも,CVC挿入時は超音波ガイド法が推奨されている4).超音波ガイド法は優れた方法であるが,超音波は二次元画像であり,穿刺針が目的の静脈をすでに貫通していても先端が静脈内にあるかのような画像となることがある5).これにより穿刺針の位置を誤認して,予想外に深部の穿刺となってしまうというピットフォールもあり,術者には超音波画像に関して十分な理解が求められる.
CVC挿入の最も高頻度の合併症は不整脈であるが,動脈穿刺はそれに続く頻度の合併症である6).内頸静脈穿刺では12.54%の頻度で動脈穿刺が生じると報告されているが,鎖骨下静脈穿刺では7.88%程度とされ,動脈穿刺は内頸静脈穿刺の方がより来しやすいと考えられている1).血腫形成は挿入に複数回の穿刺を要した例,マルチルーメンのCVCを挿入した場合に多い1).特に穿刺回数に関して,初回穿刺で挿入しえた場合は動脈穿刺や気胸などの合併症は1%未満であるのに対し,合併症が起こった症例の40~50%は2回以上の穿刺が行われたと報告されている7).本症例では,超音波ガイド法で行われたものの試験穿刺で2回,本穿刺で1回穿刺の計3回穿刺していた.出血リスクに関する患者側の危険因子として,基礎疾患や併存症,常用薬などによる出血傾向,動脈硬化による血栓塞栓症の高リスク状態,手術や骨折の影響での血管の解剖学的走行変化などが含まれる6).以前カテーテルを挿入した同一部位の再穿刺,局所放射線療法の既往,胸骨縦切開の既往,最近の心筋梗塞,血小板減少症,穿刺部位の静脈血栓,線溶療法もリスク因子として報告されている2).本症例でも,クロピドグレル,バイアスピリン,ワルファリンの術前休薬の置換としてヘパリンの持続投与を行っていた.
胸肩峰動脈は腋窩動脈の前壁から起始する短く細い血管である.その起源は一般的に小胸筋の上縁と重複し,烏口鎖骨靭帯を貫通し,胸筋枝・肩峰枝・鎖骨枝・三角筋枝の4枝に分かれる6)8).本症例での損傷血管である鎖骨枝は,胸鎖関節に向かって頭側・内側に走行し,鎖骨部に至り,胸鎖関節と鎖骨下筋を栄養する.一方,腋窩静脈は一般的に腋窩動脈の尾側を走行し,第一肋骨直下に入り鎖骨下静脈となる.鎖骨下動脈損傷を防ぐ観点では末梢側ほど動脈が頭側に離れていくので,穿刺位置を末梢にすれば動脈穿刺の危険性は低下し,かつ胸腔からの距離も遠くなるが,胸肩峰動脈や外側胸動脈などの動脈の分枝は末梢側ほど多くなる9).よって,解剖学的視点からは腋窩静脈中間位,もしくはそのやや末梢で穿刺するのがよい9).
腋窩動脈は小胸筋,前鋸筋,鎖骨下筋が構成する疎な組織内を走行するため,腋窩動脈や胸肩峰動脈を損傷した際には,第5,6肋骨近傍から胸筋・大胸筋の付着部まで至るような巨大血腫をつくりうると推察されている7).本症例からは胸肩峰動脈の分枝の損傷であっても同様に巨大血腫を作りうることが示唆された.
鎖骨下静脈穿刺での動脈損傷は,鎖骨下動脈を最多とし内胸動脈や腋窩動脈でも報告があるが,胸肩峰動脈の損傷は調べうるかぎり本邦では文献的報告はなく,海外で数例の報告を認めるのみである6)7)9)10).このうちBourgonjonら6)は,全身麻酔導入後に鎖骨下静脈にCVCを挿入し,術直後覆布を外した際に胸肩峰動脈損傷による血腫が発覚した1例を報告した.その他の症例報告では挿入直後のバイタルサインの変化から動脈損傷が疑われ,血管造影検査で確定診断に至り,塞栓術が行われている7)9)10).
胸肩峰動脈は鎖骨下静脈穿刺における穿刺経路上に位置する小血管であり,超音波では同定可能であるが,しばしば気づかれずに穿刺されてしまうとされる5).前述の報告例においても,胸肩峰動脈の本幹の損傷であるのか,もしくは分枝の損傷であるのかまで断定できている症例はない.このことからは,報告例よりも多くの胸肩峰動脈損傷が実際には発生しているものの,正しい診断にたどり着いていない症例があることが考えられる.日本医療安全機構による中心静脈穿刺合併症に係る死亡の分析11)では,内頸静脈穿刺前に静脈の性状,深さ,動脈との位置関係を確認するためにプレスキャンを行うことが推奨されている.鎖骨下静脈穿刺においても同様にプレスキャンは重要と考えられ,胸肩峰動脈など腋窩動脈の分枝の走行も意識しておくべきと考えられる.よって,手技を行う際は常に胸肩峰動脈の存在を念頭に置いてプレスキャンの段階で穿刺経路に分枝動脈が走行していないか入念に確認しておくことも重要である.
本症例は術中体位を水平仰臥位として手技を行った.ランドマーク法では仰臥位を基本とするが,超音波ガイド下穿刺においては上肢を外転させると超音波のブラインドになる鎖骨が頭側に移動し,エコーで観察される腋窩静脈が長くなる5).本症例では穿刺に難渋したこともリスクの一因であったと考えられるため,穿刺前ならびに初回穿刺を失敗した時点で体位の調整を行い,より確実に目的血管を穿刺できる環境を整えるべきであったと考えられる.また,本症例は針の進行面と血管の長軸像を描出し,針全体を描出しながら穿刺するin-plane法を用いたが,この方法では動脈との位置関係を確認しながら穿刺することができないため,血管の短軸像を描出させて,針の一部を確認しながら穿刺するout-of-plane法が,動静脈を確認しながら穿刺できる点でより安全であった可能性がある5).
CVC留置による巨大血腫や縦郭出血,出血性ショックなどの致死的合併症はまれであるが,鎖骨下静脈の穿刺で動脈を誤穿刺した場合,外部からの圧迫による止血が困難で重篤化することがある12).一方,内頸静脈穿刺時は動脈を誤穿刺したとしても圧迫により止血が得られることが多いため,抗凝固療法中や易出血性の状態にある場合は内頸静脈へのCVC留置の方が望ましいと考えられる.8 Fr以上の太さのカテーテルが動脈を損傷した場合,安易にカテーテルを抜去すると持続出血,脳梗塞,動静脈漏,血胸などを来す場合があると報告されており13),この状況でのCVC抜去は血管外科医のいる環境で細心の注意を払って施行されるべきである.血管損傷の診断には造影CTが用いられることが多いが,血管造影は血管の損傷や走行異常を確認するうえでは非常に有用であり,かつ必要時にはステント治療や塞栓術といった治療に繋げることができる.一般に鎖骨下動脈損傷や腋窩動脈損傷は手術加療やステントグラフトによって加療されるが,胸肩峰動脈は小血管ゆえに,塞栓術が考慮されることが多い7).本症例においても,造影CTで胸肩峰動脈損傷を疑い,血管造影を行うことで胸肩峰動脈の鎖骨枝の損傷であると確定診断した.その結果,鎖骨枝のみを選択的に塞栓するという最も効果的で他の血管への影響がない治療を行うことが可能であった.
本症例のように抗凝固療法中のCVC挿入においては遅発性に出血に気づかれる症例も報告されている13).抗凝固療法による易出血性の影響で少量の出血が持続し,血腫が体表面から目視されることなく大胸筋下を広がり,バイタルサインが変化してはじめて出血に気づかれることが原因と推察されている.また,上肢のリハビリ後に出血が顕在化した症例も報告されており,リハビリなどの軽度の労作による静脈内のカテーテルのわずかな移動も出血の引き金になりうると推察される9).
CVC挿入手技は超音波技術の発達によってますます安全になってきているが,特に抗凝固療法中など易出血性の素因がある例では遅発性の出血も含めて留意する必要がある.また,エックス線検査やエコー検査上は正常に留置されているように思えても損傷を併発している可能性もあることを念頭におかねばならない.
利益相反:なし
文献
- 1) Hodzic S, Golic D, Smajic J, Sijercic S, Umihanic S, Umihanic S. Complications related to insertion and use of central venous catheters (CVC). Med Arch. 2014 Oct;68(5):300–303.
- 2) Parienti J, Mongardon N, Megarbane B, Mira J. Intravascular complications of central venous catheterization by insertion site. N Engl J Med. 2015;373:1220–1229.
- 3) Polderman KH, Girbes AJ. Central venous catheter use. Part 1: mechanical complication. Intensive Care Med. 2002;28:1–17.
- 4) 認定病院患者安全推進協議会(PSP).中心静脈カテーテル挿入・管理に関する指針 改定第3版2020[Internet].公益社団法人日本医療機能評価機構 教育研修事業部 認定病院患者安全推進課;[cited 2020 Apr].Available from: https://www.psp-jq.jcqhc.or.jp/post/proposal/7014
- 5) 野村 岳志.安全な腋窩静脈穿刺中心静脈カテーテル挿入法.日本集中治療医学会雑誌.2009;16:135–138.
- 6) Bourgonjon B, Fontaine M, Verbessem D, De Keukeleire K, Speybrouck S, Poelaert J. Thoracoacromial artery perforation in subclavian vein catheterization: a rare complication. Acta Anaesth Belg. 2017;68:43–47.
- 7) Vandaele P, Heye S, Maleux G. Therapeutic embolization of a thoracoacromial artery perforated by placement of a deep venous catheter. JBR-BTR. 2005;88:75–77.
- 8) 佐藤 泰司, 高藤 豊治.日本人成人の腋窩動脈について.杏林医学会雑誌.1987;18:195–211.
- 9) Wicky S, Meuwly JY, Doenz F, Uské A, Schnyder P, Denys A. Life-threatening vascular complications after central venous catheter placement. Eur Radiol. 2002;12:901–907.
- 10) Abi-Jaoudeh N, Turba UC, Arslan B, Hagspiel KD, Angle JF, Schenk WG, et al. Management of subclavian arterial injuries following inadvertent arterial puncture during central venous catheter placement. J Vasc Interv Radiol. 2009 Mar;20(3):396–402.
- 11) 一般社団法人日本医療安全調査機構.中心静脈穿刺合併症に係る死亡の分析―第1報―医療事故の再発防止に向けた提言 第1号.2018[Internet].医療事故・支援センター;[cited 2018 Mar].Available from: https://www.medsafe.or.jp/uploads/uploads/files/publication/teigen-01.pdf
- 12) 日本麻酔科学会.安全な中心静脈カテーテル挿入・管理のためのプラクティカルガイド2017[Internet].公益社団法人 日本麻酔科学会 安全委員会;[cited 2017 Jun].Available from: https://anesth.or.jp/users/person/guide_line
- 13) Shinzato T, Fukui M, Kooguchi K, Sakaguchi M, Joo WJ. Hemorrhagic shock 3 days after catheterization from the axillary vein. J Anesth. 2010;24:290–292.