Abstract
症例は83歳の女性で,上行結腸癌術後5年目に行った造影CTにて,肝S5とS4にまたがる部位に動脈相で軽度造影され門脈相で肝実質よりも弱い造影効果を呈する14 mm大の腫瘍を認めた.肝原発の悪性腫瘍もしくは転移性腫瘍を否定できず,腹腔鏡下肝S5・S4a区域切除術を施行した.病理組織学的検査ではリンパ上皮腫様癌を認め,全身検索にて原発巣となりうる病変が確認されなかったことから肝原発と診断した.術後1年目のCTにて肝十二指腸間膜近傍に43 mm大のリンパ節腫大を認めた.超音波内視鏡下生検の結果,リンパ上皮腫様癌の転移と診断した.他に明らかな転移所見を認めずリンパ節再発巣に対して放射線治療を施行した.治療後,腫瘍は消失し,以後6か月間再発を認めていない.肝原発リンパ上皮腫様癌は非常にまれであり,その治療方針は確立されていない.今後の症例の集積が待たれる.
Translated Abstract
An 83-year-old woman had been followed up after radical resection for ascending colon cancer. Five years after the operation, she underwent contrast-enhanced CT, which revealed a 14-mm tumor in S5 and S4 of the liver with mild contrast in the arterial phase and weaker contrast in the portal venous phase compared to the hepatic parenchyma. Laparoscopic S5/S4a segmentectomy was performed under a diagnosis of hepatocellular carcinoma or metastatic tumor. Histopathological examination showed lymphoepithelioma-like carcinoma of the liver. One year later, CT showed a 43-mm lymph node in the hepatoduodenal ligament. Endoscopic ultrasound biopsy revealed metastasis of lymphoepithelioma-like carcinoma. Radiotherapy was administered to the lymph node recurrence since there were no other metastatic sites. After completion of radiotherapy, the tumor showed a complete response and the patient has been disease-free for 6 months. Lymphoepithelioma-like carcinoma of the liver is extremely rare. A treatment strategy has not been established and further accumulation of cases is warranted.
はじめに
リンパ上皮腫様癌(lymphoepithelioma-like carcinoma;以下,LELCと略記)はまれな組織型であり,唾液腺,胸腺,肺,胃,皮膚,子宮頸部などに発生するとされている1).中でも肝原発のLELCは非常にまれであり,その治療方針はいまだ定まっていない.今回,我々は肝原発LELCに対して肝切除を施行し,その後のリンパ節再発に対して放射線療法が奏効した1例を経験したので文献的考察とともに報告する.
症例
患者:83歳,女性
主訴:肝腫瘤
既往歴:慢性腎不全,C型肝硬変
家族歴:特記事項なし.
現病歴:77歳時に上行結腸癌,胆石症に対して腹腔鏡下結腸右半切除術,胆囊摘出術を施行した.病理組織学的診断はpT2N0M0 pStage I(大腸癌取扱い規約第8版)であった.術後5年目のCTにて肝S5に単発の腫瘍を指摘された.
現症:147 cm,53 kg.腹部は平坦,軟.
血液検査所見:AST 26 U/l,ALT 14 U/l,T-Bil 0.64 mg/gl,Alb 4.7 g/dl,PT 116%と肝機能に異常を認めず,CEA 3.1 ng/ml,CA19-9 6.7 U/ml,PIVKA-II 15 mAU/ml,AFP 5.9 ng/mlと腫瘍マーカーの上昇は認めなかった.Cre 1.05 mg/dl,eGFR 38.4 ml/min/1.73 m2と腎機能障害を認めた.HBs抗原は陰性,HCV抗体は陽性であった.
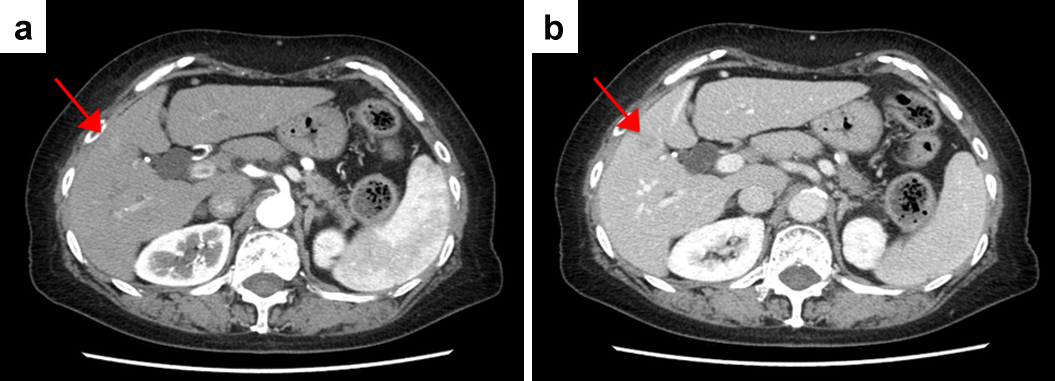
腹部造影CT所見:肝S5からS4にまたがる長径14 mm大の単発の腫瘍を認め,動脈相で軽度造影され,門脈相で周囲肝実質よりも弱い造影効果を呈した.その他の臓器に特記所見は認めなかった(Fig. 1).
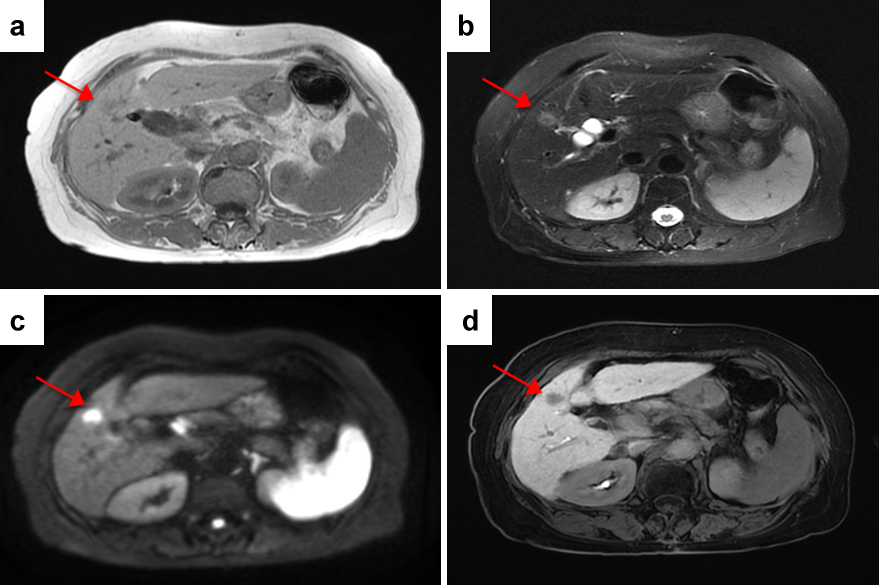
Gd-EOB-DTPA造影MRI所見:CTと同様の部位に長径14 mm大の腫瘍を認め,T1強調像にて軽度低信号,脂肪抑制T2強調像にて軽度高信号,拡散強調像にて高信号,ADC値低値を呈した.ダイナミック造影では早期相では軽度増強され,後期相以降で周囲肝実質より弱い増強効果を呈した.肝細胞相では周囲肝実質より低信号を呈した(Fig. 2).
腹部エコー所見:肝S5に15 mm×16 mm大の境界明瞭で,内部は低エコーと淡い高エコーが混在する腫瘍を認めた.
以上より,転移性肝腫瘍もしくは原発性肝腫瘍を否定できず,腹腔鏡下肝切除術の方針とした.
手術所見:6ポートで行った.腫瘍の肝表への露出は認めなかった.S5およびS4aグリソンを一括処理し,indocyanine green(ICG)蛍光法を用いて切除範囲を同定し,腹腔鏡下に系統的S5・S4a区域切除術を施行した.手術時間は5時間30分,出血量26 mlであった(Fig. 3).
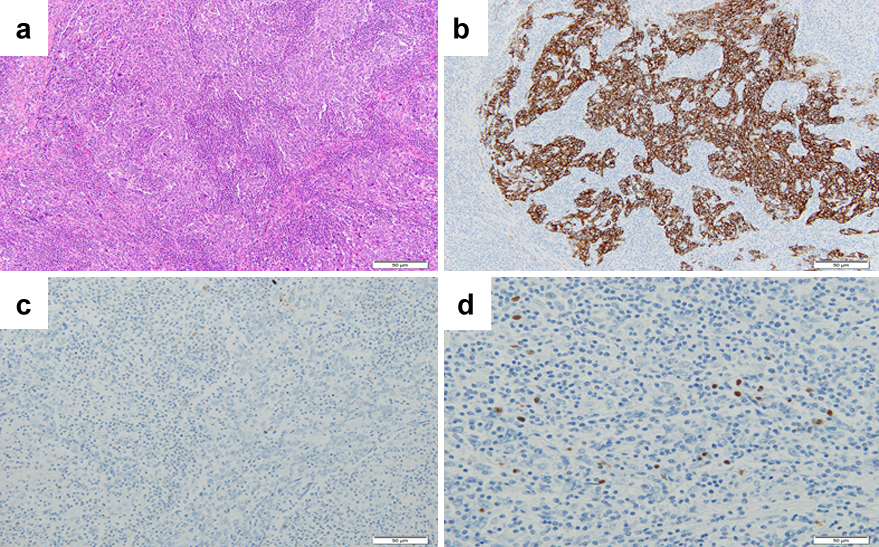
病理組織学的検査所見:ヘマトキシリン・エオジン染色(HE染色)では,異型細胞を背景としてリンパ球や形質細胞の高度浸潤を伴って増殖していた.免疫染色検査では,異型細胞はCAM5.2に陽性を呈する上皮細胞で,CK7陰性,CK20一部弱陽性,Hepatocyte陰性,CDX2陰性であった.背景のリンパ球にEBV encoded small RNA(EBER)陽性所見が散在性にみられた.以上より,LELCと診断した(Fig. 4).
全身検索にてその他に原発巣となりうる病変を認めず,まれではあるが肝原発と診断した.
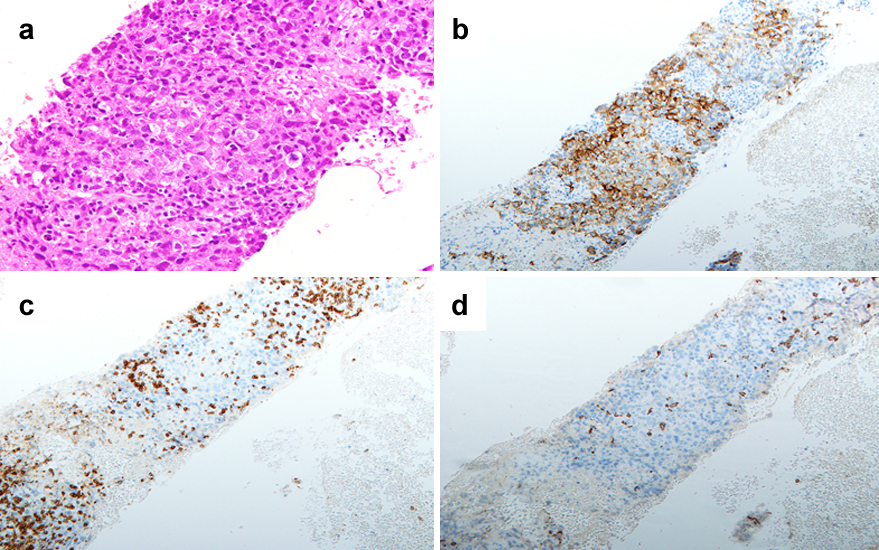
術後経過:術後合併症はなく第7病日に退院となった.術後1年目のCTにて肝十二指腸間膜近傍に長径43 mm大の腫瘍を認め,超音波内視鏡下穿刺生検を施行した(Fig. 5a).病理組織学的検査所見では,ヘマトキシリン・エオジン染色(HE染色)にて初回手術時の所見と同様に異型細胞とリンパ球や形質細胞の高度浸潤を伴った増殖を認めた.免疫染色検査ではMNF116陽性,背景にはCD3/CD5とCD20/CD79a陽性のリンパ球を認め,LELCのリンパ節再発の診断となった(Fig. 6).後方視的には術後6か月のCTにて同様の部位に扁平な腫瘍を認めており,その後,同腫瘍が増大したものと考えられた(Fig. 5b).化学療法も検討したが,高齢であること,腎機能低値であったことと患者の希望を踏まえ,再発巣に対して総線量46.8 Gy(1.8 Gy×26回)の放射線療法を施行した.照射後は腫瘍の消失を認め(Fig. 5c),以後6か月間新たな転移の出現を認めていない.
考察
LELCは,上咽頭発生の未分化癌であるリンパ上皮腫癌に類似した組織像を呈する腫瘍であり,著明なリンパ球浸潤を伴う低分化な癌腫とされる.Béginら2)によって肺原発LELCとして初めて報告され,その他に唾液腺,胸腺,肺,胃,皮膚,子宮頸部,乳腺,膀胱などに発生するとされている1).
肝原発LELCは,WHO分類では肝内胆管癌の1亜型と分類され非常にまれであり,1996年にHsuら3)によって初めて報告された.LELCの原因としてはEBVとの関連が指摘されているが,肺原発や乳腺原発では無関係とする報告もあり,原発臓器によって異なる可能性もある4)5).近年LELCを病理組織学的検査によってlymphoepithelioma-like hepatocellular carcinoma(以下,LEL-HCCと略記)とlymphoepithelioma-like intrahepatic cholangiocarcinoma(以下,LEL-ICCと略記)に分類する報告が多く存在する.Solinasら6)やZhangら7)の報告では,免疫染色検査に関してはLEL-ICCではCK7やCK19の陽性率,EBV感染率が高い傾向にあることが示されており,両者におけるリンパ球浸潤における相違点も論じられている.また,臨床学的相違として,LEL-HCCではHCV陽性率が,LEL-ICCではHBV陽性率が高い傾向にあることや,人種に関してはLEL-HCCではコーカソイドに多く,LEL-ICCではアジア人に多い傾向にあることが示唆されている.アジア人では乳幼児期にEBVに感染することが多いこともあり,発症にはやはりEBVの関与の可能性が考えられる8)9).ただし,いずれもいまだ定まった見解はなく,両者を鑑別するうえでさらなる症例の集積と検討が必要である.
医学中央雑誌で「リンパ上皮腫様癌」,「肝臓」をキーワードに検索すると,1964年から2020年までの期間において会議録を4例認めるのみであった.一方PubMedで1950年から2020年までの期間で「lymphoepithelioma-like carcinoma」,「liver」をキーワードに検索すると,近年その報告例は増加しており,100例を超える報告を認めた.その中で,個々の臨床経過が記載されていること,肝原発であることが確認されていることを条件とし,かつ英語で書かれた原著論文において報告された46症例2)3)6)7)10)~38)に,自験例を含めた47症例のみを対象に検討を行った(Table 1).年齢の中央値は61歳(19~83歳)で,性別は女性に比較的多く認めた.人種はアジア人に最も多く,20人であった.また,EBV陽性者は47人中20人であり,うちアジア人は本症例を含め9人,非アジア人は3人,国籍不明が8人であった.
Table 1
Reported cases of lymphoepithelioma-like carcinoma in the liver
|
|
n=47 |
| Age (years) |
|
61 (19–83) |
| Sex (M/F) |
|
17/30 |
| Tumor size (mm) |
|
37.5 (10–130) |
| 1st treatment |
surgery/chemotherapy |
47/0 |
| Ethnicity |
Asian/Caucasian/Hispanic/NA |
20/10/1/16 |
| HBV |
+/–/NA |
17/30/0 |
| HCV |
+/–/NA |
10/35/2 |
| EBV |
+/–/NA |
20/26/1 |
診断においては,画像所見ではLELCとして特異的な所見は呈さず,肝腫瘍として指摘はされるものの術前に確定診断に至った報告はない.そのため,原発性肝腫瘍や転移性肝腫瘍を疑われ全例で手術による切除が施行されていた.肺原発のLELCでは,FDG-PET/CTで高度集積を呈し診断に有用であったとする報告があるが39),補助診断としての位置付けと考えられる.また,肺原発のLELCでは気管支鏡下生検で診断が得られていることから術前診断を目的とした肝生検が考慮されるが,悪性腫瘍であった場合の播種のリスクに配慮する必要がある.
原発巣に対する治療に関しては手術による切除が第一選択になると考えられるが,局所切除か系統的切除のいずれが治療効果の点で優れているかは不明である.また,前縦隔原発や膀胱原発のLELCの原発巣に対して根治目的で放射線療法を行い良好な病勢コントロールを得ている報告があり40),肝原発においても有用な治療である可能性がある.
肝切除後の再発は47例中16例に認められた.術後のフォローアップ期間の中央値は20か月(1か月~108か月)であった(Table 2).
Table 2
Reported cases of lymphoepithelioma-like carcinoma in the liver
|
n=47 |
| Follow-up (month) |
20 (1–108) |
| Recurrence +/–/NA |
16/26/5 |
| Treatment for recurrence |
|
| chemotherapy |
5 |
| chemotherapy+radiotherapy |
2 |
| radiotherapy |
2 |
| surgery |
1 |
| observation |
3 |
| NA |
3 |
再発部位はリンパ節再発が8例,肝内再発が3例,肺転移が2例,脾臓転移が2例,不明が3例であり,リンパ行性に転移しやすい傾向が示唆された(Table 3).リンパ節再発部位は肝十二指腸間膜が4例,大動脈周囲が2例,後腹膜が2例であった.リンパ節再発の半数が肝十二指腸間膜内であることを考慮すると,肝十二指腸間膜内のリンパ節郭清が再発や予後の改善に寄与する可能性がある.
Table 3
Cases of recurrence of lymphoepithelioma-like carcinoma in the liver
| No. |
Author |
Year |
Age |
Sex |
EBV |
Treatment for recurrence |
Outcome |
Recurrence site |
No. of lesions |
FU (mo) |
OS (mo) |
RFS (mo) |
| 1 |
Hsu3) |
1996 |
47 |
F |
P |
N |
AWD |
Liver lung spleen rib |
NA |
21 |
21 |
8 |
| 2 |
Vortmeyer10) |
1998 |
71 |
F |
P |
CT |
AWD |
Liver lung spleen |
NA |
NA |
NA |
24 |
| 3 |
Ortiz12) |
2000 |
19 |
F |
P |
N |
DOD |
NA |
NA |
44 |
44 |
2 |
| 4 |
Jeng14) |
2001 |
47 |
F |
P |
N |
DOD |
NA |
NA |
48 |
48 |
8 |
| 5 |
Si16) |
2004 |
39 |
F |
P |
NA |
DOD |
Abdominal aorta |
multiple |
5 |
5 |
3 |
| 6 |
Chen17) |
2007 |
56 |
M |
N |
CT |
DOD |
Abdominal aorta |
multiple |
21 |
21 |
5 |
| 7 |
Shinoda22) |
2013 |
79 |
M |
N |
CT |
AWD |
NA |
NA |
20 |
|
6 |
| 8 |
Patel23) |
2014 |
74 |
F |
N |
NA |
DOD |
Retroperitorneal |
multiple |
24 |
24 |
NA |
| 9 |
Patel23) |
2014 |
78 |
M |
N |
NA |
AWD |
NA |
NA |
48 |
|
NA |
| 10 |
An24) |
2015 |
50 |
M |
N |
CT |
AWD |
Portal space |
multiple |
6 |
|
1 |
| 11 |
Shih33) |
2018 |
77 |
F |
N |
RT |
AWD |
Liver |
NA |
28 |
28 |
6 |
| 12 |
Zhang7) |
2018 |
63 |
F |
N |
CT+RT |
AWD |
Portal space |
NA |
60 |
|
12 |
| 13 |
Zhang7) |
2018 |
50 |
M |
N |
CT+RT |
DOD |
Retroperitoneal |
NA |
24 |
24 |
1 |
| 14 |
Qian37) |
2020 |
41 |
F |
P |
CT |
DOD |
NA |
multiple |
5 |
5 |
4 |
| 15 |
Our case |
|
83 |
F |
P |
RT |
AWD |
Portal space |
NA |
18 |
|
|
DOD: death of disease, AWD: alive with disease, NA: not available, N: negative, P: positive, FU: follow up, RT: radiation therapy, CT: chemotherapy, OS: overall survival, RFS: recurrence-free survival
再発巣に対する治療に対して定まった方針はなく,化学療法が5例,放射線療法が2例,化学療法と放射線療法の併用が2例,手術が1例,経過観察が3例,不明が3例であった.化学療法の薬剤選択はさまざまであり,5-fluorouracil,cisplatin,mitoxantroneを6か月間行った症例24)やoxaliplatin,tegafurgimeracilを3コース投与した後にpaclitaxel,cisplatinを3コース投与した症例37)など,腫瘍の縮小を得られた症例が報告されていた.ただし,化学療法の選択に関する根拠や基準についての記載は確認できず,また治療後のフォローアップ期間も短期にとどまるため,その有効性は不明である.肺原発,胃原発,乳腺原発のLELCではそれぞれ肺癌,胃癌,乳癌に準じた治療が報告されており4)5)41),肝原発LELCの場合はWHO分類に従って肝内胆管癌の化学療法に準じた治療も選択肢となりうる.本症例では再発巣に対して肝内胆管癌に準じてcisplatin+gemcitabineの投与が検討されていたが,高齢であったこと,腎機能障害があったこと,また患者が化学療法を希望しなかったことから放射線療法を選択した.放射線療法に関しては,既報でも再発巣に対して放射線療法で腫瘍の増大や再発なく術後6か月生存している症例もあり33),放射線療法が有効である可能性が示唆される.本症例でも再発巣に対する放射線療法終了後約6か月が経過しているが,腫瘍は消失し他に転移や再発所見は認めていない.
再発巣に対する切除は1例のみ行われていた.肝切除後に出現した下大静脈前面の単発のリンパ節再発に対して3年間の経過観察の後に切除がなされ,その後再発や転移なく経過しており,限局したリンパ節再発に対しては切除も選択肢となる可能性もある.
LELCは肝原発肝癌に比べ予後良好とする報告がある42).特に胃原発においてはEBV陽性のLELCは予後良好であり43),肝原発においても実際に再発後の治療により長期生存が得られている症例も少なくない.今後,症例が集積されることにより病態が明らかとなり治療法が確立されることに期待したい.
非常にまれな肝原発LELCの1例を経験したため報告した.
利益相反:なし
文献
- 1) Kijima Y, Hokita S, Takao S, Baba M, Natsugoe S, Yoshinaka H, et al. Epstein-Barr virus involvement is mainly restricted to lymphoepithelial type of gastric carcinoma among various epithelial neoplasms. J Med Virol. 2001;64(4):513–518.
- 2) Bégin LR, Eskandari J, Joncas J, Panasci L. Epstein-Barr virus related lymphoepithelioma-like carcinoma of lung. J Surg Oncol. 1987;36(4):280–283.
- 3) Hsu HC, Chen CC, Huang GT, Lee PH. Clonal Epstein-Barr virus associated cholangiocarcinoma with lymphoepithelioma-like component. Hum Pathol. 1996;27(8):848–850.
- 4) 古堅 智則, 平良 尚広, 伊地 隆晴, 久志 一朗, 饒平名 知史, 河崎 英範,ほか.高齢者に発症した肺原発リンパ上皮腫様癌の2例.国立沖縄病院医学雑誌.2017;37:35–38.
- 5) 松田 有希, 八谷 泰孝, 堀岡 宏平, 藤本 崇聡, 中本 充洋, 槇原 康亮,ほか.乳腺原発リンパ上皮腫様癌の1例.日本臨床外科学会雑誌.2020;81(10):1969–1974.
- 6) Solinas A, Calvisi DF. Lessons from rare tumors: hepatic lymphoepithelioma-like carcinomas. World J Gastroenterol. 2015;21(12):3472–3479.
- 7) Zhang JW, Yang HY, Xu YY, Sang XT, Yu SN, Huang HC, et al. Surgical treatment for metastasis from lymphoepithelioma-like cholangiocarcinoma in the liver: a case report. Medicine (Baltimore). 2018;97(19):e0666.
- 8) Weiss LM, Gaffey MJ, Shibata D. Lymphoepithelioma-like carcinoma and its relationship to Epstein-Barr virus. Am J Clin Pathol. 1991;96(2):156–158.
- 9) Han AJ, Xiong M, Gu YY, Lin SX, Xiong M. Lymphoepithelioma-like carcinoma of the lung with a better prognosis. A clinicopathologic study of 32 cases. Am J Clin Pathol. 2001;115(6):841–850.
- 10) Vortmeyer AO, Kingma DW, Fenton RG, Curti BD, Jaffe ES, Duray PH. Hepatobiliary lymphoepithelioma-like carcinoma associated with Epstein-Barr virus. Am J Clin Pathol. 1998;109(1):90–95.
- 11) Kim YB, Park YN, Han JY, Hong KC, Hwang TS. Biliary lymphoepithelioma-like carcinoma not associated with Epstein-Barr virus. Arch Pathol Lab Med. 1999;123(5):441–443.
- 12) Ortiz MR, Garijo G, Adrados M, López-Bonet E, Acero D, Bernadó L. Epstein-Barr virus-associated cholangiocarcinoma with lymphoepithelioma-like component. Int J Surg Pathol. 2000;8(4):347–351.
- 13) Chen TC, Ng KF, Kuo T. Intrahepatic cholangiocarcinoma with lymphoepithelioma-like component. Mod Pathol. 2001;14(5):527–532.
- 14) Jeng YM, Chen CL, Hsu HC. Lymphoepithelioma-like cholangiocarcinoma: an Epstein-Barr virus-associated tumor. Am J Surg Pathol. 2001;25(4):516–520.
- 15) Huang Y, Tsung JS, Lin CW, Cheng TY. Intrahepatic cholangiocarcinoma with lymphoepithelioma-like carcinoma component. Ann Clin Lab Sci. 2004;34(4):476–480.
- 16) Si MW, Thorson JA, Lauwers GY, DalCin P, Furman J. Hepatocellular lymphoepithelioma-like carcinoma associated with epstein barr virus: a hitherto unrecognized entity. Diagn Mol Pathol. 2004;13(3):183–189.
- 17) Chen CJ, Jeng LB, Huang SF. Lymphoepithelioma-like hepatocellular carcinoma. Chang Gung Med J. 2007;30(2):172–177.
- 18) Adachi S, Morimoto O, Kobayashi T. Lymphoepithelioma-like cholangiocarcinoma not associated with EBV. Pathol Int. 2008;58(1):69–74.
- 19) Nemolato S, Fanni D, Naccarato AG, Ravarino A, Bevilacqua G, Faa G. Lymphoepitelioma-like hepatocellular carcinoma: a case report and a review of the literature. World J Gastroenterol. 2008;14(29):4694–4696.
- 20) Henderson-Jackson E, Nasir NA, Hakam A, Nasir A, Coppola D. Primary mixed lymphoepithelioma-like carcinoma and intra-hepatic cholangiocarcinoma: a case report and review of literature. Int J Clin Exp Pathol. 2010;3(7):736–741.
- 21) Lee W. Intrahepatic lymphoepithelioma-like cholangiocarcinoma not associated with epstein-barr virus: a case report. Case Rep Oncol. 2011;4(1):68–73.
- 22) Shinoda M, Kadota Y, Tsujikawa H, Masugi Y, Itano O, Ueno A, et al. Lymphoepithelioma-like hepatocellular carcinoma: a case report and a review of the literature. World J Surg Oncol. 2013;11:97.
- 23) Patel KR, Liu TC, Vaccharajani N, Chapman WC, Brunt EM. Characterization of inflammatory (lymphoepithelioma-like) hepatocellular carcinoma: a study of 8 cases. Arch Pathol Lab Med. 2014;138(9):1193–1202.
- 24) An SL, Liu LG, Zheng YL, Rong WQ, Wu F, Wang LM, et al. Primary lymphoepithelioma-like hepatocellular carcinoma: report of a locally advanced case and review of literature. Int J Clin Exp Pathol. 2015;8(3):3282–3287.
- 25) Aosasa S, Maejima T, Kimura A, Nishiyama K, Edo H, Shinmoto H, et al. Intrahepatic cholangiocarcinoma with lymphoepithelioma-like carcinoma components not associated with Epstein-Barr virus: report of a case. Int Surg. 2015;100(4):689–695.
- 26) Cacciato Insilla A, Faviana P, Pollina LE, De Simone P, Coletti L, Filipponi F, et al. Lymphoepithelioma-like hepatocellular carcinoma: case report and review of the literature. World J Gastroenterol. 2015;21(36):10468–10474.
- 27) Lee SD, Chiu YL, Wu CS, Peng NJ. 18F-FDG PET/CT of liver lymphoepithelioma-like carcinoma. Clin Nucl Med. 2015;40(9):732–733.
- 28) Liao TC, Liu CA, Chiu NC, Yeh YC, Chiou YY. Lymphoepithelioma-like cholangiocarcinoma: a mimic of hepatocellular carcinoma on imaging features. World J Gastroenterol. 2015;21(13):4089–4095.
- 29) Wei J, Liu Q, Wang C, Yu S. Lymphoepithelioma-like hepatocellular carcinoma without Epstein-Barr virus infection: a case report and a review of the literature. Indian J Pathol Microbiol. 2015;58(4):550–553.
- 30) Miyasaka C, Ishida M, Ito H, Kaibori M, Uemura Y, Tsuta K. Lymphoepithelioma-like hepatocellular carcinoma: a case report with emphasis on the cytological features. Int J Clin Exp Pathol. 2017;10(7):7893–7897.
- 31) Wang JK, Jin YW, Hu HJ, Regmi P, Ma WJ, Yang Q, et al. Lymphoepithelioma-like hepatocellular carcinoma: a case report and brief review of literature. Medicine (Baltimore). 2017;96(51):e9416.
- 32) Filotico M, Moretti V, Floccari F, D’Amuri A. Very rare liver neoplasm: lymphoepithelioma-like (LEL) hepatocellular carcinoma. Case Rep Pathol. 2018;2018:2651716.
- 33) Shih EJ, Chau IY, Yeh YC, Chau GY. Synchronous hepatocellular carcinoma and lymphoepithelioma-like carcinoma arising from 2 different sites of the liver: a case report. Medicine (Baltimore). 2018;97(40):e12548.
- 34) Ding Y, Sun Z, You W, Zhang S, Chang C, Yan S, et al. Lymphoepithelioma-like intrahepatic cholangiocarcinoma with Epstein-Barr virus infection: report of a rare case. Ann Transl Med. 2019;7(18):497.
- 35) Gearty SV, Al Jurdi A, Pittman ME, Gupta R. An EBV+ lymphoepithelioma-like cholangiocarcinoma in a young woman with chronic hepatitis B. BMJ Case Rep. 2019;12(7):e229520.
- 36) Ling W, Lu C, Huang H, Qiu T, Lu Q, Huang C, et al. Ultrasonographic findings of intrahepatic lymphoepithelioma-like cholangiocarcinoma associated with Epstein-Barr virus: two cases report. Medicine (Baltimore). 2019;98(3):e14206.
- 37) Qian XH, Zhou DK, Wang WL. Surgical treatment of Epstein-Barr virus-associated lymphoepithelioma-like carcinoma occurring in both the posterior mediastinum and liver: case report. Medicine (Baltimore). 2020;99(52):e23610.
- 38) Zhang K, Tao C, Tao Z, Wu F, An S, Wu J, et al. Lymphoepithelioma-like carcinoma in liver not associated with Epstein-Barr virus: a report of 3 cases and literature review. Diagn Pathol. 2020;15(1):115.
- 39) Kim JW, Kim JH, Kim HM. Incidence and survival rates of lymphoepithelioma-like gastric carcinoma: analysis of the Korea Central Cancer Registry Database. Scand J Gastroenterol. 2021;56(10):1182–1186.
- 40) Kozyrakis D, Petraki C, Prombonas I, Grigorakis A, Kanellis G, Malovrouvas D. Lymphoepithelioma-like bladder cancer: clinicopathologic study of six cases. Int J Urol. 2011;18(10):731–734.
- 41) 田村 淳, 北口 和彦, 平良 薫, 馬場 信雄.S-1+CDDPによる術前化学療法にて組織学的CRが得られた胃髄様癌の1例.日本臨床外科学会雑誌.2009;70(4):1071–1076.
- 42) Labgaa I, Stueck A, Ward SC. Lymphoepithelioma-like carcinoma in liver. Am J Pathol. 2017;187(7):1438–1444.
- 43) Cheng N, Hui DY, Liu Y, Zhang NN, Jiang Y, Han J, et al. Is gastric lymphoepithelioma-like carcinoma a special subtype of EBV-associated gastric carcinoma? New insight based on clinicopathological features and EBV genome polymorphisms. Gastric Cancer. 2015;18(2):246–255.