2020 年 15 巻 3 号 p. 199-204
2020 年 15 巻 3 号 p. 199-204
【緒言】血管内大細胞型B細胞リンパ腫が疑われた患者が過活動型せん妄を呈し,ステロイド投与が過活動型せん妄に有効であった1例を経験したので報告する.【症例】67歳男性.発熱と貧血,高LDH血症を認め,精査中に,過活動型せん妄をきたした.抗精神病薬のみでは症状緩和が困難であった.血管内大細胞型B細胞リンパ腫による微小血管閉塞がせん妄の直接因子となっていることが強く疑われたため,骨髄検査と皮膚生検を施行したうえで,プレドニゾロンを増量したところ,速やかに症状が改善した.【考察】血管内大細胞型B細胞リンパ腫の症例においては,微小血管梗塞や中枢神経病変といった原病によるせん妄に対し,ステロイド投与が症状緩和に寄与する可能性がある.
血管内大細胞型B細胞リンパ腫(intravascular large B-cell lymphoma: IVLBCL)は非ホジキンリンパ腫の一種で,びまん性大細胞型B細胞リンパ腫の亜型であり,さまざまな臓器の中小の血管内腔に選択的に大型の腫瘍細胞が増殖する疾患である1).侵された臓器により多彩な臨床像を呈し,約20〜40%の症例で診断時に認知機能障害や麻痺,けいれんといった中枢神経症状を認める2〜4).2016年に報告されたメタアナリシスでは,中枢神経症状のなかで,61%の症例で認知機能障害を認め,四肢麻痺は22%,けいれんが13%の症例で出現し,認知機能障害が最も多いことが報告されている2).中枢神経症状は,腫瘍細胞による微小血管障害による虚血性変化によって引き起こされ,脳MRI上拡散強調画像で異常信号を呈する5).本症例では,臨床症状や検査所見からIVLBCLが強く疑われたが,診断前に過活動型せん妄の悪化を認めた.抗精神病薬の効果が乏しく,IVLBCLへの治療としてステロイドを増量したところ速やかに反応し,せん妄症状が改善した症例を経験したため報告する.
【症 例】67歳男性
【主 訴】入眠困難,幻覚,焦燥感
【既往歴】胃潰瘍穿孔に対して胃部分切除術後
【家族歴】特記すべきことなし
【現病歴】2017年2月に全身性のけいれん発作を認め,当院に救急搬送され,同日に精査加療目的に,内科に入院となった.入院時の頭部MRIでは明らかな異常所見を認めなかった.熱源が不明の38℃台の発熱が続き,白血球数3400/μl,赤血球数256万/μl,ヘモグロビン(以下Hb)濃度7.0 g/dl,血小板数15.0万/μlと貧血,軽度白血球減少を認め,LDH 535.0 U/L(施設基準値上限229.0 U/L)と高LDH血症を呈していたため,血液疾患を疑われ3月に血液内科に紹介となり,骨髄検査および皮膚生検を施行した.骨髄のスメア標本上,リンパ腫細胞の浸潤を疑う所見を認めた.IVLBCLが強く疑われ,プレドニゾロン15 mg/日を開始した.しかし,ステロイド投与前に提出した骨髄病理検査および皮膚生検の病理検査では腫瘍細胞を同定できなかった.ステロイド投与により解熱し,白血球数9100/μl,Hb 11.3/dlと白血球減少,貧血の改善を認めたものの,診断が困難であったため,4月上旬よりプレドニゾロンを漸減し,4月下旬に5 mg/日まで減量したところ,38℃台の発熱を認めた.骨髄検査と皮膚生検を再度施行したが,腫瘍細胞を同定できなかった.頭部MRIを再検査したところ,拡散強調画像で右頭頂葉皮質下白質にスポット状の高信号域を認めた.2回目の骨髄検査,皮膚生検でも腫瘍細胞が同定できなかったため,5月上旬に3回目の骨髄検査と皮膚生検を施行した.38℃台の発熱が持続し,Hb 8.5 g/dlと貧血も再度認めるようになった.5月下旬,妄想,注意障害,幻覚,入眠障害,運動活動量の増加を認め,過活動型せん妄と診断した.
【臨床所見】(緩和ケアチーム介入時)[理学所見]体温37.9℃,血圧 98/72 mmHg,脈拍113/分,胸部 呼吸音清,腹部平坦軟,腸蠕動音亢進.[神経学的所見]意識 JCS I-2,GCS E4V4M5,見当識障害,幻覚,錯覚,妄想を認める.視線は合うが持続しない.眼球運動障害なし,顔面神経麻痺なし,構音障害なし,四肢麻痺なし,感覚障害は評価困難.[血液検査所見]白血球数 7000/μl, 赤血球数283万/μl, Hb 7.9 g/dl, 血小板数14.0万/μl, TP 5.5 g/dl, alb 2.7 g/dl, AST 24.1 IU/l, ALT 23.2 IU/l, ALP 589.0 IU/l, γ-GTP 233.6 IU/l, T-bil 0.6 mg/dl, LDH 703.5 IU/l, BUN 24.4 mg/dl, Cr 0.87 mg/dl, Na 133.7 mEq/l, K 4.4 mEq/l, Cl 99.3 mEq/l, Ca 8.7 mg/dl, 補正Ca 10.0 mg/dl, CRP 4.27 mg/dl. [画像所見]頭部MRI:拡散強調画像で左小脳半球や脳梁膨大部,左前頭深部白質にスポット状の高信号域を認める.
【臨床経過】過活動型せん妄に対し,クエチアピン25 mgを開始したところ,4時間の睡眠を確保できた.(せん妄発症日を第0病日とする.)点滴の自己抜針もあり,点滴持続静注は困難となった.第1病日,39℃台の発熱を認めた.3回目の骨髄検査,皮膚生検の結果が判明し,リンパ腫の診断には至らなかったため,同日,4回目の骨髄穿刺,骨髄生検,皮膚生検を実施した.また,頭部MRIの拡散強調画像において,血管支配に一致しない高信号域が散在し,4月と比較して増加していた(図1,付録図1).リスペリドン0.5 mg夕食後,クエチアピン定期50 mg眠前および頓用1回25 mgを2回,計100 mg用いてもほとんど睡眠を確保できなかったため,その翌日に緩和ケアチーム依頼となった.第2病日,緩和ケアチーム介入時には,見当識障害,幻覚・妄想,焦燥感を認めた.Memorial Delirium Assessment Scale(MDAS)は21点であった6).胆道系酵素の軽度上昇は認めるものの総ビリルビンは基準範囲内であり,貧血や電解質異常,腎機能障害や肝酵素の上昇は認めず,いずれもせん妄の直接因子とは考えられなかった.プレドニゾロンは5 mg/日に減量しており,15 mg/日を内服している際にもせん妄をきたしておらず,直接因子から除外した.プレドニゾロン以外の内服薬はプロトンポンプ阻害薬と抗真菌剤,スルファメトキサゾール・トリメトプリムであり,直前の2カ月間で投薬内容に変化なく,せん妄の要因としては除外した.IVLBCLによる微小血管閉塞がせん妄の直接因子となっていることが強く疑われた.また,4月下旬から持続した発熱を認めており,せん妄の促進因子であると推測した.IVLBCLとの病理結果は得られていなかったため,抗がん剤の投与は控えるべきであると判断し,悪性リンパ腫の治療において通常用いるレジメンで使用されるプレドニゾロンの量を参考にして,同日のプレドニゾロンを55 mg/日(=1 mg/kg/日)に増量したところ,同日午後には焦燥感の軽減を認めた.夕食後のリスペリドンを1 mgに増量したうえで,ベンゾジアゼピン受容体作動薬を併用することとした.以前用いて問題のなかったロルメタゼパム 1 mgを眠前内服としたところ,同日より夜間睡眠を確保することができた.第3病日以降は解熱し,焦燥感,幻覚は徐々に改善した.第5病日には日中の眠気や嚥下困難を認め,抗精神病薬を漸減したが,過活動型せん妄の悪化は認めなかった(図2).抗精神病薬の減量により,嚥下困難は改善した.第6病日,LDHが439.2 U/Lと第0病日の703.5 U/Lと比較して,低下傾向となっており,ステロイド増量による抗腫瘍効果が得られていると判断した.4回目の骨髄穿刺の病理所見で,CD20陽性の腫瘍細胞浸潤が明らかとなり,臨床像と合わせて,IVLBCLと診断できたため(図3),第9病日にCHOP療法へ移行した.同日,抗がん剤の髄腔内投与時に髄液検査を施行した.髄液中の細胞数の増加は認めず,髄液細胞診は陰性であった.化学療法施行後,意識レベル清明となり,第14病日よりクエチアピンを中止としたが,せん妄の悪化なく経過した.第24病日にリツキシマブを投与した.第23病日に自宅退院し,外来でR-CHOP療法および抗がん剤の髄腔内投与を継続し完全寛解に到達した.頭部MRI上も拡散強調画像においてスポット状の高信号域は消失し,認知機能は回復した.治療終了後,せん妄の再発は認めず,外来で無治療経過観察中である.
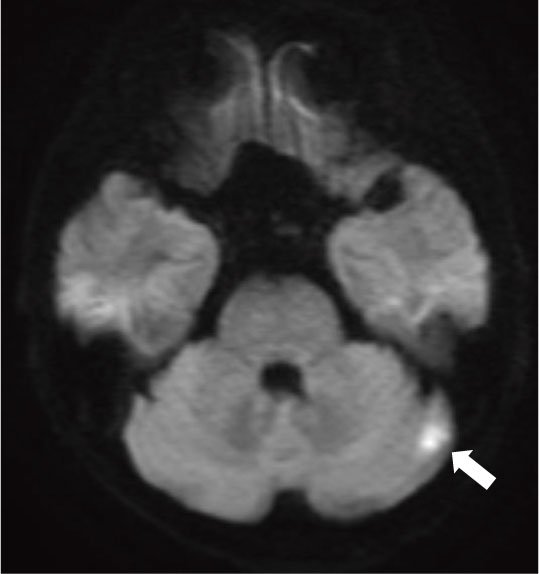
小脳半球や左前頭葉深部大脳白質,脳梁膨大部に拡散強調画像で高信号域が出現した.
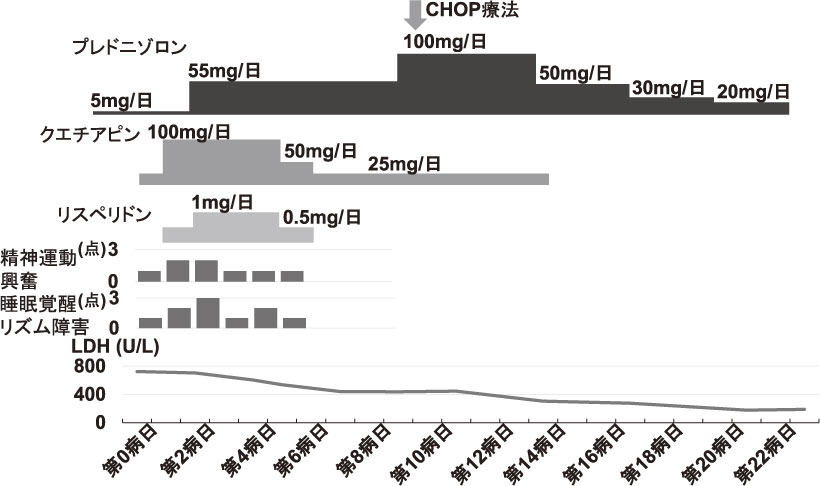
せん妄発症日を第0病日とした.クエチアピンを増量しても,せん妄の改善を認めなかったが,プレドニゾロンを増量したところ,せん妄は改善し,睡眠を確保できた.睡眠覚醒リズム障害と精神運動興奮はMDASの項目に基づいて点数化した6).
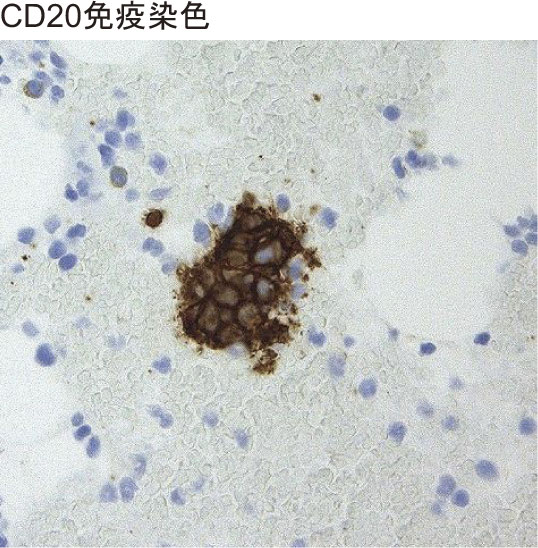
免疫染色で一部にCD20陽性大型異型Bリンパ球が集簇する像を散在性に認めた,IVLBCLの所見.
本症例は,IVLBCLによる微小血管障害が直接因子となって過活動型せん妄を認め,抗精神病薬によって症状緩和が困難であったが,ステロイド投与量の増量によりせん妄が改善し,リツキシマブを含む化学療法で寛解を得た.
本症例では,頭部MRI上多発小梗塞を疑う所見を認め,せん妄の出現とともに増加していた.脳内の血管内腔にリンパ腫細胞が増殖し,微小血管障害を引き起こし,せん妄の直接因子となっていると考えられた.3週間にわたり,発熱が持続しており,せん妄の促進因子であると考えた.プレドニゾロン5 mg/日を内服中であり,プレドニゾロンがせん妄の直接因子となっている可能性についても検討したが,すでに2カ月にわたり投与されており,15 mg/日内服時にもせん妄を呈していなかったため,ステロイドは直接因子ではないと考えた.ステロイド投与により,睡眠障害をやせん妄を引き起こすため7,8),抗精神病薬を投与しても症状緩和が困難な過活動型せん妄を呈していた本症例において,ステロイドの増量はせん妄を悪化させることが懸念された.しかし,本症例ではIVLBCLが強く疑われたが,確定診断が得られる前であり,抗がん剤治療が困難であったため,ほかに有効な治療選択肢がなく,ステロイドの増量を行ったところ奏功した.
ステロイドは非ホジキンリンパ腫に対して抗腫瘍効果を有し,初発,再発を問わず多くの治療レジメンにステロイドが含まれている9).初回治療のステロイドの量はレジメンによって異なるが,通常のレジメンではプレドニゾロン100 mg/日を5日間投与し,高齢者を対象としたレジメンではプレドニゾロン40 mg/m2/日を5日間用いる10,11).日常診療において,全身状態が不良で化学療法の実施が困難な非ホジキンリンパ腫の症例に対し,プレドニゾロンを先行投与し,全身状態が改善し,化学療法が実施可能となることはしばしば経験する.抗腫瘍効果を期待したプレドニゾロンの投与量としては,全身状態や患者の背景も踏まえ,1 mg/kg/日から100 mg/日を投与することが多い.本症例においては5 mg/日から55 mg/日(=1 mg/kg/日)にプレドニゾロンを増量することでIVBCLに対する治療効果を得られ,せん妄の改善につながった.また,ステロイド投与により解熱したことも,せん妄の改善に寄与したと考えられる.未治療のIVLBCLの患者がせん妄を合併していた場合に,ステロイドの投与が困難と結論づける必要はなく,症状緩和の治療選択肢となり得ることが示唆された.
IVLBCLは診断が困難な疾患であり,以前の報告では,症例の半数は死後,剖検で診断された12).しかし,疾患の認識が広まり,骨髄生検やランダム皮膚生検といった診断技術の進歩により,生前診断が可能となってきている13,14).また,CD20モノクローナル抗体であるリツキシマブの導入により,導入以前と比較してIVLBCL長期予後の改善を認めている3,15).IVLBCLはステロイドのみでは長期の腫瘍制御は困難であり,リツキシマブを含む化学療法の実施が必須である.本症例においても,ステロイド増量によってせん妄が改善し,IVLBCLの病理診断確定後にリツキシマブを含む化学療法に移行し,完全寛解に到達,認知機能も回復し,2年以上にわたり寛解を維持することができた.
IVLBCLによる過活動型せん妄に対して,抗精神病薬での症状コントロールが困難であったが,ステロイド増量によって症状を軽減し,安全に化学療法を施行することが可能であった症例を経験した.IVLBCLによるせん妄に対し,ステロイド投与が抗腫瘍効果による症状緩和に寄与する可能性が示唆された.
著者の申告すべき利益相反なし
木原は研究の構想,デザイン,研究データの収集,分析,解釈,原稿の起草に貢献;藤野は研究データの収集,分析,研究データの解釈,原稿の内容に関わる批判的な推敲に貢献;山添,浅井,足立,桒原,佐部利,小田切,綿本,渡邊は研究データの解釈,原稿の内容に関わる批判的な推敲に貢献した.すべての著者は投稿論文ならびに出版原稿の最終承認,および研究の説明責任に同意した.