小児骨髄炎の画像診断は,単純X線写真,次にMRIが第一選択であり,骨髄炎の存在診断および広がり診断,デブリドマンを必要とする膿瘍の有無,骨端線をこえる病変など成長障害リスク因子の評価,血栓症など随伴合併症の有無の判断が求められる.そのために発達過程の骨の解剖学的・生理学的特性を理解し,年齢に応じたMRIプロトコールの組み立てが望まれる.読影におけるポイントとしてブドウ球菌等の急性細菌性骨髄炎とマイコバクテリウム等の弱毒菌による画像所見の差異,亜急性・慢性骨髄炎の画像所見を述べる.小児の骨髄炎では晩期合併症としての成長障害が大きな問題となるため,的確な早期診断が望まれる.
Radiographs followed by magnetic resonance imaging (MRI) are the first-choice modality for pediatric osteomyelitis imaging. Imaging aims to diagnose the presence and extent of osteomyelitis, assess the need for debridement of abscesses, evaluate risk factors, such as lesions extending the growth plate that may lead to growth disturbances, and determine the presence of complications, such as thrombosis and ischemia. It is essential to understand the anatomical and physiological characteristics of developing bones and tailor MRI protocols according to age. Key points in image interpretation include the differences between acute bacterial osteomyelitis, such as that caused by staphylococcus, and osteomyelitis caused by low-virulence bacteria, such as mycobacterium, as well as imaging features of subacute and chronic osteomyelitis. Growth disturbances as late complications are a significant concern in pediatric osteomyelitis, highlighting the need for an accurate early diagnosis.
感染症の画像診断における役割として,1.非侵襲的かつ迅速な存在診断,2.炎症,感染部位の特定,3.広がり診断,4.合併症の検出,5.起因菌の推定,6.治療効果判定の6つがあげられる.前提として,感染症における画像は,生体の免疫システムの反応の結果として表現されていることを念頭におく必要があり,患者の免疫状態の情報が有用となる.小児骨軟部感染症は,骨髄炎,軟部組織感染,関節炎の大きく3つに分類され,単純X線撮影,超音波,MRIを適宜組み合わせて画像検査を行う1).本項では,その中でも治療方針決定に大きな影響を与える骨髄炎にフォーカスをして述べる.
小児骨軟部感染症は,発達過程の骨の解剖学的・組織学的特性,生理的な免疫システムの未熟性,臨床症状の非特異性ゆえに,成人より臨床診断はしばしば難しい.米国の小児感染症学会の2021年のガイドラインでは,急性骨髄炎の発生率は年間に10万人あたり1.2–13件と報告されている2).また,モダリティの第一選択は単純X線写真,次にMRIとされ,MRIはCT,超音波検査,シンチグラフィと比較して診断精度が優れると述べられている.臨床的には,若年性特発性関節炎,非感染性骨髄炎などのリウマチ性疾患,転移性骨腫瘍や血液腫瘍の骨浸潤など腫瘍性疾患としばしば症状が類似する.壊血病などの代謝性骨疾患も骨関節症状が前面に出ると,“骨髄炎疑い”と臨床診断されることもある.骨髄炎の画像診断は,まずこれらの疾患との鑑別,その他に起因菌の推定,炎症波及の範囲やデブリドマンを必要とする膿瘍の有無,骨端病変など成長障害リスク因子の評価,血栓症など随伴合併症の有無の判断が求められる.それらの評価が可能なMRIプロトコールの組み立ても重要な課題である.
小児の骨髄炎は長管骨では骨幹端に好発する.内軟骨性骨化が生じる長管骨骨幹端では血流が非常に豊富で,かつ終末動脈網に血流の停滞が生じやすいという解剖学的な特性がある3).扁平骨においては,同様の解剖学的特性をもつ骨幹端相当(metaphyseal equivalent)と呼ばれる部位,すなわち仙腸関節や坐骨結節,腸骨稜などに骨髄炎が好発する4,5)(Fig. 1).小児骨髄炎では骨幹端あるいは骨幹端相当から,隣接する軟部組織,骨膜下,骨幹方向の髄内,隣接する成長板から骨端や関節腔内へと炎症波及する6).年齢とともに,“菌血症からの骨髄炎”が,“外傷・軟部組織感染からの骨髄炎”へと主病因が変化していく.成長発達中の骨膜はcambiumと呼ばれる血流の多い内層と,強靭な線維層である外層の2層に分かれており,この2層の間の潜在腔へ炎症波及すると骨膜下膿瘍を形成する(Fig. 2).骨膜は長管骨の血流供給に重要であり,大きな骨膜下膿瘍が存在すると,骨への血流が阻害され虚血を引き起こすことがある7).骨内虚血病巣は成長障害および慢性骨髄炎へのリスクとなり重要な画像所見である8).

左仙腸関節部にT1WIで低信号,STIRで高信号を呈する領域があり(矢印),仙腸関節部前面から腸骨筋にそった浮腫性変化を伴い(矢頭),感染性の仙腸関節炎に矛盾しない所見である.

大腿骨骨幹端部に骨髄炎に伴うT1WIで低信号,STIRで高信号を呈する領域が広がり,背側に骨膜下膿瘍(矢印)を認める.
骨幹端と骨端の血流供給には年齢による解剖学的差異がある.1歳6か月までは骨端と骨幹端の間を貫通する血管が存在しており,同年齢では骨幹端に生じた感染が同血管を介して骨端に直接,炎症波及が生じる(Fig. 3).1歳6か月をすぎると,この骨端と骨幹端の間を貫通する血管に退縮が生じるが,およそ5歳までは骨幹端の炎症は骨端に波及しうる.5歳をすぎ成長板が閉鎖するまでは若年層と同様に成長板への終末血管が存在するが,その後,終末血管が退縮し,成人と同様の病態生理となる.

大腿骨遠位骨端核にT1WIで低信号,STIRで高信号を呈する領域がみられ(黄矢印),関節液の増量(赤矢印)を伴う.
脊椎についても少し触れる.椎体終板の血管供給網の差異があり,成人と小児で広がり方が異なる.新生児では椎間板の血流が豊富であるため感染はまず椎間板におよび,その後椎体終板に進展する一方,成人では一つの同じ分節動脈から隣接する上下2つの椎体終板に血管が供給されるため,椎体終板から炎症が始まり,その後椎間板に感染が広がり,さらに下方の椎体終板にも広がるパターンを呈する9).感染性脊椎炎は成人でも小児でも菌血症を背景に血行性に生じることが多く腰椎が好発部位である10).
生理的な赤色髄から脂肪髄への発達過程を述べる.新生児の骨髄はほぼ全てが赤色髄であり,水分含有量が多く,脂肪含有量が極めて少ない.その後,成長に伴い全身においては末梢から中枢に向かって骨髄の転換が始まり,成人初期に脊椎の黄色髄化で完了する.長管骨の脂肪髄化は骨端から始まる.単純X線撮影で骨端の二次骨化中心出現後,約半年で同部位の脂肪髄化が生じる.次に骨幹が転換され,両骨端方向へと進行し,最後に骨幹端から骨端線が脂肪髄化して終了となる11).
骨髄炎の評価に必須のMRIシーケンスはT1強調画像とfluid-sensitiveシーケンス(脂肪抑制T2強調画像やSTIR像)である.骨髄炎では浮腫を反映して前者で低信号,後者で高信号を呈するが,正常な造血髄(赤色髄)も水分含有量が多く,同様の信号強度を呈する.したがって,上述した赤色髄の分布を意識したMRIの読影が極めて重要である12).ただし実際は,不均一な赤色髄の残存や個体差,時に左右差もあり,赤色髄の信号か炎症による信号変化を見ているか判断に迷うことは多々ある.
乳児期以降の造血髄は,正常では4割近い脂肪を含んでいるため,T1強調画像で筋肉より若干高信号を呈する.これはT1強調画像で筋肉よりも低信号を呈する骨髄炎との鑑別に有用である6).しかし新生児では赤色髄の脂肪含有はさらに少なく,骨髄の信号のみから炎症の有無を評価するのは困難である.骨髄炎が存在すれば隣接する脂肪や筋肉など周囲軟部組織の炎症性変化を伴うことが一般であるため,新生児や乳児のfluid-sensitiveシーケンスにおいて,軟部組織のわずかな浮腫性変化の広がりのみが骨や骨化前の軟骨感染の可能性を示唆する唯一の手がかりとなりえる(Fig. 4).このような時期には超音波検査の有用性が特に高く,膿瘍を含む骨化前の軟骨病巣の検出に優れる(Fig. 5).
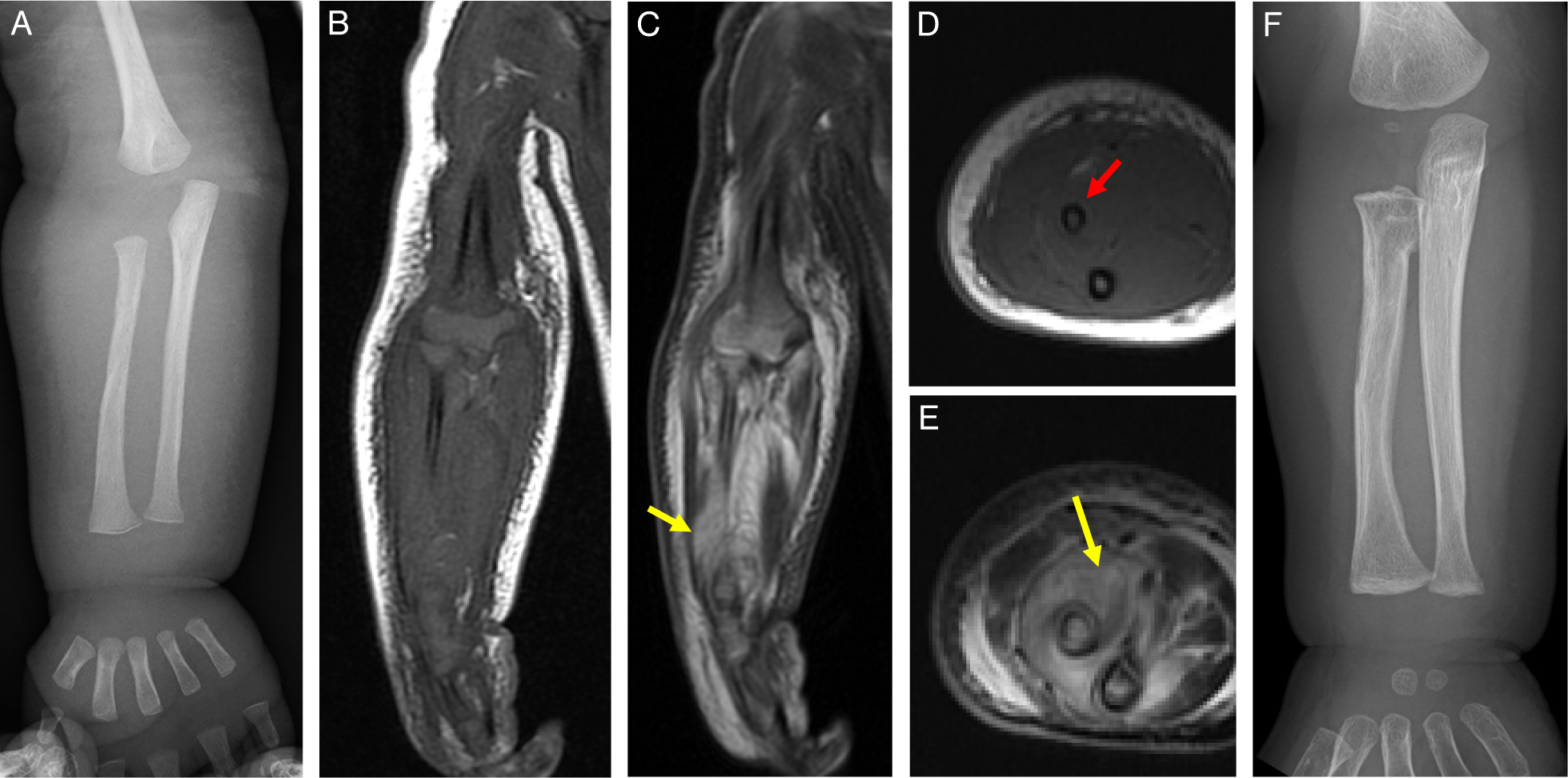
(A)単純X線撮影で明らかな異常を指摘できない.(B–E)同時期は全身の骨髄が赤色髄であるため,STIRだけでは存在診断も広がり診断も困難であるが,軟部組織の浮腫性変化(黄矢印)とT1WIでの橈骨骨髄内の信号強度が尺骨と比して低く,かつ筋肉よりも低信号を呈していることが髄内の異常信号をとらえる手がかりになる(赤矢印).(F)1年後の単純X線撮影で橈骨近位骨幹端から骨幹にかけて変形とリモデリングが見られ,広範な骨髄炎後の所見である.

(A–C)左膝関節部周囲の皮下軟部組織に浮腫性変化と考えるSTIRで高信号を呈する領域が見られる(赤矢印).骨端軟骨部はSTIRで生理的な信号上昇により病変がマスクされ,対側と比較しても骨内の炎症巣は同定困難である.(D)超音波検査では左大腿骨骨端軟骨に骨内膿瘍を考える高輝度領域が見られる(黄矢印).
造影剤の使用に関しては議論があるが,新生児と乳児においては造影剤を用いた検査が推奨される7).新生児・乳児期は前述した正常な赤色髄の水分含有量が高く,骨髄炎で見られる浮腫性変化がマスクされてしまい,単純MRIでは診断できない骨端軟骨部の感染を含む骨髄炎が造影剤使用で可視化しうる.未骨化の骨端軟骨は,造影では軟骨内の血管が明瞭に描出され,実質は相対的に造影効果は乏しく見えるものの,基本的に造影される.したがって健側比較のために,両側が撮像範囲に含まれる方が良い.ただし,感染巣が虚血のために局所的あるいは全体的な造影欠損として見られることがある点については注意が必要である.年長児以降については造影剤を追加しても骨髄炎の診断能は本質的にはかわらないとされる13).ただし,膿瘍のような合併症評価や読影者の診断確信度向上には造影が有用との報告があり,少なくとも造影前の画像で異常信号が見られる場合に造影剤投与を考慮されても良い.年長児以降でも新生児と同様に,骨の虚血があると造影効果の減弱や欠損が見られる.広範な虚血は抗菌剤の治療効果が低下し,慢性骨髄炎への移行や病的骨折などの合併症リスクが高まり重要な予後因子となる14).
追加シーケンスとして,水の拡散性に関する情報を提供し,膿瘍や腫瘍の定性・定量診断に有用である拡散強調画像(DWI)が骨髄炎診断の一助になりえる.骨髄炎疑いの時には我々は追加しており,微小膿瘍の診断でしばしば有用であることを経験してきた(Fig. 6).しかし,新生児・乳児で問題となる赤色髄は富細胞性であり拡散能は制限されるため,その月齢における骨髄炎による骨内膿瘍や腫瘍性病変との鑑別には限界もある12,15).

大腿骨骨幹端外側に骨髄炎と考えるT1WIで低信号,STIRで高信号を呈する領域がみられ(赤矢印),辺縁に微小膿瘍を考える拡散制限を伴う(黄矢印).
広範囲撮像か,局所撮像にするか,撮像視野(field of view; FOV)の設定には議論があり容易ではない.1歳6か月未満では体格が小さいため,全身の冠状断を1–2回で撮像が可能であること,臨床的に正確な感染部位を同定するのが困難であることから,大きなFOVで広範囲をfluid-sensitiveシーケンスの冠状断を用いて最初に撮像するのが良い.利点は多発骨髄炎の特定と合併症の検出が可能であること,腫瘍性病変などの他の病態の鑑別に有用であること,片側性や限局性の病巣の場合,他の正常造血髄をコントロールとして比較できることがあげられる16).1歳6か月以上5歳未満においては,大きなFOVで広範囲のfluid-sensitiveシーケンスでの撮像は有用であるが,小児のサイズによっては2–3回の撮像ステーションが必要になることもあり,ケースに応じて使い分ける必要がある.75%の感染は骨盤や下肢に存在するという事実からは骨盤から足をカバーしたFOVでfluid-sensitiveシーケンスの冠状断を一つ含めておくのが有用かもしれない6).5歳以上では症状の局在診断が可能であり,体格が大きいことからも広範囲撮像の有用性は低下し,局所撮像が基本である.骨髄炎に関節炎の合併がしばしばあるため,目的部位に隣接する関節までを含む撮像範囲が推奨である17).
単純X線撮影では最も早期には隣接する軟部組織の腫脹が見られ,脂肪層の変化や関節液貯留を描出できることがある一方,骨内の変化を捉えるのは難しい.小児では発症から約1週間程度で骨吸収,骨膜変化,骨侵食/破壊が顕在化する.MRIは感染後1–2日程度で画像所見を検出しうる.上述した骨髄浮腫が初期の兆候であり,経過とともに骨侵食/骨破壊や膿瘍が検出可能である.感染性脊椎炎では椎間板の液体貯留,傍脊椎組織や硬膜外の炎症所見,椎体の骨侵食や破壊像が観察される(Fig. 7).

(A)CTでは第10胸椎の前方隅角から椎体にかけて溶骨性病変がみられる(黄矢印).(B–D)MRIでは第10胸椎全体の骨髄浮腫と椎体前面の膿瘍が描出される(赤矢印).
骨髄炎で見られる有用な画像所見・サインがある.一つめは,膿瘍や骨髄炎病巣内に見られうるT1強調画像で高信号を呈する小さな球状の脂肪成分(fat globule)である18).成因については明らかではないが,骨髄内圧の上昇により虚血を生じ,脂肪細胞が脂肪成分を放出するという説が考えられている.二つめは,penumbraサインである19)(Fig. 8).T1強調画像で骨内病巣の辺縁が相対的に高信号のrimで覆われる画像所見である.肉芽組織を反映したもので,骨軟部感染症に特徴的であり,いずれのサインも腫瘍との鑑別に有用である.

(A)単純X線撮影では,脛骨遠位骨幹端に透亮像があり,周囲には硬化巣を伴う(赤矢印).(B–E)MRIでは単純X線撮影の硬化巣に一致した低信号があり(黄矢印),周囲には浮腫性変化が広がる(黄矢印).拡散強調画像において膿瘍を示唆する拡散制限を伴う(矢頭).
急性細菌性骨髄炎はブドウ球菌によるものが頻度的に高いが,鑑別にマイコバクテリウムをはじめとする弱毒菌による骨髄炎がある.臨床症状に大きな差があるが,画像所見についても差異が知られている.急性細菌性骨髄炎では初回の単純X線撮影では異常がないことが多い.我々の検討では急性細菌性骨髄炎40例中6例(15%)にのみしか溶骨が見られず,溶骨があっても非常に小さな範囲であった20).一方でマイコバクテリムなど弱毒菌による骨髄炎では初回の単純X線写真でしばしば明瞭な溶骨像が認められ,細菌性骨髄炎と比較して,周囲の(反応性)浮腫性変化が乏しい割に大きな膿瘍を形成することが特徴であり,cold abscessと言われる特徴を示す(Fig. 9).これらは,病原体の強さによる発症から来院までの時間経過の差を反映したものと考えられる.小児,特に2歳以下で弱毒菌による骨髄炎を示唆する所見が認められる場合にはBCGによる骨髄炎(画像所見は結核性骨髄炎に準ずる)の可能性を忘れてはならない.また多発例では免疫不全症の可能性も考慮する必要がある.Brodie膿瘍は,初期の急性感染を排除しきれず,細菌の毒性よりも宿主の防御反応が相対的に勝っている場合に生じる亜急性ないし慢性骨髄炎である.長管骨の骨幹端に好発し,ブドウ球菌が起因菌として多い.単純X線写真では,周囲に反応性の骨硬化像を伴う透亮像を示し,MRIでは上述したPenumbraサインが特徴である(Fig. 8)21).慢性骨髄炎は感染症状が6か月以上続くものであるが,以下に述べる腐骨が細菌の温床となるため,保存的治療での根治は難しい.骨内感染巣で骨破壊が進むと,骨組織が壊死に陥るが,破骨細胞に吸収されず,周囲の生きた骨と肉芽組織により隔離されて腐骨となる.腐骨を包含する膿瘍の周りには骨柩と呼ばれる反応性の骨形成を生じる.感染が持続すると,骨柩にはcloacaと言われる開口部が生じ,皮膚に瘻孔(sinus tract)が形成され,持続的に膿瘍が排出されるようになる.この腐骨,骨柩,瘻孔が慢性骨髄炎の特徴的な画像所見である22).慢性骨髄炎への移行リスクに急性感染時における初回造影MRIでのサブトラクション画像による骨内虚血病巣の検出が有用とされる8).

胸骨の骨破壊および骨外にまで広がる膿瘍が見られるが(黄矢印),骨髄を含めた周囲の浮腫性変化に乏しい.DWI/ADC mapにて拡散制限があり,膿瘍であることが示唆される(赤矢印).
骨髄炎の鑑別に悪性腫瘍が時に問題となる.骨髄炎では,骨髄信号の正常と異常の境界部においてT1強調画像で境界不明瞭な広がりを示すのに対して,悪性腫瘍では明確な移行が見られる.またDWIでは骨髄炎は,悪性腫瘍と比較して,拡散係数(apparent diffusion coefficient; ADC)が高くなる傾向があり鑑別に有用になりうる.ただし,両者のADC値に顕著なオーバーラップがあり,カットオフ値で鑑別するのは難しいとの報告もあり,コンセンサスは得られていない.もう一つの追加シーケンスとしては微量な脂肪を検出できるchemical shift imagingがある.年長児以降では骨髄炎と腫瘍を区別するのに有用となり得るが,前述した赤色髄のため,新生児・乳児については非常に限定的である15).
小児骨軟部感染症の画像診断について,骨髄炎のMRIを中心に概説した.成長発達過程に伴う骨髄信号の生理的変化と解剖学的特性の理解が重要であり,それを踏まえた上で,年齢区分毎の撮像や読影におけるピットフォールと,MRIの基本的事項を押さえる必要がある.小児の骨髄炎では晩期合併症として成長障害があり,早期治療のためにも的確に早期診断を行うように心がけたい.