- |<
- <
- 1
- >
- >|
-
山口 庄太郎2022 年 60 巻 6 号 p. 263
発行日: 2022/06/01
公開日: 2023/06/01
ジャーナル フリーPDF形式でダウンロード (482K)
-
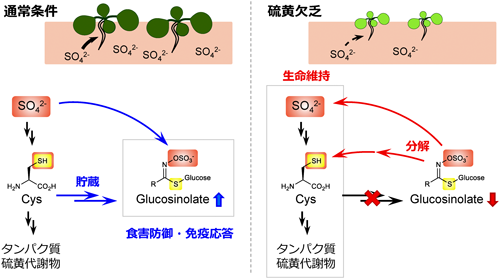
防御物質グルコシノレートは硫黄の栄養源として再利用される杉山 龍介, 平井 優美2022 年 60 巻 6 号 p. 264-266
発行日: 2022/06/01
公開日: 2023/06/01
ジャーナル フリーPDF形式でダウンロード (1195K) -
抗昆虫タンパク質ATS3およびPLATとカイワレ大根スプラウトの一過的発現系北島 佐紀人2022 年 60 巻 6 号 p. 267-268
発行日: 2022/06/01
公開日: 2023/06/01
ジャーナル フリーPDF形式でダウンロード (2459K) -
胎盤とウイルスの意外な関係唄 花子, 川原 学, 高橋 昌志2022 年 60 巻 6 号 p. 269-271
発行日: 2022/06/01
公開日: 2023/06/01
ジャーナル フリーPDF形式でダウンロード (1579K)
-
学理とその応用椿 俊太郎2022 年 60 巻 6 号 p. 272-277
発行日: 2022/06/01
公開日: 2023/06/01
ジャーナル フリーマイクロ波照射により,物質高選択的に熱的非平衡反応場を形成し,化学反応を促進することができる.本稿では,マイクロ波が触媒反応を加速する機構の解明と,環境に調和した新化学プロセスへの応用研究について紹介する.
 抄録全体を表示PDF形式でダウンロード (3478K)
抄録全体を表示PDF形式でダウンロード (3478K) -
KLF15の重要性矢作 直也2022 年 60 巻 6 号 p. 278-283
発行日: 2022/06/01
公開日: 2023/06/01
ジャーナル フリー三大栄養素(タンパク質・糖質・脂質)は,ヒトの身体を動かす主要なエネルギー源であり,エネルギー産生栄養素とも呼ばれる.肥満・糖尿病などの過栄養病態では,糖質から脂質へのエネルギー(カーボン)フローが亢進し,逆に,サルコペニア・フレイルなどの低栄養病態ではタンパク質から糖質へのエネルギーフローが増加する.また,絶食時にはタンパク質から糖質へ変換され,食後には糖質から脂質へのフローが増加する.しかし,糖質から脂質へのフローも,タンパク質から糖質へのフローも逆流することはない(脂肪酸から糖を合成することはできず,また,糖質の代謝産物からはアミノ基転移反応によりアミノ酸が生じ得るものの,マクロに見た場合のエネルギーフロー(カーボンフロー)として,糖質からタンパク質へいくことはない).すなわち,三大栄養素間のエネルギーフローは一方向性であり,ゆえにそれらの間のバランス維持は厳密に制御されているはずである.筆者は,この「三大栄養素間のエネルギーフローの一方向性」を,「栄養学のセントラルドグマ」(図1)と呼んでいる.本稿では,これらの三大栄養素間のエネルギーフローの調節機構について最新のニュートリゲノミクス研究の知見を中心に解説する.
 抄録全体を表示PDF形式でダウンロード (2524K)
抄録全体を表示PDF形式でダウンロード (2524K) -
抗体代替ペプチドのデザイン戦略門之園 哲哉2022 年 60 巻 6 号 p. 284-289
発行日: 2022/06/01
公開日: 2023/06/01
ジャーナル フリーがんなどの分子標的治療薬として,抗体医薬が盛んに開発されている.抗体医薬を筆頭とする高分子医薬は,従来の低分子医薬と比べると標的への特異性が高く,高い治療効果と副作用の軽減が期待できる.一方で,分子量が大きく複雑な構造を持つため,製造方法が限られることや組織への浸透性が低いことなど,新たな課題も顕在化してきている.そこで注目されているのが,抗体医薬の機能を代替する医薬(抗体代替医薬)としての利用が期待できる,ペプチドや小型タンパク質などの中分子サイズの抗原結合分子である.本稿では,このような中分子医薬のデザイン戦略を中心に,中分子創薬について概説する.
 抄録全体を表示PDF形式でダウンロード (1316K)
抄録全体を表示PDF形式でダウンロード (1316K) -
そのゲノムならびに粒子構造に関する特殊性武村 政春, 深谷 将, 緒方 博之, 村田 和義2022 年 60 巻 6 号 p. 290-294
発行日: 2022/06/01
公開日: 2023/06/01
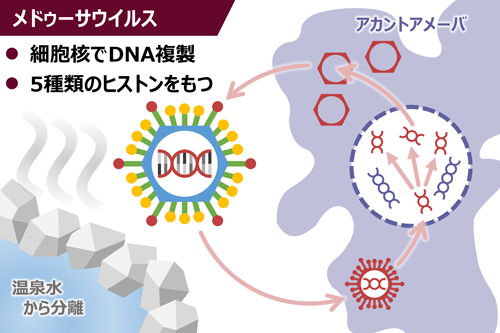
ジャーナル フリー2003年以降,主にアカントアメーバ属を宿主として分離が相次いでいる「巨大ウイルス」は,粒子径,ゲノムサイズ,遺伝子数などがそれまでのウイルスに比べて大きく,バクテリアや真核細胞のそれに達するほど大きなものも存在する.これらのウイルスには,アミノアシルtRNA合成酵素など翻訳に関わる複数の遺伝子を自らコードするものも存在する.その中で,メドゥーサウイルスと名付けられた巨大ウイルスのゲノムには,ヒストンやサイクリンなど細胞核機能と密接に関わる遺伝子がコードされていること,粒子構造にもほかのウイルスにはない興味深い特徴が存在することが明らかとなってきた.メドゥーサウイルスとは,果たして何者なのだろうか.
 抄録全体を表示PDF形式でダウンロード (3217K)
抄録全体を表示PDF形式でダウンロード (3217K) -
中分子デザイン系としての可能性と魅力梅村 舞子2022 年 60 巻 6 号 p. 295-303
発行日: 2022/06/01
公開日: 2023/06/01
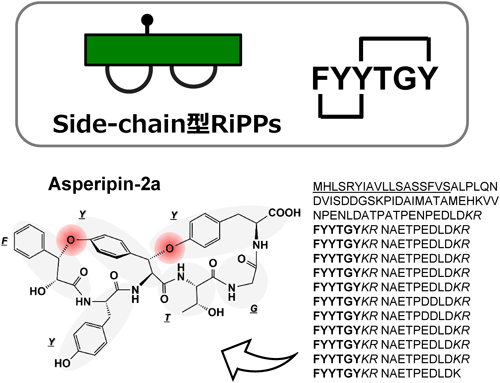
ジャーナル フリー植物や微生物が産生する環状ペプチドは生理活性を持つものが多く,構造多様性と安定性,膜透過性の観点から,化学合成可能な低分子薬とサイズが大きい抗体医薬の間を埋める中分子医薬品の重要な候補である.中でもリボソーム経由で生合成されるribosomally synthesized and post-translationally modified peptides(RiPPs)は,その改変・修飾容易性から,デザイン可能な創薬ターゲットとして近年特に注目されている.本稿で取り上げる真核生物由来RiPPsは,側鎖間で環化し両親媒性を示すものを多く含むため,標的タンパク質と特異的に相互作用する環状ペプチドをデザインする系として期待される.
 抄録全体を表示PDF形式でダウンロード (3022K)
抄録全体を表示PDF形式でダウンロード (3022K)
-
ツシマヤマネコ保護増殖事業の概要中島 絵里2022 年 60 巻 6 号 p. 304-309
発行日: 2022/06/01
公開日: 2023/06/01
ジャーナル フリーPDF形式でダウンロード (6268K)
-
北本勝ひこ著 四六判,330頁,本体価格4,000円 丸善出版,2021年6月鈴木 チセ2022 年 60 巻 6 号 p. 310
発行日: 2022/06/01
公開日: 2023/06/01
ジャーナル フリーPDF形式でダウンロード (196K) -
西村敏英,黒田素央編 A5判,256頁,本体価格4,000円 恒星社厚生閣,2021年7月久保田 紀久枝2022 年 60 巻 6 号 p. 311
発行日: 2022/06/01
公開日: 2023/06/01
ジャーナル フリーPDF形式でダウンロード (188K)
- |<
- <
- 1
- >
- >|